鎂作為最輕的結構金屬具有低密度、高比強度和良好的生物相容性等優點,已廣泛應用于航空航天、便攜式電子設備及生物醫學等方面。但是,鎂的化學性質很活潑,極易發生嚴重腐蝕,因此研發耐蝕鎂合金仍是一項具有挑戰性的任務。合金的腐蝕行為常通過極化曲線表征腐蝕電位及腐蝕電流密度之間的關系。然而,實驗中的試錯過程效率較低,限制了人們從原子及電子層面深入探索復雜的腐蝕機制。
第一性原理密度泛函理論可以提供關鍵參數(如功函數),用于表征腐蝕特性。根據傳統理論,材料表面的功函數越高,相應的耐蝕性就越突出。但最新的研究表明,這一方法僅適用于不同金屬間耐蝕性的判斷,對于同類合金或者更微觀的同一材料不同晶面的耐蝕性則無法判斷。例如,Song等人發現盡管純鎂的基面(0001)的功函數略小于柱面(10-10)的功函數,但前者的耐蝕性比后者高15-20倍。Ma等人考慮到功函數、表面能密度、吸附能和空位能,開發了一種合理的方法來模擬陽極溶解曲線。該模型解釋了鎂的各向異性腐蝕行為,并提供了6種可以有效降低陽極溶解速率的合金元素。Taylor等人為了評估鎂的腐蝕性能,還利用表面原子溶解能和過渡態能壘來預測鎂基面的溶解和析氫速率。因此,通過密度泛函理論建立腐蝕模型為我們設計具有高耐蝕性的金屬材料提供了可能性。
在本工作中,南京理工大學劉偉教授和東北大學張濤教授團隊精心設計了一種全新的電化學方法,用以模擬水溶液中鎂的陽極和陰極極化曲線。新模型通過從鎂的表面去除一系列電子模擬陽極溶解過程。在此過程中形成的極化電流可以通過經典電化學公式進一步轉化獲得。通過計算不同鎂晶面上的水解反應、Tafel反應和Heyrovsky反應的過渡能壘,獲得了陰極的析氫反應速率。利用這一模型,作者成功地預測出鎂的腐蝕各項異性,基面與不同柱面之間的耐蝕性以如下方式排列:(0001) > (10-10)A > (11-20) >( 10-10)B。這一模型揭示了,材料的耐蝕性由表面空位能、接觸電勢以及析氫反應的過渡態能壘共同決定。相關研究成果以題“First-principles modeling of the anodic and cathodic polarization to predict the corrosion behavior of Mg and its alloys”發表在Acta Materialia上。
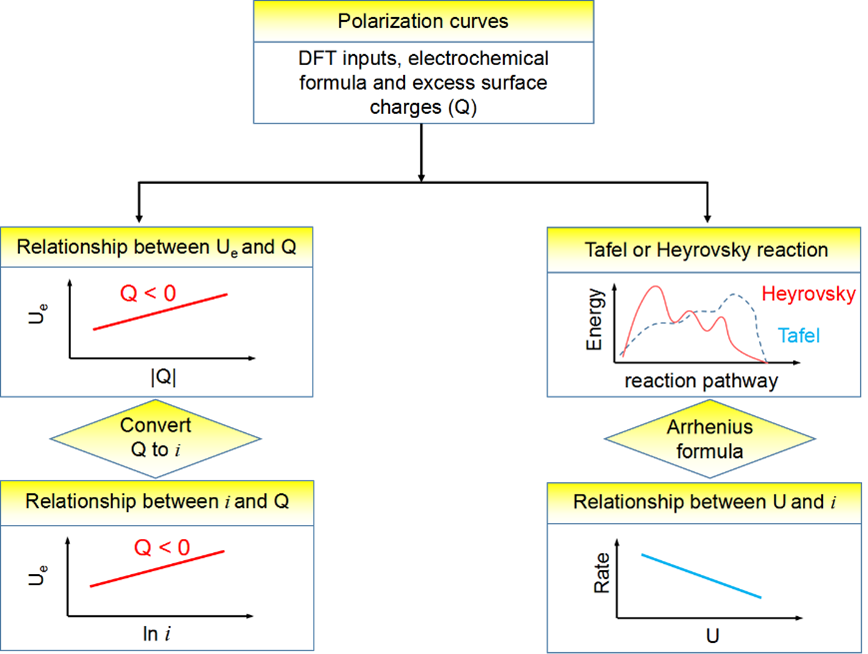
圖1. 計算陽極和陰極極化曲線的示意圖。該模型基于DFT輸入、電化學公式和過量表面電荷Q。通過引入Q和計算的陰極反應能壘,可以從熱力學和動力學中獲得陽極腐蝕電流密度i和陰極腐蝕速率。
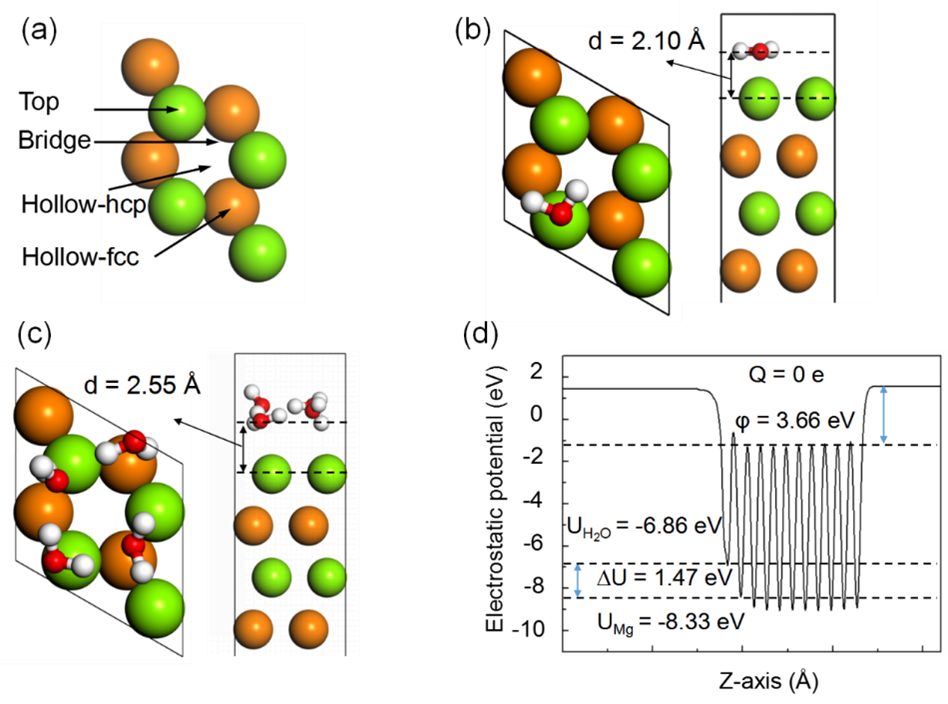
圖2.(a)水分子在鎂的基面上的四種可能的吸附構型。HCP結構中的A類和B類原子分別由綠色和橙色球表示。(b)單個H2O分子在吸附在Mg的基面上的Top位置為最穩定的優化結構。水分子中的氫原子和氧原子用白色和紅色的球表示。(c)單層水分子吸附在鎂基面上的優化結構,其中每個H2O子初始都吸附在Top位置。(d)鎂基面上吸附單層H2O結構的靜電勢。
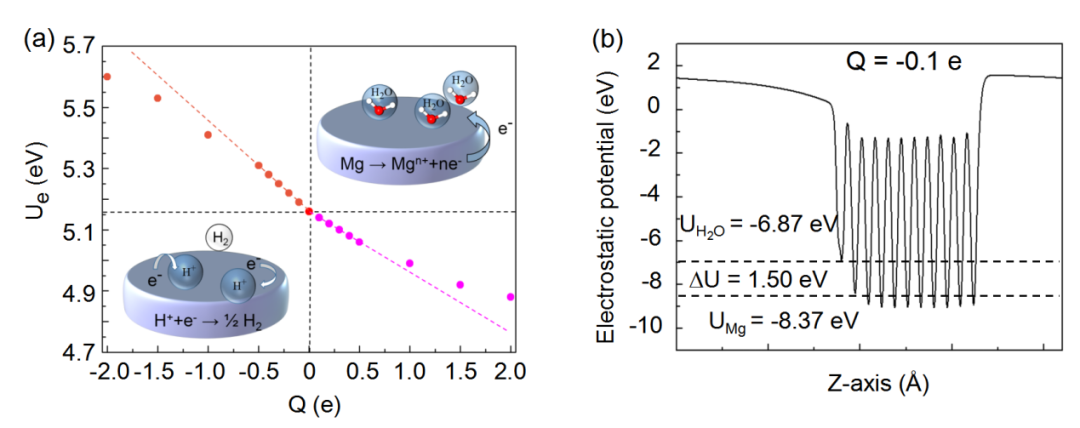
圖3.(a)基面的腐蝕電位U隨過量表面電荷Q而變化。當Q小于0.5e時,U隨Q線性變化。然而,當Q大于0.5e時電極電位偏離線性結果,這意味著增加更大的電荷會破壞系統的穩定性。(b)Mg基面上吸附單層H2O結構的靜電勢,Q= - 0.1e。
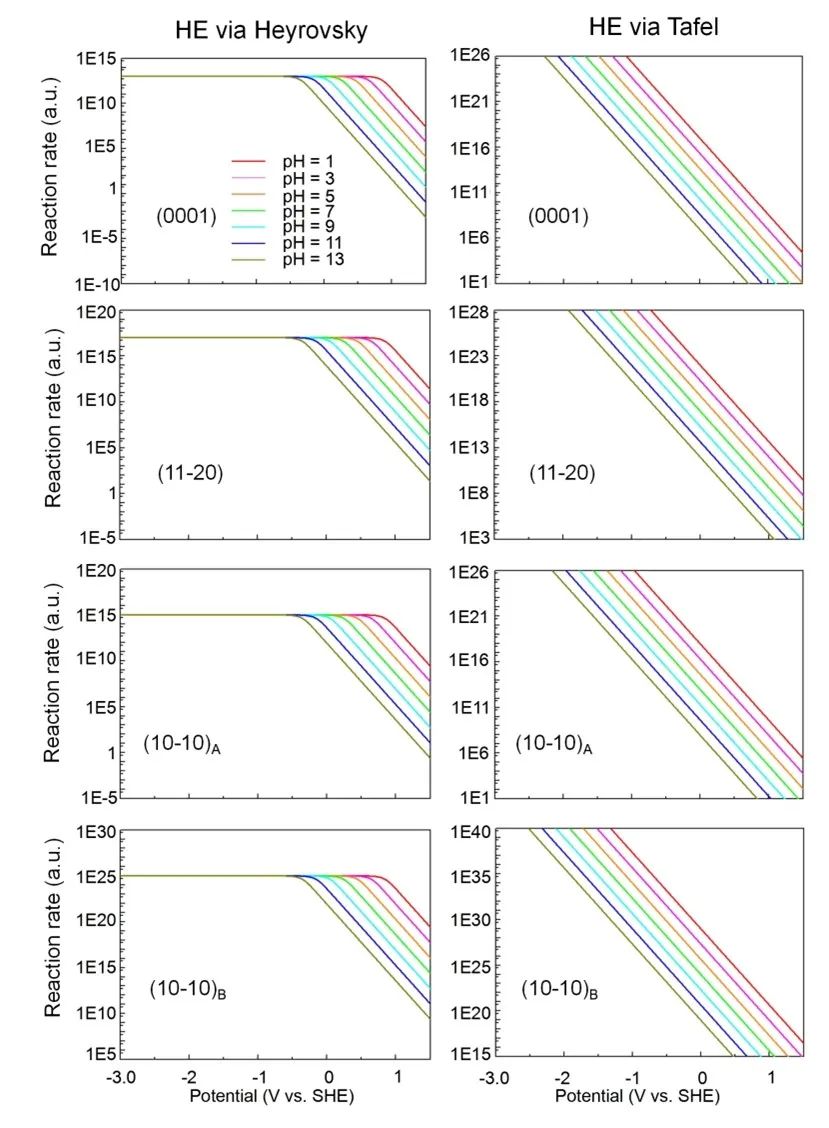
圖4.不同Mg晶面上的析氫反應速率與施加的電勢U和pH的函數關系。
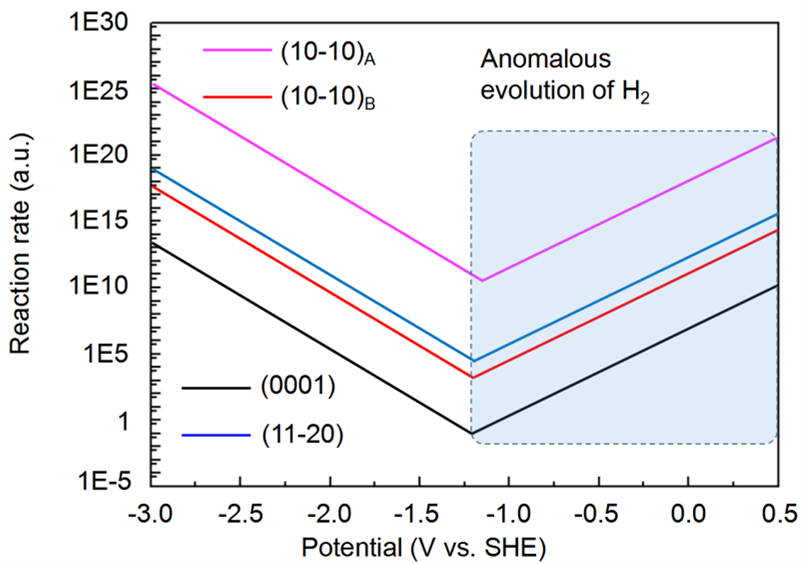
圖5. 總析氫反應速率與不同Mg晶面上施加的電勢U的函數關系。交叉點代表平衡電位。陰影區域表示負差異效應的過程。
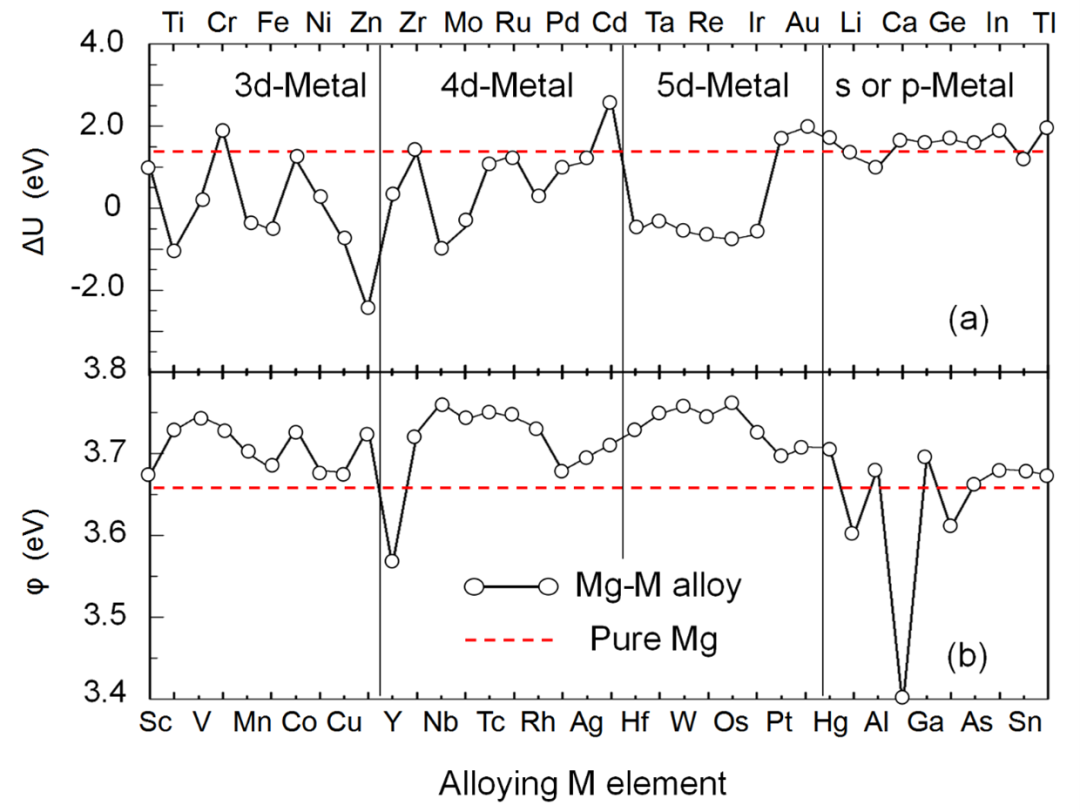
圖6.(a)接觸電勢ΔU和(b)Mg-M合金基面的功函數,合金元素選擇3d、4d、5d和一些選定的s和p金屬。紅色虛線表示純鎂的結果作為比較。
最終,通過將密度泛函理論與電化學公式相結合,作者開發了一種新的理論模型來確定鎂及其合金的腐蝕極化曲線。利用該模型,研究了鎂的不同晶面的腐蝕行為并發現:鎂基面的耐蝕性優于柱面的耐蝕性,這是因為前者的空位形成能和析氫反應能壘較低。同時,陽極極化曲線表明,添加Cr、Cd、Pt、Au、Hg、Ga、Ge、as、In和Tl等元素,可有效地提高鎂合金的耐蝕性,與實驗觀察結果高度一致。
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 腐蝕與防護網官方QQ群:140808414