摘要
針對3A21鋁合金在乙二醇冷卻液中的腐蝕問題,采用浸泡實驗和表面分析技術(shù)系統(tǒng)研究了痕量Cl-和Cu2+對3A21鋁合金在50 ℃乙二醇-水冷卻液中腐蝕行為的影響。結(jié)果表明,Cl-引發(fā)了鋁合金的點腐蝕,隨著Cl-濃度增大,鋁合金點蝕敏感性增大。Cu2+促進(jìn)鋁合金鈍化膜的破裂,并與Al發(fā)生置換反應(yīng)沉積在鋁合金表面,電偶作用加速了鋁合金的腐蝕。Cl-和Cu2+共存時,鈍化膜破裂和電偶作用導(dǎo)致鋁合金腐蝕加劇。
關(guān)鍵詞: 3A21鋁合金 ; 乙二醇 ; 痕量離子 ; 點蝕
乙二醇型冷卻液廣泛應(yīng)用于交通、能源、儀表、無線通訊等工業(yè)領(lǐng)域鋁合金設(shè)備的冷卻。在使用中,鋁合金的腐蝕造成流道穿孔和堵塞等問題[1,2],嚴(yán)重影響設(shè)備的正常工作。
鋁合金在水介質(zhì)中的腐蝕主要表現(xiàn)為點蝕[3-6],但鋁合金在乙二醇冷卻液中的腐蝕缺乏系統(tǒng)的研究。鋁合金在乙二醇冷卻液中的腐蝕除受本身影響外[7,8],其腐蝕行為更依賴于離子種類及濃度[9-13]。通常,水質(zhì)原因造成Cl-污染,銅材腐蝕導(dǎo)致Cu2+污染[14-16]。對于高功率雷達(dá)冷卻器,離子濃度低至mg/L級,研究痕量離子對鋁合金腐蝕行為的影響對預(yù)測設(shè)備壽命及冷卻液的運維具有重要意義。
本文系統(tǒng)研究了痕量Cl-和Cu2+對3A21鋁合金腐蝕行為的影響,確定影響鋁合金腐蝕的關(guān)鍵因素,為乙二醇型冷卻液的使用和維護(hù)提供一定的參考。
1 實驗方法
實驗材料為厚度為3 mm的3A21鋁合金板材,其化學(xué)成分 (質(zhì)量分?jǐn)?shù),%) 為:Mn 1.13,F(xiàn)e 0.50,Si 0.32,Cu 0.06,Zn 0.05,Mg 0.02,Ti 0.01,Al余量。
采用線切割將3A21鋁合金板材切割成20 mm×20 mm試樣,用耐水砂紙逐級打磨至800#后,再用丙酮和乙醇混合液超聲波清洗10 min,取出并用冷風(fēng)吹干后放在干燥器中待用。
冰點為-45 ℃的冷卻液由分析純乙二醇和去離子水按57∶43的體積比配制而成。冷卻液中的痕量污染物Cl-和Cu2+分別由分析純NaCl和CuSO4·5H2O配制。首先分別稱取1.65 g NaCl和3.93 g CuSO4·5H2O,配制Cl-和Cu2+濃度均為1000 mg/L的溶液,然后分別量取10,20,50和100 mL溶液并稀釋至1000 mL,即制得Cl-和Cu2+濃度為10,20,50和100 mg/L的溶液。
將預(yù)處理后的3A21鋁合金樣品放入預(yù)加熱到 (50±2) ℃的冷卻液中,浸泡385 h后將樣品取出并用去離子水沖洗干凈,冷風(fēng)吹干。按下式計算腐蝕速度。測試采用3片平行樣品。

式中:v為腐蝕速度,mg/cm2,mt為浸泡后試樣質(zhì)量,g,m0為浸泡前試樣質(zhì)量,g,S為試樣總表面積,cm2。
采用FEI INSPECT F 50掃描電鏡 (SEM) 和OXFORD X-Max X射線能譜儀 (EDS) 研究鋁合金腐蝕后的微觀形貌和成分,采用PANalytical X' Pert PRO X射線衍射儀 (XRD) 分析鋁合金的腐蝕產(chǎn)物。
2 結(jié)果與討論
2.1 3A21鋁合金腐蝕形貌
2.1.1 Cl-的影響
圖1是3A21鋁合金在50 ℃含不同濃度Cl-的乙二醇-水冷卻液中腐蝕后的SEM形貌。鋁合金在乙二醇-水冷卻液中腐蝕后 (圖1a),表面沒有出現(xiàn)明顯的腐蝕產(chǎn)物,EDS定性分析檢測到Al、O和C及少量的Mn,表明鋁合金在乙二醇-水冷卻液中生成了Al的氧化物或氫氧化物,與鋁合金在水溶液中的情況類似[17],并伴隨乙二醇的吸附[18],或與Al反應(yīng)形成穩(wěn)定的醇化鋁膜[19]。

圖1 3A21鋁合金在含Cl-的冷卻液中腐蝕后的微觀SEM形貌
當(dāng)冷卻液中含有10 mg/L Cl-時,絕大部分鋁合金表面保持完好 (圖1b),但存在少量腐蝕點 (圖1c),表明Cl-引發(fā)了鋁合金的點蝕。白色腐蝕產(chǎn)物主要由Al、O、C構(gòu)成,并含有少量的Fe、Mn、Si和Zn。XRD分析表明3A21鋁合金主要由α-Al基體和Al6Mn第二相構(gòu)成 (圖2),鋁合金的腐蝕起源于第二相,第二相Al6Mn的電位高于基體α-Al的電位[20],基體優(yōu)先腐蝕造成第二相沉積。當(dāng)冷卻液中Cl-濃度進(jìn)一步增大為20 mg/L時,腐蝕產(chǎn)物數(shù)量明顯增多、尺寸增大 (圖1d),表明鋁合金的腐蝕更嚴(yán)重,白色的腐蝕產(chǎn)物元素構(gòu)成沒有發(fā)生變化。當(dāng)冷卻液中的Cl-濃度達(dá)到50和100 mg/L時,腐蝕形態(tài)沒有發(fā)生顯著改變,但腐蝕產(chǎn)物數(shù)量更多、尺寸更大,腐蝕進(jìn)一步加劇 (圖1e和f)。
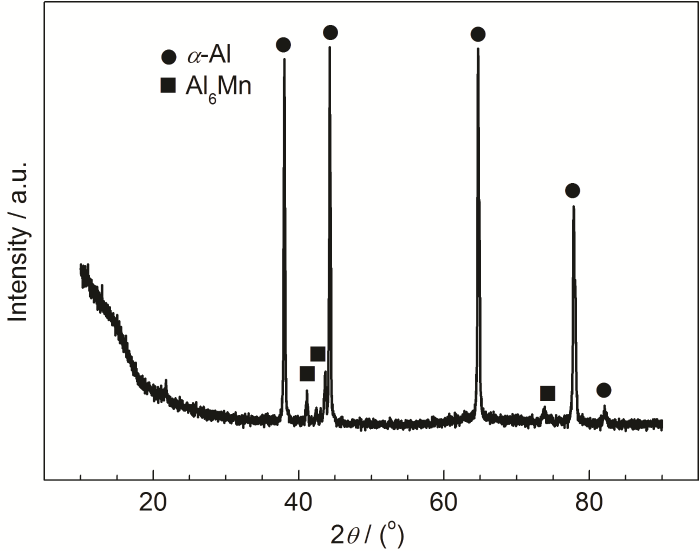
圖2 3A21鋁合金XRD譜
2.1.2 Cu2+的影響
圖3是3A21鋁合金在50 ℃含不同濃度Cu2+的乙二醇-水冷卻液中腐蝕后的SEM形貌。當(dāng)冷卻液中含有10 mg/L Cu2+時,鋁合金表面膜破裂 (圖3a),EDS結(jié)果表明腐蝕產(chǎn)物主要由Al、O和C構(gòu)成,并檢測到Si、Mn和Cu,Si和Mn來源于鋁合金基體。Cu的出現(xiàn)表明Cu2+與Al發(fā)生置換反應(yīng),腐蝕產(chǎn)物中Cu的含量約為1% (質(zhì)量分?jǐn)?shù))。當(dāng)冷卻液中Cu2+濃度為20 mg/L時,鋁合金發(fā)生局部腐蝕 (圖3b),在未發(fā)生局部腐蝕區(qū)域 (圖3c),鋁合金表面沉積了數(shù)量眾多、尺寸較大的金屬Cu顆粒,并夾雜大量細(xì)小、絮狀腐蝕產(chǎn)物。當(dāng)冷卻液中Cu2+濃度為50 mg/L時,鋁合金同樣發(fā)生局部腐蝕,腐蝕產(chǎn)物存在大量裂紋 (圖3d),并伴隨更大尺寸Cu顆粒的沉積 (圖3e)。當(dāng)冷卻液中的Cu2+濃度為100 mg/L時,鋁合金發(fā)生嚴(yán)重局部腐蝕 (圖3f),并沉積更多金屬Cu顆粒 (圖3g)。

圖3 3A21鋁合金在含Cu2+的冷卻液中腐蝕后的微觀SEM形貌
2.1.3 Cl-和Cu2+的影響
圖4是3A21鋁合金在同時含Cl-和10 mg/L Cu2+的冷卻液中腐蝕后的SEM形貌。鋁合金在所有溶液中均發(fā)生嚴(yán)重的點蝕,點蝕周圍的氧化膜破裂,腐蝕坑邊緣堆積了大量的腐蝕產(chǎn)物,隨Cl-濃度增大,腐蝕產(chǎn)物逐漸由顆粒狀轉(zhuǎn)變?yōu)樾鯛睿?dāng)Cl-濃度高于50 mg/L時尤為明顯,表明鋁合金的腐蝕加劇。EDS分析表明,腐蝕坑邊緣的腐蝕產(chǎn)物中Cu的質(zhì)量分?jǐn)?shù)約為0.5%~6%,沉積Cu的部位Cu含量超過60%,表明發(fā)生了嚴(yán)重的金屬Cu沉積。

圖4 3A21鋁合金在含Cl-和10 mg/L Cu2+的冷卻液中腐蝕后的微觀SEM形貌
2.2 3A21鋁合金重量變化
圖5a是3A21鋁合金在50 ℃含Cl-和Cu2+的冷卻液中腐蝕385 h后的重量變化。當(dāng)冷卻液中只含有Cl-時,3A21鋁合金表現(xiàn)為增重,隨Cl-濃度的增大增重量增大 (圖5b)。在含Cu2+的冷卻液中表現(xiàn)為增重,隨Cu2+濃度的增加,增重量增大,但到高濃度時重量變化較穩(wěn)定。鋁合金在含Cu2+的冷卻液中腐蝕增重大于在只含Cl-的冷卻液中的增重源于溶液中Cu2+與Al發(fā)生置換反應(yīng)生成金屬Cu沉積在鋁合金表面,如圖6中XRD所示,在含Cu2+的冷卻液中腐蝕后檢測到金屬Cu。Cu2+濃度越大,反應(yīng)生成的Cu越多,故增重越多。3A21鋁合金在同時含不同濃度Cl-和10 mg/L Cu2+的冷卻液中同樣表現(xiàn)為增重,當(dāng)Cl-的濃度小于20 mg/L時,鋁合金的增重隨Cl-濃度的增大而增大,而后降低,是由于鋁合金發(fā)生更嚴(yán)重的腐蝕溶解造成的。相比于在只含Cu2+的冷卻液中,鋁合金在含Cl-和Cu2+的冷卻液中腐蝕增重較少,一方面是由于溶液的腐蝕性增強(qiáng),形成的腐蝕產(chǎn)物溶于溶液造成的。另一方面是由于溶液中Cu2+濃度低 (10 mg/L) 造成沉積的金屬Cu較少。相比于在只含10 mg/L Cu2+溶液中,當(dāng)溶液同時含有10 mg/L Cl-時,鋁合金的增重量明顯增大,表明Cl-首先破壞鋁合金表面鈍化膜,暴露更多的新鮮表面,加劇了Al與Cu2+之間的置換反應(yīng),導(dǎo)致增重量增大。3A21鋁合金的增重一部分源于溶液中Cu2+與鋁發(fā)生置換反應(yīng)生成金屬Cu的沉積,另一部分來源于鋁合金的腐蝕而生成的粘附的鋁氧化物或氫氧化物 (鋁合金在不含離子的乙二醇-水溶液中表現(xiàn)為增重)。
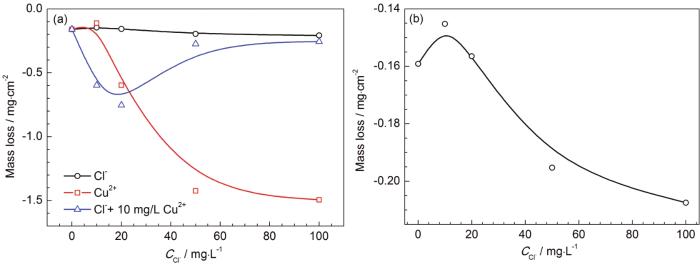
圖5 3A21鋁合金腐蝕質(zhì)量變化
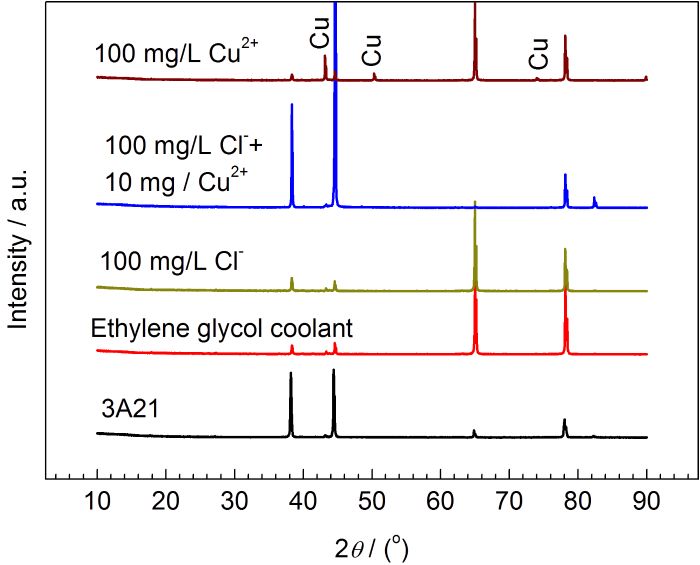
圖6 3A21鋁合金腐蝕產(chǎn)物XRD譜
2.3 3A21鋁合金腐蝕機(jī)理
以上研究結(jié)果表明,Cl-引發(fā)3A21鋁合金的點腐蝕,Cu2+促進(jìn)鋁合金鈍化膜破裂,而在含Cl-和Cu2+的冷卻液中發(fā)生嚴(yán)重的點蝕,鋁合金的腐蝕更嚴(yán)重。
鋁合金在中性水溶液和非水溶液中常發(fā)生點蝕[19,21],通常以方程式 (2) 和 (3) 發(fā)生Al的陽極溶解和陰極氧還原反應(yīng)。

在含Cl-介質(zhì)中,根據(jù)點蝕形成和生長機(jī)制[22],Cl-優(yōu)先于O2吸附于鋁合金表面,導(dǎo)致鈍化膜破壞。Cl-的吸附降低了鋁合金表面O2的吸附,導(dǎo)致鋁合金鈍化膜不能修復(fù)。
在含Cl-介質(zhì)中,鋁合金的陽極反應(yīng)以方程式 (4)~(6) 進(jìn)行[23]。
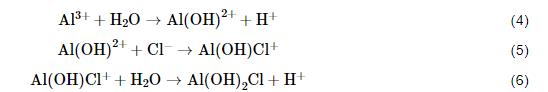
隨著Cl-濃度增大,反應(yīng) (5) 加快,造成中間反應(yīng)產(chǎn)物Al(OH)2+不斷消耗,根據(jù)質(zhì)量作用定律反應(yīng) (4) 和 (6) 速度加快,致使鋁合金的陽極反應(yīng)加速、鈍化膜溶解,最終形成點蝕。
Cu2+對3A21鋁合金加速腐蝕作用一方面由于Cu2+以方程式 (7) 發(fā)生水解反應(yīng),造成局部酸性環(huán)境,促進(jìn)了鋁合金表面鈍化膜的溶解以及Al的腐蝕,如方程式 (8) 和 (9) 所示。Cu2+濃度越大,水解作用越強(qiáng),H+濃度越大,pH值越低,鋁合金氧化膜和鋁基體溶解加快。
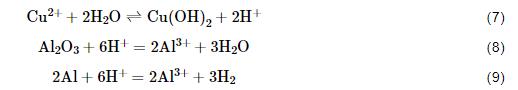
XRD結(jié)果表明,腐蝕后鋁合金表面存在金屬Cu,表明Cu2+與Al發(fā)生了置換反應(yīng),如方程式 (10) 所示,由于Cu的電極電位遠(yuǎn)遠(yuǎn)高于Al的電極電位[24],二者之間的巨大電位差引起的電偶作用加速了鋁合金的腐蝕,在沉積Cu顆粒部位形成點蝕,Cu2+的濃度越大,沉積的金屬Cu越多,腐蝕越顯著。

當(dāng)Cl-和Cu2+在冷卻液中共存時,Cl-破壞鋁合金表面鈍化膜導(dǎo)致更多新鮮表面暴露于溶液中,Cu2+與Al發(fā)生反應(yīng)的幾率增大,造成鋁合金加速腐蝕。加之Cu2+本身即可造成鋁合金表面鈍化膜破裂,因此,在Cl-和Cu2+共存時,鋁合金的腐蝕尤為嚴(yán)重。
3 結(jié)論
(1) Cl-的濃度越大,3A21鋁合金的點敏感性越大,腐蝕越嚴(yán)重。
(2) 鋁合金在只含痕量Cu2+的冷卻液中,Cu2+破壞了鋁合金表面鈍化膜,并與Al發(fā)生置換反應(yīng)生成金屬Cu沉積在鋁合金表面,Cu與鋁之間的電偶作用加速了鋁合金的腐蝕。
(3) 當(dāng)Cl-和Cu2+共存時,即使二者的濃度低至10 mg/L,由于鋁合金鈍化膜的破裂協(xié)同Cu-Al電偶作用,促進(jìn)了鋁合金點蝕的發(fā)生和發(fā)展,大大加速了鋁合金的腐蝕。
參考文獻(xiàn)
1 Wang C, Yao Y, Zhong J F. Research survey of corrosion resistance techniques for aluminum alloy flow channel [J]. Electro-Mech. Eng., 2014, 30(2): 1
1 王超, 姚曄, 鐘劍鋒. 鋁合金流道防腐蝕技術(shù)研究概況 [J]. 電子機(jī)械工程, 2014, 30(2): 1
2 Zhao T L, Zhang L J, Qian J Y, et al. Corrosion behavior of Al-alloys 3A21, 5A05 and 6063 in low-conductive ethylene glycol coolant [J]. Corros. Sci. Prot. Technol., 2017, 29: 507
2 趙天亮, 張梁娟, 錢吉裕等. 3A21、5A05和6063鋁合金在低電導(dǎo)率乙二醇冷卻液中的腐蝕行為 [J]. 腐蝕科學(xué)與防護(hù)技術(shù), 2017, 29: 507
3 Alodan M A, Smyrl W H. Detection of localized corrosion of aluminum alloys using fluorescence microscopy [J]. J. Electrochem. Soc., 1998, 145: 1571
4 Fole R T. Localized corrosion of aluminum alloys-a review [J]. Corrosion, 1986, 42: 277
5 Lenderink H J W, Linden M V D, De Wit J H W. Corrosion of aluminium in acidic and neutral solutions [J]. Electrochim. Acta, 1993, 38: 1989
6 Davoodi A, Pan J, Leygraf C, et al. In situ investigation of localized corrosion of aluminum alloys in chloride solution using integrated EC-AFM/SECM techniques [J]. Electrochem. Solid State Lett., 2005, 8: B21
7 Fan J L, Gong M, Hou X, et al. Corrosion behavior of 3A21 aluminum alloy in ethylene glycol-water solution [J]. Corros. Prot., 2014, 35: 1116
7 范金龍, 龔敏, 侯肖等. 3A21鋁合金在乙二醇水溶液中的腐蝕行為 [J]. 腐蝕與防護(hù), 2014, 35: 1116
8 Hu G G, Yang J, Zheng X W. Corrosion behavior of aluminum cold plate in ethylene glycol coolant [J]. Corros. Prot., 2017, 38: 871
8 胡國高, 楊俊, 鄭興文. 鋁制冷板在乙二醇冷卻液中的腐蝕行為 [J]. 腐蝕與防護(hù), 2017, 38: 871
9 Mazhar A A, Arab S T, Noor E A. Electrochemical behaviour of Al-Si alloys in acid and alkaline media [J]. Bull. Electrochem., 2001, 17: 449
10 Liu D Q, He X, Guo X L, et al. Research progress of corrosion of aluminum alloys in ethylene glycol solution [J]. Hot-Work. Technol., 2019, 48(2): 36
10 劉德慶, 何瀟, 郭新良等. 鋁合金在乙二醇溶液中的腐蝕研究進(jìn)展 [J]. 熱加工工藝, 2019, 48(2): 36
11 Chen X, Tian W M, Li S M, et al. Effect of chloride ion and temperature on corrosion of aluminum alloy in coolant [J]. J. Beijing Univ. Aeronaut. Astronaut., 2016, 42: 2243
11 陳鑫, 田文明, 李松梅等. 氯離子和溫度對鋁合金在冷卻液中腐蝕的影響 [J]. 北京航空航天大學(xué)學(xué)報, 2016, 42: 2243
12 Gao S L, Yu M, Liu J H, et al. Effects of cupric ions on the corrosion behavior of aluminum alloy 5A02 in ethylene glycol-water solution [J]. Int. J. Min. Met. Mater., 2017, 24: 423
13 Abiola O K, Otaigbe J O E. Effect of common water contaminants on the corrosion of aluminium alloys in ethylene glycol-water solution [J]. Corros. Sci., 2008, 50: 242
14 May P M, Ritchie I M, Tan E T. The corrosion of copper in ethylene glycol-water mixtures containing chloride ions [J]. J. Appl. Electrochem., 1991, 21: 358
15 Samiento-Bustos E, Rodriguez J G G, Uruchurtu J, et al. Effect of inorganic inhibitors on the corrosion behavior of 1018 carbon steel in the LiBr+ethylene glycol + H2O mixture [J]. Corros. Sci., 2008, 50: 2296
16 Danaee I, Khomami M N, Attar A A. Corrosion of AISI 4130 steel alloy under hydrodynamic condition in ethylene glycol+Water+NO2- solution [J]. J. Mater. Sci. Technol., 2013, 29: 89
17 Wang B, Zhang L W, Su Y, et al. Investigation on the corrosion behavior of aluminum alloys 3A21 and 7A09 in chloride aqueous solution [J]. Mater. Des., 2013, 50: 15
18 Bazeleva N A, Herasymenko Y S. Corrosion-electrochemical behavior of aluminum alloys in aqueous ethylene glycol media [J]. Mater. Sci., 2007, 43: 851
19 Zhang G A, Xu L Y, Cheng Y F. Mechanistic aspects of electrochemical corrosion of aluminum alloy in ethylene glycol-water solution [J]. Electrochim. Acta, 2008, 53: 8245
20 Hung Y C, Zhu H Y, Xiao Z B. Effects of aging processes on microstructure, specific capacitance and surfacial corrosion morphology of 3003 aluminum alloy cathode foil [J]. Mater. Mech. Eng., 2013, 37(1): 25
20 黃元春, 朱弘源, 肖政兵. 時效工藝對3003鋁合金陰極箔組織、比電容和表面腐蝕形貌的影響 [J]. 機(jī)械工程材料, 2013, 37(1): 25
21 El-Etre A Y. Inhibition of aluminum corrosion using Opuntia extract [J]. Corros. Sci., 2003, 45: 2485
22 Badawy W A, Al-Kharafi F M, El-Azab A S. Electrochemical behaviour and corrosion inhibition of Al, Al-6061 and Al-Cu in neutral aqueous solutions [J]. Corros. Sci., 1999, 41: 709
23 Szklarska-Smialowska Z. Pitting corrosion of aluminum [J]. Corros. Sci., 1999, 41: 1743
24 Cao C N. Principles of Electrochemistry of Corrosion [M]. 3rd Ed. Beijing: Chemical Industry Press, 2008
24 曹楚南. 腐蝕電化學(xué)原理 [M]. 第3版. 北京: 化學(xué)工業(yè)出版社, 2008
免責(zé)聲明:本網(wǎng)站所轉(zhuǎn)載的文字、圖片與視頻資料版權(quán)歸原創(chuàng)作者所有,如果涉及侵權(quán),請第一時間聯(lián)系本網(wǎng)刪除。

官方微信
《中國腐蝕與防護(hù)網(wǎng)電子期刊》征訂啟事
- 投稿聯(lián)系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護(hù)網(wǎng)官方QQ群:140808414





