摘要
采用干/濕交替的實驗方法模擬大氣腐蝕過程。運用X射線衍射、3D激光測量顯微鏡、電化學阻抗譜以及極化曲線等手段,研究了O3/SO2復合大氣環境中Q235B鋼的腐蝕演化特性。結果表明,O3和SO2的交互作用對Q235B鋼的腐蝕有明顯的抑制作用。腐蝕演化特性方面,當模擬環境中Na2SO3濃度為0.01 mol/L時,O3/SO2復合大氣環境中Q235B鋼的腐蝕速率呈先迅速增大而后緩慢減小的趨勢; 當模擬環境中Na2SO3濃度為0.05 mol/L時,O3/SO2復合大氣環境中Q235B鋼的腐蝕速率呈先緩慢增大后迅速下降的趨勢; 當模擬環境中Na2SO3濃度為0.10 mol/L時,O3/SO2復合大氣環境中Q235B鋼的腐蝕速率呈先增大而后緩慢減小的趨勢。相比于不含O3的大氣環境,當模擬大氣中SO2含量較低時,O3和SO2的交互作用會促進具有保護性腐蝕產物中α-FeOOH生成;而當大氣中SO2含量較高時,O3對腐蝕產物相組成影響不明顯。
關鍵詞: Q235B鋼 ; O3 ; 大氣腐蝕 ; 腐蝕產物
鋼鐵的大氣腐蝕是指鋼鐵表面與其周圍大氣環境之間發生的涉及多種氣象因素、多種污染物組分參與、以及界面經歷干/濕交替變化并伴有腐蝕產物生成的多種物理化學過程的綜合體現,該腐蝕過程會受大氣中的各種污染氣體在表面薄液膜中溶解的影響[1-3]。因此,研究多環境因素交互作用下鋼鐵的大氣腐蝕演化特征與機制十分必要。
鋼鐵的大氣腐蝕環境按空氣中腐蝕性介質的種類與含量的不同可以分為工業大氣 (腐蝕性介質主要為SO2)、海岸大氣 (腐蝕性介質主要為Cl-)、工業-海岸大氣、城市大氣和鄉村田園大氣等[4,5]。在海岸大氣中,Cl-對鋼鐵腐蝕影響的研究已經較為成熟,學術界普遍認為起到促進作用。Henriksen等[6]研究表明:NaCl先從空氣中吸收水分,然后在鋼表面發生O2的去極化,從而促進了鋼的腐蝕。文獻[1,7]認為在海岸大氣中由于Cl-體積較小,可以穿透腐蝕產物層到達鋼鐵表面誘發腐蝕。文獻[8,9]表明在Cl-濃度低的地方有利于生成α-FeOOH和γ-FeOOH;在Cl-濃度高的地方更易于生成β-FeOOH。在工業大氣中,SO2對鋼鐵腐蝕的影響更為復雜。Evans等[10,11]研究表明,SO2可引起“酸的再生循環”,從而加速鋼鐵腐蝕。而Leygraf等[12]則認為,具有保護性的α-FeOOH更容易在SO2濃度較高的大氣中生成,從而又起到延緩鋼鐵腐蝕的作用。Allam等[13]認為在腐蝕初期Cl-因侵蝕性較強而起主導作用,而在腐蝕后期SO2又成了促進腐蝕的首要因素。Asami等[14]通過對日本四日市 (工業-海岸大氣地區) 17年的大氣腐蝕曝曬實驗研究表明,普通碳鋼和耐候鋼的鐵銹均由α-FeOOH、β-FeOOH、γ-FeOOH、Fe3O4以及非晶組成。但Wang等[15]在青島 (工業-海岸大氣地區) 的鋼曝曬實驗中并沒有檢測到明顯的β-FeOOH,這應該是由于四日市和青島兩地區的SO2濃度不同所造成的。陳文娟等[4,5]研究認為,在Cl-和SO2交互作用的工業-海岸大氣中,當SO2濃度較低時,鋼鐵遵循只含Cl-大氣環境的腐蝕特性;當SO2濃度較高時,鋼鐵遵循只含SO2大氣環境的腐蝕特性。王振堯等[16]研究表明,SO2和Cl-的協同效應會加速碳鋼的腐蝕,但二者比例的變化對碳鋼腐蝕失重及腐蝕產物成分的影響并不明顯。
近幾年來,大氣中的次生污染物 (如O3等) 的濃度逐漸上升[17-21],含有O3的大氣腐蝕體系成為了大氣腐蝕領域新的研究熱點。Wiesinger等[22]研究了在一定相對濕度 (0%、50%和90%) 的大氣環境中,高純多晶銀樣品與臭氧的相互作用,認為氧化物的形成和腐蝕速率取決于大氣中的相對濕度,表明在50%相對濕度時O3對銀具有強烈的腐蝕作用。Augusto等[23]認為,在意大利空氣中O3的濃度已達到導致石灰石和Cu發生腐蝕的臨界濃度。Oesch等[24]研究表明,O3對Cu腐蝕的促進作用要強于SO2和NO2。陳文娟等[25]研究表明,O3和Cl-的交互作用對Q235B鋼的腐蝕有明顯的促進作用。Aastrup等[26]研究表明,當O3與SO2聯合作用時,會明顯增加Cu的腐蝕速率。而O3與SO2聯合作用對低碳鋼腐蝕的影響還有待進一步探索。
本工作采用實驗室模擬大氣腐蝕干/濕交替實驗 (CCT)[27-29]的方法,結合電化學測量、3D激光測量顯微鏡以及X射線衍射 (XRD) 等手段,研究了O3/SO2復合大氣環境下,低碳鋼的腐蝕速率、腐蝕演化特性、腐蝕產物相組成及腐蝕機理。
1 實驗方法
實驗材料為Q235B鋼,其化學成分 (質量分數,%) 為:C 0.210,Si 0.210,Mn 0.580,S 0.036,P 0.017,Cu 0.020,Fe為余量。采用精密線切割機床對鋼材進行線切割,得到尺寸為30 mm×30 mm×5 mm的實驗樣品供干/濕交替腐蝕增重實驗和腐蝕產物分析用,尺寸為10 mm×10 mm×1 mm的實驗樣品供阻抗譜、極化曲線以及3D激光測量顯微鏡測量用。干/濕交替腐蝕增重實驗[25,27]的流程為:(1) 采用分析天平稱量樣品的初始質量;(2) 往實驗樣品表面按40 μL/cm2滴加腐蝕溶液,并使其鋪展均勻;(3) 設定HWS-70BX恒溫恒濕實驗箱內的溫度和相對濕度分別為30 ℃和60%。當箱內的溫度、相對濕度以及O3濃度穩定后,放置實驗樣品于實驗箱內至設定的時間 (12 h);(4) 樣品干燥后取出實驗樣品再次稱重;(5) 用蒸餾水洗鹽以避免鹽粒在樣品表面上聚集。以上為1個腐蝕周期 (1 CCT);(6) 樣品表面干燥之后,重復第2~5步直到設定的干/濕交替周次。每種環境的腐蝕增重實驗均采用3個平行樣品,并分別進行稱量,之后用3者的平均值繪制出腐蝕增重隨腐蝕周期變化的曲線。模擬大氣所用電解質溶液采用不同濃度的Na2SO3溶液,O3由臭氧發生器 (AZ-1000MG-G) 產生。每次模擬環境中Na2SO3的濃度和O3的含量如表1所示。實驗所用溶液均采用分析純試劑和去離子水配制。
表1 模擬大氣環境中Na2SO3的濃度和O3的含量
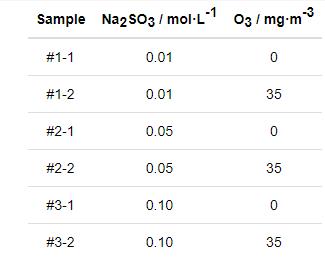
采用DX-2700B X射線衍射 (XRD) 分析經過不同時間腐蝕后得到的腐蝕產物相組成。粉末樣品的制備過程是:將鋼鐵樣品表面銹層刮下,研磨后制成粉末樣品。衍射測量時掃描速度為2°/min。采用對比XRD結果中各個相的相對峰強進行相組成的半定量分析[25,27]。采用VK-X2503D激光測量顯微鏡,觀察材料表面輪廓并進行形狀的三維測試與定量分析。
采用CS310電化學工作站進行電化學測試,采用三電極體系,工作電極為不同干/濕交替周次腐蝕后的帶銹鋼樣;輔助電極為4 cm2的Pt片;參比電極為飽和甘汞電極 (SCE)。溶液與參比電極之間采用魯金毛細管相連,魯金毛細管口靠近工作電極表面 (約1 mm距離),以減小溶液歐姆電位降。工作溫度為室溫 (25 °C),所有的電位值均是相對于飽和甘汞電極的電位。實驗過程中所用的電解液分別為各自的模擬大氣腐蝕的溶液。電化學阻抗譜 (EIS) 的頻率范圍為105~10-2 Hz,測試時施加的擾動交流電位幅度為10 mV。動電位極化曲線掃描電位范圍為±0.3 V vsEcorr (相對于自腐蝕電位),掃描速度為0.1 mV/s。
2 實驗結果
2.1 腐蝕動力學
圖1所示為Q235B鋼在6種模擬大氣環境中的腐蝕增重曲線。可見,在所有模擬環境中鋼的腐蝕增重隨干/濕交替次數增加而增大。當模擬環境中Na2SO3濃度相同時,Q235B鋼在O3/SO2復合大氣環境中的腐蝕增重均明顯小于僅含SO2的大氣環境中的腐蝕增重。這說明O3和SO2的交互作用抑制了Q235B鋼的大氣腐蝕。此外,對比圖1a~c還可以看出,在O3/SO2復合大氣環境中,Q235B鋼的腐蝕增重隨著SO2濃度的升高而逐漸增大。
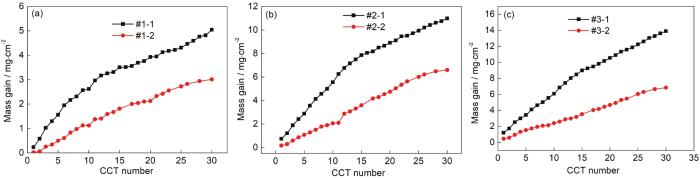
圖1 Q235鋼模擬大氣環境中低碳鋼的腐蝕增重曲線
鋼鐵大氣腐蝕動力學符合冪函數規律如式 (1) 所示[1,2],其中W為單位面積的腐蝕增重,N為干/濕交替腐蝕周期數 (CCT次數),A和n為常數。從式 (1) 可以得到腐蝕速率公式 (2):

對6種模擬環境中的腐蝕增重曲線依次進行分段擬合得到腐蝕速率隨干/濕交替次數變化的曲線如圖2所示。圖2a表明,當模擬環境中Na2SO3濃度為0.01 mol/L時,腐蝕速率變化規律為:僅含SO2的大氣環境中Q235B鋼的腐蝕速率呈先迅速增大后又急劇減小的趨勢;O3/SO2復合大氣環境中Q235B鋼的腐蝕速率呈先迅速增大而后緩慢減小的趨勢。對比兩條腐蝕速率曲線還可以發現,在20 CCT之前O3/SO2復合大氣環境中低碳鋼的腐蝕速率均明顯低于僅含SO2的大氣環境中低碳鋼的腐蝕速率;在20 CCT之后O3/SO2復合大氣環境中低碳鋼的腐蝕速率略高于僅含SO2的大氣環境中低碳鋼的腐蝕速率。圖3b表明,當模擬環境中Na2SO3濃度為0.05 mol/L時,腐蝕速率變化規律為:僅含SO2的大氣環境中Q235B鋼的腐蝕速率呈逐漸減小的趨勢;O3/SO2復合大氣環境中Q235B鋼的腐蝕速率基本呈先緩慢增大后下降的趨勢。對比兩條腐蝕速率曲線還可以發現,在15CCT之前O3/SO2復合大氣環境中低碳鋼的腐蝕速率均明顯低于僅含SO2的大氣環境中低碳鋼的腐蝕速率;在16~25 CCT,O3/SO2復合大氣環境中低碳鋼的腐蝕速率略高于僅含SO2的大氣環境中低碳鋼的腐蝕速率;在26 CCT之后,O3/SO2復合大氣環境中低碳鋼的腐蝕速率遠低于僅含SO2的大氣環境中低碳鋼的腐蝕速率。這說明此大氣環境中O3和SO2的交互作用可以抑制鋼鐵的腐蝕。圖3c表明,當模擬環境中Na2SO3濃度為0.10 mol/L時,腐蝕速率變化規律為:僅含SO2的大氣環境中Q235B鋼的腐蝕速率呈逐漸減小的趨勢;O3/SO2復合大氣環境中Q235B鋼的腐蝕速率呈先增大而后緩慢減小的趨勢。對比兩條腐蝕速率曲線還可以發現,在整個腐蝕過程中,O3/SO2復合大氣環境中低碳鋼的腐蝕速率均明顯低于僅含SO2的大氣環境中低碳鋼的腐蝕速率,這也說明此大氣環境中O3和SO2的交互作用可以抑制鋼鐵的腐蝕。此外,從圖3a~c可以看出,Q235B鋼的腐蝕速率逐漸增加。這表明,隨著大氣環境中SO2含量的增加,O3/SO2復合大氣環境對低碳鋼的腐蝕抑制作用越來越明顯。
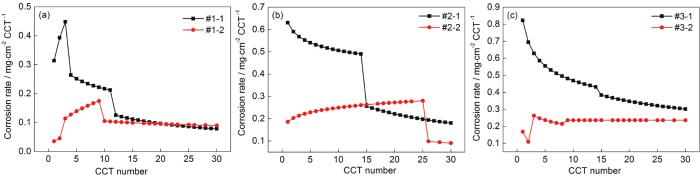
圖2 Q235B鋼在模擬大氣中腐蝕速率隨干/濕交替次數變化的曲線
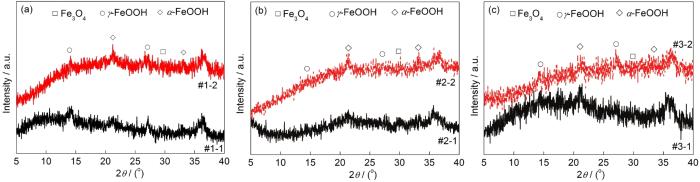
圖3 Q235B鋼在模擬大氣中經過30 CCT后腐蝕產物的XRD譜
2.2 銹層相組成
圖3為Q235B鋼在不同模擬液環境中經干/濕交替腐蝕30 CCT后腐蝕產物的XRD譜。圖3a表明,當模擬環境中SO2濃度為0.01 mol/L時,腐蝕產物均主要由α-FeOOH和γ-FeOOH組成。此外還可以看出,在此SO2濃度的模擬環境中O3和SO2的交互作用會抑制γ-FeOOH的生成,同時促進α-FeOOH的生成。圖3b表明,當模擬環境中SO2濃度為0.05 mol/L時,腐蝕產物主要由α-FeOOH和少量的γ-FeOOH和Fe3O4組成。此外還可以看出,與僅含SO2的大氣環境相比,O3/SO2復合大氣環境下銹層相組成中α-FeOOH的衍射峰相對強度較高,而Fe3O4的衍射峰相對強度較弱,說明在此SO2濃度的大氣環境中O3和SO2的交互作用會促進α-FeOOH同時抑制Fe3O4的生成。圖3c表明,當模擬環境中SO2濃度為0.10 mol/L時,腐蝕產物均主要由α-FeOOH和γ-FeOOH組成。O3和SO2的交互作用對腐蝕產物的影響不明顯。
以上結果表明,當模擬大氣中SO2含量較低時,O3和SO2的交互作用有利于具有保護性腐蝕產物中α-FeOOH生成;而當大氣中SO2含量較高時,O3和SO2的交互作用對腐蝕產物相組成影響不明顯。
2.3 銹層電化學性質
圖4為經過不同干/濕循環次數腐蝕后的Q235B鋼帶銹電極在大氣模擬環境中的極化曲線。當模擬環境中SO2濃度為0.01 mol/L時,帶銹電極極化曲線的變化規律為:如圖4a1所示,在僅含SO2的大氣環境中帶銹電極的腐蝕電位從1 CCT至30 CCT正移,陰極和陽極電流密度增加,這意味著隨著腐蝕的進行促進了陰極和陽極的反應過程;如圖4a2所示,在O3/SO2復合大氣環境腐蝕過程中,帶銹電極腐蝕電位以及陰極和陽極電流密度隨著腐蝕時間延長逐漸波動,這可能是由于腐蝕過程中銹層交替開裂與修復所造成的。當模擬環境中SO2濃度為0.05 mol/L時,帶銹電極極化曲線的變化規律為:如圖4b1所示,在僅含SO2的大氣環境中帶銹電極極化曲線的變化規律與圖4a2所示相似;如圖4b2所示,在O3/SO2復合大氣環境中帶銹電極的腐蝕電位從1 CCT至10 CCT正移,陰極和陽極電流密度增加,這意味著隨著腐蝕的進行促進了陰極和陽極的反應過程,而在10 CCT之后腐蝕電位、陰陽極電流密度基本穩定。當模擬環境中SO2濃度為0.10 mol/L時,帶銹電極極化曲線的變化規律為:如圖4c1所示,在僅含SO2的大氣環境中帶銹電極極化曲線的變化規律與圖4a2所示相似;如圖4c2所示,在O3/SO2復合大氣環境中帶銹電極在整個30 CCT的腐蝕過程中腐蝕電位變化不大,陰極和陽極電流密度略有波動。
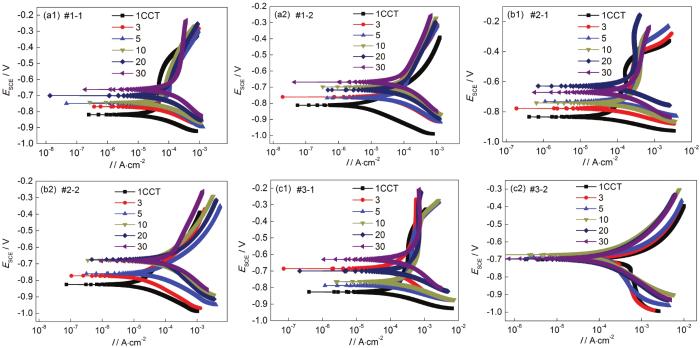
圖4 大氣環境中帶銹電極的極化曲線結果
Icorr與極化電阻Rp之間的關系可以用Stern公式[31]表示:

式中B為常數,其值取決于陰、陽極反應過程的動力學常數的大小。當腐蝕過程是受電極/溶液界面的電荷轉移控制時,腐蝕的陽極溶解過程與陰極還原過程遵循Tafel關系式:

式中,βa和βc分別為陽極和陰極反應的Tafel斜率,其中陰極Tafel斜率βc為負數。然而,當腐蝕過程由陰極還原的擴散過程控制時,βc為負無窮 (-∞),B可以表示為:

此外,βa值的范圍為13~52 mV,βc值通常小于-52 mV。如果βa為52 mV,βc為-52 mV,得到B為26 mV。如果βa為13 mV,βc為-52 mV,得到B為10 mV。此外,當βc為負無窮 (-∞) 時,得到B為52 mV。所以,B值的范圍為10~52 mV。目前的研究表明,帶銹電極的陰極過程不僅包含溶解氧的還原還有腐蝕產物的還原,因而在本文中B值假設為17 mV[5]。
圖5為對圖4進行線性擬合得到的Icorr隨干/濕交替周次變化的曲線。當模擬環境中SO2濃度為0.01 mol/L時,如圖5a所示,帶銹電極腐蝕電流密度的變化規律為:在僅含SO2的大氣環境中電極的腐蝕電流密度先增大,后緩慢下降,之后略有升高;在O3/SO2復合大氣環境電極的腐蝕電流密度先增大,后緩慢下降;通過對比兩條曲線發現,在O3/SO2復合大氣環境電極的腐蝕電流密度總體低于僅含SO2的大氣環境中電極的腐蝕電流密度。當模擬環境中SO2濃度為0.05 mol/L時,如圖5b所示,帶銹電極腐蝕電流密度的變化規律為:在僅含SO2的大氣環境中電極的腐蝕電流密度先增大,后下降;在O3/SO2復合大氣環境電極的腐蝕電流密度呈逐漸增大的趨勢;通過對比兩條曲線發現,在O3/SO2復合大氣環境電極的腐蝕電流密度低于僅含SO2的大氣環境中電極的腐蝕電流密度。當模擬環境中SO2濃度為0.10 mol/L時,如圖5c所示,帶銹電極腐蝕電流密度的變化規律為:在僅含SO2的大氣環境中電極的腐蝕電流密度先增大,后下降;在O3/SO2復合大氣環境電極的腐蝕電流密度呈先減小之后基本穩定的趨勢;通過對比兩條曲線發現,在O3/SO2復合大氣環境電極的腐蝕電流密度在腐蝕初期高于僅含SO2的大氣環境中電極的腐蝕電流密度,之后又低于僅含SO2的大氣環境中電極的腐蝕電流密度。以上表明腐蝕電流密度曲線與腐蝕動力學規律基本一致,在這3種不同濃度的SO2的大氣環境中,O3和SO2的交互作用會起到抑制低碳鋼腐蝕的作用。

圖5 Q235B鋼樣品在模擬大氣中經過不同干/濕交替周次腐蝕后的帶銹電極極化電阻曲線
圖6為經干/濕循環腐蝕作用后Q235B鋼帶銹電極在各自模擬溶液中EIS的Bode圖。在整個腐蝕過程中頻率-相角圖均呈現2個峰和1個谷。其中,高頻峰是由飽和甘汞電極與測試用電解質溶液間產生的高頻相移造成的,低頻峰主要與銹層的狀態和性質相關[32,33]。圖6顯示,在不同模擬大氣環境中,低頻區 (0.01 Hz) 和高頻區 (104 Hz) 的阻抗模值均隨干/濕交替次數的增加基本呈不斷波動的趨勢,表明隨著腐蝕時間的延長,銹層與鋼基體間的界面結構處于不穩定狀態。
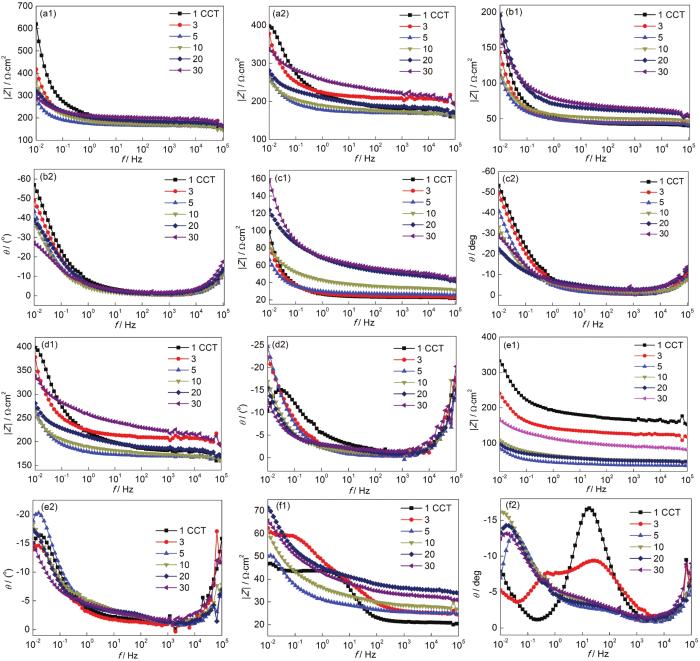
圖6 Q235B 鋼帶銹電極在大氣模擬液中的Bode圖
圖7所示為擬合圖6中各個EIS用的等效電路,其中,Rs,Rr,Rct分別代表溶液電阻,銹層電阻和電荷轉移電阻;常相位角元件Qp,Qr和Qdl分別代表高頻相移電容,銹層電容和雙電層電容;ZW為擴散阻抗,ZW的值依賴于角頻率ω:
圖7 擬合模擬大氣中帶銹電極的電化學阻抗譜的等效電路

其中,Yw是常數,j是虛數單位。Yw值越大,表明介質的擴散阻力越小。對于帶銹電極而言,Yw值越大,銹層對擴散傳質的阻擋能力越弱,表明銹層的致密性越差。
圖8a1~c3分別為擬合EIS圖譜得到的Rr,Rct以及Yw隨干/濕交替周次變化的曲線,擬合過程中的統計方差均小于10-4。圖8a1和b1顯示,當模擬環境中SO2濃度為0.01和0.05 mol/L時,在這4種模擬環境中Rr值均隨干/濕交替周次的增加而不斷波動,這表明隨著時間的延長銹層生成/開裂交替進行。圖8c1顯示,當模擬環境中SO2濃度為0.10 mol/L時,在這2種模擬環境中Rr值均隨干/濕交替周次的增加而增大,這表明隨著時間的延長銹層在不斷增厚。圖8a2表明,當模擬環境中SO2濃度分別為0.01 mol/L時,在僅含SO2的大氣和O3/SO2復合大氣環境中Rct值均隨干/濕交替周次的增加而呈逐漸減小后基本穩定的趨勢,表明電荷轉移過程在初期更容易,之后達到穩定狀態。圖8b2表明,當模擬環境中SO2濃度分別為0.05 mol/L時,在僅含SO2的大氣環境中Rct值隨干/濕交替周次的增加而呈先增大后減小的趨勢;在O3/SO2復合大氣環境中Rct值隨干/濕交替周次的增加而呈逐漸減小后增大的趨勢。圖8c2表明,當模擬環境中SO2濃度為0.10 mol/L時,在僅含SO2的大氣和O3/SO2復合大氣環境中Rct值隨干/濕交替周次的增加而呈逐漸增大的趨勢,表明電荷轉移過程變得越來越困難。從圖8a2,b2和c2還可以看出,在整個腐蝕過程中在O3/SO2復合大氣環境中Rct值基本均比在僅含SO2的大氣環境中大。此外,對比圖8a2,b2和c2可以看出,在O3/SO2復合大氣環境中,隨著模擬環境SO2含量的升高Rct值逐漸減小。因為腐蝕速率與Rct成反比[31],Rct越大則表明其腐蝕速率越小,因而圖8a2,b2和c2中Rct值隨SO2濃度變化規律與圖2所示的腐蝕速率曲線結果基本一致。圖8a2,b2和c2表明,當模擬環境中SO2濃度分別為0.01,0.05以及0.10 mol/L時,在僅含SO2的大氣和O3/SO2復合大氣環境中Yw值均隨干/濕交替周次的增加而呈先增大后減小的趨勢,表明在這些模擬環境中,隨著腐蝕產物的不斷生成,腐蝕產物在腐蝕初期促進鋼基體的腐蝕,后期銹層對粒子擴散的阻力持續增加,即銹層致密性增強。從圖8a3,b3和c3還可以看出,帶銹電極在O3/SO2復合大氣環境中的Yw值比在僅含SO2的大氣環境中小。這說明,O3和SO2的交互作用會增加鋼鐵銹層的致密性。
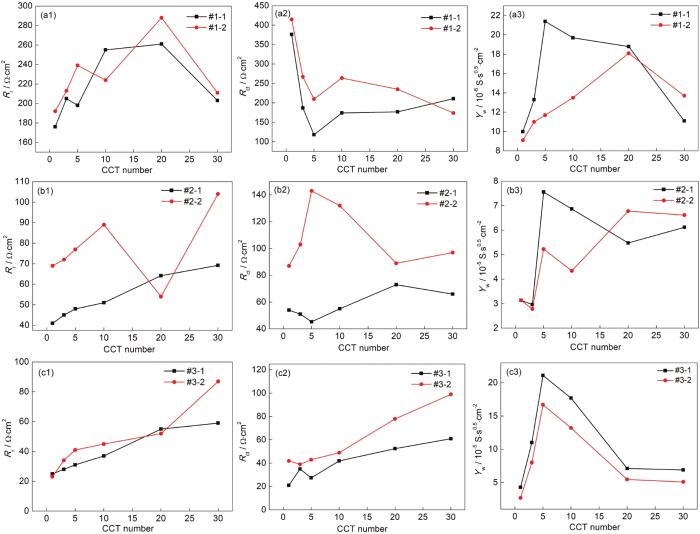
圖8 Q235B鋼帶銹電極大氣模擬液中EIS擬合結果
圖9a為Q235B鋼在模擬大氣中經過不同腐蝕周次腐蝕后表面的3D激光顯微鏡照片。從圖9可以看出,經過2 CCT后,所有樣品均表現為腐蝕產物在中心位置的粗糙度高于四周的粗糙度,這是因為樣品表面薄液膜在腐蝕初期為“半凸透鏡”狀,樣品中心處O2濃度較低,而四周O2濃度較高,這樣樣品中心處與四周之間會形成氧濃差電池,樣品中心處作為陽極快速溶解,造成此處腐蝕產物隨著腐蝕時間的延長不斷積累使得表面粗糙度增加。圖9b和c可以看出,經過一段時間腐蝕后,表面腐蝕產物在四周位置也不斷生成,此時整個樣品表面覆蓋了一層厚厚的銹層,這也與薄液膜的形狀受表面腐蝕產物的影響有關。

圖9 Q235B鋼在模擬大氣中經過2 CCT,10 CCT和30 CCT腐蝕后表面的3D激光顯微鏡照片
此外,對比圖9可見,對于同一種模擬環境中的樣品,其同一位置的表面粗糙度會隨腐蝕時間呈不斷變化的趨勢,這與樣品在腐蝕過程中銹層不斷發生“開裂-剝落-修復”的這個交替過程有關。
為了進一步分析表面粗糙度對低碳鋼大氣腐蝕速率的影響,通過3D激光顯微鏡測量得到了Q235B鋼樣品在模擬大氣中經過不同時間腐蝕后的平均表面粗糙度,如圖10所示。圖10a顯示,當模擬環境中SO2濃度為0.01 mol/L時,在僅含SO2的大氣環境中,帶銹電極的表面粗糙度從2 CCT至10 CCT增大,10 CCT至30 CCT基本保持不變;在O3/SO2復合大氣環境中,帶銹電極的表面粗糙度從2 CCT至30 CCT逐漸增大;對比兩組直方圖可以看出,在2 CCT時,在O3/SO2復合大氣環境中帶銹電極的表面粗糙度比在僅含SO2的大氣環境中的大;在10 CCT時,在O3/SO2復合大氣環境中帶銹電極的表面粗糙度比在僅含SO2的大氣環境中的小;在30 CCT時,在O3/SO2復合大氣環境中帶銹電極的表面粗糙度與在僅含SO2的大氣環境中的相近。圖10b顯示,當模擬環境中SO2濃度為0.05 mol/L時,在僅含SO2的大氣環境中,帶銹電極的表面粗糙度從2 CCT至30 CCT逐漸增大;在O3/SO2復合大氣環境中,帶銹電極的表面粗糙度從2 CCT至30 CCT先增大后基本維持不變;對比兩組直方圖可以看出,在2 CCT時,在O3/SO2復合大氣環境中帶銹電極的表面粗糙度與在僅含SO2的大氣環境中的相近;在10 CCT時,在O3/SO2復合大氣環境中帶銹電極的表面粗糙度比在僅含SO2的大氣環境中的小;在30 CCT時,在O3/SO2復合大氣環境中帶銹電極的表面粗糙度遠小于在僅含SO2的大氣環境中的粗糙度。圖10c顯示,當模擬環境中SO2濃度為0.10 mol/L時,在僅含SO2的大氣環境和在O3/SO2復合大氣環境中,帶銹電極的表面粗糙度從2 CCT至30 CCT均先增大后基本維持不變;對比兩組直方圖可以看出,在2 CCT時,在O3/SO2復合大氣環境中帶銹電極的表面粗糙度與在僅含SO2的大氣環境中的相近;在10 CCT和30 CCT時,在O3/SO2復合大氣環境中帶銹電極的表面粗糙度均遠小于僅含SO2的大氣環境中的粗糙度。以上結果說明,帶銹電極表面腐蝕產物的粗糙度隨腐蝕時間和外界環境中腐蝕介質的不同而發生變化,而一般表面粗糙度越大越會促進金屬的腐蝕。因而,在相同SO2濃度的模擬大氣環境中,O3/SO2復合大氣環境中帶銹電極的表面狀態相對于僅含SO2的大氣環境中更有利于抑制金屬的腐蝕,而且隨著模擬環境中SO2濃度的升高這種抑制作用越明顯,這與腐蝕速率曲線基本一致。
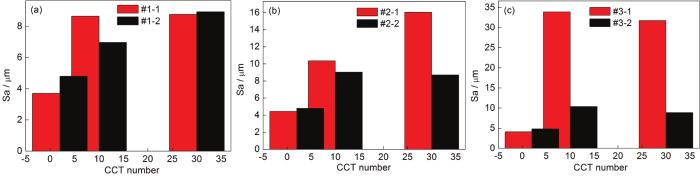
圖10 Q235B鋼在模擬大氣中經過不同時間腐蝕后的表面粗糙度
3 分析討論
前人研究結果表明[23-27],O3具有強的氧化性,在海岸大氣環境中Cl-和O3交互作用可以促進鋼鐵的腐蝕,此外,O3和SO2的交互作用會促進銅的大氣腐蝕,據此推測在工業大氣環境中O3和SO2交互作用也可以促進鋼鐵的腐蝕。但通過30次干/濕交替模擬大氣腐蝕實驗,可見,與僅含有SO2的模擬環境對比,O3和SO2的交互作用的大氣環境反而會抑制低碳鋼的大氣腐蝕。這與我們之前的預測結果不同。根據實驗數據結果及已有的研究成果分析如下:
(1) 在腐蝕初期,陰極過程主要為O2的還原反應,腐蝕速率與O2的極限擴散電流密度成正比。在含有O3的模擬電解質溶液中溶解了大量的O3,而O3很容易分解為O2和單個原子氧:

從式 (7) 可以看出,O3在分解過程中一方面會讓溶于電解質溶液中的O2含量增加,提高了O2的極限擴散電流密度,從而使得低碳鋼的腐蝕速率增加;另一方面,單個原子氧具有更強的氧化性,促進還原性腐蝕產物 (如Fe3O4) 的氧化過程進行,從而有利于腐蝕產物中穩定性較強的α-FeOOH生成,從而形成保護性的銹層。
(2) 金屬表面的粗糙度值的大小與金屬腐蝕的程度呈正相關。通過3D激光顯微鏡的測量結果可以看出,O3和SO2的交互作用會降低銹層表面粗糙度,也就是促進腐蝕產物顆粒細化,這會有利于在鋼基體表面形成一層致密的保護膜,阻止腐蝕性氣體或液體通過表面的微觀凹谷滲入到鋼基體內層,從而延緩了鋼鐵腐蝕。
(3) 實驗室加速實驗模擬環境中所用的O3的濃度比一般大氣環境中O3的濃度高,而不同的O3濃度可能產生不同的實驗結果。因此,在接下來的研究中將考慮O3濃度對SO2大氣環境中鋼鐵腐蝕行為的影響,探究在較低的O3濃度下,O3和SO2的交互作用將如何影響低碳鋼的腐蝕。
4 結論
(1) O3和SO2的交互作用對Q235B鋼的腐蝕有明顯的抑制作用。
(2) 腐蝕演化特性方面,當模擬環境中Na2SO3濃度為0.01 mol/L時,O3/SO2復合大氣環境中Q235B鋼的腐蝕速率呈先迅速增大而后緩慢減小的趨勢; 當模擬環境中Na2SO3濃度為0.05 mol/L時,O3/SO2復合大氣環境中Q235B鋼的腐蝕速率呈先緩慢增大后迅速下降的趨勢;當模擬環境中Na2SO3濃度為0.10 mol/L時,O3/SO2復合大氣環境中Q235B鋼的腐蝕速率呈先增大而后緩慢減小的趨勢。
(3) 與僅含有SO2的大氣環境相比,當模擬大氣中SO2含量較低時,O3和SO2的交互作用會促進具有保護性腐蝕產物中α-FeOOH生成;而當大氣中SO2含量較高時,O3對腐蝕產物相組成影響不明顯。
參考文獻
1 Corvo F, Betancourt N, Mendoza A. The influence of airborne salinity on the atmospheric corrosion of steel [J]. Corros. Sci., 1995, 37: 1889
2 Dong J H, Han E-H, Ke W. Introduction to atmospheric corrosion research in China [J]. Sci. Technol. Adv. Mater., 2007, 8: 559
3 Persson D, Thierry D, Karlsson O. Corrosion and corrosion products of hot dipped galvanized steel during long term atmospheric exposure at different sites world-wide [J]. Corros. Sci., 2017, 126: 152
4 Chen W J, Hao L, Dong J H, et al. Effect of SO2 on corrosion evolution of Q235B steel in simulated coastal-industrial atmosphere [J]. Acta Metall. Sin., 2014, 50: 802
4 陳文娟, 郝龍, 董俊華等. 模擬工業-海岸大氣中SO2對Q235B鋼腐蝕行為的影響 [J]. 金屬學報, 2014, 50: 802
5 Chen W J, Hao L, Dong J H, et al. Effect of sulphur dioxide on the corrosion of a low alloy steel in simulated coastal industrial atmosphere [J]. Corros. Sci., 2014, 83: 155
6 Henriksen J F. The distribution of NaCl on Fe during atmospheric corrosion [J]. Corros. Sci., 1969, 9: 573
7 Graedel T E, Frankenthal R P. Corrosion mechanisms for iron and low alloy steels exposed to the atmosphere [J]. J. Electrochem. Soc., 1990, 137: 2385
8 Songdao Y, translated by Jin Y K. Development and Research of Low Alloy Corrosion Resistant Steel [M]. Beijing: Metallurgical Industry Press, 2004: 235
8 松島巖著, 靳裕康譯. 低合金耐蝕鋼—開發、發展及研究 [M]. 北京: 冶金工業出版社, 2004: 235
9 Ishikawa T, Miyamoto S, Kandori K, et al. Influence of anions on the formation of β-FeOOH rusts [J]. Corros. Sci., 2005, 47: 2510
10 Evans U R, Taylor C A J. Mechanism of atmospheric rusting [J]. Corros. Sci., 1972, 12: 227
11 Evans U R. Electrochemical mechanism of atmospheric rusting [J]. Nature, 1965, 206: 980
12 Leygraf C, Graedel T E. Atmospheric Corrosion [M]. New York: Wiley-Interscience, 2000
13 Allam I M, Arlow J S, Saricimen H. Initial stages of atmospheric corrosion of steel in the Arabian Gulf [J]. Corros. Sci., 1991, 32: 417
14 Asami K, Kikuchi M. In-depth distribution of rusts on a plain carbon steel and weathering steels exposed to coastal-industrial atmosphere for 17 years [J]. Corros. Sci., 2003, 45: 2671
15 Wang S T, Yang S W, Gao K W, et al. Corrosion behavior and corrosion products of a low-alloy weathering steel in Qingdao and Wanning [J]. Int. J. Min. Met. Mater., 2009, 16: 58
16 Guo M X, Pan C, Wang Z Y, et al. A study on the initial corrosion behavior of carbon steel exposed to a simulated coastal-industrial atmosphere [J]. Acta. Metall. Sin., 2018, 54: 65
16 郭明曉, 潘晨, 王振堯等. 碳鋼在模擬海洋工業大氣環境中初期腐蝕行為研究 [J]. 金屬學報, 2018, 54: 65
17 Ge S J, Wang S J, Xu Q, et al. Ozone impact minimization through coordinated scheduling of turnaround operations from multiple olefin plants in an ozone nonattainment area [J]. Atmos. Environ., 2018, 176: 47
18 Wei W, Lv Z F, Li Y, et al. A WRF-Chem model study of the impact of VOCs emission of a huge petro-chemical industrial zone on the summertime ozone in Beijing, China [J]. Atmos. Environ., 2018, 175: 44
19 Carro-Calvo L, Ordó?ez C, García-Herrera R, et al. Spatial clustering and meteorological drivers of summer ozone in Europe [J]. Atmos. Environ., 2017, 167: 496
20 Pendlebury D, Gravel S, Moran M D, et al. Impact of chemical lateral boundary conditions in a regional air quality forecast model on surface ozone predictions during stratospheric intrusions [J]. Atmos. Environ., 2018, 174: 148
21 Jing P, Lu Z F, Steiner A L. The ozone-climate penalty in the Midwestern U.S. [J]. Atmos. Environ., 2017, 170: 130
22 Wiesinger R, Martina I, Kleber C, et al. Influence of relative humidity and ozone on atmospheric silver corrosion [J]. Corros. Sci., 2013, 77: 69
23 Screpanti A, De Marco A. Corrosion on cultural heritage buildings in Italy: a role for ozone? [J]. Environ. Pollut., 2009, 157: 1513
24 Oesch S, Faller M. Environmental effects on materials: The effect of the air pollutants SO2, NO2, NO and O3 on the corrosion of Copper, Zinc and Aluminium. A short literature survey and results of laboratory exposures [J]. Corros. Sci., 1997, 39(9): 1505
25 Chen W J, Chen Y Q, Pan G. Corrosion evolution characteristics of Q235B steel in an O3/Cl- containing atmosphere [J]. Corros. Sci. Prot. Technol., 2019, 31: 8
25 陳文娟, 陳翌慶, 潘剛. O3/Cl-復合大氣環境中Q235B鋼的腐蝕演化特性 [J]. 腐蝕科學與防護技術, 2019, 31: 8
26 Aastrup T, Wadsak M, Leygraf C, et al. In situ studies of the initial atmospheric corrosion of copper influence of humidity, sulfur dioxide, ozone, and nitrogen dioxide [J]. J. Electrochem. Soc., 2000, 147: 2543
27 Chen W J, Hao L, Dong J H, et al. Effect of pH value on the corrosion evolution of Q235B steel in simulated coastal-industrial atmospheres [J]. Acta Metall. Sin., 2015, 51: 191
27 陳文娟, 郝龍, 董俊華等. 模擬工業-海岸大氣中pH值對Q235B鋼腐蝕行為的影響 [J]. 金屬學報, 2015, 51: 191
28 Kawasaki Y, Tomoda Y, Ohtsu M. AE monitoring of corrosion process in cyclic wet-dry test [J]. Constr. Build. Mater., 2010, 24: 2353
29 Thee C, Hao L, Dong J H, et al. Atmospheric corrosion monitoring of a weathering steel under an electrolyte film in cyclic wet-dry condition [J]. Corros. Sci., 2014, 78: 130
30 Stern M, Geary A L. Electrochemical polarization. I. A theoretical analysis of the shape of polarization curves [J]. J. Electrochem. Soc., 1957, 104: 56
31 Mansfeld F. 1988 Whitney Award Lecture: Don't be afraid of electrochemical techniques-but use them with care! [J]. Corrosion, 1988, 44: 856
32 Mansfeld F, Lin S, Chen Y C, et al. Minimization of high-frequency phase shifts in impedance measurements [J]. J. Electrochem. Soc., 1988, 135: 906
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《中國腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護網官方QQ群:140808414





