B30銅鎳合金作為銅合金的一種,憑借良好的力學性能,抗海水腐蝕,抗沖刷腐蝕,優異的耐海洋生物污損等優點[1,2],20世紀30年代起被廣泛用于艦船中船用冷凝器的制造[3-5]。
雖然B30銅鎳合金應用于船用冷凝器的制造時間已久,但是在實際運行中仍然存在著嚴重的腐蝕問題,其中以孔蝕尤為突出,在使用中造成了巨大的危害[6-10],本文針對船用冷凝器出現的孔蝕問題進行研究。船用冷凝器投入應用前,需要在一定流速的海水中進行預處理,使其表面形成致密的保護膜,從而提高材料耐蝕性[11-15]。在進行預處理時,海水環境中影響B30銅鎳合金成膜的因素有很多[16],最為重要的為海水的溶解氧濃度及流速。在不同的海域,海水鹽度和溫度的不同會影響海水的溶解氧濃度,同時海水的流速也會影響成膜過程中船用冷凝器周圍海水中溶解氧濃度的變化[17-22]。成膜環境中海水流速的變化除了影響溶解氧濃度外,還會影響試樣的表面狀態。
本文以B30銅鎳合金作為研究對象,通過改變海水中的溶解氧濃度以及海水的流速,研究B30銅鎳合金的成膜機理及其在海水中的電化學特性,分析這兩種因素對于成膜的影響,得到B30銅鎳合金成膜的最佳條件,對實際工況中成膜工藝進行指導,幫助解決船用冷凝器存在的孔蝕問題。
1 實驗方法
本文研究對象為B30銅鎳合金,其化學成分為 (質量分數,%):C 0.05,Si 0.15,Mn 1.2,P 0.006,S 0.01,Pb 0.05,Fe 0.9,Ni+Co 29-33,Cu為余量。電化學測試的試樣尺寸為10 mm×10 mm×3 mm,保留1 cm2工作面,其余面用環氧樹脂密封。表面觀察試樣尺寸50 mm×10 mm×3 mm。試樣表面依次用800#、1000#、2000#砂紙打磨,打磨后的試樣依次用蒸餾水和無水乙醇清洗,吹干備用。
實驗介質為青島沙子口海域天然海水。海水的pH值為7.8,實驗在室溫下進行。實驗中分別通過通氮氣、不通氣和通氧氣的方式來控制海水的溶解氧濃度,采用YSI200溶解氧測量儀測試溶解氧濃度分別為:(3.5±0.1)、(8.0±0.1) 和 (14.0±0.1) mg/kg;通過調節磁力攪拌器的轉速來控制海水流經試樣表面的線速度,分別為:0,0.8和2.0 m/s。
電化學測試Gamry reference 600+電化學工作站上進行,采用三電極體系,工作電極為在不同海水體系中預處理后的B30銅鎳合金,參比電極為飽和甘汞電極 (SCE),輔助電極為混合金屬氧化物電極 (MMO),電化學阻抗 (EIS) 在開路電位下進行,施加幅值為10 mV的正弦波電位,掃描頻率范圍為105~10-2 Hz,對數掃頻,每倍頻程10個點。采用Gmini300的掃描電子顯微鏡 (SEM) 對材料表面保護膜進行形貌觀察;采用ESCALAB 250Xi的X射線光電子能譜 (XPS) 對保護膜成分進行分析。
2 結果與討論
2.1 海水中的溶解氧濃度對成膜的影響
開路電位在一定程度能夠反映試樣的腐蝕傾向。圖1為B30銅鎳合金在不同溶解氧濃度海水中的開路電位。
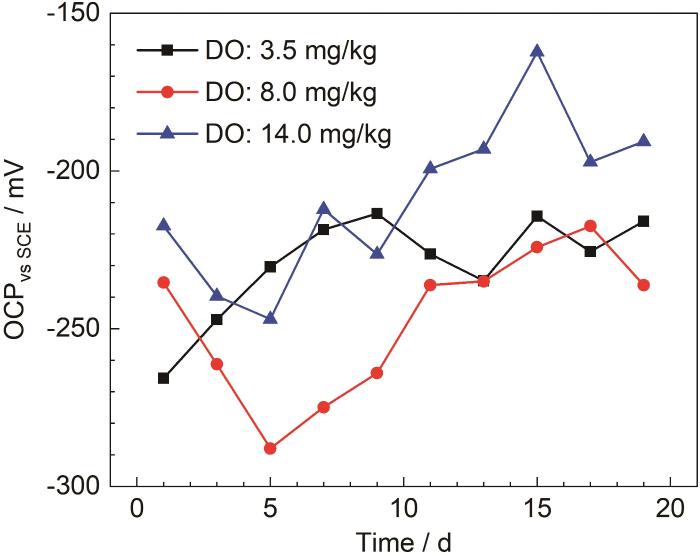
圖1 B30銅鎳合金在不同溶解氧濃度海水中的開路電位
由1 d的開路電位可以看出,海水中的溶解氧濃度越高,開路電位越正,腐蝕傾向越小,說明隨著溶解氧濃度的提高,試樣表面初期成膜越快。在DO為3.5 mg/kg的海水中,初期開路電位正移,腐蝕傾向減小,保護膜初步形成,9 d開始上下波動,膜層進入形成與溶解的波動狀態。在DO為3.5和8.0 mg/kg的海水中,11 d前開路電位處于波動狀態,膜層處于波動溶解階段,11 d后開路電位趨于穩定,此時腐蝕傾向最小,表面形成保護膜,陽極溶解減緩[23]。11~19 d在DO為14.0 mg/kg的海水中開路電位相較其他兩種海水更正,腐蝕傾向更小。
電化學阻抗譜 (EIS) 能夠表征B30銅鎳合金表面膜層的狀態。圖2為B30銅鎳合金在不同溶解氧濃度海水中的EIS圖。
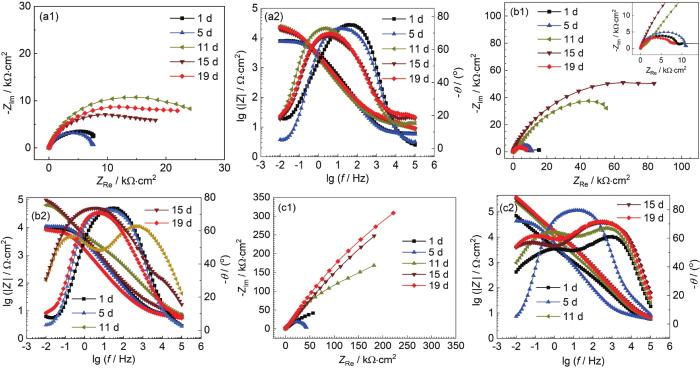
圖2 B30銅鎳合金在不同溶解氧濃度海水中的EIS圖
由Nyquist圖可見,在3種溶解氧濃度的海水中,容抗弧半徑均波動增大。容抗弧半徑的增大是由于試樣表面形成了具有保護性的膜層,膜電阻增大,膜層增厚會阻礙陽極溶解過程,導致電荷轉移電阻增大。對比3種溶解氧濃度海水的Nyquist圖可以看出,隨著溶解氧濃度的增大,容抗弧半徑增大。在DO為3.5和8.0 mg/kg的低溶解氧濃度的海水中,形成的膜層較慢且不穩定,膜層仍然處于波動溶解狀態,膜層溶解導致膜電阻減小,同時膜層的破裂導致電荷轉移電阻減小,所以15~19 d,容抗弧仍有減小的趨勢。
由Bode圖可以看出,隨著溶解氧濃度的提高,模值呈現增大的趨勢,試樣表面形成的膜層阻抗值增大。在DO為3.5 mg/kg的海水中,隨著浸泡時間的延長,相位角向低頻區移動,試樣表面膜層致密性較差。在DO為8.0 mg/kg的海水中,11 d相位角圖呈現明顯的兩個相位角峰,試樣表面形成了兩層膜;11~19 d高頻區的相位角峰值逐漸減小,試樣表面膜層穩定性變差,膜層進入波動溶解狀態。在DO為14.0 mg/kg的海水中,在1 d時就形成了兩個相位角峰,保護膜形成較快;5~11 d后,相位角峰轉變為一個,試樣表面膜層進入波動溶解階段;11~19 d再次出現兩個相位角峰且隨時間增長峰值略有增大,但并不明顯,此時試樣表面膜層仍在形成,但已基本形成了致密穩定的膜層。
圖3為B30銅鎳合金在海水中電化學阻抗擬合的等效電路圖。Rs是溶液電阻,Rct是電極反應的電荷轉移電阻,Rct值可以反映試樣表面發生反應的難易程度;Rf為膜電阻;CPEf由膜電容Cf和彌散指數nf組成,CPEdl由雙電層電容Cdl和彌散指數ndl組成,由nf的值可以得出試樣表面保護膜的完整性,當nf趨近于1時,保護膜趨于完整。
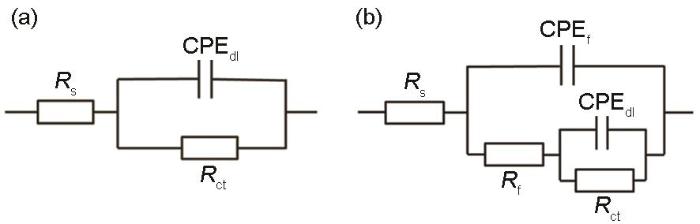
圖3 B30銅鎳合金在海水中電化學阻抗擬合等效電路圖
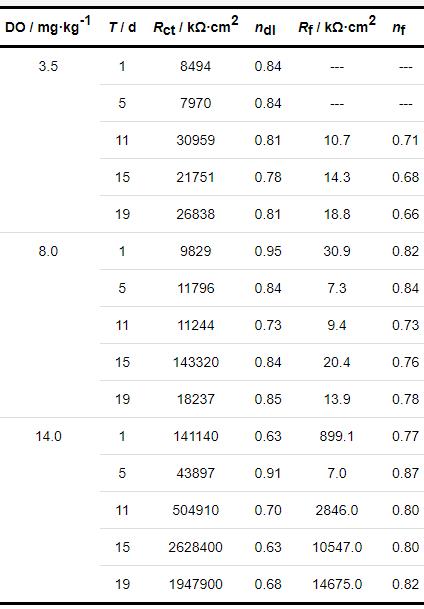
將B30銅鎳合金在不同溶解氧濃度海水中EIS用圖3a和3b所示等效電路擬合,擬合數據呈現于表1。由Rf值可見,在DO為8.0和14.0 mg/kg的海水中,1 d時試樣表面開始成膜,在DO為3.5 mg/kg的海水中,浸泡5 d后還未成膜。整體來看在DO為14.0 mg/kg的海水中,Rf明顯大于DO為3.5和8.0 mg/kg的海水,膜層質量更高。溶解氧濃度增高,使得OH-濃度的增加,影響了試樣的陽極溶解過程,從而成膜更快且保護性更強。由nf值可以看出,除在DO為14.0 mg/kg海水中浸泡1 d數據外,相同天數不同溶解氧濃度海水中的nf值為:14.0 mg/kg>8.0 mg/kg>3.5 mg/kg,隨著溶解氧濃度的提高,試樣表面膜層越發完整。由Rct值可以看出,DO為14.0 mg/kg海水中的Rct明顯高于DO為3.5和8.0 mg/kg的海水中的Rct,這是由于試樣表面膜層的逐漸形成影響了試樣的陽極溶解過程,從而使Rct增大,這點與Rf、nf的擬合數據相吻合。
表1 B30銅鎳合金不同溶解氧濃度的海水中電化學阻抗擬合數據
XPS能夠表征試樣表面膜層的成分,判斷膜層是否具有保護性。表2為B30銅鎳合金在不同溶解氧濃度海水中的XPS圖擬合結果。由Cu譜的擬合數據可以看出,隨著溶解氧濃度的提高,表面膜層中Cu2O和CuCl所占的比例顯著提高,CuO和CuCl2的含量則呈現降低的趨勢。
表2 B30銅鎳合金在不同溶解氧濃度海水中的XPS圖擬合結果
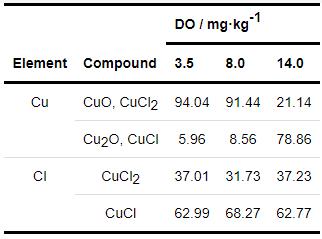
B30銅鎳合金在海水環境中成膜,其反應過程已經有了一定的研究[22,23],試樣表面會先形成CuCl鹽膜 (反應2),CuCl可與Cl-進一步螯合生成可溶性的CuCl2- (反應3),溶解的CuCl2-繼續發生沉積反應,形成Cu2O膜 (反應4)。Cu2O是一種半導體,合金元素Ni可以通過占據Cu2O中的陽離子空穴或替代銅離子摻雜到有缺陷的Cu2O點陣中去,提高膜的耐蝕性[24-27],增強了膜層與基體的結合能力[20]。隨著浸泡時間的增加,Cu2O會進一步發生反應生成CuO、Cu2(OH)3Cl等保護性較差的腐蝕產物 (反應5、6)。結合表3數據,由此可以看出,隨著溶解氧濃度的提高,Cu2O和CuCl所占的比例提高,試樣表面膜層更具保護性。
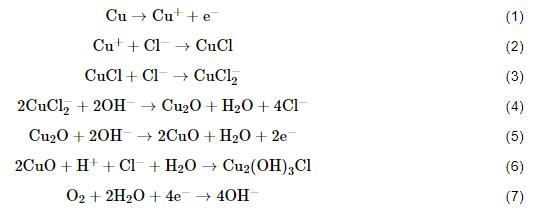
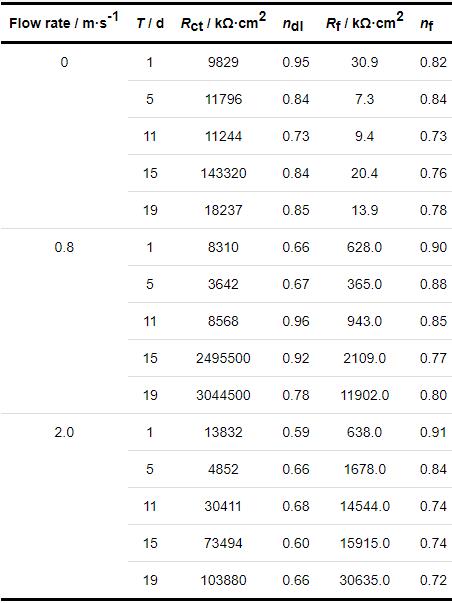
表3 B30銅鎳合金在不同流速海水中的電化學阻抗擬合數據
海水中溶解氧濃度的增大會加快成膜反應中陰極氧的去極化反應 (反應7),使得OH-濃度的增加,進而影響陽極反應過程 (反應5、6),使得CuO和Cu2O的含量可以持續提高,試樣表面膜層逐漸增厚。膜層的增厚會在一定程度上影響Cl-、OH-等離子的滲透,影響膜層的進一步形成,從而影響陽極反應的進行 (反應3、4、5),已經形成的CuCl鹽膜較難進一步生成CuO和Cu2O,從而導致在DO為8.0 mg/kg的海水中CuCl的含量有一定的提升。當溶解氧濃度提高到14.0 mg/kg時,陰極氧的去極化反應增強,從而使OH-濃度顯著增大。滲透進膜層內部的離子進一步增多,陽極過程得以繼續,膜層持續增厚,這也導致膜層中的CuCl可以持續發生轉化,因此CuCl所占的比例并沒有出現同DO為8.0 mg/kg的海水中一般有所提升的現象。在膜層內層Cu2O致密,不易發生脫落,但外層的CuO由于其疏松的性質,持續增厚后會出現脫落的現象,所以Cu2O所占比例明顯增多,使得膜層的保護效果增強。
圖4為B30銅鎳合金在不同溶解氧濃度海水中浸泡20 d的SEM圖。由圖可見,在DO為3.5和8.0 mg/kg的海水中,試樣表面覆蓋一層疏松多孔的膜層。在DO為14.0 mg/kg的海水中,試樣表面形成的膜層與其他兩種溶解氧濃度海水中的明顯不同,膜層更加致密,膜層更具保護性,這點與電化學阻抗的擬合數據相符。根據反應 (4) 和 (5) 可知,試樣表面形成的疏松多孔的物質主要為CuO和Cu2(OH)3Cl。而在DO為14.0 mg/kg的海水中,形成的較為致密的膜層主要為CuCl以及Cu2O,這一點與XPS分析結果相吻合。

圖4 B30銅鎳合金在不同溶解氧濃度海水中浸泡20 d的SEM圖
2.2 海水的流速對成膜的影響
海水的流速能夠改變試樣周圍的環境和表面的狀態,對于B30銅鎳合金的成膜具有重要影響,因此研究流速對于成膜的影響十分重要[28]。圖5為B30銅鎳合金在不同流速海水中的開路電位。由圖5可見,試樣在不同流速海水中的開路電位均先發生負移,腐蝕傾向逐漸增大。隨著試樣表面膜層的形成,阻礙了陽極溶解過程,開路電位開始正移,腐蝕傾向減小[29]。在流速為0.8和2.0 m/s的流動海水中,開路電位在1 d開始正移,而在0 m/s海水中,開路電位在5 d時才發生正移,說明在流動的海水中,試樣表面能夠較快的形成具有保護性的膜層。當流速為0.8 m/s時,開路電位一直處于一個較為穩定的狀態,腐蝕傾向變化不大,表面形成的膜層保護性強。流速為2.0 m/s的海水中,在3 d后出現開路電位負移的狀況,接著出現產生波動,并在9 d左右腐蝕傾向會超過0 m/s的海水,說明在流速2.0 m/s的海水中,試樣表面膜層的完整性和致密性受到影響。
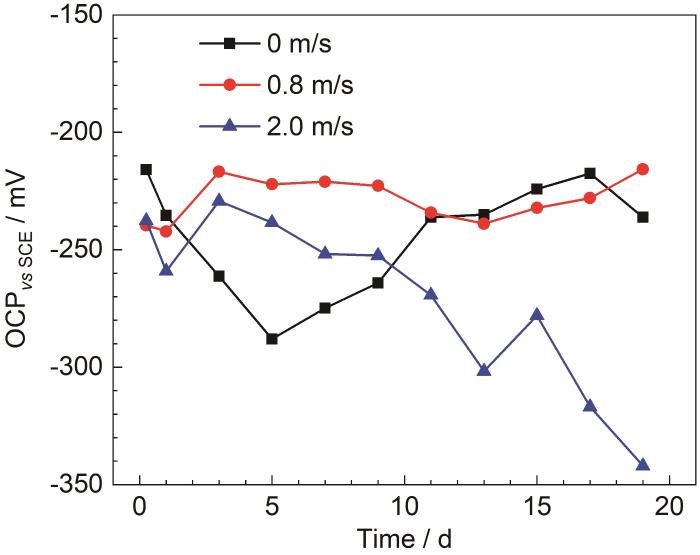
圖5 B30銅鎳合金在不同流速海水中的開路電位
圖6為B30銅鎳合金在不同流速海水中的EIS圖。由Nyquist圖可見,各流速海水中容抗弧均處于波動增長的狀態,15 d后流速為0.8 m/s的海水比0 m/s海水的容抗弧半徑更大,阻抗值變大,說明一定的流速有利于致密膜層的形成。流速為0.8 m/s的海水與2.0 m/s的海水中B30銅鎳合金的容抗弧半徑在11 d前數值相近,但11 d后0.8 m/s的海水中容抗弧半徑更大。在0.8 m/s的海水中,Nyquist圖在11 d時產生一個感抗弧,這是由于溶液中大量的Cl-、OH-等侵蝕性離子在電極表面大量聚集,由于這種現象,加速了內層致密膜層的形成,因此B30銅鎳合金在0.8 m/s的海水中形成了比在2.0 m/s的海水中更具保護性的膜層。上述數據證明海水的流速對B30銅鎳合金表面形成的保護有一定影響且有一個臨界值[30],一定的流速有利于致密膜層的形成,但流速過大時,卻不利于表面膜層的穩定。
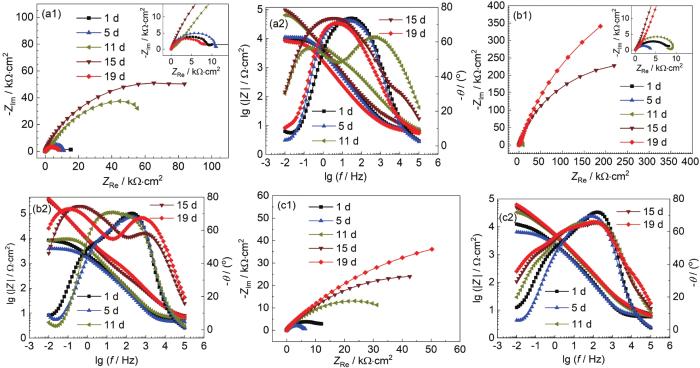
圖6 B30銅鎳合金在不同流速海水中的EIS圖
由Bode圖中低頻區的模值大小可知不同流速海水中表面膜阻抗值的大小:0.8 m/s>2.0 m/s>0 m/s。由相位角可見,在流速為0 m/s的海水中,11 d開始出現兩個相位角峰。11~19 d低頻區的相位角峰峰值增大,但高頻區的相位角峰峰值減小,說明在流速為0 m/s的海水中試樣表面形成的膜層致密性較差且不穩定。流速為0.8 m/s的海水相較流速為0 m/s的海水中,1 d時相位角峰位置向高頻區偏移,試樣表面開始形成致密的膜層。11~19 d出現兩個相位角峰,高頻區的相位角峰持續向高頻區移動,膜層的致密性提高,低頻區出現明顯的相位角峰,初期形成的致密膜層外部覆蓋疏松的物質,形成兩層膜[31-33]。流速為2.0 m/s的海水中,相位角峰同樣在1 d時向高頻區移動,這說明高致密性的保護膜已經形成,隨時間延長,高頻區的相位角峰未向高頻區移動,但相位角峰值上下波動,膜層的完整性受到影響,低頻區出現微弱的相位角峰且不穩定,試樣表面覆蓋的疏松性的物質無法在該流速下穩定存在[34]。
采用圖3b所示等效電路對B30銅鎳合金在不同流速海水中的EIS進行擬合,擬合結果呈現于表3。由Rf值可見,在流速為0.8和2.0 m/s的海水中,Rf值明顯大于在0 m/s的海水,且有著數量級上的差異。這是由于流動的海水中,能為試樣表面源源不斷的提供溶解氧,成膜過程中形成Cu2O的步驟 (反應5) 能夠不斷進行,使得膜層不斷完善。在2.0 m/s的海水中,B30銅鎳合金的Rf值略大于0.8 m/s的海水中的Rf,這是說明隨著流速的增大,試樣表面膜層的致密性或者完整性有所提升。由nf值擬合數據可知,在0.8 m/s的海水中,試樣表面膜層的完整性最好,這也就證明了流速為2.0 m/s的海水中,Rf值略大于0.8 m/s的海水的原因是由于膜層的致密性有一定的提高。由Rct值可知,在流動的海水中,Rct值后期能夠保持穩定,但在流速為0 m/s的海水體系中,Rct值在15 d后急劇下降。這是由于在成膜的過程中,試樣周圍溶解氧消耗,從而導致生成Cu2O過程緩慢[35],且疏松的CuCl鹽膜堆積,直至發生脫落,對陽極溶解的阻礙作用降低,從而導致Rct值減小。15~19 d,在0.8 m/s的海水中的Rct值與其他兩種流速海水中相差較大,這說明在該流速下試樣表面形成的膜層較其他兩種流速更好。
結合表1和表3數據分析流速與溶解氧之間的關系。對比試樣在流速為0.8 m/s的海水以及DO為14.0 mg/kg的海水中的成膜,可以看出試樣在這兩種情況下的電化學阻抗的擬合數據相似,Rct值相對其他情況都有著數量級的差異,由此可見,流動的海水主要是通過改變試樣周圍介質溶液的溶解氧濃度來影響成膜。由Rf值可知,流速為0.8 m/s的海水中試樣的成膜較DO為14.0 mg/kg的海水中的成膜慢,推測可能流速的增大還會對試樣表面的成膜產生其他影響。
表4為B30銅鎳合金在不同流速海水中的Cu譜和Cl譜擬合數據,由Cu譜的擬合數據可以看出B30銅鎳合金在流速為0.8和2.0 m/s的海水中Cu2O和CuCl所占的比例明顯高于0 m/s的海水中所占的比例,且流速為2.0 m/s的海水中Cu2O和CuCl所占的比例也比0.8 m/s所占的比例略高,因此流速為2.0 m/s的海水比流速為0.8 m/s的海水中形成的膜層更具保護性,這點與電化學阻抗擬合數據中的Rf值的變化相符。由Cl譜的擬合數據可以看出,在流動的海水中,CuCl的含量較低,這是由于流動的海水可以使試樣周圍一直保持較高的溶解氧濃度,從而一定程度加速了CuCl水解成為Cu2O的過程。
表4 B30銅鎳合金在不同流速海水中的XPS擬合結果
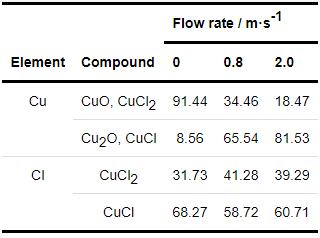
結合表2與表4數據分析流速和溶解氧之間關系。由表4可以看出在流動的海水中Cu2O和CuCl所占的比例與DO為14.0 mg/kg (表2) 海水中Cu2O和CuCl所占的比例類似,因此在流動的海水中試樣表面溶解氧濃度的改變是影響成膜的一個主要因素,此結果與電化學阻抗數據相符。在流速為2.0 m/s的海水中,試樣表面膜層中Cu2O和CuCl的含量高于流速為0.8 m/s的海水中,也高于在DO為14.0 mg/kg的海水,由此可見,流速的增加除了為試樣表面提供溶解氧外還會對形成的膜層的表面狀態產生影響。
圖7為B30銅鎳合金在不同流速海水中浸泡20 d的SEM圖。由圖可見,相較0 m/s的海水,0.8 m/s的海水中成膜更加致密完整。當流速達到2.0 m/s時,試樣的表面產生了沖刷作用,從而使表面膜層發生破裂,因此B30銅鎳合金在流速為2.0 m/s的海水中相比0.8 m/s成膜質量下降,這也與表3所示的不同流速海水下的電化學阻抗擬合數據中nf值的變化相符。流動的海水會對試樣表面產生沖刷作用,這也導致在DO為14.0 mg/kg的靜止海水中11 d左右就形成了較為致密的膜層,而在流速為0.8 m/s的海水中在15 d左右才形成了致密的膜層。
圖7 B30銅鎳合金在不同流速海水中浸泡20 d的SEM圖
流動的海水主要通過改變試樣周圍海水中的溶解氧濃度來促進其膜層的形成,但其產生的沖刷作用會破壞其膜層的完整性。由表3 B30銅鎳合金不同流速海水中的電化學阻抗的擬合數據可以看出,流速即使達到2.0 m/s,B30銅鎳合金表面形成的膜層的有效性仍然大于在0 m/s的海水中,這說明在流速低于2.0 m/s時,海水流動導致的溶解氧濃度提高對試樣成膜的正向作用仍然大于其沖刷腐蝕對于試樣表面膜層的破壞作用,由此可知試樣周圍介質溶液中的溶解氧濃度的改變是影響成膜的最主要的因素。
3 結論
(1) 海水的溶解氧濃度和流速對B30銅鎳合金的成膜影響明顯,隨著溶解氧濃度的提高,形成的膜層更加致密;隨著流速的提高,表面膜層的質量呈現先變好再變差的趨勢,在0.8 m/s的低流速海水中更易形成致密完整的膜層。
(2) 流速主要通過改變B30銅鎳合金周圍海水的溶解氧濃度以及海水流動產生的沖刷作用來影響材料表面致密完整膜層的形成;且在流速低于2.0 m/s的海水中,合金周圍海水中溶解氧濃度的改變在成膜過程中占據主導作用。
參考文獻
1 Shi Z Y, Liu B, Liu Y, et al. Progress of corrosion behavior and anti-corrosion technology for typical copper-nickel alloys under marine environment [J]. Equip. Environ. Eng., 2020, 17(8): 38
1 石澤耀, 劉斌, 劉巖 等. 典型銅鎳合金在海洋環境中腐蝕行為與防護技術研究進展 [J]. 裝備環境工程, 2020, 17(8): 38
2 Zhu X L, Lin L Y, Lei T Q. Process of formation of corrosion films on alloy 70Cu-30Ni in seawater [J]. Acta Metall. Sin., 1997, 33: 1256
2 朱小龍, 林樂耘, 雷廷權. 70Cu-30Ni合金海水腐蝕產物膜形成過程 [J]. 金屬學報, 1997, 33: 1256
3 Li Y X, Ives M B, Coley K S, et al. Corrosion of nickel-containing stainless steel in concentrated sulphuric acid [J]. Corros. Sci., 2004, 46: 1969
doi: 10.1016/j.corsci.2003.10.017
4 Glover T J. Copper-Nickel alloy for the construction of ship and boat hulls [J]. Br. Corros. J., 1982, 17: 155
doi: 10.1179/000705982798274228
5 Alfantazi A M, Ahmed T M, Tromans D. Corrosion behavior of copper alloys in chloride media [J]. Mater. Des., 2009, 30: 2425
doi: 10.1016/j.matdes.2008.10.015
6 Lin L Y, Liu S F, Zhu X L. Seawater-corrosion-induced intergranular precipitation in Cu-Ni alloy [J]. J. Chin. Soc. Corros. Prot., 1997, 17: 1
6 林樂耘, 劉少峰, 朱小龍. 海水腐蝕導致銅鎳合金的沿晶析出 [J]. 中國腐蝕與防護學報, 1997, 17: 1
7 Shen H, Gao F, Zhang G G, et al. Material selection and anti-corrosion measures of seawater piping in warship [J]. Ship Eng., 2002, 32(4): 43
7 沈宏, 高峰, 張關根 等. 艦船海水管系選材及防腐對策 [J]. 船舶工程, 2002, 32(4): 43
8 Ravindranath K, Tanoli N, Gopal H. Failure investigation of brass heat exchanger tube [J]. Eng. Fail. Anal., 2012, 26: 332
doi: 10.1016/j.engfailanal.2012.07.018
9 Yan Y M, Lin L Y, Zhu X L. Effect of residual stress on corrosion resistance of copper tube BFe30-1-1 in 3.5%NaCl [J]. J. Chin. Soc. Corros. Prot., 1994, 14: 59
9 嚴宇民, 林樂耘, 朱小龍. 殘余應力對BFe30-1-1銅管耐蝕性能的影響 [J]. 中國腐蝕與防護學報, 1994, 14: 59
10 Admiraal L, Ijsseling F P, Kolster B H, et al. Influence of temperature on corrosion product film formation on CuNi10Fe in the low temperature range: part 2: Studies on corrosion product film formation and properties in relation to microstructure and iron content [J]. Br. Corros. J., 1986, 21: 33
doi: 10.1179/000705986798272451
11 Hack H P. Role of the corrosion product film in the corrosion protection Cu-Ni alloys in saltwater [D]. State College: Pennsylvania State University, 1987
12 Zhang Z, Yao L A, Gan F X. Effect of surface film on electrochemical behavior of Cu-Ni alloy [J]. J. Chin. Soc. Corros. Prot., 1987, 7: 143
12 張哲, 姚祿安, 甘復興. 銅鎳合金表面膜對其電化學行為的影響 [J]. 中國腐蝕與防護學報, 1987, 7: 143
13 Bai M M, Bai Z H, Jiang L, et al. Corrosion behavior of H62 brass alloy/TC4 titanium alloy welded specimens [J]. J. Chin. Soc. Corros. Prot., 2020, 40: 159
13 白苗苗, 白子恒, 蔣立 等. H62黃銅/TC4鈦合金焊接件腐蝕行為研究 [J]. 中國腐蝕與防護學報, 2020, 40: 159
14 Ma A L, Jiang S L, Zheng Y G, et al. Corrosion product film formed on the 90/10 copper-nickel tube in natural seawater: composition/structure and formation mechanism [J]. Corros. Sci., 2015, 91: 245
doi: 10.1016/j.corsci.2014.11.028
15 Syrett B C, Macdonald D D, Wing S S. Corrosion of copper-nickel alloys in sea water polluted with sulfide and sulfide oxidation products [J]. Corrosion, 1979, 35: 409
doi: 10.5006/0010-9312-35.9.409
16 Wang Y Z, Beccaria A M, Poggi G. The effect of temperature on the corrosion behaviour of a 70/30 Cu-Ni commercial alloy in seawater [J]. Corros. Sci., 1994, 36: 1277
doi: 10.1016/0010-938X(94)90181-3
17 Yang F, Zheng Y G, Yao Z M, et al. Study on erosion-corrosion behavior of Cu-Ni alloy BFe30-1-1 in flowing artificial seawater [J]. J. Chin. Soc. Corros. Prot., 1999, 19: 16
17 楊帆, 鄭玉貴, 姚治銘 等. 銅鎳合金BFe30-1-1在流動人工海水中的腐蝕行為 [J]. 中國腐蝕與防護學報, 1999, 19: 16
18 Wang J H, Jiang X X, Li S Z. Microstructure and corrosion behavior of 70Cu-30Ni welded pipe [J]. Trans. Nonferrous Met. Soc. China, 1995, 5: 88
19 Macdonald D D, Syrett B C, Wing S S. The corrosion of copper-nickel alloys 706 and 715 in flowing sea water. I-effect of oxygen [J]. Corrosion, 1978, 34: 289
doi: 10.5006/0010-9312-34.9.289
20 Ekerenam O O, Ma A L, Zheng Y G, et al. Evolution of the corrosion product film and its effect on the erosion-corrosion behavior of two commercial 90Cu-10Ni tubes in seawater [J]. Acta Metall. Sin. (Engl. Lett.), 2018, 31: 1148
doi: 10.1007/s40195-018-0745-1
21 Chi C Y, Li N, Xue J J, et al. Electrochemical behavior of B30 Cu-Ni alloy in seawater [J]. Mater. Prot., 2009, 42(8): 19
21 遲長云, 李寧, 薛建軍 等. B30銅鎳合金在海水中的電化學行為 [J]. 材料保護, 2009, 42(8): 19
22 Milo?ev I, Kova?evi? N, Kova? J, et al. The roles of mercapto, benzene and methyl groups in the corrosion inhibition of imidazoles on copper: I. Experimental characterization [J]. Corros. Sci., 2015, 98: 107
doi: 10.1016/j.corsci.2015.05.006
23 Aben T, Tromans D. Anodic polarization behavior of copper in aqueous bromide and bromide/benzotriazole solutions [J]. J. Electrochem. Soc., 1995, 142: 398
doi: 10.1149/1.2044031
24 North R F, Pryor M J. The nature of protective films formed on a Cu-Fe alloy [J]. Corros. Sci., 1969, 9: 509
doi: 10.1016/0010-938X(69)90021-3
25 Feng L, Wang Y H, Zhong L, et al. Influence of short-term storage on corrosion behavior of copper [J]. J. Chin. Soc. Corros. Prot., 2016, 36: 375
25 馮林, 王燕華, 鐘蓮 等. 短期貯存對金屬銅腐蝕電化學行為的影響 [J]. 中國腐蝕與防護學報, 2016, 36: 375
26 North R F, Pryor M J. The influence of corrosion product structure on the corrosion rate of Cu-Ni alloys [J]. Corros. Sci., 1970, 10: 297
doi: 10.1016/S0010-938X(70)80022-1
27 Wang J M, Yang H D, Du M, et al. Corrosion of B10 Cu-Ni alloy in seawater polluted by high concentration of NH4 + [J]. J. Chin. Soc. Corros. Prot., 2021, 41: 609
27 王家明, 楊昊東, 杜敏 等. B10銅鎳合金在高濃度NH4 +污染海水中腐蝕研究 [J]. 中國腐蝕與防護學報, 2021, 41: 609
28 Wang G Y, Wang H J, Li X L, et al. Corrosion and Protection of Natural Environment [M]. Beijing: Chemical Industry Press, 1997
28 王光雍, 王海江, 李興濂 等. 自然環境的腐蝕與防護: 大氣·海水·土壤 [M]. 北京: 化學工業出版社, 1997
29 Ding G Q, Li X Y, Zhang B, et al. Variation of free corrosion potential of several metallic materials in natural seawater [J]. J. Chin. Soc. Corros. Prot., 2019, 39: 543
29 丁國清, 李向陽, 張波 等. 金屬材料在天然海水中的腐蝕電位及其變化規律 [J]. 中國腐蝕與防護學報, 2019, 39: 543
30 Fang Z G, Liu B. Corrosion and Protection of Submarine Structures [M]. Beijing: National Defense Industry Press, 2017
30 方志剛, 劉斌. 潛艇結構腐蝕防護 [M]. 北京: 國防工業出版社, 2017
31 Yuan S J, Pehkonen S O. Surface characterization and corrosion behavior of 70/30 Cu-Ni alloy in pristine and sulfide-containing simulated seawater [J]. Corros. Sci., 2007, 49: 1276
doi: 10.1016/j.corsci.2006.07.003
32 Kato C, Pickering H W. A rotating disk study of the corrosion behavior of Cu-9.4Ni-1.7Fe alloy in air-saturated aqueous NaCl solution [J]. J. Electrochem. Soc., 1984, 131: 1219
doi: 10.1149/1.2115791
33 Chauhan P K, Gadiyar H S. An xps study of the corrosion of Cu-10Ni alloy in unpolluted and polluted sea-water; the effect of FeSO4 addition [J]. Corros. Sci., 1985, 25: 55
doi: 10.1016/0010-938X(85)90088-5
34 Chang Q P, Chen Y Y, Song F, et al. Corrosion properties of B30 Cu-Ni alloy and 316L stainless steel in a heat pump system [J]. J. Chin. Soc. Corros. Prot., 2014, 34: 544
34 常欽鵬, 陳友媛, 宋芳 等. B30銅鎳合金和316L不銹鋼在熱泵系統中的耐腐蝕性能 [J]. 中國腐蝕與防護學報, 2014, 34: 544
35 Badaw W A, Ismail K M, Fathi A M. Effect of Ni content on the corrosion behavior of Cu-Ni alloys in neutral chloride solutions [J]. Electrochim. Acta, 2005, 50: 3603
doi: 10.1016/j.electacta.2004.12.030
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 腐蝕與防護網官方QQ群:140808414






