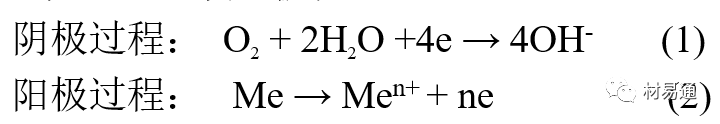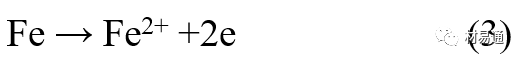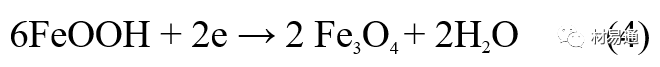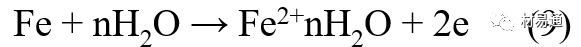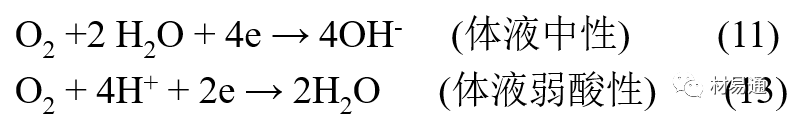金屬腐蝕是指在環境介質的化學作用下,在和物理、機械或生物學因素的共同作用下金屬產生的破壞,即金屬在它所處環境的作用下所產生破壞。
本期主要介紹金屬在不同環境中的腐蝕,包括在大氣中、海水中、土壤中、工業環境以及人體環境中的腐蝕情況。
金屬在大氣中的腐蝕
01 大氣腐蝕概述
金屬材料或構筑物在大氣條件下發生化學或電化學反應引起材料的破損稱為大氣腐蝕。大氣腐蝕是常見的一種腐蝕現象。全世界在大氣中使用的鋼材量一般超過其生產總量的60%。例如,鋼梁、鋼軌、各種機械設備、車輛等都是在大氣環境下使用。大氣腐蝕而損失的金屬約占總的腐蝕量的50%以上,因此了解和研究大氣腐蝕的機理、影響因素及防止方法是非常必要的。
02 大氣腐蝕分類
全球范圍大氣主要成分幾乎不變的,其中的水分含量將隨地域、季節、時間等條件而變化。參與大氣腐蝕過程的是氧和水氣,二氧化碳。根據金屬表面的潮濕程度的不同,把大氣腐蝕分為三類:
1)干大氣腐蝕。干大氣腐蝕是在金屬表面不存在液膜層時的腐蝕。特點是在金屬表面形成不可見的保護性氧化膜(1~10nm)和某些金屬失澤現象。如銅、銀等在被硫化物污染的空氣中所形成的一層膜。
2)潮大氣腐蝕。潮大氣腐蝕是指金屬在相對濕度小于100%的大氣中,表面存在肉眼看不見的薄的液膜層(10nm~1μm)發生的腐蝕。如鐵沒受雨淋也會生銹。
3)濕大氣腐蝕。濕大氣腐蝕指金屬在相對濕度大100%,如水分以雨、霧、水等形式直接濺落在金屬表面上,表面存在肉眼可見的水膜(1μm ~1mm)發生的腐蝕。
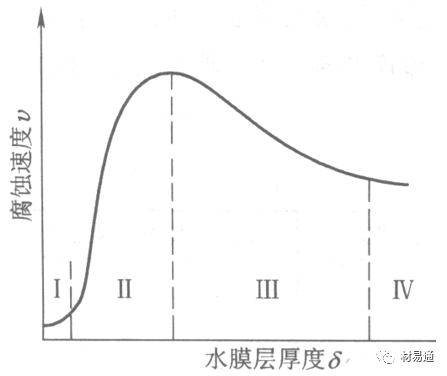
圖1大氣腐蝕速度與金屬表面水膜厚度的關系
根據上圖解釋腐蝕速度與水膜厚度的規律:
1)區域I 金屬表面只有約幾個水分子厚(1~10nm)水膜,還沒有形成連續的電解質溶液,相當于干的大氣腐蝕.腐蝕速度很小。
2)區域II 金屬表面水膜厚度約在1μm時,由于形成連續電解液層,腐蝕速度迅速增加,發生潮的大氣腐蝕。
3)區域III 水膜厚度增加到1mm時,發生濕的大氣腐蝕,氧通過該膜擴散到金屬表面顯著困難,因此腐蝕速度明顯下降。
4)區域IV 金屬表面水膜厚度大于1mm,相當于全浸在電解液中的腐蝕,腐蝕速度基本不變。
通常所說的大氣腐蝕是指在常溫下潮濕空氣中的腐蝕。
03 大氣腐蝕機理
大氣腐蝕特點是金屬表面處于薄層電解液下的腐蝕過程,腐蝕規律符合電化學腐蝕規律。
當金屬表面形成連續的電解液薄層時,大氣腐蝕的陰極過程主要是氧去極化。
鐵、鋅等金屬全浸在還原性酸溶液中,陰極過程主要是氫去極化,城市污染的大氣所形成的酸性水膜下,這些金屬的腐蝕主要是氧去極化腐蝕。
在薄液膜下,陽極過程受較大阻滯,氧更易到達金屬表面,生成氧化膜或氧的吸附膜,使陽極處于鈍態。陽極鈍化及金屬離子化過程困難造成陽極極化。
當液膜增厚,相當于濕的大氣腐蝕時,氧到達金屬表面有一個擴散過程,腐蝕過程受氧擴散過程控制。
潮的大氣腐蝕主要受陽極過程控制; 濕大氣腐蝕主要受陰極過程控制。
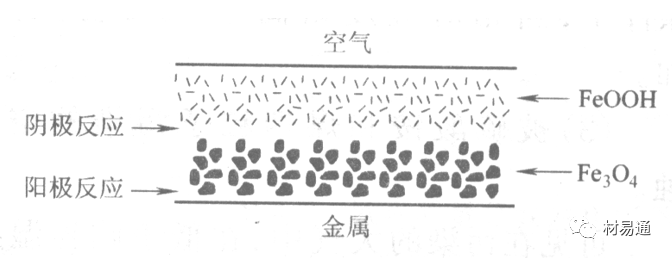
大氣腐蝕條件不同,銹層成分和結構是很復雜的。Evans認為大氣腐蝕的銹層處在潮濕條件下,銹層起強氧化劑作用,在銹層內陽極反應發生在金屬/Fe3O4界面上:
陰極反應發生在Fe3O4/FeOOH界面上:
銹層參與了陰極過程,圖2為Evans銹層模型圖。
由圖可見,銹層內發生Fe3+→Fe2+的還原反應,銹層參與了陰極過程。
銹層干燥時,外部氣體相對濕度下降時,銹層和底部基體鋼在大氣中氧的作用下,銹層重新氧化成Fe3+的氧化物,在干濕交替的條件下,銹層加速鋼腐蝕過程。碳鋼銹層結構一般分內外兩層:
內層緊靠鋼和銹的界面上,附著性好,結構較致密,主要由致密的帶少許Fe3O4晶粒和非晶FeOOH構成;
外層由疏松的結晶α-FeOOH和γ-FeOOH構成。
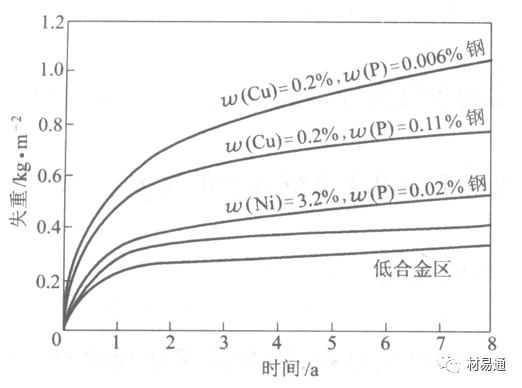
銹層生成的動力學如圖3所示,其曲線遵循冪定律;
P—失重量;K—常數;t—暴露時間;n—常數。
上式也適用于鋼的鍍鋅和鍍鋁層及W(A1)=55%的Al-Zn鍍層的大氣試驗數。
04 工業大氣中金屬腐蝕特點
工業大氣中的SO2、NO2、H2S、NH3等都增加大氣的腐蝕作用,加快金屬的腐蝕速度.
石油、煤等燃科的廢氣中含SO2最多,在城市和工業區SO2的含量可達0.1~100mg/m3。
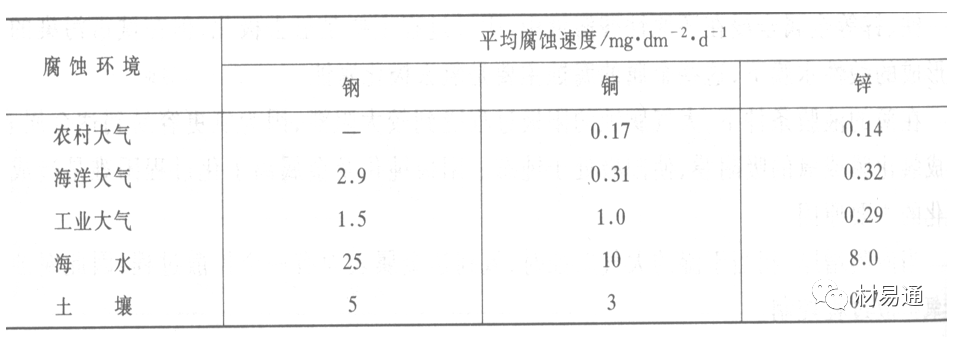
常用金屬在不同大氣環境中的平均腐蝕速度。
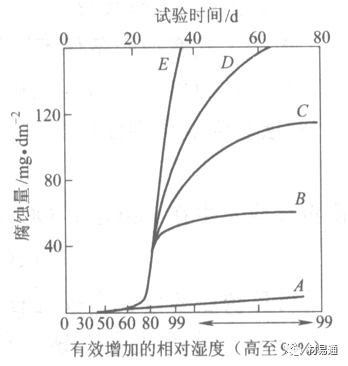
1)Air很純時,腐蝕速度很小,隨濕度增加僅有輕微增加。
2)在污染的空氣中,空氣相對濕度低于70%時,即便長期暴露,腐蝕速度也是很慢。但SO2有存在的條件下,當相對濕度略高于70%時,腐蝕速度急劇增加。
3)被硫酸銨和煤煙粒子污染的空氣加速金屬腐蝕。
圖中A-純凈空氣, B-有(NH4)2SO4, C-0.01%SO2, D-(NH4)2SO4+0.01%SO2, E-煙粒+0.01%SO2。
污染Air,低于臨界濕度,金屬表面沒有水膜,金屬受化學作用引起的腐蝕,腐蝕速度很小。高于臨界濕度,水膜的形成,電化學腐蝕,腐蝕速度急劇增加。
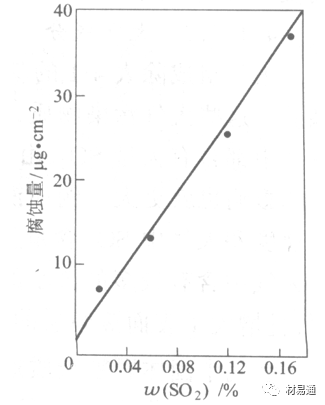
大氣中SO2對不耐H2SO4腐蝕的金屬,如Fe、Zn、Cd、Ni的影響十分明顯。呈直線關系上升。
SO2促進金屬大氣腐蝕的機制
SO2的腐蝕作用機制是硫酸鹽穴自催化過程。
SO2促進金屬大氣腐蝕的機制,主要有兩種方式:
一是部分SO2在空氣中能直接氧化成SO3,SO3溶于水形成H2SO4;
二有一部分SO2吸附在金屬表面上,與Fe作用生成易溶的硫酸亞鐵,FeSO4進一步氧化并由于強烈的水解作用生成了H2SO4,H2SO4再與Fe作用,按這種循環方式加速腐蝕。
整個過程具有自催化作用,即所謂銹層中硫酸鹽穴的作用。
銹層中硫酸鹽穴的作用
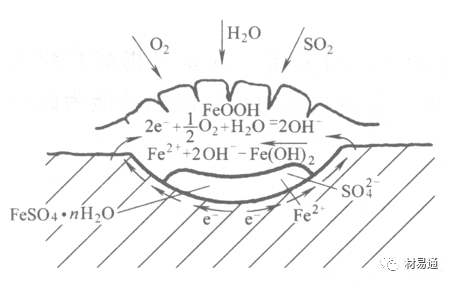
Schwarz:銹層內FeSO4生成機構如圖下所示的模型。銹層的保護能力受其形成時占主導地位的條件影響。如生成的銹層被硫酸鹽侵蝕,銹層幾乎無保護能力。相反,如最初銹層很少受硫酸鹽污染,其保護性較好。
圖5 銹層內FeSO4生成機構
05 影響大氣腐蝕的因素及防蝕方法
濕度
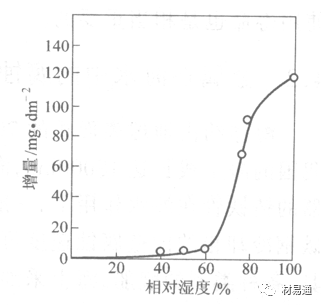
濕度是決定大氣腐蝕類型和速度的一個重要因素。把大氣腐蝕速度開始劇增時的大氣相對濕度值稱為臨界濕度。對于鐵、鋼、銅、鋅,臨界濕度約在70%~80%之間。由圖7可見,濕度小于臨界濕度,腐蝕速度很慢,幾乎不腐蝕。若把濕度降至臨界濕度以下,可防止金屬發生大氣腐蝕。
圖7 鐵在質量分數為0.01%的SO2的空氣中經55天后
大氣成分
地理環境不同,有SO2、H2S、NaCl及塵埃等雜質。它們不同程度地加速腐蝕。特別是SO2。煤、石油燃燒的廢氣中都含有大量SO2, 冬季燃料消耗多,SO2污染更嚴重,對腐蝕的影響也就更大。
鐵、鋅等金屬在SO2大氣中生成易溶的硫酸鹽化合物,它們的腐蝕速度和大氣中SO2含量呈直線關系上升。
海洋大氣中含有較多的微小的NaCl顆粒,它們落在金屬的表面上,有吸濕作用,增大了表面液膜層的電導,氯離子本身有很強的侵濁性,因而使腐蝕變得更嚴重。
大氣中固體顆粒稱為塵埃。其組成復雜,除海鹽粒外,還有碳和碳化物、硅酸鹽、氮化物、銨鹽等固體顆粒。城市大氣中塵埃含量約2mg/m3,工業大氣中的塵埃甚至可達1000mg/m3以上。
塵埃對大氣的影響有以下幾點:
1)塵埃本身具有腐蝕性,如銨鹽顆粒能镕入金屬表面的水膜,提高電導或酸度促進腐蝕。
2)塵埃本身無腐蝕作用,但能吸附腐蝕物質,如碳粒能吸附SO2和水氣生成腐蝕性的酸性溶液。
3)塵埃沉積在金屬表面形成縫隙而凝聚水分,形成氧濃差引起縫隙腐蝕。
露置在大氣環境中的金屬構件和儀器設備應當防塵。
防止大氣腐蝕的方法:
1)提高金屬材料的耐蝕性 在碳鋼中加入Cu、P、Cr、Ni及稀土元素可提高其耐大氣腐蝕性能。例如,美國的Cor-Ten鋼(Cu-P-Cr-Ni系低合金鋼),其耐大氣腐蝕性能為碳鋼的4~8倍。
2)采用有機和無機涂層及金屬鍍層。
3)采用氣相緩蝕劑。
4)降低大氣濕度, 主要用于倉儲金屬制品的保護。
合理設計構件.防止縫隙中存水,去除金屬表上的灰塵等都有利于防蝕, 開展環境保護,減少大氣污染,不僅有利于人民健康, 而且對延長金屬材料在大氣中使用壽命也是相當重要的。
金屬在海水中的腐蝕
01 海水腐蝕概述
海洋占地球表面積70%,海水是自然界中數量最大且具有腐蝕性的天然電解質。我國海岸線長達18000km,海域廣闊。沿海地區的工廠常用海水作為冷卻介質,冷卻器的鑄鐵管在海水作用下,一般只能使用3~4年;海水泵的鑄鐵葉輪只能使用3個月左右;碳鋼冷卻箱的內壁腐蝕速度可達1mm/a以上。近年來海洋開發受到重視,海上運輸工具、海上采油平臺,開采和水下輸送及儲存設備等金屬構件受到海水和海洋大氣腐蝕的威脅愈來愈嚴重;研究海洋環境中金屬的腐蝕及其防護有重要意義。
02 海水腐蝕特點
鹽類及導電率
海水為腐蝕性介質,特點是含多種鹽類,鹽分中主要是NaCl,常把海水近似地看作質量分數為3%或3.5%的NaCl溶液。
鹽度是指1000g海水中溶解固體鹽類物質的總克數,一般海水的鹽度在3.2%~3.75%之間,通常取3.5%為海水的鹽度平均值。海水中氯離子的含量很高,占總鹽量的58.04%,使海水具有較大的腐蝕性。
海水平均電導率為4×10-2S/cm,遠超過河水和雨水的電導率。
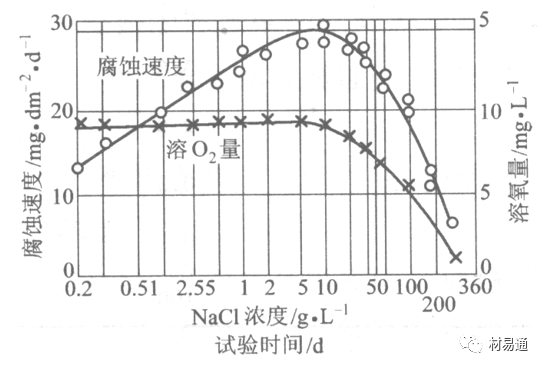
溶解氧
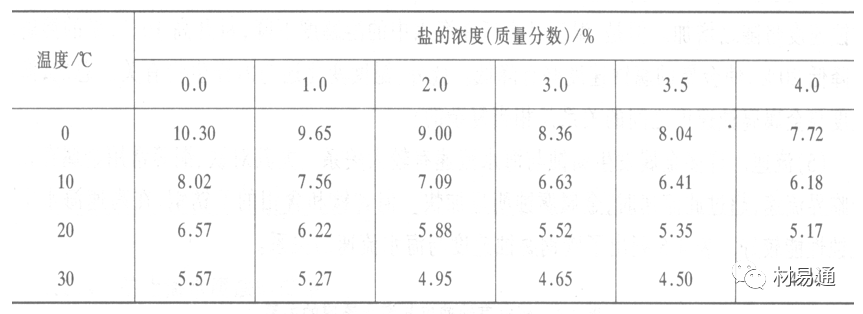
海水中溶解氧,是海水腐蝕的重要因素。正常情況下海水表面層被空氣飽和,氧的濃度隨水溫一般在(5~10)×10-6cm3/L范圍內變化。由表看出鹽的濃度和溫度愈高,氧的溶解度愈小。
表1 氧在海水中的溶解度
海水的電化學特點
1)多數金屬,除特別活潑金屬鎂及其合金外,海水中的腐蝕過程都是氧去極化過程, 腐蝕速度由氧擴散過程控制。
2)大多數金屬(鐵、鋼、鋅等),在海水中發生腐蝕時,陽極過程的阻滯作用很小,海水中Cl-離子濃度高,海水中用增加陽極阻滯方法來減輕海水腐蝕的可能性不大,添加合金元素鉬,才能抑制Cl-對鈍化膜的破壞作用,改進材料在海水中的耐蝕性。
3)海水電導率很高,電阻性阻滯很小,對海水腐蝕,微觀電池的活性較大,宏觀電池活性也較大。在海水中,異種金屬接觸引起的電偶腐蝕有相當大的破壞作用。如艦船的青銅螺旋槳可引起遠達數十米處的鋼船殼體的腐蝕。
4)海水中金屬易發生局部腐蝕破壞。如點蝕,縫隙腐蝕,湍流腐蝕和空泡腐蝕等。
03 影響海水腐蝕的因素
海水中鹽類,溶解氧、海洋生物和腐爛的有機物,海水的濕度、流速與pH值等都對海水腐蝕有很大的影響。
1)鹽類。
以NaCl為主,海水中鹽的濃度與鋼的腐蝕速度最大的鹽濃度范圍相近,當溶鹽濃度超過一定值,因氧溶解度降低,金屬腐蝕速度下降,見圖8。
2)pH值。海水pH值在7.2~8.6之間。pH值可因光合作用而稍有變化;在深海處pH值略有降低, 不利于金屬表面生成保護性的鹽膜。
3)溶解氧。海水中的溶解氧是海水腐蝕的重要因素。大多數金屬在海水中的腐蝕受氧去極化作用控制。
溶解氧含量隨海水深度不同而變化. 海水表面與大氣接觸含氧量高達12×10-6。海平面至-800m深處,含氧量逐漸減少并達到最低值; 海洋動物要消耗氧氣;-800m再降-1000m,溶氧量又上升,接近海水表面的氧濃度,因為深海水溫度較低、壓力較高的緣故。
4)溫度。海水溫度每升高10℃,化學反應速度提高約10%,海水中金屬的腐蝕速度將隨之增加。但溫度升高,氧在海水中的溶解度下降,每升高10℃,氧的溶解度約降低20%,使金屬的腐蝕速度略有降低。
溫度變化與海洋生物有關。海水溫度與金屬腐蝕速度之間的關系是相當復雜的。
5)流速。許多金屬發生腐蝕與海水流速有較大關系。尤其對鐵、銅等常用金屬存在一個臨界流速,超過此流速時,金屬腐蝕明顯加快。但含鈦和含鉬的不銹鋼,在高速海水中的抗蝕性能較好
6)海洋生物 海洋生物在船舶或海上構筑物表面附著形成縫隙,易誘發縫隙腐蝕。
微生物的生理作用會產生氨、CO2和H2S等腐蝕物質,如硫酸鹽還原菌作用產生S2- ,會加速金屬腐蝕。
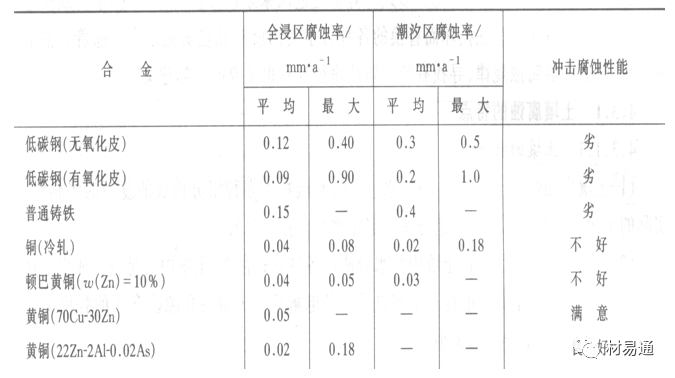
04 水中常見金屬材料的耐蝕性
金屬材料在海水中的耐蝕性差別很大,耐蝕性最好的是鈦合金和Ni-Cr合金,而鑄鐵和碳鋼耐蝕性較差。不銹鋼的均勻腐蝕速度雖然很小,但在海水中易產生點蝕。常用金屬材料耐海水腐蝕性能見表2。
05 防止海水腐蝕的措施
1)研制和應用耐海水腐蝕的材料;如鈦、鎳、銅及其合金,耐海水鋼(Mariner)。
2)陰極保護 腐蝕最嚴重處采用護屏保護較合理,亦可采用簡易可行的犧牲陽極法。
3)涂層 除應用防銹油漆外,還可采用防止生物沾污的雙防油漆,對于潮汐區和飛濺區的某些固定的鋼結構可以使用蒙乃爾合金包覆。
金屬在土壤中的腐蝕
01 土壤腐蝕概述
土壤是由土粒、水溶液、氣體、有機物、帶電膠粒和粘液膠體等多種組分構成的極為復雜的不均勻多相體系。因土壤的組成和性能的不均勻,極易構成氧濃差電池腐蝕,使地下金屬設施遭受嚴重局部腐蝕。埋在地下的油、氣、水管線以及電纜等因穿孔而漏油、漏氣或漏水。或使電信設備發生故障。這些往往很難檢修,帶來很大的損失和危害。
土壤腐蝕是一種很重要的腐蝕形式。先進國家,地下的油、氣百萬公里以上,每年因腐蝕損壞而替換的各種管子費用就有幾億美元之多。隨石油工業的發展,研究土壤腐蝕規律,尋找有效的防蝕途徑具有很重要的實際意義。
02 壤腐蝕特點
土壤特性
1)土壤多相性。土壤是由土粒、水、空氣,有機物等多種組分構成的復雜的多相體系。實際的土壤一般是這幾種不同組分按一定比例組合在一起的。
2)土壤導電性。由于在土壤中的水分能以各種形式存在,土壤中總是存在一定的水分,因此土壤有導電性。土壤也是一種電解質。土壤的孔隙及含水的程度又影響著土壤的透氣性和電導率的大小。
3)土壤不均勻性。土壤中氧氣,有溶解在水中,有存在于土壤的縫隙中。土壤中氧濃度與土壤的濕度和結構都有密切關系,氧含量在干燥砂土中最高,在潮濕的砂土中次之,而在潮濕密實的粘土中最少。這正是造成氧濃差電池腐蝕的原因。
4)土壤的酸堿性。
大多數土壤是中性的,pH值在6.0~7.5之間。 有的土壤是堿性的,如我國西北的鹽堿土pH值為7.5~9.0; 一些土壤是酸性的,如腐殖土和沼澤土pH值為3~6。一般認為pH值越低,土壤腐蝕性越大。
大多數金屬在土壤中的腐蝕都屬于氧去極化腐蝕。金屬在土壤中的腐蝕與在電解液中的腐蝕本質是一樣的。以Fe為例:
陽極過程:
陽極反應速度主要受金屬離子化過程難易程度控制。 在pH值低的土壤中,OH-很少。由于不能生成Fe(OH)2,Fe2+離子濃度在陽極區增大。在中性和堿性土壤中生成的Fe(OH)2溶解度很小, 沉淀在鋼鐵表面上,對陽極溶解有一定的阻滯作用。土壤中含有碳酸鹽, 可能在陽極表面生成不溶性沉積物,起保護膜的作用。土壤中氯離子和硫酸根離子能與Fe2+離子生成可溶性的鹽,加速陽極溶解。
陰極過程:
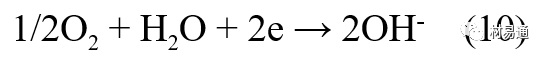
在弱酸性、中性和堿性土壤中,陰極反應主要是氧的去極化作用。土壤中的水溶解氧是有限的,對土壤腐蝕起主要作用的是縫隙和毛細管中的氧。土壤中的傳遞過程比較復雜,進行得也比較慢。在潮濕的粘性土壤中,由于滲水能力和透氣性差, 氧的傳遞是相當困難的,使陰極過程受阻。當土壤水分的pH值大于5時,腐蝕產物能形成保護層。
03 土壤腐蝕的形式
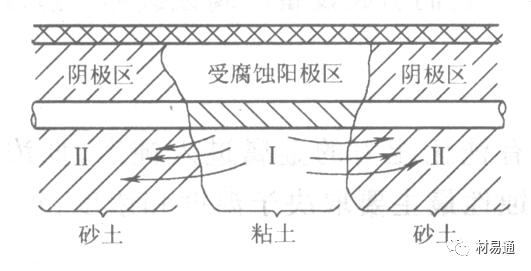
充氣不均勻引起的腐蝕
這種腐蝕主要指地下管線穿過不同的地質結構及潮濕程度不同的土壤帶時,由于氧濃度差別引起的宏觀電池腐蝕,如圖9。
圖9 管道在結構不同的土壤中所形成的氧濃差電池
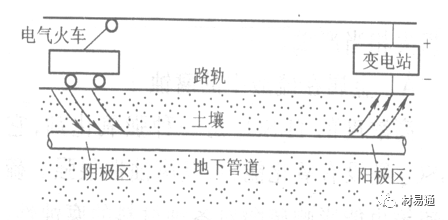
雜散電流引起的腐蝕
雜散電流是一種漏電現象。來源用直流電的大功率電氣裝置,電氣鐵路,電解及電鍍、電焊機等裝置。圖10為雜散電流腐蝕實例示意圖。
圖10
鐵軌與土壤間的絕緣不良,有一部分電流就會從鐵軌漏失到土壤中。鐵軌附近埋設有金屬管道,雜散電流經土壤進入金屬管道后,再經土壤及軌道返回到電源。這相當兩個宏觀電池作用:鐵軌-陽極,土壤-電解質,管道-陰極,管道-陽極,土壤-電解質,鐵軌(地面)-陰極。
微生物引起的腐蝕
對腐蝕有作用的細菌不多,其中最重要的是硫酸桿菌和硫酸鹽還原菌(厭氧菌)。
這兩種細菌能將土壤中硫酸鹽還原產生S2-,其中小部分消耗在微生物自身的新陳代謝上,大部分可作為陰極去極化劑, 促進腐蝕反應。
土壤的pH值在4.5~9.0時,最適宜硫酸鹽還原菌生長; 11 <pH值<3.5時,這種菌的活動及生長就很難了。
04 止土壤腐蝕的措施
1) 采用涂料或包覆玻璃布防水;
2) 采用電化學保護,多采用犧牲陽極法,陰極保護與涂料聯合使用效果更好;
3) 采用金屬涂層或包覆金屬,鍍鋅層等。
金屬在工業環境中的腐蝕
01 金屬在酸溶液中的腐蝕
酸是一類能在水溶液中電離,形成H3O+離子化合物的總稱。一般用H+代表H3O+。
氧化性酸與非氧化性酸對金屬的腐蝕情況大不相同。
腐蝕過程中,非氧化性酸的特點是腐蝕的陰極過程基本上是氫去極化過程,增加溶液酸度相應地會增加陰極反應,并使金屬腐蝕速度增加。
氧化性酸的特點是陰極過程主要是氧化劑的還原過程引起金屬腐蝕(如硝酸根還原成亞硝酸根)。但氧化性酸濃度超過某一臨界值時,使鈍化型金屬進入鈍態,抑制了腐蝕。酸溶液腐蝕性一方面與酸的強弱,同時也與酸的陰離子的氧化能力有關。
工業無機酸有硫酸、硝酸、鹽酸, 他們引起的設備腐蝕破壞和造成的經濟損失相當嚴重。
金屬在硫酸中的腐蝕:
高濃度H2SO4是強氧化劑,能使具有鈍化能力的金屬進入鈍態,低濃度的H2SO4則沒有氧化能力,其腐蝕性很強。
硫酸的腐蝕性最主要取決于溫度和濃度,氧化劑、流速等也能影響硫酸對各種材料的腐蝕性。
工業上耐硫酸的材料為價廉的碳鋼和鉛及鉛合金,圖11、圖12分別顯示出鐵、鉛的腐蝕速度與硫酸質量分數的關系。
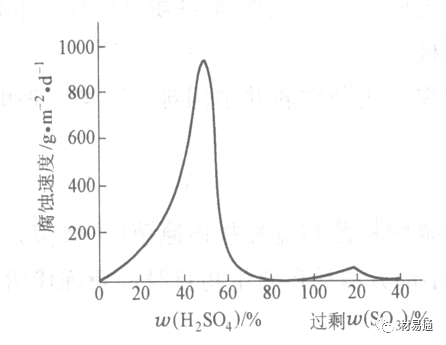
圖11 鐵的溶解速度與硫酸濃度的關系
鐵的腐蝕速度與硫酸質量分數的關系
硫酸質量分數低于50%時,碳鋼的腐蝕速度隨濃度增加腐蝕速度急劇增加;
當質量分數超過50%時,隨濃度增加,腐蝕急劇下降;
當質量分數超過70%時,碳鋼幾乎不腐蝕。鋼表面生成硫酸鹽(FeSO4)保護膜。因此制造質量分數超過70%的濃硫酸的儲罐與運輸管線可用鋼鐵材料。
當質量分數超過101%的中溫發煙H2SO4時,應注意兩個問題:①濃H2SO4是一種強吸水劑;②硫酸鹽保護膜(FeSO4)易受破壞。
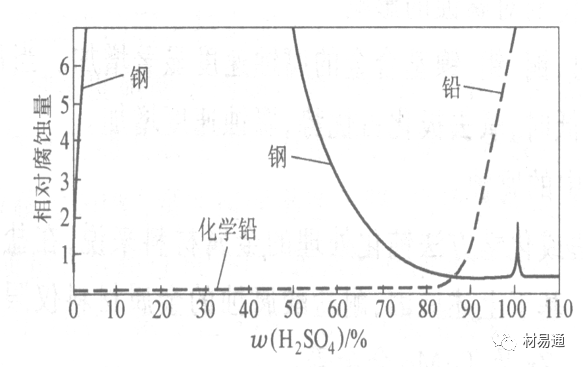
當硫酸質量分數低于70%時,應采用鉛制的設備,鉛表面可以生成PbSO4的保護膜。在硫酸環境中,鋼和鉛具有互補性。
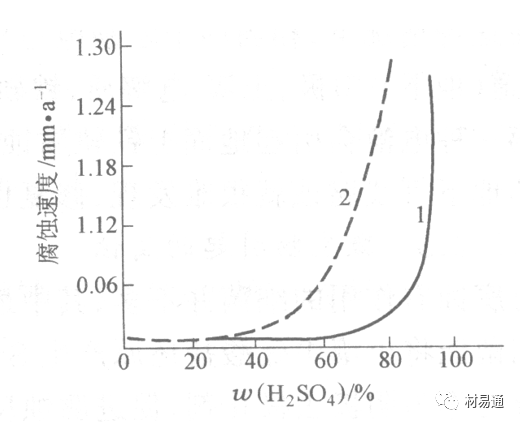
圖12 鉛的腐蝕速度與硫酸濃度的關系
在硫酸環境中,鋼和鉛具有互補性.
圖 13 鋼和鉛的腐蝕規律(常溫)
流速對腐蝕影響
表3示出了輸送H2SO4時濃度與流動速度對鋼管壽命的影響。隨濃度增加,流速增大,鋼管壽命降低,輸送硫酸時,不宜采用高的流動速度.
表3 硫酸輸送管的壽命與硫酸濃度的關系
金屬在鹽酸中的腐蝕
HCl強酸, 除銀、鈦等少數金屬外,大多數金屬或合金在HCl中都不能生成難溶的金屬鹽膜。
HCl中Cl-有極強性,除鈦等少數鈍性優異的金屬外,金屬表面的鈍化膜在鹽酸中都因受到氯離子的破壞而發生點蝕。
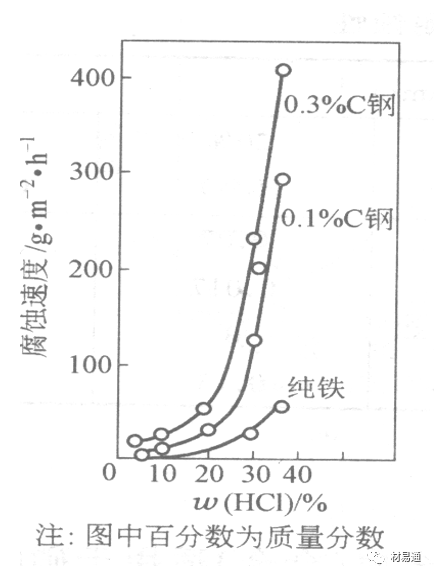
a 鹽酸濃度與腐蝕速度的關系
工業純鐵與碳鋼的腐蝕速度隨鹽酸的濃度成指數關系增加,鋼不能用于鹽酸介質中。
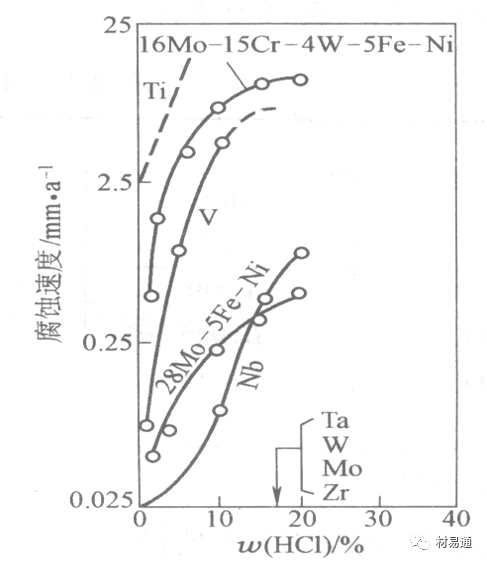
沸HCl中各種金屬腐蝕速度與HCL濃度關系
鹽酸中溶氧或氧化劑對腐蝕的影響
HCl中存在氧化劑時,銅、鉬、鎳基合金的腐蝕速度顯著增加。當HCl濃度高時,陰極為氫去極化,但當鹽酸濃度低時,氧去極化占優勢,腐蝕速度增加。
鈍態金屬在鹽酸中的腐蝕
對可電化學方法或化學方法鈍化處理的金屬材料,在HCl中它們的鈍態區很窄或不存在。因此,耐HCl腐蝕的金屬材料僅限于有極強鈍化性能特殊金屬及合金,如Ta、Zr及Ti-Mo合金等。
耐鹽酸腐蝕的材料
1)Ti-Mo合金
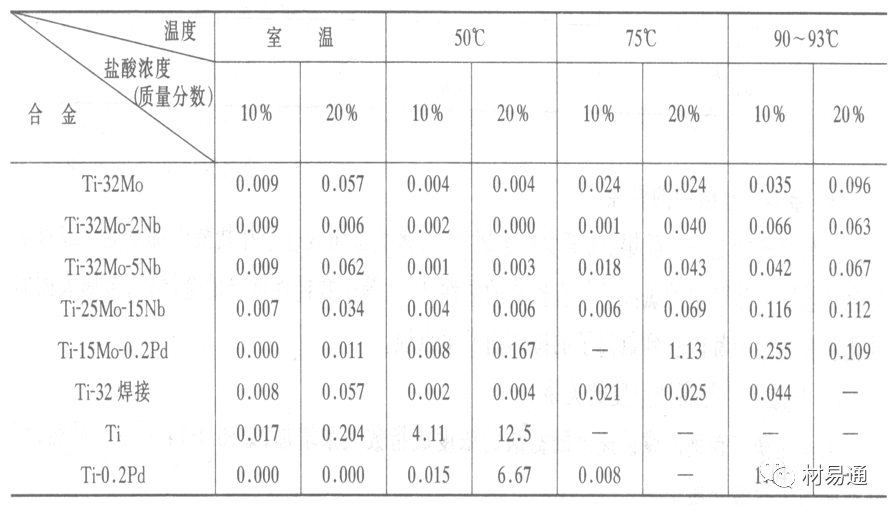
耐蝕Ti合金的研制是為改善純Ti在強還原介質中的耐蝕性。W.L.Finlay發現Ti-Mo合金對強還原性硫酸、鹽酸具有優異的耐蝕性。Ti-30~40Mo合金在沸騰的質量分數為20%的HCl中的腐蝕率為10mm/a; 工業純鈦只能用于室溫質量分數為3%~10%的HCl中 當前Ti-30Mo、Ti-32Mo是在還原性酸中最耐蝕的Ti合金,不合稀貴金屬,因而受到廣泛重視。
表5 Ti合金在HCl中的腐蝕率/mma-1
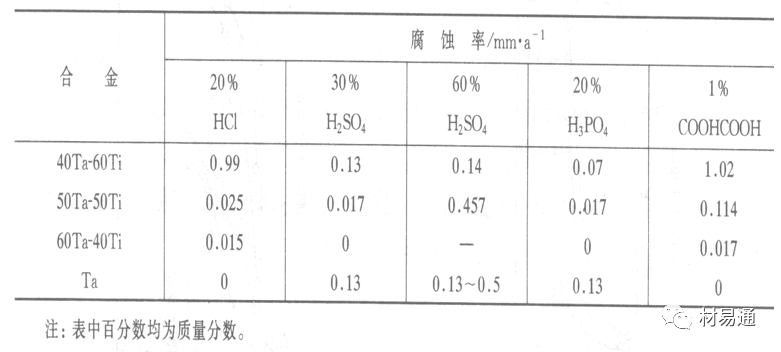
2)Ti-Ta合金
鉭能提高Ti在還原性介質中的耐蝕性,且能改善鈦在氧化性介質中的耐蝕性。
金屬在硝酸中的腐蝕
HNO3氧化性的強酸,在其中能鈍化的金屬適用于HNO3,Ag、Ni、Pb、Cu不耐硝酸腐蝕。
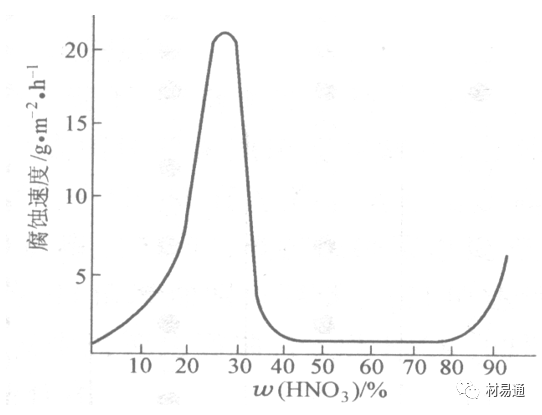
1)碳鋼。碳鋼在HNO3中的腐蝕行為見圖16
02 不同鋼在硝酸中的腐蝕行為
1)碳鋼
硝酸質量分數低于30%時,碳鋼的腐蝕速度隨酸濃度增加而增加,當質量分數約在30%附近時腐蝕速度達到最大值。
質量分數超過30%,腐蝕速度迅速下降;
質量分數達到50%時,腐蝕速度最小, 說明鋼鈍化了。當質量分數超過80%時,碳鋼的腐蝕速度再次急劇增加,鋼出現過鈍化溶解。
鐵或鋼適用于HNO3濃度在30%~80%(質量分數)范圍內。
2)不銹鋼。
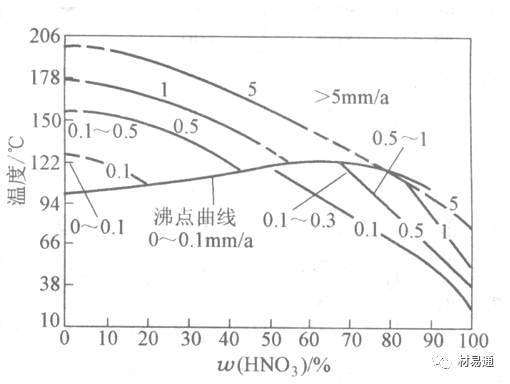
對硝酸有良好的耐蝕性。圖4-17是18-18不銹鋼在硝酸中腐蝕圖。不銹鋼是硝酸系統中大量使用的耐蝕材料,如硝銨、硝酸生產中大部分設備都是用不銹鋼制造的。濃度超過70%熱硝酸中易發生過鈍化腐蝕。
3)Al及其合金。
對中等溫度的發煙HNO3良好蝕性,[HNO3]<85%時,在室溫,Al耐蝕性也不好。
4)高硅鑄鐵。
Si質量分數>13%合金鑄鐵稱為高硅耐酸鑄鐵。對各種無機酸包括鹽酸均有良好的耐蝕性。
高硅鑄鐵中Si的質量分數一般不超過15%,否則會生成介穩定的脆性η相(Fe5Si2)。
金屬在人體環境中的腐蝕
01 金屬植入材料
植入材料是指用于制造人體內部的人工器官、小型監測儀器和治療裝置等植入器件。
整形外科中用于修復人體所使用的材料,以及用于義齒及人工齒根等方面的材料。植入材料也稱生物醫學材料。
特定的金屬材科、有機高分子材料和陶瓷材料。陶瓷材料即生物陶瓷材料,目前尚不成熟,高分子材料中只有超高分子聚乙烯是目前國際上普遍采用的人工關節塑料材料。
金屬植入材料在人體內應用部位是多種多樣的,人體具有高度腐蝕性的環境,對金屬植人材料的耐腐蝕性能的要求是相當重要的。
02 人體環境特點
人體環境由體液構成。體液(生理液)是質量分數約1%的NaCl、少量其他鹽類及有機化合物的充氣溶液。溫暖的海水相似。
人體環境復雜,活體,對其變化規律還缺乏足夠認識。
金屬植入材料在人體環境中可能發生多種腐蝕行為交織在一起,互相影響。
人體敏感性,要求植入材料達到很好修復和治療目的,應對周圍的組織、血液及對人體不產生有害的影響。
體液是典型電解質溶液, 電化學腐蝕基本規律對人體環境中植入材料的腐蝕完全適用。體液一般pH值中性,有時幾何原因或生理條件限制,導致氧的供應受限,局部體液成弱酸性,含H+,植入材料易點蝕。
金屬植入材料腐蝕屬于氧去極化腐蝕,其陰極過程:
陽極過程:
微電池陽極反應是金屬失掉電子的溶解反應,造成金屬離子遷移,植入金屬部件患者體液以及植入部件周圍的組織中存在著鈷、鉻、鎳、鉬、鈦等金屬離子。它們能否引起新陳代謝異常,對人體有干擾和毒性,這和植入材料耐蝕性與生物相溶性密切相關。
植入材料可能發生的腐蝕形態與工業金屬材料腐蝕破壞形式基本相同.因發生在特定的人體環境中,腐蝕危害更大。
03 人體環境中可能發生的腐蝕形式
1)均勻腐蝕
人體中,植入材料腐蝕減薄而喪失結構強度不是主要問題,問題是均勻腐蝕產物的生物相容性,增加病人痛苦甚至危及生命。
人體中金屬植入材料均勻腐蝕速度比一般工業材料的腐蝕速度低2~3個數量級。均勻腐蝕是大面積上發生,金屬離子進入到人體組織里的量還是相當可觀的。對金屬植入材料耐均勻腐蝕性能的要求更高,年失厚率應該不大于0.254μm。由于鈦的鈍化性能非常好.所以在外科植入材料中是令人滿意的。
2)點腐蝕
點腐蝕條件及破壞見3.2節。植入的金屬材料有不銹鋼、鈷基、鐵基合金,均系易鈍化合金,有鈍化膜。人體中用的不銹鋼耐蝕性能不太令人滿意。鈷鉻合金植入器件的強制取出率為3%,且未見明顯點腐蝕,而316不銹鋼的點腐蝕明顯。
模擬生理鹽液點蝕傾向研究表明,鈦合金及鈷鉻鉬合金點蝕傾向非常小,而不銹鋼點蝕傾向大。含Mo的不銹鋼抗點蝕,但Mo含量不足也會發生點蝕。對承載力大與骨骼部件,最好采用抗點蝕的不銹鋼及鈦合金。
3)電偶腐蝕
電偶腐蝕在多個零件構成的植入器件中尤其重要。
如果選用材料不同(電位差異)就容易產生電偶腐蝕。
如骨板和螺釘。
手術器械與植人材料間也可能引起電偶腐蝕。金屬切屑與未經過強烈變形的同種材料接觸時也會引起電偶腐蝕。
4)縫隙腐蝕
多零件植入裝置,特別是骨板和螺釘,會遭受縫隙腐蝕,不銹鋼植入器件的縫隙腐蝕是一種重要腐蝕現象。取出的多零件植入裝置中,有50%遭縫隙腐蝕。強制取出率表明,縫隙腐蝕僅次于均勻腐蝕。
5)磨損腐蝕、晶間腐蝕
磨損腐蝕是由于植入器件之間反復的、相對的滑動所造成的表面磨損與腐蝕環境的綜合作用結果。
晶間腐蝕是不銹鋼最易發生的一種腐蝕形式,其危害是相當嚴重的。
制作醫用不銹鋼植入器件過程中必須避開材料的敏化溫度。
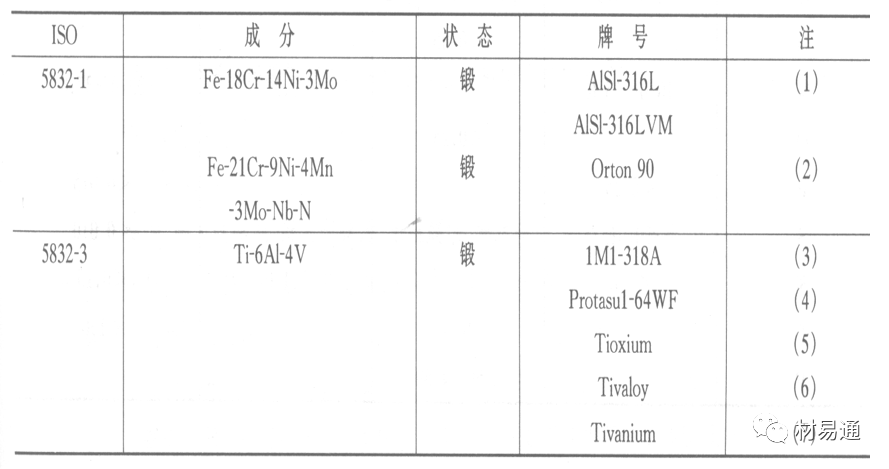
碳的質量分數降到0.03%以下,可以消除不銹鋼的晶間腐蝕。現用的醫用不銹鋼按ISO832/1國際標準規定,C的質量分數均低于0.03%。
6)腐蝕疲勞
金屬材料在交變應力與介質的共同作用下產生的斷裂現象為腐蝕疲勞。
人體下肢所用的植入器件,特別是髖關節植入器件,耐腐蝕疲勞性能是至關重要的。
腐蝕疲勞裂紋是從植人器件表面發生,對植入器件進行噴丸處理可提高疲勞壽命。
鑄造合金對腐蝕疲勞是敏感的,臨床表明鍛造合金對腐蝕疲勞斷裂敏感性小得多。
對承受高應力植入器件優先考慮采用熱壓和鍛造的方法制造。
04 常用金屬植入材料
植入材料的要求
人體環境的復雜程度幾乎無法模擬。對植入材料耐蝕性要求更高。
對植入材料要求主要有三個方面:材料與人體的生物相容性、在人體環境中的耐腐蝕性能以及植入材料的力學性能。
生物相容兩個方面:一是人體組織對植入材料的作用,即植入材料的腐蝕、斷裂、失效;另一個是植入材料腐蝕產物、磨損產物對人體組織的作用。
常用金屬植入材料有不銹鋼、鈷鉻鉬合金及鈦合金。
人工髖關節使用的金屬植入材料
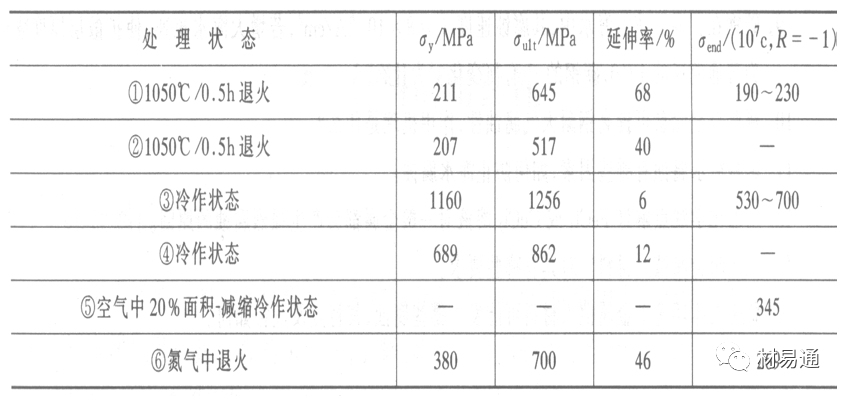
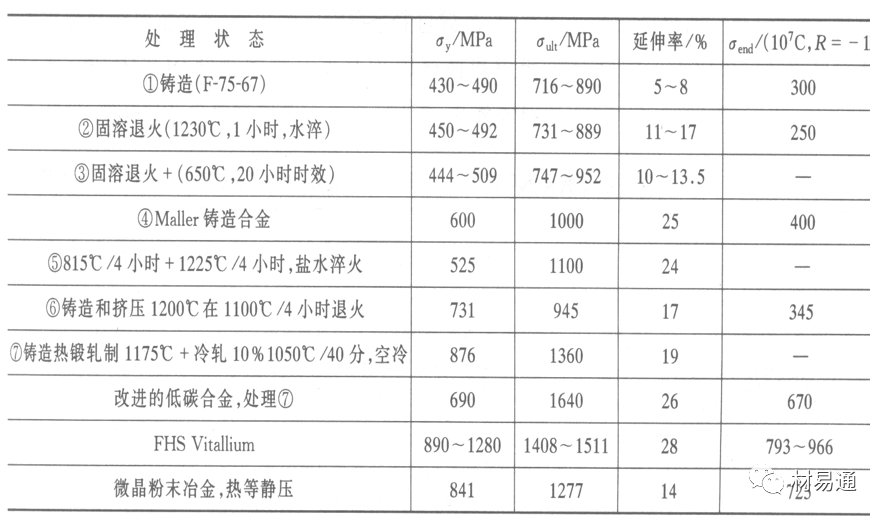
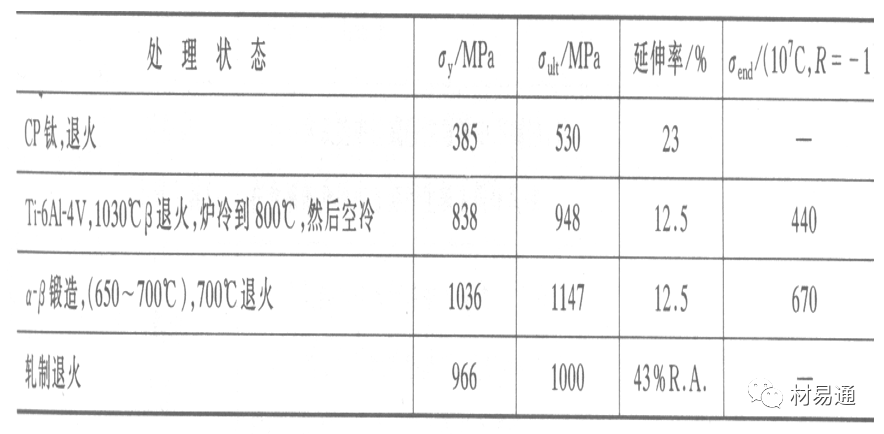
可植入不銹鋼的力學性能
Co-Cr-Mo合金的力學性能
鈦 及其合金的力學性能
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606
- 郵箱:fsfhzy666@163.com
- 腐蝕與防護網官方QQ群:140808414