細胞里面的生命活動井然有序,每一個部分都有其特定的結構,承擔不同的功能。生物大分子則是一切生命活動的最終執行者,它們主要是核酸和蛋白。核酸攜帶了生命體的遺傳信息,而蛋白是生命活動的主要執行者。自現代分子生物學誕生以來的半個世紀里,解析和分析生物大分子的結構、進而闡釋其功能機制一直都是現代生命科學的核心問題之一。
事實上,一切自然科學都涉及物質結構及結構間的相互作用為核心的研究方向,天文學研究宇宙、星體等的結構及其相互作用,粒子物理研究物質世界的基本粒子的結構和相互作用,甚至包括應用性很強的材料科學都是以研究新型材料的結構和性質等為核心。結構生物學研究的直接目的是弄清楚生命大分子結構,從而更好地理解生命,理解這個自然界中“逆熱力學第二定律”而誕生的奇跡;最終目標是公眾通常關心的實用價值。
像數學物理公式不會直接造出飛機、導彈、計算機一樣,蛋白質結構這樣的基礎研究不會直接轉化為人們生產生活的必須物品。比較具體的應用,如藥物設計、疫苗開發、醫療診斷和蛋白質分子性能改造(如科學實驗或工業生產中酶活性穩定性優化)等是蛋白質結構研究比較容易被大眾所理解的一個方向,但卻只是其研究價值的一個側面而已。
蛋白質結構如同生命科學里的數學公式和物理定律,甚至在以后會充當生命科學里面的“化學元素周期表”,除了幫助發現或設計新藥等,它更重要的價值是作為最基礎最上游的研究之一,通過影響一切與其密切相關的下游科學和技術,從而改變我們的世界。
結構生物學最早誕生于上個世紀中葉,它是一門通過研究生物大分子的結構與運動來闡明生命現象的學科,在其發展史上有兩個里程碑式的事件,一個是 DNA雙螺旋結構的發現,另一個肌紅蛋白(Myglobin)晶體結構的解析,這兩個事件都是上個世紀最重要的革命性科學進展,均在劍橋MRC分子生物學實驗室完成,并且都于1962年獲得了諾貝爾獎(一個生理學或醫學獎,一個化學獎)。同時它們都是最早使用X射線的方法來解析生物大分子結構,而這個方法在過去半個世紀里,一直占據結構生物學的統治地位。
在當今結構生物學研究中普遍使用的冷凍電鏡,是上個世紀七八十年代開始出現、近兩年飛速發展的革命性技術,它可以快速、簡易、高效、高分辨率解析高度復雜的超大生物分子結構(主要是蛋白質和核酸),在很大程度上取代并且大大超越了傳統的X射線晶體學方法。
革命性的冷凍電鏡技術
冷凍電鏡并不是這兩年才建立的。在蛋白質X射線晶體學誕生大約10多年以后的1968年, 作為里程碑式的電鏡三維重構方法,同樣在劍橋MRC 分子生物學實驗室誕生,Aron Klug教授因此獲得了1982年的諾貝爾化學獎。另一些突破性的技術在上世紀70年代和80年代中葉誕生,主要是冷凍成像和蛋白快速冷凍技術。這里面的代表科學家有Ken Taylor, Robert Glaeser和Jacques Dubochet等。
快速冷凍可以使蛋白質和所在的水溶液環境迅速從溶液態轉變為玻璃態,玻璃態能使蛋白質結構保持其天然結構狀態,如果以緩慢溫和的方式冷凍,這個過程會形成晶體冰,生物分子的結構將被晶格力徹底損壞。低劑量冷凍成像能夠保存樣品的高分辨率結構信息,確保了從電鏡圖形中解析蛋白質結構的可能性。與此同時Joachim Frank等則在電鏡圖像處理算法方面奠定和發展了這項技術的理論基礎。由此冷凍電鏡的雛形基本建立,總的思路為:
1)樣品冷凍(保持蛋白溶液態結構);
2)冷凍成像(獲取二維投影圖像);
3)三維重構(從二維圖像通過計算得到三維密度圖)。
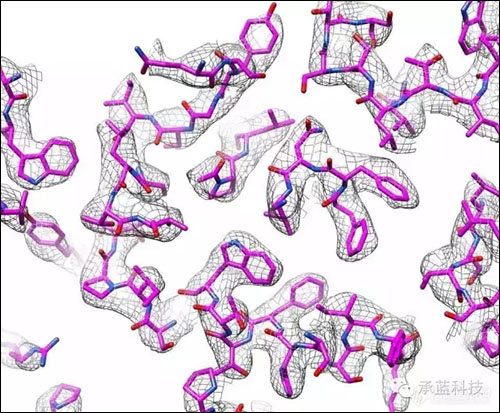
該方法為生物大分子結構研究提供了一個和X射線晶體學完全不一樣的、全新的思路。但是由于技術方法的瓶頸,在此后30多年的時間里只能做一些相對低分辨率的結構解析工作,在分辨率上一直不能和X射線晶體學比較,甚至一度被嘲笑為“blob-ology”(英文諷刺語,“一坨輪廓的技術”)。
但對于冷凍電鏡來說,技術難點遠非單純冷凍。冷凍成像和圖像處理算法一直都是瓶頸。從冷凍電鏡技術誕生以來的近30年時間里,其一直都有進展,只是相對比較緩慢。
最重要的革命性事件大約發生在兩三年前:一個是直接電子探測器的發明,另一個是高分辨率圖像處理算法的改進。MRC分子生物學實驗室的兩位科學家Richard Henderson和Sjors Scheres在這次革命中起了關鍵作用。
Richard Henderson是探測器方面的先驅,而Sjors Scheres則因他設計的Relion程序而名聲大噪,他們由此當選為《自然》雜志2014年“十大科學進展年度人物”。兩位科學家一個從硬件,一個從軟件將冷凍電鏡技術推向了巔峰,將冷凍電鏡技術的分辨率推向了新高度。
和此前使用的CCD相比,新發展的直接電子探測器不僅在電鏡圖形質量上有了質的飛躍,同時在速度上大幅提高,還可以以電影的形式快速記錄電鏡圖像。這些特性同時也伴隨著電鏡圖像處理方面的重大變革,電鏡技術此前在分辨率上的一個主要瓶頸是電子束擊打生物樣品造成的圖像漂移和輻射損傷。有了快速電影記錄,我們就可以追蹤圖像漂移軌跡而對圖像做運動矯正和輻射損傷矯正,大大提高數據質量。
盡管如此,電鏡圖像處理一直都是一項極具挑戰性的任務,主要的問題是冷凍電鏡的圖像噪音極高、信號極低,而我們的目標是從中提取近原子分辨率的結構信息,這就像在一個機器轟鳴的工廠里監測一只螞蟻爬行的聲音。冷凍電鏡科學家就是要完成這項艱巨的任務,并且真的做到了。有了硬件和軟件方面的雙重提高,冷凍電鏡的分辨率目前已得到了極大的提高,可以和晶體學相媲美;并且在其它方面已經大大超越了晶體學。
主要體現在下面幾個方面:
第一,不需要結晶,研究對象范圍大大擴展,研究速度大大提高。對于小分子,比方說無機鹽礦物質等自發就能長出晶體,小而且穩定的蛋白質目前來說結晶并不困難,但是這類意義重大的蛋白幾乎都已經解析完了,在科學上沒有任何重大意義;當今時代,小蛋白已經完全不能滿足科學家們強烈的探索欲望,結構生物學研究的對象越來越大,體系越來越復雜,結晶幾乎成為不可能的事情,即使能結晶,也不一定衍射,有衍射也不一定能得到原子分辨率結構。
多年前,許多蛋白質晶體科學家為了完成一項艱巨的任務,一個課題少則5到10年,多則20年,核糖體從上世紀80年代初首次長出晶體到 2000年左右最終拿到原子分辨率結構整整經歷了20年;線粒體呼吸鏈復合物I從上世紀90年代初研究,第一次報道完整晶體結構大約是20年以后。
而冷凍電鏡方法跳過超大分子復合物結晶難的這層技術屏障,以直接解析復合物的溶液狀態的結構為目標。
現在利用這項技術,在MRC-LMB一周時間就可以解析一個新的核糖體結構;英國皇家學會主席、MRC-LMB結構中心主任 Venki Ramakrishnan 教授,因為核糖體的晶體結構研究而獲得2009年諾貝爾化學獎。他的實驗室在2014年發表了最后一篇晶體結構文章,此后的文章全部以冷凍電鏡為主。哥倫比亞大學有一個非常執著的博士后,研究蘭尼堿受體(Ryanodine Receptor)晶體結構長達十年之久,最后放棄了晶體,轉向了冷凍電鏡技術,同時與清華大學教授顏寧和LMB的Scheres研究組合作,幾個月就解決了這個難題,并且達到近原子分辨率。
第二,樣品需求量小,樣品制備快,可重復性高。重要生物樣品都是非常珍貴的,總體來說是以微克或者最多以毫克來計量,即使得到這點樣品,也要花費生物學家幾周、幾個月甚至更長的時間(大多數時候都需要摸索各種條件使樣品處于相對穩定的狀態,以便做進一步結構研究)。
蛋白質晶體一般要求高濃度大體積,沒有量變就沒有質變。而同樣量的蛋白可以稀釋以后制備若干冷凍電鏡樣品,每個樣品有成百上千的區域,每個區域有幾百個小孔,每一個小孔甚至可以收集多張照片。解析一般蛋白的原子結構需要幾萬個顆粒,而對于高對稱性的樣品幾千個顆粒就足夠。
第三,可以研究天然的、動態的結構。X射線晶體學研究生物大分子結構的一個主要弱點是無法拿到天然的動態的結構,這是因為研究人員無論如何也無法繞開結晶這個過程。冷凍電鏡就是要做這件事情:直接解析天然的、溶液態的、動態的(dynamic),甚至原位(in situ)的結構,從而理解生命分子如何在空間和時間兩個尺度上以活的動態的方式發揮功能。
晶體學只能嘗試不同的條件獲得生物大分子某個或者某些固定的狀態,而且容易出現晶體堆積引起的不真實相互作用方式。形象地說,冷凍電鏡可以制作完整的高清電影,晶體學只能從電影里截屏。
第四,技術革命還將開啟巨大的潛在醫療價值。冷凍電鏡技術方法在時間和精度方面的大幅度提高有時會導致不可預測的重大科學和應用價值。比如,活體病毒結構分析如果可以在分鐘級別完成,這將有可能轉化為潛在的醫療檢測手段:從病人體內抽取血樣或感染組織細胞,幾分鐘以后,非常清晰明了地展現病人在細胞內部結構層面的異常狀況,甚至給出局部的原子結構圖,從而給出精準的治療方案。這個想法現在可能聽起來有點像笑話,或許再過若干年人們就不這樣認為了。
當然冷凍電鏡的革命性不僅僅體現在上述四方面,在此就不一一列舉。有關冷凍電鏡更加詳細的介紹,可參見筆者等2010年的中文綜述(《生物物理學報》,2010年7月,第26卷,第7期: 533-559)。文章中對未來幾年的發展趨勢所做的展望,如直接電子探測器的普及、非對稱性蛋白復合物近原子分辨率結構解析、冷凍電鏡相關計算性能的大規模提升等等,目前絕大多數都在過去的兩三年內得以實現并飛速發展。
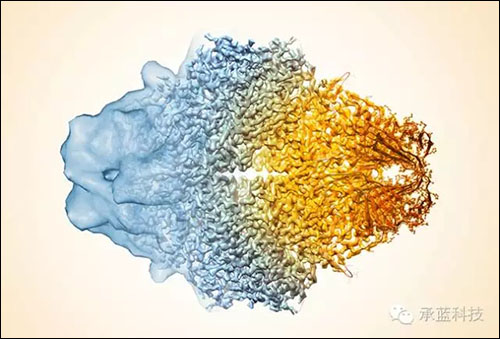
華人學者在冷凍電鏡領域的貢獻
在冷凍電鏡的這場技術革命中,華人科學家功不可沒,在某些方面甚至獨領風騷,做出了諸多重大成果。
加州大學舊金山分校(UCSF)的華人科學家程亦凡教授在2013年底,首次利用冷凍電鏡技術解析近原子分辨率膜蛋白結構,這項成果在業界引起了巨大轟動。原因在于當所有電鏡結構生物學家還在討論膜蛋白到底能不能利用冷凍電鏡技術看到二級結構,也是通常我們認為的中等分辨率水平的時候,程亦凡教授研究組直接解析了TRPV1 這個膜蛋白3.3埃近原子分辨率的結構(Nature,504:107–112)。
筆者曾在該文章發表的半年前在一次國際會議上和冷凍電鏡領域頂級學者深入討論過如何獲得清晰的膜蛋白α-螺旋結構,對方給出了悲觀的結論:“恐怕不太可能,至少最近兩年不可能”。
事實上,此前蛋白質晶體學家已經有所耳聞“冷凍電鏡可能在未來幾年會超越并且取代晶體學”,但是誰也沒想到會是以這樣快速和震撼的方式登場,這在某種程度上引發了不少蛋白質晶體學家的“職業恐慌感”。這項成果的兩個共同第一作者廖茂福、曹爾虎也都是非常杰出的青年華人科學家。
加州大學洛杉磯分校的周正洪教授早在2008年到2010年左右,在這場電鏡技術革命來臨之前,在各項技術條件尚未成熟的情況下解析了一系列近原子分辨率病毒結構。當時采用的是傳統膠片來成像,任務非常艱巨,連他還在上學的兒子也都幫忙一起洗膠片。張興博士在這一系列稍早的重要成果中充當了先鋒。早在2008年,第一個近原子分辨率的冷凍結構,也即3.8埃輪狀病毒就是張興博士作為第一作者完成的(PNAS, 105(6): 1867-1872)。從1968年Aaron Klug創立電鏡三維重構理論,到2008年人們首次看到通過冷凍電鏡獲得近原子分辨率結構,整整用了40年。
在國內,清華大學的隋森芳院士是我國冷凍電鏡領域的先驅,不僅德高望重,還培養了一大批優秀的青年科學家,包括清華大學的王宏偉教授以及 MRC-LMB的白曉晨和暢磊福博士等等。王宏偉早年在隋老師實驗室做研究生的時候,在我國研究設備和條件全面落后于國外的情況下依舊做出了許多非常出色的工作。
MRC-LMB的多位青年華人研究人員對冷凍電鏡發展都做出了重要貢獻。白曉晨博士在MRC-LMB首次使用直接電子探測設備Falcon I 和Sjors Scheres博士的新程序Relion,獲得了第一個不對稱樣品核糖體的近原子分辨率冷凍電鏡結構,打響了冷凍電鏡革命的第一槍,隨后解析了一系列核糖體和蛋白復合物結構。暢磊福博士在LMB首次獲得非核糖體不對稱蛋白樣品APC復合物的近原子分辨率結構,闡明了蛋白質泛素化的重要機理。筆者主要在LMB的Andrew Carter博士實驗室從事動力蛋白結構和功能研究,并成功解析動力蛋白激活因子Dynactin結構,提出了目前為止動力蛋白最詳盡可靠的運動和激活機制(Science, 347(6229):1441-1446. 封面文章),同時獨立發展冷凍電鏡技術方法。
1953年4月25日,MRC沃森和克里克在《自然》雜志發表DNA雙螺旋結構,61年后的同一天,我國科學家、中科院生物物理研究所的朱平和李國紅研究員在《科學》雜志以長文形式發表了30nm染色質冷凍電鏡結構(DNA雙螺旋之雙螺旋)(Science , 344(6182): 376-380)。這項工作是冷凍電鏡在核心生命科學問題中的成功應用,冷凍電鏡部分的工作主要是筆者在生物物理所的同學宋峰博士完成的。
生物物理所的程凌鵬博士(當前單位為清華大學)獲得國內本土第一個原子分辨率的冷凍電鏡結構,構建了蠶多角體病毒(CPV)的完整三維原子模型(PNAS,108(4):1373-1378)。筆者也參與了部分工作, 被其高質量、干凈的電子密度圖震撼。近期程凌鵬與劉紅榮博士合作,在國際上首次發表了CPV完整基因組和RNA聚合酶“原位三維結構” (Science, 2015, 349(6254):1347-50), 引起了很大轟動,這項成果是我國本土冷凍電鏡技術和生物學應用的雙重突破,被多名同行科學家稱贊為“里程牌式發現”。
我國著名科學家施一公最近發表了一系列重大蛋白復合物的冷凍電鏡結構,包括γ-secretase、spliceosome等,被譽為過去幾十年我國科學家對基礎生物學領域的最大貢獻。
另外,在歐美和中國本土還有一大批華人學者在冷凍電鏡或密切相關領域(cryoET等)做出諸多突破性成果,例如匹茲堡大學的張佩君教授(艾滋病毒結構研究),德克薩斯大學的劉俊教授(細菌運動,噬菌體結構等研究)等,由于時間和篇幅問題,無法一一介紹。
冷凍電鏡的未來展望
冷凍電鏡技術目前仍然在快速發展中,未來冷凍電鏡能做什么取決于這項技術能發展到什么程度。現代科學技術革命的一個最大特點是發展速度極其迅速,誰也不知道明天會發生什么,當然也不能十分準確的預知一個領域的發展方向。即便如此,筆者還是對這個領域有一些預測或期待(僅技術角度,不涉及具體生物學研究)。
1)超大規模、超快速度數據采集和處理。和晶體學相比,冷凍電鏡的效率在某些方面已經異常驚人。比如筆者近期與牛津大學王祥喜博士合作,在幾個小時以內就可以拿到完整甲肝病毒原子結構,而此前王祥喜博士花費近一年時間。
但目前來說,結構生物學的巨大轉型必須建立在速度和效率的雙重前提下。這需要硬件、軟件以及其它交叉學科等多方面的共同發展。
除了生物學研究應用,筆者一直致力于冷凍電鏡技術的發展,最近在提高電鏡數據處理結果可靠性和分辨率前提下,上千倍地提高了其中幾個環節,過去幾百到上千CPU小時的事情,現在幾分鐘到幾十分鐘就完成了。但是這只是部分環節,在其它方面依舊非常耗時,整個技術的各個環節如何全面高效高速地完成還需要更多的優秀人才參與。對硬件的發展方面筆者并不是很熟悉,預計在未來會出現超高速度的電子顯微鏡,大幅度提高電鏡原始數據的數量和質量。
2)大尺度、高分辨率、高動態的生物大分子結構解析。理論上,冷凍電鏡可像高清數碼攝像機拍電影一樣對生物大分子成像和重現其動態結構,研究深層機理。就目前而言,這一方面在技術上遠未成熟。大尺度、高分辨率、高動態這幾點拆解開來,每一個都不算太難,但是同時滿足這幾項需求幾乎成為不可能的事情。但是這是未來結構生物學的方向,我們不僅僅要看簡單的幾張靜態照片,我們還想看高清電影。
關于這一點,筆者需要強調一下結構生物學和動力學模擬的區別。結構生物學的動態結構目的是以實驗手段完整復原自然狀態的動態結構,理解其中機理,是從實驗數據出發“重現大自然原貌”的過程,是完完全全可靠的實驗結果。而動力學模擬是從已有的理論或經驗性的物理學規律出發預測一個生物大分子的動態特性,存在巨大的不確定性,其結果可靠性較差。期待在未來的某個時刻,兩者會像上個世紀的理論物理和實驗物理一樣完美地結合,相互促進。
大尺度復雜生物系統的高分辨率、動態機理研究涉及諸多學科,不是冷凍電鏡一項技術就可以完成的,需要多學科科學家共同參與完成。
3)高分辨單分子及原位結構研究。目前的結構生物學,無論晶體學、冷凍電鏡還是核磁共振主要還是在研究“群體”結構。冷凍電鏡相對晶體學在這一方面已經有了大幅度提高,可以通過分類的方法研究群體結構中的每一類結構。但實際上每個分子在時間和空間上除了共性,也必然有特性,如果一種方法強大到可以測得單個分子的高分辨率結構,這必然導致巨大革命,使得人們發現許許多多在群體結構研究層次上無法發現也無法理解的大量規律。
注意這里強調的是單分子“高分辨率”結構,而不僅僅是單分子結構。單分子結構我們目前可以使用比如冷凍斷層成像(cryoET)的手段獲得,但是分辨率非常低,在如此低分辨率情況下,別說個體差異,很多群體結構差異都值得嚴重質疑。或許冷凍電鏡技術若干年以后會實現這個目標,或許永遠都不可能,或許這個目標被另外一個全新的技術徹底取代,冷凍電鏡從此退出歷史舞臺。
冷凍電鏡:一個高度交叉的學科
冷凍電鏡領域一直是多學科高度交叉和相互促進才誕生的一個奇跡。數學、物理、化學、材料、計算機、軟件、機械及自動化、精密儀器儀表等等缺一不可,當然最終的核心是生命科學(作者注:此處僅從結構生物學角度分析,并非泛指一般意義上生命科學是一切學科的核心)。生命科學提出問題,其它所有學科相互結合產生更好的解決方案。通過這些解決方案,發現更多神秘的生命現象,從而提出新的問題,誕生新的技術。
舉個例子,冷凍電鏡圖像信噪比極低,沒有科學家的雄心勃勃,沒有大批信號分析、圖像處理甚至數學家的參與是不可能完成這樣艱巨的任務。同時冷凍電鏡領域的一些發現或需求,也為其它領域的科學家提供靈感來源和新的研究思路。MRC-LMB作為現代分子生物學的發源地和近兩年來飛速發展的冷凍電鏡技術核心研究機構,其一大特點就是多學科“零距離交叉”。從半個世紀前的DNA雙螺旋模型、肌紅蛋白晶體結構等到近兩年冷凍電鏡技術革命,一直將這一理念體現得淋漓盡致。技術的發展和重大科學問題的解決幾乎都是同時進行的,當然科學問題或應用價值始終是核心和最終驅動力,脫離科學和應用需求的技術發展是沒有意義的。
另外一個比較具體的例子是筆者此前思考過的一個問題。在電鏡領域出現直接電子探測設備之后,MRC-LMB的兩臺高端電鏡,每天產生5到10T 的數據量,近期正在調試第三臺,也許不久的將來,超大數據、超快速度電鏡就會投入生產,這些將會導致全世界各個研究機構普遍出現一個嚴重的技術問題,就是如何高效、無損、快速地進行數據壓縮存儲和數據處理,當然這里的無損是相對特定生物樣品和特定目標分辨率而言。這或許會引起一些信號處理和圖像壓縮方面的研究人員的興趣。
隨著冷凍電鏡對生物大分子復合物高分辨率結構研究趨于成熟,更加復雜的動態機理研究是必然趨勢,這是冷凍電鏡技術發展的一個潛在可能性。但是復雜生物體系的深入研究需要解決一系列數學理論、物理、計算難題,有的可能甚至超出了這些學科目前的研究范疇。近些年比較現實可行的是通過冷凍電鏡手段,對特定蛋白復合物非隨機情況下的高分辨連續動態構象進行分析。筆者認為,專業數學家的參與會大大加速冷凍電鏡技術在這些方面的發展。
生命體高度復雜,充滿很多未知的和未被闡述清楚的規律,這里面有成千上萬的生物大分子復合物,每一個復合物又與其它若干分子或復合物相互作用、相互影響,深入再深入地理解生命本質一直都會是冷凍電鏡的重要方向。冷凍電鏡是強大的基礎研究手段,它通過解析高度復雜的生物大分子結構,幫助人們更好地理解生命規律,從而影響生命科學相關的一切下游學科和技術,當然也包括更好的發現和設計藥物、醫療診斷等具體應用。我們期待在不久的將來,冷凍電鏡技術會對科學研究和社會發展等方方面面都產生巨大影響。
更多關于材料方面、材料腐蝕控制、材料科普等方面的國內外最新動態,我們網站會不斷更新。希望大家一直關注中國腐蝕與防護網http://www.ecorr.org
責任編輯:王元
投稿聯系:編輯部
電話:010-62313558-806
中國腐蝕與防護網官方 QQ群:140808414
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《中國腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護網官方QQ群:140808414





