第四章 局部腐蝕
4.1 點蝕
Vol.4.1.5
影響壓力容器點蝕的主要因素
自上世紀30年代至今,國內外對不銹鋼點蝕形核機制的探索從未間斷。點蝕的最初位置一直被認為“隨機而不可預測”,國內外有關研究表明,鋼中非金屬夾雜物是點蝕的主要誘發源,其中硫化物夾雜誘發點蝕最為明顯。沈陽材料科學國家(聯合)實驗室馬秀良研究員領導的團隊利用高分辨率透射電子顯微技術,發現不銹鋼中存在的氧化物納米八面體似微小“腫瘤”,是產生點蝕的原因,研究表明,在一定的介質條件下硫化錳的局域溶解正是起源于它與“腫瘤”之間的界面處,并由此逐步向材料體內擴展,并且,氧化物納米八面體使得硫化錳的局域溶解存在速度上的差異。在此基礎上,該研究小組與英國貝爾法斯特女王大學的胡培君教授合作,確定出具有強的活性、易使其周圍硫化錳快速溶解的氧化物納米八面體具有以金屬離子作為其外表面的特征,類似于“惡性腫瘤”;相反,較低活性的納米八面體則以氧離子作為其外表面,類似于“良性腫瘤”。這一發現為揭示不銹鋼點蝕初期硫化錳溶解的起始位置提供了直接的證據,使人們對不銹鋼點蝕機理的認識從先前的微米尺度提升至原子尺度。
影響金屬材料點蝕性能的因素可以歸納為3方面:材料因素、環境因素和電化學因素。
01 材料因素
①合金成分
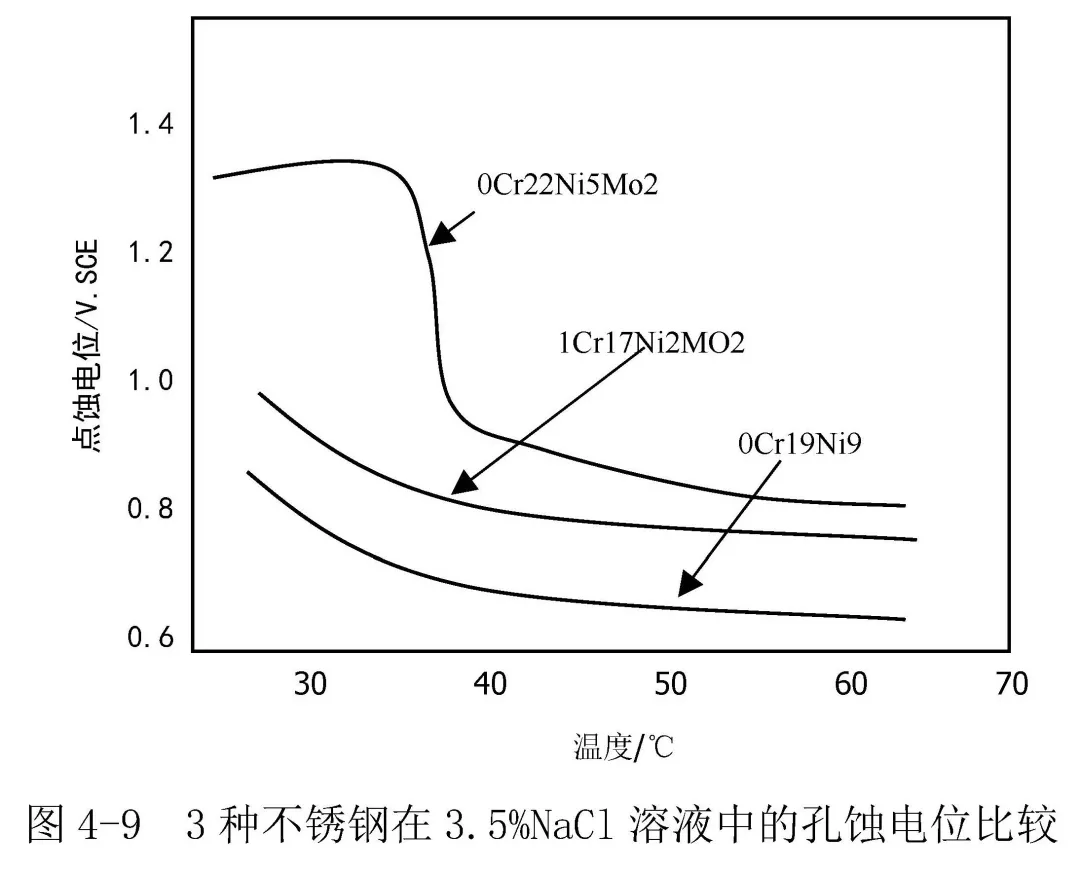
對不銹鋼來說,鋼中的含C量越低,抗點蝕能力越強。S、P、Se等雜質元素對抗點蝕不利。高純化對耐點蝕性能的改善是因為減少了硫化物夾雜和碳化物的原因。原田研究了3種不銹鋼在NaCl介質的點蝕臨界電位,圖4-9,表明含Mo量高的奧氏體不銹鋼點蝕臨界溫度明顯較高;含Mo量相同時,含C量較低、含Cr較高的雙相鋼點蝕臨界溫度較高。Cr、Mo、Ni及N等元素是使合金具有良好抗點蝕性能的主要合金元素,增加Cr含量能提高鈍化膜的穩定性,即提高Eb值。如圖4-10,為S31603和Incoloy 825 按 GB/T 17897[1]、ASTM G48[2],在35℃±1℃,6%(mass)FeCl3+0.05M HCl溶液中,對試樣進行24h試驗后的腐蝕形貌,可以明顯看出Incoloy 825抗點蝕性能大大優于S31603。
目前通常用抗點蝕當量PRE(Pitting Resistance Equivalent)來表征不銹鋼的抗點蝕性能,也有用抗點蝕當量數PREN(pitting resisitance equivalent number,FPREN)來表示。在不銹鋼的成分與綜合耐蝕性之間已推導出一些公式,并在不銹鋼的標準中也已體現。EN 10088-1[3]、ASTM A240[4],A789[5],A790[6]及A959[7]明確規定式(4-2)是奧氏體不銹鋼、雙相不銹鋼及鐵素體不銹鋼的PRE計算公式,PRE數值越大,表明不銹鋼的耐蝕性越好。

由于這些公式應用甚少,沒有得到不銹鋼標準的認可,應用在某些特殊場合。
PRE可作為不銹鋼一般綜合耐蝕性的標示方法,為綜合耐蝕性的相對性能,用于不同牌號成分的耐蝕性排隊比較,不是耐蝕性的絕對性能;PRE只考慮了材料成分,沒有考慮熱處理狀態,只適用固溶態或退火態耐蝕性能的比較。因敏化作用而析出高鉻(鉬)相(碳化物、氮化物、σ相等金屬間化合物)及貧Cr(Mo)區時,對耐蝕性的影響應另行考慮[8]。
鉬含量對合金點蝕敏感性的影響還可用臨界點蝕溫度(Critical Pitting Temperature , CPT,℃)來表示,對于18Cr鐵素體不銹鋼:
CPT(℃)= 2.5 + 3.5×Mo×100 (4-9)
對18Cr奧氏體不銹鋼:
CPT(℃)= 5+7×Mo×100 (4-10)
鋼中其它合金元素的影響:
C:以固溶態形式存在于鋼中時,無影響。以碳化物沉淀形式存在時,可使鐵素體鋼和奧氏體鋼的點蝕敏感性增大,特別是在敏化條件下影響更大;
Si:在Cr-Ni奧氏體鋼中的加入可明顯地提高其耐點蝕性能,但這僅發生在Si以固溶態形式存在時,若Si在晶界偏聚或以夾雜物形式存在,則硅及其化合物對耐點蝕性表現出有害的影響;
Mn:在18Cr-5Ni鋼中添加質量分數5.7%~15%Mn嚴重降低其鈍化能力和耐點蝕性能。鋼中錳與硫生成的MnS或(Mn,Fe)Sx夾雜常成為點蝕萌生源。但若錳以固溶狀態存在并參與鈍化膜的形成,則能改善抗點蝕性;
Cu:在不含鉬的鋼中,銅無影響,有鉬存在時,銅表現出較輕微的不利影響;
B:存在于固溶體中時有益,形成金屬間化合物沉淀時則有害。也曾發現在S30408不銹鋼中,硼可阻止Cr23C6的沉積,因而有利于提高其耐點蝕性以及敏化條件下的耐晶間腐蝕性能。
②顯微組織
不銹鋼的顯微組織對合金抗點蝕性能起著重要作用。各種析出相,如硫化物夾雜、δ鐵素體,σ相、α相,沉淀硬化不銹鋼中的強化沉淀相、敏化的晶界以及焊縫等都是點蝕敏感的部位;
③熱處理
奧氏體不銹鋼在一定溫度范圍內熱處理,會發生敏化作用,敏化的不銹鋼Cr(及Mo)的碳化物M23C6沿晶界析出,導致鄰近區域的貧Cr(及貧Mo),因而對晶間腐蝕和點蝕均敏感;
④冷加工
冷加工對點蝕的影響較為復雜,它與金屬組織結構的變化,與非金屬夾雜物的第二相沉積物的分布以及鈍化膜的性能等有關。因而對不同材料而言,影響途徑也不一樣。一般來說,冷加工對點蝕電位的影響不大,但冷加工通常使點蝕密度增加,這是因為冷加工增加位錯密度,而位錯在表面露頭處容易生成點蝕坑。對奧氏體不銹鋼進行冷加工的研究表明,冷加工后試樣表面的點蝕坑數目增多和蝕坑的尺寸變小。冷加工對奧氏體不銹鋼和金屬鎳有相似的影響趨勢,點蝕總面積及點蝕電流密度隨變形量增加而變大,點蝕數目也隨之增加。
⑤表面狀態
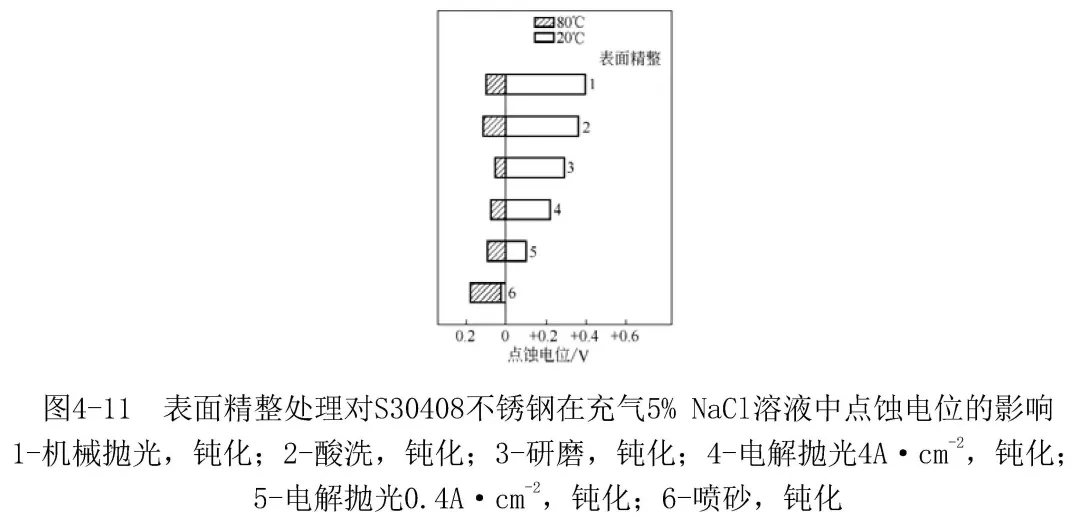
關于表面粗糙度對不銹鋼點蝕性能影響情況見圖4-11[9]。在同樣的材料環境體系中,若表面粗糙度不同,其點蝕電位的差別可在0.4V以上。研究結果表明,與粗糙的不銹鋼表面相比,在光滑的不銹鋼表面上亞穩態蝕點的產生與生長更加難以進行,早期點蝕敏感性越小[10]。不銹鋼由焊接所產生的氧化膜對合金在氯化物溶液中的抗點蝕性能是不利的。鈍化處理的主要作用是溶解不銹鋼表面的夾雜物和污染物,它還可去掉表面的硫化錳夾雜,從而改善不銹鋼的抗點蝕性能。
鈍化膜厚度和狀態對點蝕的影響有:
a.對均質膜而言,在某一厚度以內,點蝕誘導時間隨膜厚增加而線性增長;
b.厚且多孔性膜,點蝕誘導期較短;
c.點蝕電位與膜厚無關;
d.溶液中有Cl-存在時所生成的膜比無Cl-存在時所生成的膜要厚;
e.氧化膜電學性能。對19Cr10Ni不銹鋼在150~400℃空氣中生成的氧化膜的研究結果表明,隨著處理條件的不同,氧化膜表現出n型或p型半導體性質。n型氧化膜的陽極轉換系數(αA)低,點蝕敏感性大,p型氧化膜的αA高,點蝕敏感性小。
02 環境因素

①鹵素離子及其它陰離子
溶液中存在活性陰離子,是發生點蝕的必要條件。很多不銹鋼等耐蝕合金壓力容器設備的點蝕是由于含鹵素離子的介質所引起,其中Cl-對點蝕電位的影響最大。一般認為,點蝕只有當鹵素離子在溶液中達到某一濃度以上時才產生,且該濃度界限因材料和介質溫度、組分而異。產生點蝕的最小濃度可以作為評定點蝕趨勢的一個參量。在氯化物中,鐵、鎳、鋁、鈦、鋯及其合金均可能產生點蝕,Br-、I-對點蝕也有—定影響。對鐵和鋁基合金,C1-的侵蝕性高于Br-和I-,對鈦和鉭情況則相反。含F-的溶液幾乎不引起鋼的點蝕,其原因是,有氟化物存在時,鈍態金屬的溶解速度增加,即全面腐蝕加速,故不引起點蝕。
鋁及其合金對點蝕的敏感性比鋼更大,多種陰離子均能導致它們產生點蝕,其中包括氯化物、溴化物、碘化物、氟化物、高氯酸鹽、硫氰化物、硝酸鹽等。
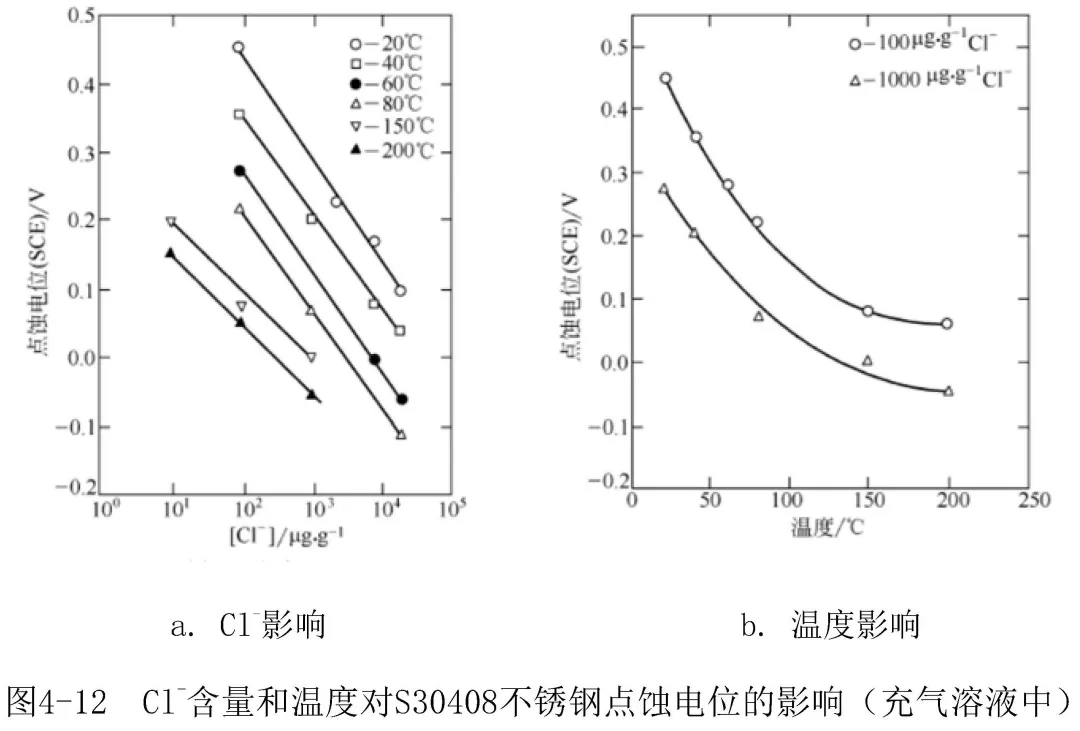
對不同溫度(20~200℃)下C1-濃度對S30408不銹鋼點蝕電位Enp(Eb)的影響的研究,如圖4-12a所示,圖4-12b表示在Cl-含量為100和1000μg?g-1時,Enp與溫度的關系,表明Cl-含量或溫度上升,Enp下降。


②溶液中的陽離子和氣體物質
腐蝕介質中,金屬陽離子與侵蝕性鹵化物陰離子共存時,氧化性金屬離子,如:Fe3+、Cu2+和Hg2+對點蝕起促進作用。這是因為,這些高價陽離子能被還原成金屬或低價離子,這些反應的氧化還原電位高于點蝕電位,起到去極化作用而促進點蝕。這也正是FeCl3廣泛用于不銹鋼點蝕試驗的加速試劑的原因;
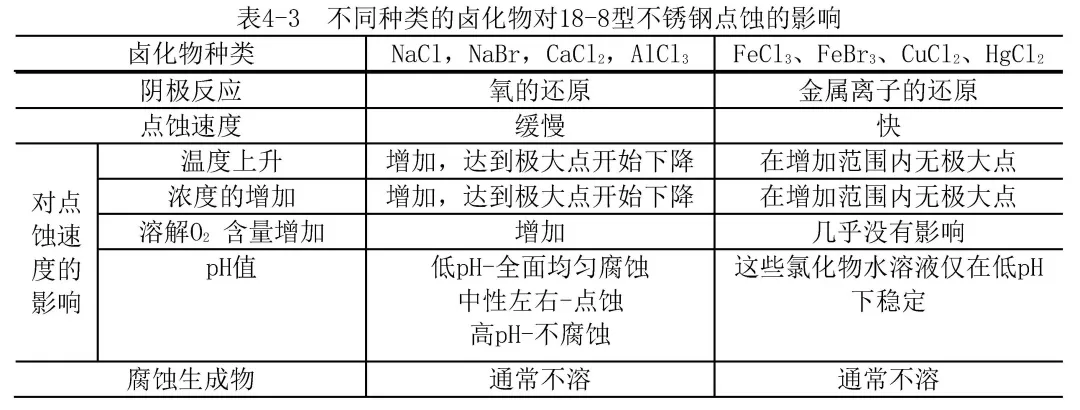
③溶液pH值
在溶液pH值低于10時,對二價金屬,如Fe、Ni、Cd、Zn和Co等,其點蝕電位與pH值幾乎無關,在pH高于10值時,點蝕電位變正。
各種不銹鋼的點蝕電位在pH值10~11.5的堿性溶液中,pH值升高,點蝕電位明顯變正,在其它范圍時,pH值影響甚小。對于430(17Cr)和S30403不銹鋼,在 pH 2~11.5之間,pH值每變化1時,Eb變化約10mV,S31608不銹鋼在pH4~9范圍內,其值不變,見圖4-14。當pH值低時(在強酸性溶液中),金屬易發生嚴重的全面腐蝕,而不是點蝕;
④介質流速
在靜止的介質中易產生點蝕,而在流動的介質中,則不易產生點蝕。這是由于溶液的停滯狀態可使陽極區保持強酸性溶液,不易同陰極區的整體溶液混合。流速提高時,減少了附著物的停滯,減輕了溶解氧的局部差異而使點蝕減少。更進一步的解釋則要涉及到流速對Cl-吸附以及對蝕孔內外溶液的質量轉移和混合等因素的影響。
試驗證明,對不銹鋼有利于減少點蝕的流速為1m·s-1左右。當流速進一步增大,出現湍流時,鈍化膜被破壞,點蝕隨之嚴重;
⑤介質溫度的影響
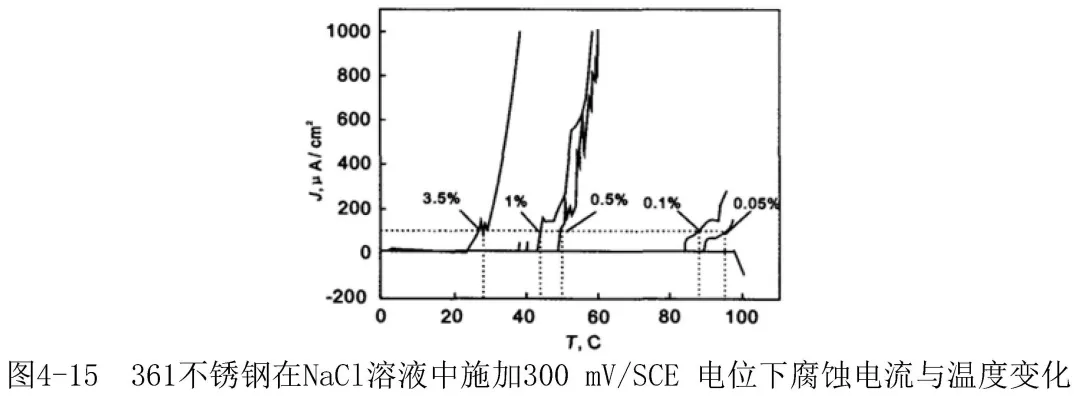
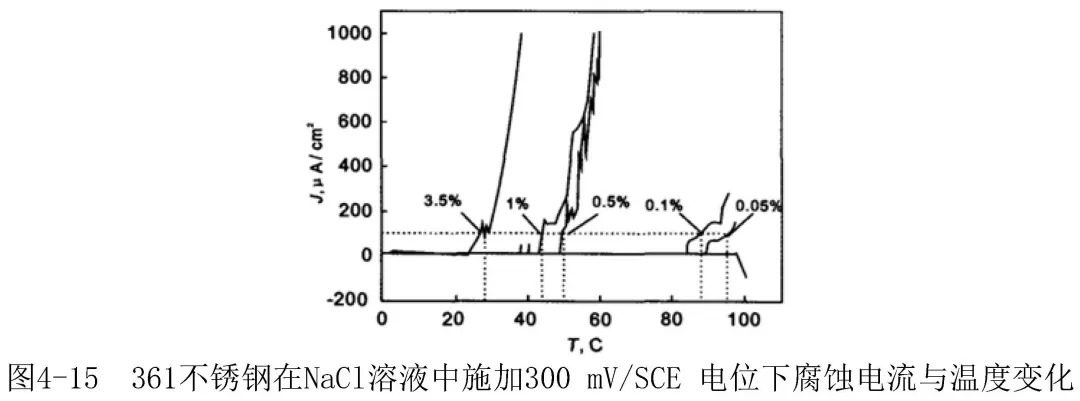
隨介質溫度的提高,不銹鋼點蝕電位降低。在含Cl-介質中,各種不銹鋼都存在臨界點蝕溫度(CPT),在這一溫度點蝕幾率增大,隨溫度升高,點蝕易產生并趨于嚴重。圖4-12b可以看出,在相同條件下,溫度升高,點蝕電位快速下降。圖4-15為S31608不銹鋼在不同濃度的NaCl溶液中腐蝕電流密度與溫度的關系[11],可以看出,隨溫度升高,在300mV的極化電位下,達到臨界電流密度的NaCl濃度顯著降低。圖4-16為S32168不銹鋼在6%(mass)的FeCl3溶液中20℃和50℃下,24h后的腐蝕宏觀形貌,可以看出,50℃的點蝕密度和點蝕孔徑較20℃的明顯增大;

⑥鐵和鋼在非鹵化物溶液中的點蝕
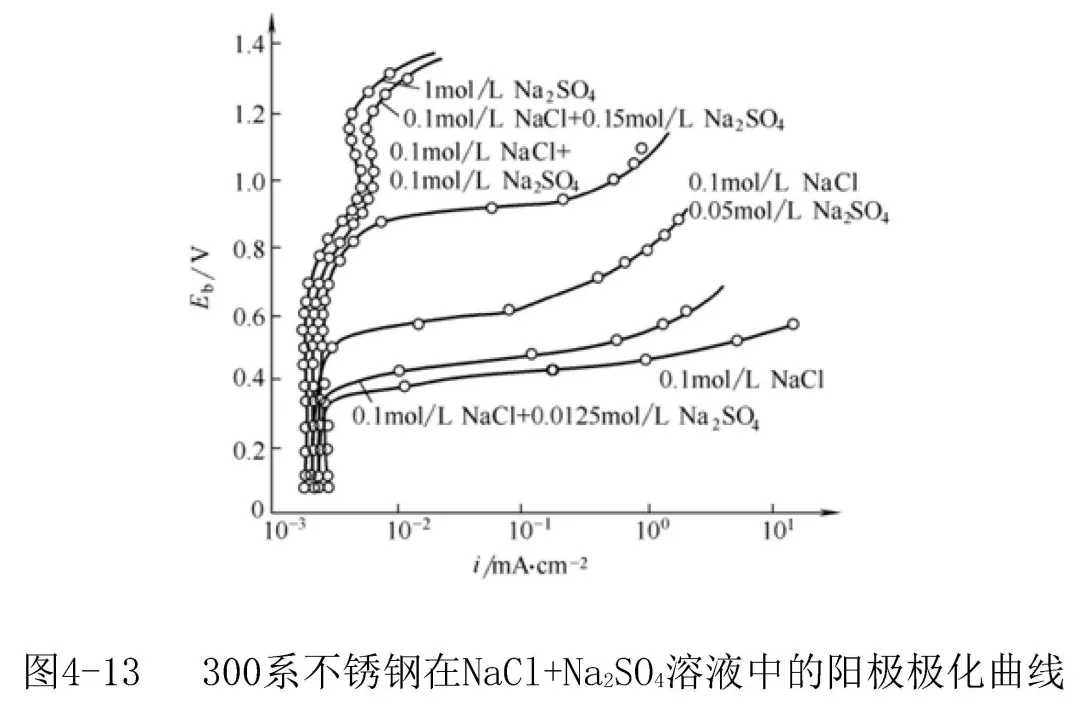
鐵和鋼的點蝕可在與非鹵素離子相接觸且在高于鈍化區某一臨界值的電位下發生,如,硫酸鹽溶液中在活化-鈍化電位區,硅酸鹽溶液中在過鈍化電位下均曾觀察到鐵的點蝕;在H2SO4 + H2S或 NaSCN+H2S溶液中也曾觀察到不銹鋼的點蝕。鋼在含氧高溫水中進行SCC試驗時,常觀察到點蝕成為裂紋源的情況,且氧含量增加時,蝕孔也增多。
03 點蝕產生的電化學條件
金屬的電位在特定的電位以上才會發生點蝕,環狀陽極極化曲線(圖4-17)上的特征電位Eb和Ep可以用來表示金屬的孔蝕傾向。Eb稱為擊穿電位或點蝕臨界電位。Ep稱為點蝕保護電位或再鈍化電位,是理論陽極極化曲線回掃,又達到鈍態時對應的電位為再鈍化電位或保護電位Ep。Eb、Ep愈正,Eb與Ep相差愈小(滯后環面積愈小),表示鈍化膜修復能力越強,則金屬材料發生點蝕的傾向愈小,耐點蝕性能愈好。為了用Eb和Ep比較各種金屬材料的耐點性能,測量Eb和Ep的實驗條件必須相同。
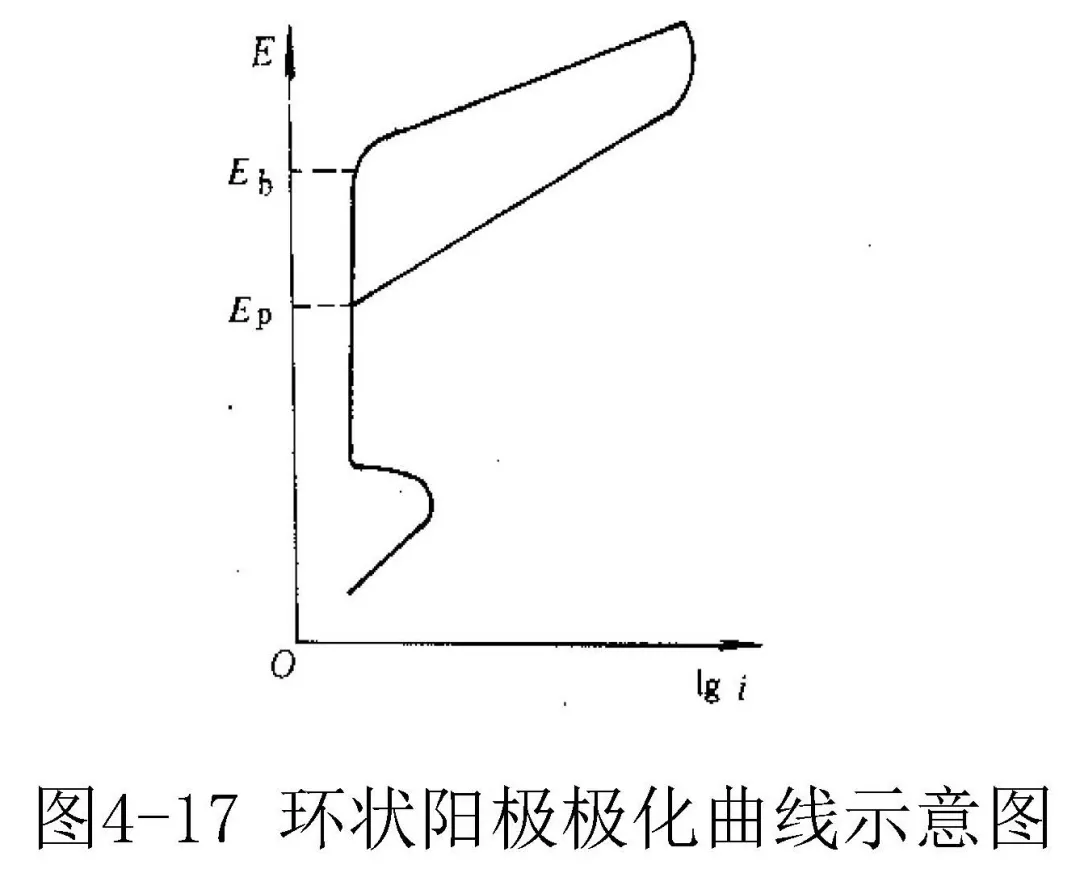
對于鈍態金屬來說,點蝕發生需要滿足電位條件,當E>Eb時,點蝕迅速發生和發展;
當Ep<E<Eb時,不產生新的蝕孔,已有的蝕孔可繼續發展;當E<Ep時,不發生點蝕。
參考文獻
[1] GB/T 17897-2016.金屬和合金的腐蝕 不銹鋼三氯化鐵點腐蝕試驗方法
[2] ASTM G48-2011(R2015).Standard Test Methods for Pitting and Crevice Corrosion Resistance of Stainless Steels and Related Alloys by Use of Ferric Chloride Solution
[3] EN 10088-1.Stainless steels - Part 1: List of stainless steel
[4] ASTM A240/A240M-2018.Standard Specification for Chromium and Chromium-Nickel Stainless Steel Plate, Sheet, and Strip for Pressure Vessels and for General Applications
[5] ASTM A789/A789M-2017.Standard Specification for Seamless and Welded Ferritic/Austenitic Stainless Steel Tubing for General Service
[6] ASTM A790/A790M-2018.Standard Specification for Seamless and Welded Ferritic/Austenitic Stainless Steel Pipe
[7] ASTM A959-2019.Standard Guide for Specifying Harmonized Standard Grade Compositions for Wrought Stainless Steels
[8]黃嘉琥,付逸芳.耐點蝕當量(PRE)與壓力容器用超級不銹鋼[J].壓力容器, 2013.30(4):41-50
[9] 天華化工機械及自動化研究設計院主編.腐蝕與防護手冊·第1卷·腐蝕理論、試驗及監測[M].第二版,北京:化學工業出版社,2008:174-198
[10] 王梅豐,李光東,杜楠.表面粗糙度對304不銹鋼早期點蝕行為影響的電化學方法[J].
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《中國腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護網官方QQ群:140808414