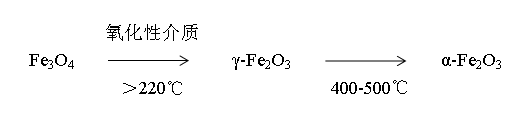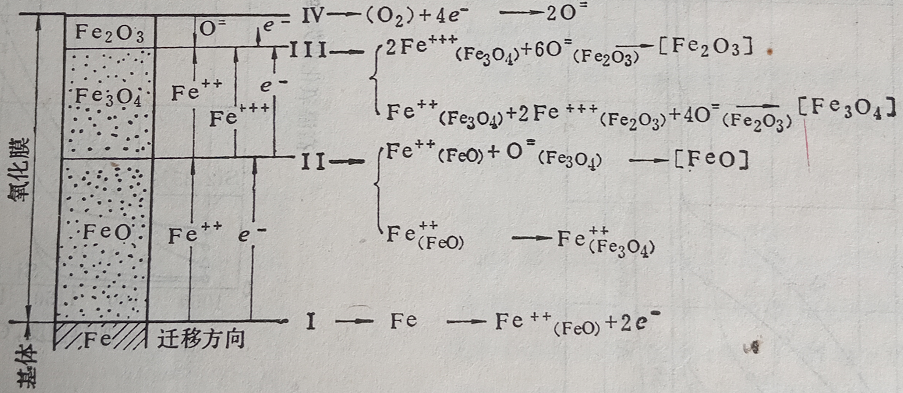01 鐵-氧平衡圖與氧化層結構
氧在鐵中的溶解度很低,湯根斯(Tankins)等人測定在體心立方鐵中氧的溶解度為:
Log[O%]=-126330/T+5.51
在常溫下α-Fe溶氧量小于0.05%,在950℃時溶氧量約0.2%,可形成含氧的固溶體。它比純鐵更具有正的化學電位,從-0.43伏到零。
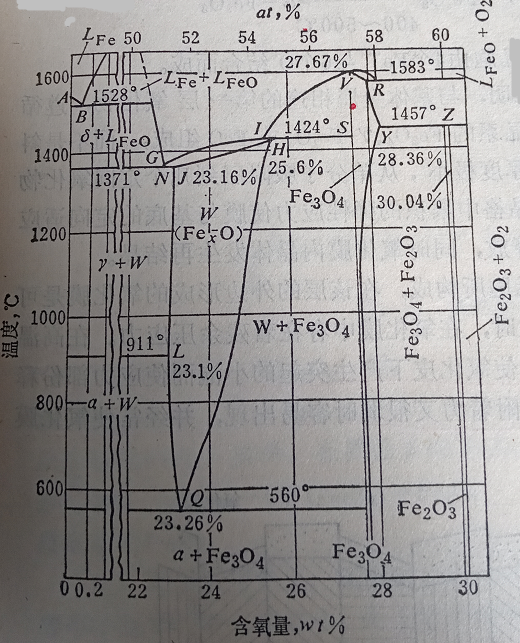
圖1 鐵氧平衡圖
圖1為鐵-氧平衡圖。氧與鐵形成不同結構的氧化膜組成相,由平衡圖上可看出依含氧量不同分別為FeO(FexO)、Fe3O4、Fe2O3。鐵的氧化物相的含氧量見表1,它們在表面的分布見圖2所示。
表1 不同氧化物相的成分
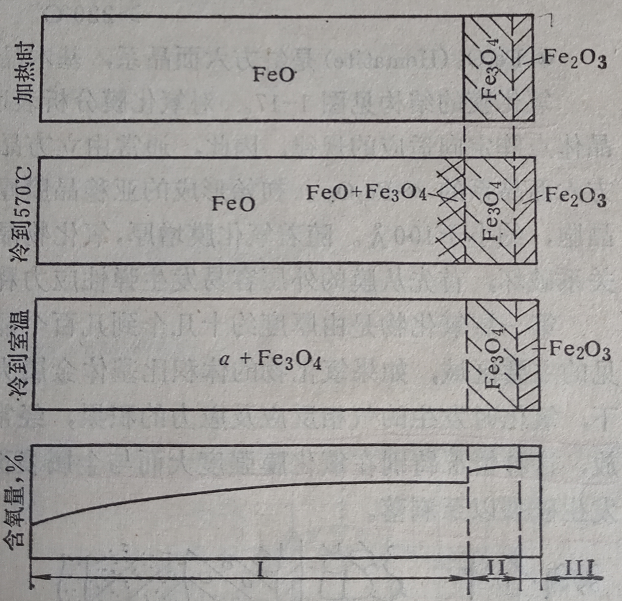
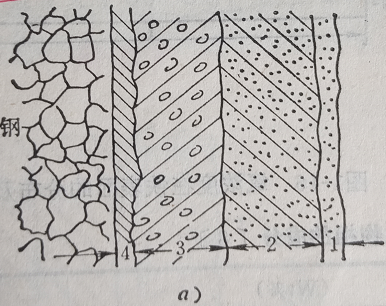
圖2 氧濃度在鐵表面的分布及各相結構
FeO又稱維氏體(Wustite),是具有巖鹽型的立方點陣的缺位固溶體,過剩的氧在FeO中以氧離子形態存在并占據晶格的陰離子結點。由于氧在FeO固溶體中有一個固溶范圍,如在1000℃時,Fe:O=1:1.05-1.14,相當于Fe0.95O-Fe0.88O(含氧的原子百分數為51.2-53.3%),所以也可寫成FexO的通用形式。
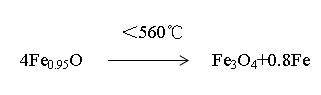
高溫氧化皮中的FeO是介穩狀態,低溫下它將分解。
Fe3O4,又稱磁性氧化鐵,具有尖晶石型點陣,它從室溫到1583℃都是穩定的,在氧化性介質中加熱時,將失去磁性。
2Fe3O4+1/2O2→3Fe2O3
α-Fe2O3是斜方六面晶系,基本晶胞由4個Fe3+與6個O-結合而成。
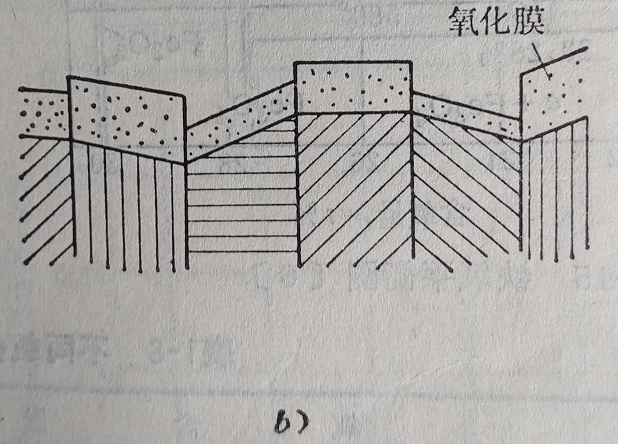
圖3 氧化膜的結構
a)鐵的氧化膜結構
b)多晶體表面開始形成的亞穩晶膜
1-Fe2O3;2-Fe3O4
3-FeO+Fe3O4;4-FeO
氧化膜的結構見圖3所示。對氧化膜分析表明,與基體金屬相連的第一層氧化物,遵循晶體點陣定向適應的規律,因此,通常由立方晶系的Fe3O4、γ-Fe2O3或FeO組成,而不是斜方六面晶系的α-Fe2O3。初始形成的亞穩晶膜厚度極小,從單分子吸附層到幾個定向氧化物晶胞,約小于100?。隨著氧化膜增厚,氧化物晶格中累積的彈性應力使膜與基底的定向適應關系破壞,首先從膜的外層容易發生彈性應力釋放,同時氧化膜內晶體發生再結晶。
圖4 產品氧化案例
第一層氧化物是由厚度約十幾個到幾百個晶胞所構成,在該層的外邊形成的氧化膜是可見的主要區域,如果氧化物的體積比基體金屬大時,在氧化膜中存在著殘余壓應力。在高溫下氧化時發生的氣相反應及應力的積累,經常使氧化皮下產生突起的小泡而使應力部分釋放,這種情況特別在氧化膜強度大而金屬表面附著力又很弱時容易出現,并經常使氧化膜發生破裂以致剝落。(注:這里解釋了產品嚴重氧化時表面氧化皮脫落的原因,可以重點記一下。)
02 氧化膜形成的機理
氧化膜的發展和形成的過程比較復雜,因此開始形成氧化膜時就將介質和金屬基體分隔開來,進一步氧化必須通過這個氧化物層。
顯然氧化過程是由金屬、金屬氧化物和氧三者之間的相互作用和氧的擴散所控制。在大多數情況下,離子或電子遷移速率控制著氧化速率,但有時界面反應也是控制氧化速率的決定因素。
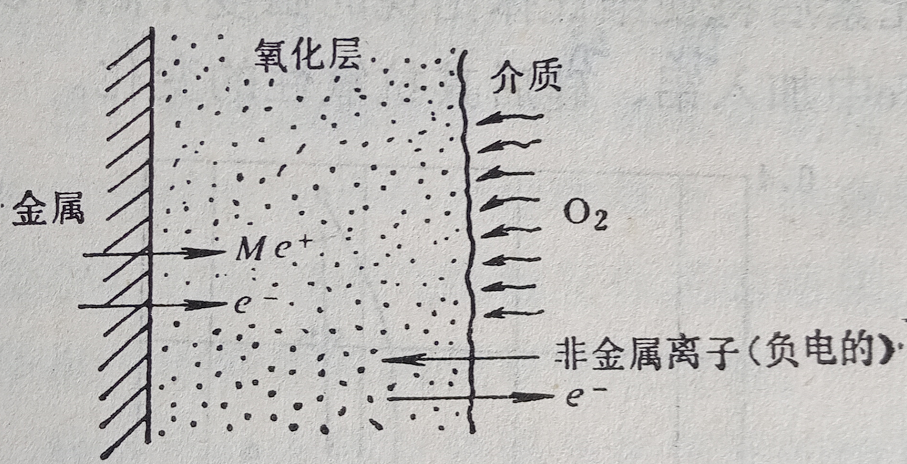
圖5 金屬表面與氧化介質間的作用
在圖5中表示氧以負離子狀態被吸附在氧化層表面上,而金屬以正離子狀態溶解在氧化膜中,所以氧化過程的推動力是濃度梯度(dc/dx)和氧化層中的電場。其中電場是由于在邊界上的電子與離子運動速度不一樣,從而形成雙電荷層而產生的。
圖6 鐵的表面氧化機理示意圖
鐵的氧化機理可以從離子-電子在界面上的遷移過程來說明(圖6所示)。
1)首先,在界面Ⅰ上的鐵原子形成Fe2+與2e-,并向FeO層中擴散,同時使界面Ⅰ向鐵的一側內移。
2)在界面Ⅱ上,FeO層中的Fe2+與來自Fe3O4層中的O-生成FeO晶格,與此同時一部分Fe2+從界面Ⅱ向Fe3O4方向擴散。
3)在界面Ⅲ的Fe3O4一側,按Fe2+(FeO)+2Fe3+(Fe2O3)+4O-(Fe2O3)→Fe3O4反應形成Fe3O4,此外,在界面Ⅲ的Fe2O3一側,按2Fe3+(Fe3O4)+6O-(Fe2O3)→Fe2O3反應形成Fe2O3。
4)在最表層Ⅳ上,O2吸附在Fe2O3表層,在Fe2O3層中O-向界面Ⅲ方向移動;由于形成速度慢,Fe2O3層很薄。
在高溫下氧化,由于氧化層中的壓應力及CO2氣體反應使氧化層發生龜裂及剝落,O2沿縫隙迅速侵入金屬內層使氧化速度急劇上升。
03 影響因素
氧化膜的形成速度主要與介質成分、加熱溫度及保溫時間、鋼材的成分等因素有關。
1 鋼成分的影響
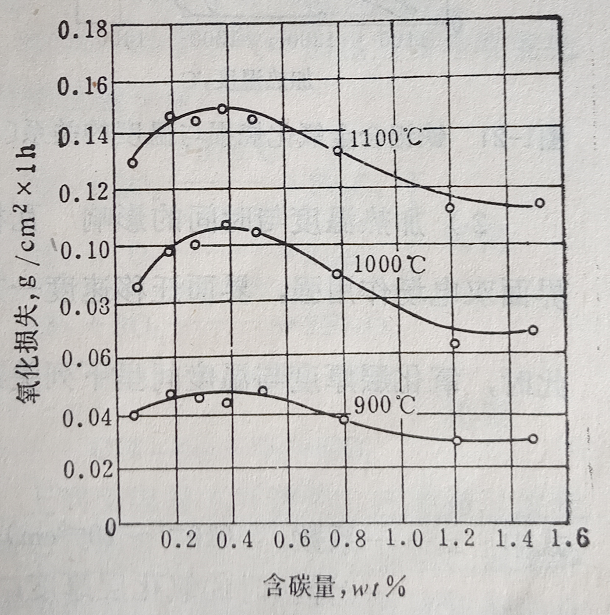
圖7是碳鋼高溫氧化的速度與含碳量的關系。
圖7 碳鋼含碳量與高溫氧化速度的關系
當含碳量小于0.04%時,氧化速度隨含碳量增長而升高;當含碳量大于0.4%時,氧化速度卻隨含碳量增加而減小。顯然是由于氧化介質與鋼中的碳相互作用形成氣體CO、CO2有關。
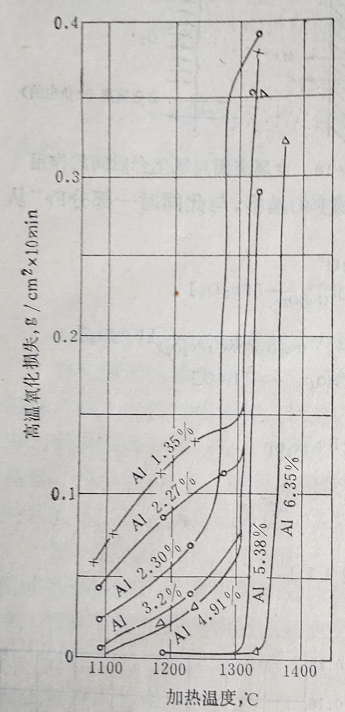
圖8 鐵鋁合金氧化燒損與溫度的關系
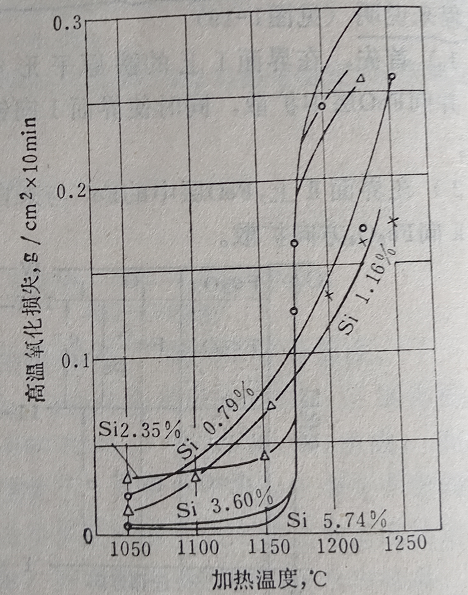
合金元素對氧化速度有很大影響,加入鉻、鋁、硅等元素可以形成致密的尖晶石型氧化物(Cr2O3、Al2O3、SiO2),這種氧化物結構對離子擴散有強烈的阻止作用,同時鐵中添加合金元素后將使維氏體出現的溫度升高,以致抗氧化能力大大提高,見圖8、圖9。表明Fe中加入鋁、硅后其抗氧化的變化。
圖9 鐵硅合金的氧化燒損與加熱溫度的關系
2 加熱溫度與時間的影響
瓦格納(Wagner)指出,在加熱初期氧化層很薄時(<100?)界面雙電場作用強,界面遷移速度一方面取決于濃度梯度dc/dx,另一方面又取決于電場強度。此時,氧化層厚度與溫度間呈下列關系:
X1/X=A-Inτ
式中:X1-系數(10-4-10-5cm),X-時間τ時的氧化層厚度,A-常數,τ-時間,上式是在薄層氧化時(氧化層厚度<100?)氧化膜成長的對數定律。
當氧化層厚時,氧化速率與層的厚度成反比,此時氧化層的增長速度服從拋物線定律:
X=Aτ1/2
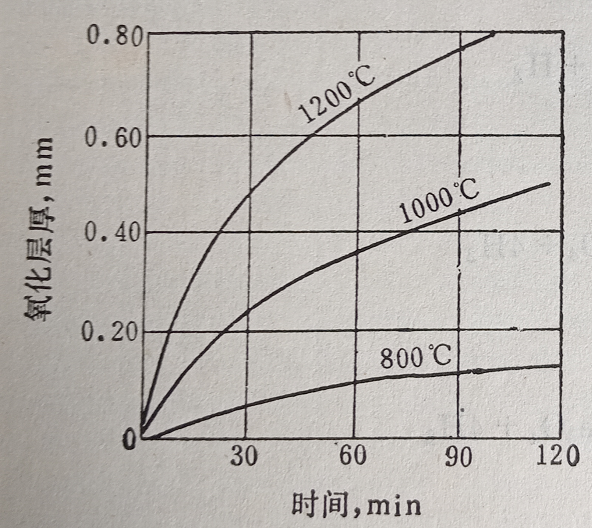
圖10為純鐵在空氣中加熱時保溫時間與氧化層厚度的關系。
圖10 純鐵在空氣中加熱時保溫時間與氧化膜厚度的關系
氧的擴散系數與溫度呈指數關系,因此,氧化膜的增厚隨加熱溫度升高也呈指數曲線上升。
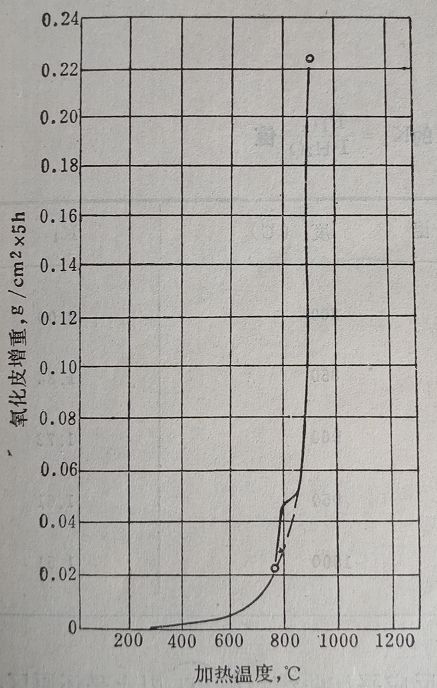
圖11 含碳0.60%鋼加熱溫度與氧化速度的關系
圖11是含碳0.6%鋼氧化溫度與氧化速度(用5小時內氧化皮增重表示)的關系。
04 結束語
氧化,是產品出現的比較嚴重的表面腐蝕現象。了解了它生成的原理,對于我們后續采取相應措施,能起到一定的指導作用。
好的,本期文章到此就結束了,欲知后續精彩內容,且看下期分解。
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。
相關文章

官方微信
《腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 腐蝕與防護網官方QQ群:140808414
點擊排行
PPT新聞
“海洋金屬”——鈦合金在艦船的
點擊數:8181
腐蝕與“海上絲綢之路”
點擊數:6497