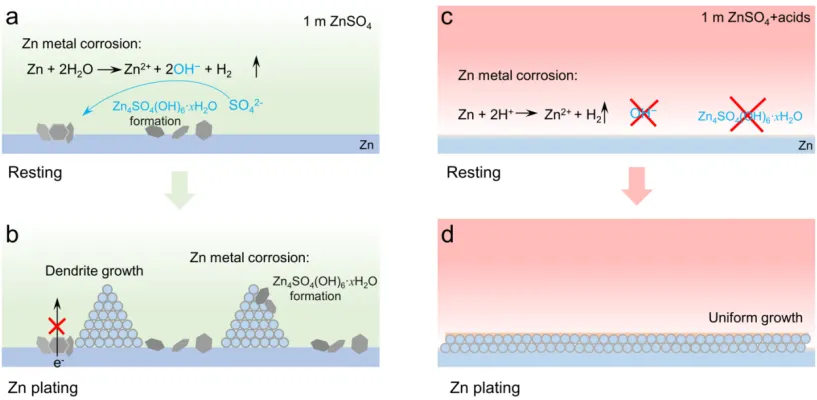
導語 成果 在鋅表面富集堿性氫氧根離子很容易誘導形成導電性差的副產物沉積,例如在典型硫酸鹽電解質中的Zn4SO4(OH)6·xH2O(ZSH)(圖1a)。電池運行前的靜置期間產生的副產物隨機分布在表面上,導致隨后的不均勻鋅金屬沉積和枝晶生長(圖1b)。利用強Brønsted酸清理鋅金屬表面堿性副產物,則可能幫助后續均勻的鋅金屬沉積,盡管質子可能與鋅金屬發生反應,但它也會避免OH¯的形成,從而抑制在鋅表面沉淀堿性副產物,為鋅的均勻沉積鋪平道路(圖1d)。 圖1 鋅表面腐蝕副產物形成及抑制示意圖 圖2 自腐蝕對電解液pH值、電極表面產物和鋅沉積的影響 添加0.1 m HTFSI電解液展現出更好的鋅負極穩定性和可逆性。添加過少的HTFSI將產生有限的效果,而添加過多的HTFSI將引發無法控制的析氫副反應。1 m ZnSO4+0.1 m HTFSI電解質中Zn沉積/剝離CE表現出快速穩定,在最初的40個循環內達到了99%。隨后,在1400個循環內達到了99.7%的CE。引入HTFSI后鋅在Cu基底上的成核過電位和生長過電位均降低。此外,使用HTFSI的Zn||Zn電池表現出穩定的極化約30.5 mV和長達2200小時的超長循環壽命,比不添加HTFSI的電池壽命長20倍(圖3e)。HTFSI的添加也顯著改善了電池倍率性能,在當前密度高達17 mA cm-2時表現出穩定的放電和充電電壓曲線。 圖3 不同電解液中鋅沉積/剝離的電化學測試研究 在1 m ZnSO4+0.1 m HTFSI電解質中,研究人員發現了密集、均勻、納米尺寸的鋅沉積物(圖4a),厚度為4.3 µm,而在1 m ZnSO4電解質中呈現出厚度為14.8 µm的苔蘚狀鋅生長(圖4a4, b4)。此外,EDS及XRD結果顯示, 1 m ZnSO4+0.1 m HTFSI電解液中未檢測到ZSH,明顯區別于1 m ZnSO4電解液。另一方面,1 m ZnSO4電解液中OH-也會擴散到正極,這將在正極表面形成ZSH并損害電池的循環穩定性。在HTFSI存在的情況下,原位拉曼結果顯示正極表面沒有明顯變化(圖4e),總結以上結果,在引入HTFSI后,負極及正極上均未檢測到腐蝕副產物ZSH的形成。 圖4 負極和正極的表征 在1 m ZnSO4電解液中,Zn||ZVO全電池觀察到了顯著容量損失,而Zn|1 m ZnSO4+0.1 m HTFSI|ZVO的循環性也得到了極大的改善。而Zn|1 m+0.1 m HTFSI|ZVO在不同電流密度下表現出更高的比容量。對全電池的自放電行為進行了探究。靜置24小時后,Zn|1 m ZnSO4+0.1 m HTFSI|ZVO保持了94.98%的原始容量,自放電現象遠低于Zn|1 m ZnSO4|ZVO的(72.85%)。 圖5 Zn||ZVO全電池的電化學性能 S 2p光譜證實了在1 m ZnSO4+0.1 m HTFSI電解液中,鋅金屬將自發形成ZnS。ZnS組分可能源自于SO42−的還原,而非TFSI-陰離子,因為F 1s XPS譜圖中沒有氟相關物種。盡管ZnF2通常被認為是鋅負極的有利SEI組分,值得注意的是ZnF2在水中的溶解度遠高于ZnS(溶解度常數Ksp=3.04*10−2 vs 2.5*10−22,25 ℃)。因此,ZnS富集的SEI層可能更有效地隔離活性Zn免受電解質腐蝕。 圖6 在1m ZnSO4+0.1m HTFSI電解液中對Zn|電解液界面的研究 總之,在電池靜置期間,HTFSI的作用機制主要可歸因于以下兩個方面: (1) 強Brønsted酸的添加可以防止Zn表面上腐蝕產物的積累; (2) 在Zn表面存在HTFSI形成了疏水的微環境,誘導了ZnS的形成并防止了Zn電極的進一步腐蝕。 這兩個方面都與TFSI¯陰離子的性質密切相關,因為具有疏水-三氟甲基基團的龐大結構不僅可以分散負電荷以增加質子給予能力,還可以促進Zn表面形成疏水界面以抑制進一步的電解質腐蝕。 結語
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606
- 郵箱:fsfhzy666@163.com
- 腐蝕與防護網官方QQ群:140808414