「摘 要」 海洋生物污損會導致燃料消耗增加,加大二氧化碳排放。為了解決這一問題,人們做了許多嘗試,其中聚合物防污涂層因其環境友好性而受到廣泛的研究。 兩性離子聚合物、多糖和聚乙二醇經常被用作表面涂層,表現出優異的海洋防污性能。然而,這些親水聚合物涂層有一個主要的缺點:當暴露在沉積物中時,各種礦物質很容易被涂層吸附,導致它們失去其固有的防污性能。因此,兩親性聚合物涂層被提出作為親水性聚合物涂層的替代品。 本文報道了由羧基甜菜堿甲基丙烯酰胺和甲基丙烯酸三氟乙酯組成的兩親性共聚物的合成及其在固體表面的固定。該方法利用與材料無關的表面涂層特性和聚多巴胺的金屬絡合物形成能力將兩親共聚物固定在固體表面上。被固定后的表面對硅藻粘附和淤泥吸附均表現出良好的防污性能。由于這是一種簡單且與底物無關的固定聚合物的方法,因此有望成為新型的海洋防污聚合物涂層。 關鍵詞:兩親性聚合物,船舶防污,金屬絡合,聚多巴胺,表面涂層 作者 | Jinhyeok Jeong, Jihwan Do, Sung Min Kang
控制海洋生物污垢,即各種海洋生物在船體上積累的生物量,是海事行業面臨的一個持續挑戰[1,2]。海洋生物污垢增加了表面摩擦,導致船舶使用更多的燃料[3]。此外,外來物種的生物污垢導致它們被遷移到新的環境,這可能威脅到國內海洋生態系統[4]。為了解決這些經濟和生態問題,具有防污、脫污或兩者兼備的表面涂層得到了廣泛的研究[1]。 最近一種減少表面污垢的策略是在固體表面涂上親水聚合物[5,6]。這些親水性聚合物涂層形成水化層,是防止海洋生物非特異性吸附的物理屏障。這些聚合物的親水性和電中性也減少了與帶電生物質的靜電相互作用[7]。 然而,最近發現了這些涂層的缺點。當暴露在海洋環境中時,由于沉積物中存在的礦物質的表面吸附,它們可能會失去防污能力。例如,Koc等人報道,硅藻土和淤泥等無機材料很容易吸附在兩性離子和乙二醇聚合物涂層上[8,9]。然而,由于表面親水性降低,兩親性共聚物涂層表現出相對較低的淤泥吸附[10]。此外,兩親性共聚物涂層的獨特優勢之一是它們能夠在表面表現出疏水性和親水性。這種特性使它們能夠向生物污垢呈現一個模糊的表面,使其成為有效的海洋防污涂層[11]。 多種多樣的兩親性共聚物已經被合成,并證明了它們的防污性能[10,12-17]。例如,Koschitzki等人制備了一組含有羧基甜菜堿和雙環戊二烯的兩親性聚合物,對海洋硅藻表現出良好的防污性能[10],多糖也被用于制備兩親性聚合物涂層[12,13]。透明質酸和硫酸軟骨素被疏水性三氟乙胺覆蓋,顯著抑制海洋細菌、游動孢子和硅藻的粘附[12]。最近,含氮共聚物被建議用于兩親性共聚物涂層[15]。一些硬污生物使用自由基交聯粘合劑;因此,當氮氧化物摻入共聚物中時,作為抗氧化劑會導致聚合物完全抑制藤壺沉降。
兩親性共聚物涂層的制備面臨的一個挑戰是它們缺乏多功能性。許多研究都是在玻璃或硅表面上進行的,因為這些表面很容易通過著名的有機硅烷化學反應進行改性。 例如,首先使用有機硅烷化合物在玻璃表面引入氨基或乙烯基,并使用光交聯劑二苯甲酮將兩親性共聚物共價接枝到功能化玻璃表面[17]。在另一項研究中,研究了基于聚二甲基硅氧烷(PDMS)的涂層[16]。合成了含有PDMS的兩親性共聚物,并將其摻入PDMS基體中以制備涂層。雖然這些方法在船舶防污涂層中取得了成功,但在涂層過程中需要加入額外的光反應基團或基質,這可能會對共聚物的固有性能產生不利影響。因此,需要一種無需額外錨定基團或基質即可應用于各種表面的方法。 在此,我們提出了一種簡單而通用的兩親性共聚物涂層的制備方法。該方法利用了聚多巴胺(pDA)與材料無關的表面涂層特性和金屬絡合物形成能力[18]將兩親性共聚物固定在固體表面上。合成了由羧基甜菜堿、甲基丙烯酰胺和甲基丙烯酸三氟乙酯組成的兩親性共聚物,并通過旋涂將其物理沉積在pDA涂層的固體表面上。沉積的共聚物通過鋯(IV)(ZrIV)介導的多重配位鍵形成與pDA交聯[19],使共聚物能夠牢固地固定在固體表面上。利用這種方法,成功地在硅、玻璃和不銹鋼基材上涂覆了兩親性共聚物,得到的表面對硅藻粘附和淤泥吸附均表現出良好的防污性能。
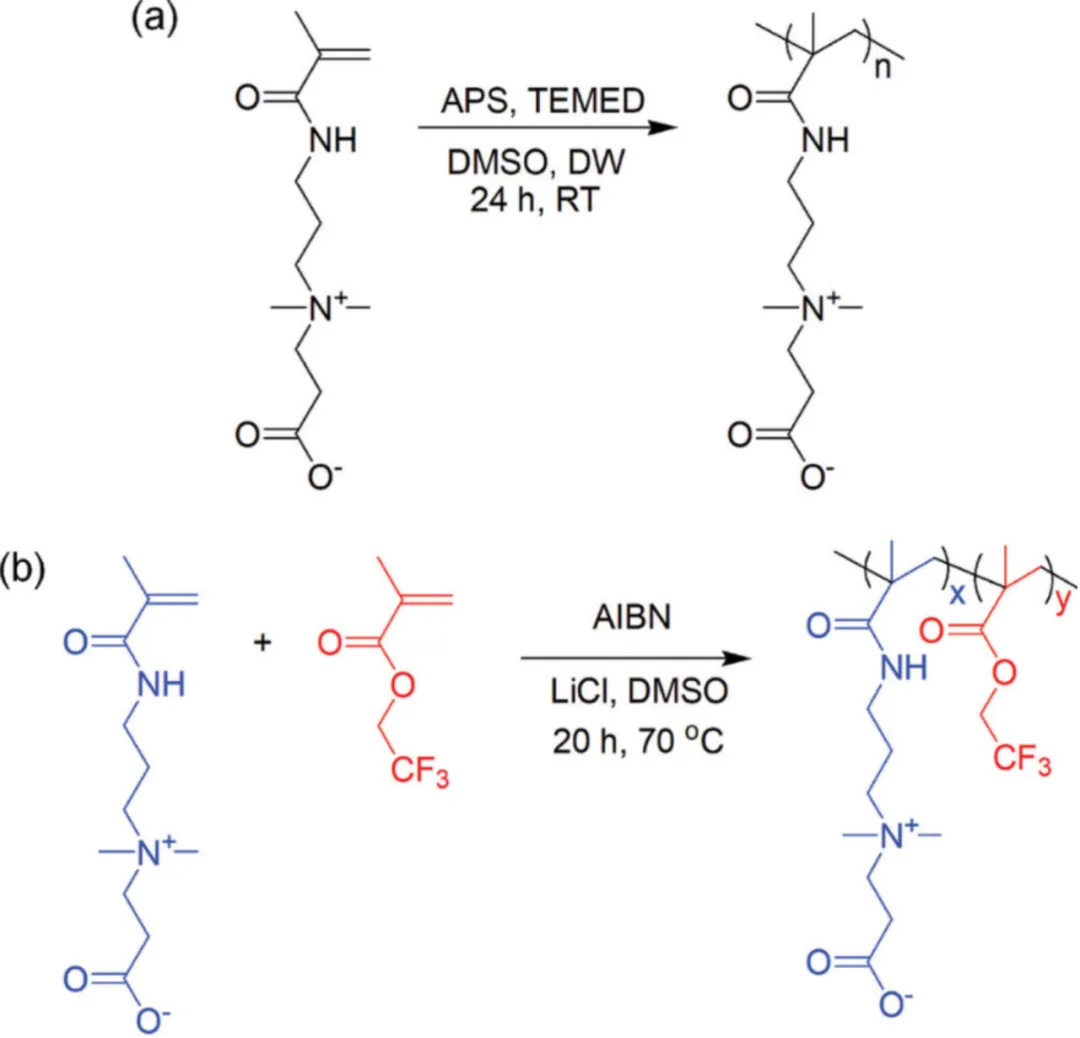
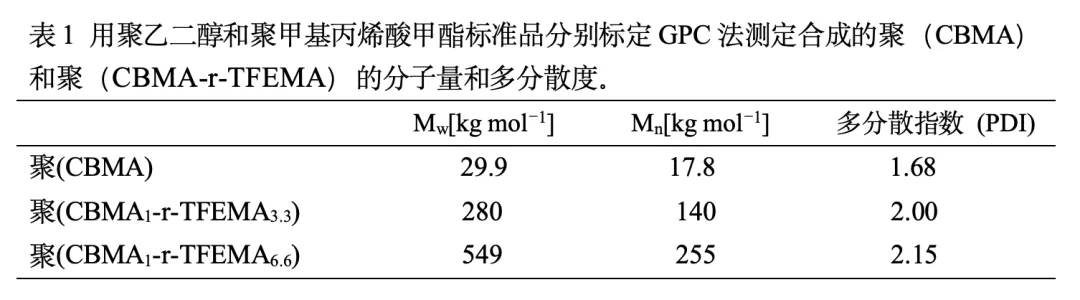
采用自由基溶液聚合法合成了聚(羧基甜菜堿甲基丙烯酰胺)(聚(CBMA))和兩種無規共聚(羧基甜菜堿甲基丙烯酰胺-r-甲基丙烯酸三氟乙酯)(聚(CBMA-r- TFEMA))共聚物(圖1)。通過控制聚合過程中單體的加入量,可以改變聚(CBMA-r-TFEMA)中CBMA與TFEMA的比率。CBMA與TFEMA的比率是通過核磁共振(NMR)波譜法確定的。 將4.2ppm時的峰積分(CF3CH2−)與2.6ppm時的峰積分(−N+(CH3)2)進行比較,結果得出聚(CBMA-r-TFEMA)的CBMA與TFEMA比率分別為1:3.3和1:6.6。這些聚合物被命名為聚(CBMA1-r-TFEMA3.3)和聚(CBMA1-r-TFEMA6.6)。通過凝膠滲透色譜法(GPC)測定合成聚合物的分子量和多分散度(表1)。聚(CBMA)、聚(CBMA1-r-TFEMA3.3)和聚(CBMA1-r-TFEMA6.6)的Mn(數均分子量)值分別為17.8、140和255 kDa。這些聚合物的分子量分布分別為1.68、2.00和2.15。
圖1. a)聚(CBMA)和b)聚(CBMA-r-TFEMA)的合成方案
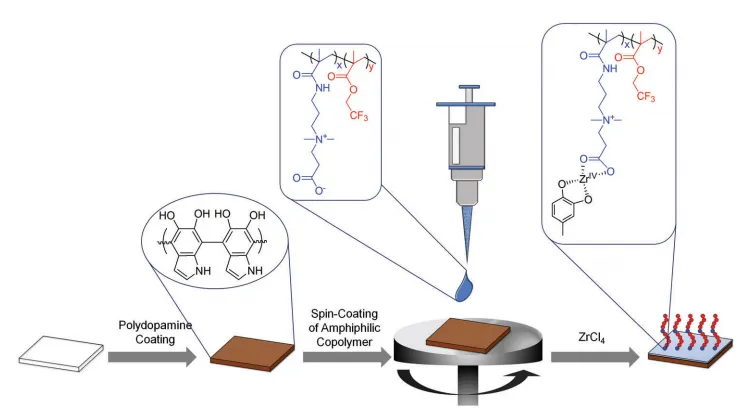
為了將合成的聚合物固定在固體表面,進行了pDA涂層。pDA涂層是一種廣為人知的涂層方法,它以與材料無關的方式形成鄰苯二酚呈現固體表面[18,20]。 本研究以固體表面的pDA鄰苯二酚基團為聚(CBMA)和聚(CBMA-r-TFEMA)的錨定位點。通過添加ZrIV離子實現了pDA介導的聚合物固定化。ZrIV可以與多種有機配體形成多個配位鍵,如鄰苯二酚、羧酸鹽[19]。因此,可以在pDA涂層表面與含CBMA的聚合物之間形成鄰苯二酚-ZrIV-羧酸鹽配位鍵,在含CBMA的聚合物之間形成羧酸鹽-ZrIV-羧酸鹽配位鍵(圖2)。Si/SiO2最初被用作表面涂層的模型底物,因為有幾種表面表征技術可用于Si/SiO2底物。
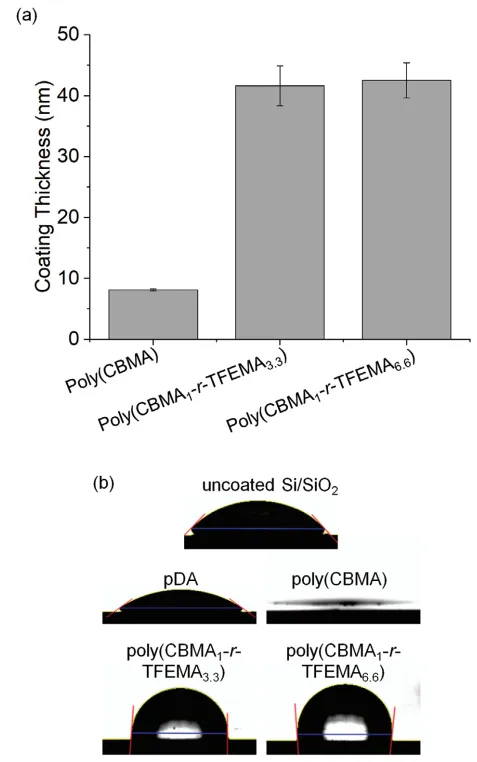
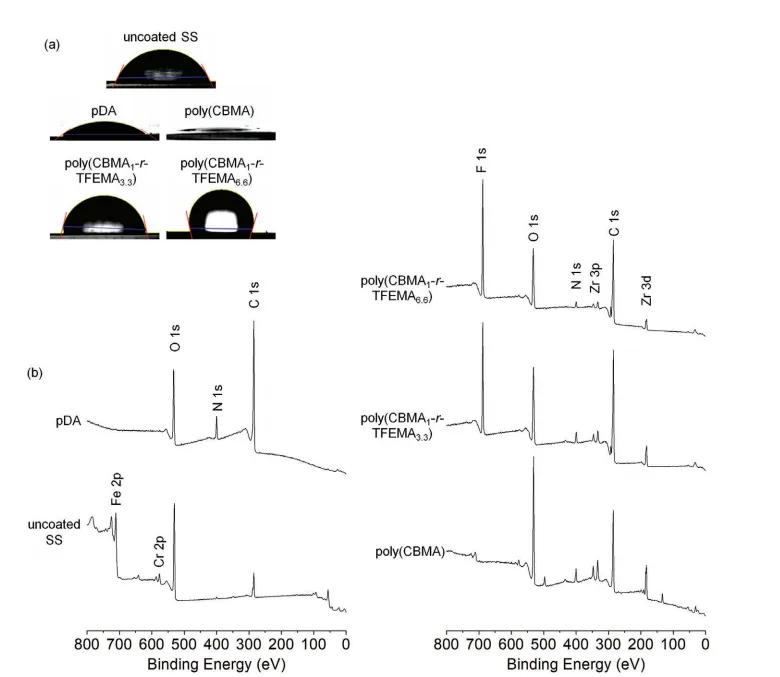
通過橢偏光譜法證實了pDA表面涂層和隨后的聚合物固定(圖3a)。結果表明,固定聚(CBMA)、聚(CBMA1-r-TFEMA3.3)和聚(CBMA1-r-TFEMA6.6)后,pDA涂層厚度分別增加了8.1±0.2、41.6±3.3和42.5±2.9nm。結果表明,共聚物的固定化效率高于聚(CBMA)。這可能是由于分子量的不同,由于羧酸鹽作為表面錨定基團,分子量越高,參與聚合物固定的羧酸鹽數量越多,從而提高了固定效率[21]。 采用水接觸角(WCA)測量法研究了聚合物固定后的表面潤濕性(圖3b)。雖然聚合物的固定效率有所不同,但通過橢偏光譜分析表明,聚合物的固定明顯改變了表面潤濕性。未涂覆Si/SiO2表面和pDA涂層的WCA分別為45.9°±1.0°和35.2°±1.0°。用聚CBMA固定后,由于CBMA對水分子具有很強的結合親和力,WCA減小到<10°[22]。而聚(CBMA1-r-TFEMA3.3)和聚(CBMA1-r-TFEMA6.6)涂層的WCA分別為88.0°±0.3°和93.0°±7.4°。這些結果表明,在干燥條件下,TFEMA主要暴露在最外層的聚(CBMA-r-TFEMA)層上,使其表面相對疏水。 由于pDA具有與材料無關的表面涂層特性,我們的制備兩親性共聚物涂層的方法具有適用于各種固體基材的優勢。為了研究其通用性,在不銹鋼(SS)基材上進行了兩親性共聚物固定化,因為不銹鋼是船體的主要成分,經常發生海洋污垢。 首先,研究了表面潤濕性的變化。與Si/SiO2表面涂層相似,經pDA涂層后,SS的WCA由65.7°±5.8°變化為36.6°±1.1°。用聚(CBMA)固定后,WCA進一步降低至<10°,并且聚(CBMA1-r-TFEMA3.3)和聚(CBMA1-r-TFEMA6.6)的固定使其表面疏水:聚(CBMA1-r-TFEMA3.3)為79.4°±2.2°,聚(CBMA1-r-TFEMA6.6)為104.7°±5.5°(圖4a)。 圖3. a)在Si/SiO2上聚(CBMA)、聚(CBMA1-r-TFEMA3.3)和聚(CBMA1-r-TFEMA6.6)涂層的厚度。b)未涂覆的Si/SiO2、pDA、聚(CBMA)、聚(CBMA1-r-TFEMA3.3)和聚(CBMA1-r-TFEMA6.6)涂層的WCA圖像。
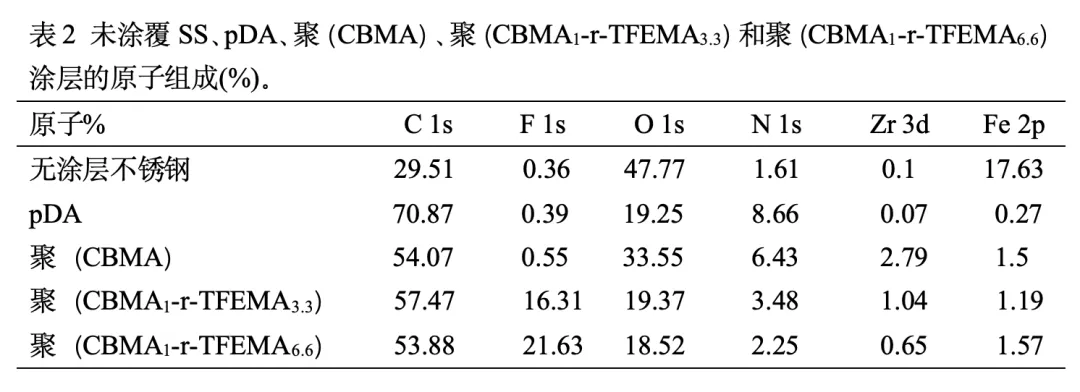
通過x射線光電子能譜(XPS)證實了聚合物的成功固定(圖4b)。無涂層的SS表面的XPS譜顯示出C 1s、O 1s和Fe 2p三個強底物峰。經pDA涂層后,Fe 2p的基材峰消失,而C 1s和N 1s的峰強度增加。這些結果表明,SS上的pDA涂層足夠厚,因此未檢測到基材峰。聚合物固定在pDA涂層上進一步改變了其表面化學成分。在聚(CBMA)固定化表面的光譜中,出現了Zr 3d和季銨的峰(圖4b)。聚(CBMA-r-TFEMA)共聚物固定化還表現為Zr 3d和F 1s峰的出現。 此外,我們利用表面原子組成數據分析了暴露在表面的CBMA和TFEMA的比例(表2)。由于共聚物的厚度大于XPS的檢測限,我們假設氮和氟僅來源于CBMA和TFEMA,而不是來源于pDA。考慮到CBMA和TFEMA單體單元分別含有2個氮原子和3個氟原子,計算得到聚(CBMA1-r-TFEMA3.3)和聚(CBMA1-r-TFEMA6.6)涂層中CBMA和TFEMA暴露于表面的比例分別為3.1和6.4。這些結果與核磁共振分析得到的共聚物的組成比(3.3和6.6)很好地一致。
圖4. a)WCA圖像和b)未涂覆SS、pDA、聚(CBMA)、聚(CBMA1-r-TFEMA3.3)和聚(CBMA1-r-TFEMA6.6)涂層的XPS光譜。
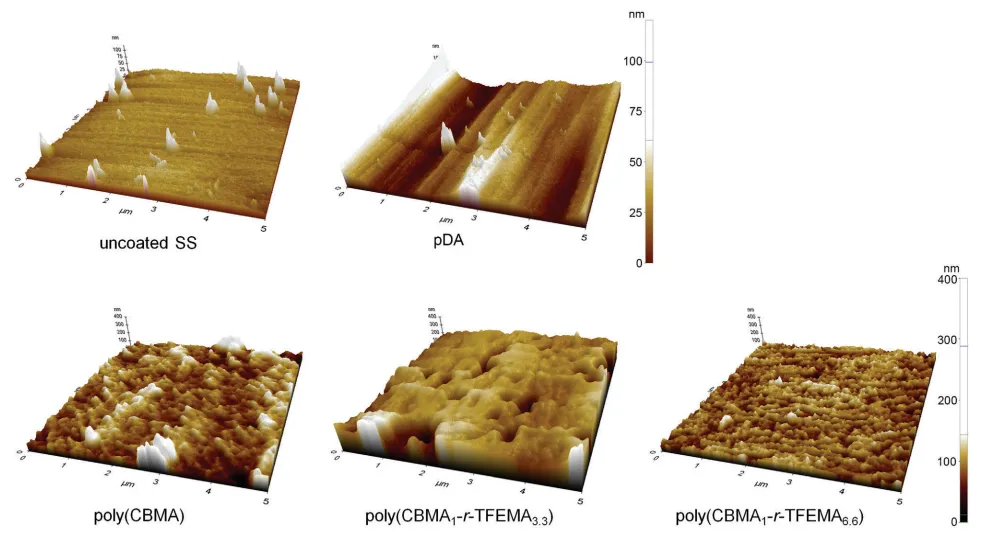
通過原子力顯微鏡(AFM)測定聚合物的表面形貌和均方根(RMS)粗糙度(圖5)。未涂層的SS和pDA涂層表現出相似的表面形貌,pDA涂層增加了RMS粗糙度(從7.6nm增加到14.7nm)。聚合物固定在pDA涂層表面上顯著改變了表面形貌;所有聚合物固定的表面上都出現了許多突起,而在未涂層和pDA涂層的SS表面上僅發現少量突起。聚(CBMA)、聚(CBMA1-r-TFEMA3.3)和聚(CBMA1-r-TFEMA6.6)涂層的RMS粗糙度值分別為26.4、43.6和15.9nm。
圖5. 未涂覆SS、pDA、聚(CBMA)、聚(CBMA1-r-TFEMA3.3)和聚(CBMA1-r-TFEMA6.6)涂層的AFM圖像。
-未完待續,下篇敬請期待- #參考文獻(滑動查看):
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606
- 郵箱:fsfhzy666@163.com
- 腐蝕與防護網官方QQ群:140808414