金屬的耐腐蝕性是指金屬材料抵抗周圍介質(zhì)腐蝕破壞作用的能力,是由材料的成分、化學性能和組織形態(tài)等決定的。傳統(tǒng)上,具有高耐蝕性的金屬或合金具備以下三個條件之一:(1)熱力學穩(wěn)定性高的金屬或合金,如Pt、Au、Ag、Cu等以及像Cu中加Au,Ni中加入Cu、Cr等;(2)易于鈍化的金屬,如Ti、Zr、Ta、Nb、Cr、Al等以及含Cr不銹鋼等;(3)表面能生成難溶的和保護性良好的腐蝕產(chǎn)物膜的金屬。人們對發(fā)展耐蝕材料的認識多停留在宏觀、統(tǒng)計和經(jīng)驗的水平上,還遠沒有達到從微納米、分子乃至原子尺度去認識材料耐蝕性的水平。實際上,由于金屬晶體材料表面各向異性的特征,不同取向的晶面具有不同的表面能和功焓,這將導致微電偶腐蝕的發(fā)生,即不同晶向晶面上的陽極溶解反應和陰極析氫反應速度存在差異。受表征手段限制,目前仍無法通過原位觀察的手段在這一微觀尺度上開展相關研究。然而,目前快速發(fā)展的計算材料學為材料耐蝕性的研究提供了一種有效的技術手段,它能夠從原子、電子等微觀角度精細、快速地計算研究材料本征的腐蝕行為,解析金屬腐蝕的內(nèi)在機制。并且可以在計算材料本征腐蝕行為的基礎上,通過構(gòu)建適當?shù)哪P脱芯亢辖饟诫s及晶體缺陷等對腐蝕的影響,為實驗提供一些理論支持。但是在材料腐蝕行為的模擬方面發(fā)展較為緩慢,還缺少相應的計算模型和算法。
建立腐蝕的計算模型需要從腐蝕的機理出發(fā)。金屬在常溫下常見的腐蝕方式是電化學腐蝕,其本質(zhì)為金屬在去極化劑的氧化作用下發(fā)生溶解生成腐蝕產(chǎn)物的過程。建立電化學腐蝕計算模型需要分別從陽極反應與陰極反應兩個方面發(fā)展模型與算法,從而解析材料的微觀特性與環(huán)境因素對腐蝕性能的影響,探索腐蝕機理,為材料耐蝕性的研究建立理論基礎。
由中科院金屬所柯偉院士、陳星秋研究員、董俊華研究員和馬會博士等組成的聯(lián)合研究小組對此開展了探索性研究。通過分析金屬陽極溶解反應過程中動力學過渡態(tài)理論(圖1所示),建立了金屬陽極溶解的計算模型。由于電化學腐蝕過程中,電極材料表面與溶液之間形成雙電層,使得金屬原子在陽極溶解過程中,不僅需要克服一個化學能壘ΔG,還需要克服電場U做功。這兩個參量直接與材料的表面特性,如組織結(jié)構(gòu)、晶粒取向及缺陷等相關聯(lián)。通過計算建模將陽極溶解過程中反應速率所涉及的化學活化能壘ΔG和電極表面與溶液之間的電勢差U分別用第一性原理可以計算的表面能、功函數(shù)以及提出的表面能量密度等參量進行表示,建立了材料的表面微觀特性與材料本征腐蝕性能間的聯(lián)系,實現(xiàn)了可以計算電化學極化曲線。利用該陽極溶解計算模型分別計算了純鎂常見的三個表面(0001)、(11-20)和(10-10)的電化學極化曲線(圖2所示),與文獻中已有的報導符合的很好,揭示了不同晶面之間的各向異性腐蝕行為的本質(zhì)是表面能量密度及功函數(shù)的不同。該工作發(fā)表在ActaMaterialia, 130 (2017) ): 137-146。
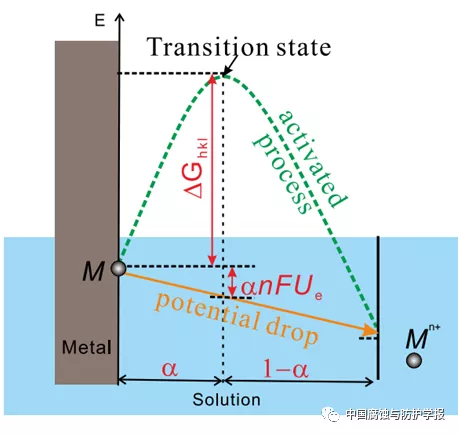
圖1 金屬陽極溶解過程示意圖。材料表面金屬原子的陽極溶解除了克服化學活化能ΔG外,還需要克服電極材料與溶液之間的電場U做功。
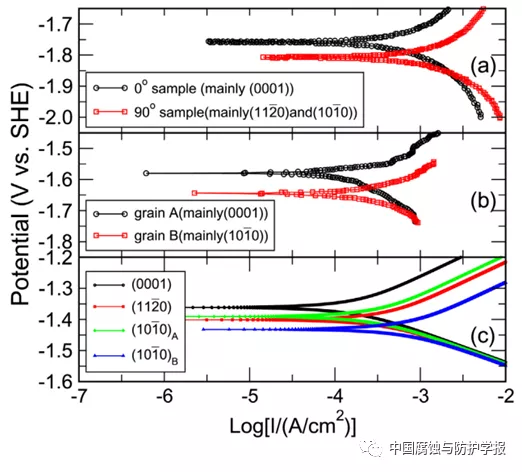
圖2 陽極溶解模型計算結(jié)果與實驗的對比。其中(a)和(b)分別是文獻中報道的包含不同晶面的鎂合金的電化學極化曲線,(c)是利用模型計算的純鎂不同晶面的極化曲線。
針對電化學腐蝕中的陰極去極化反應,發(fā)展建立了陰極析氫反應的第一性原理計算模型(圖3所示)。析氫反應是溶液中的氫離子在金屬表面得到電子生成氫分子的過程,依反應(Volmer反應、Tafel反應和Heyrowsky反應)的速率控制步驟不同,析氫反應遵循不同的動力學機制。在析氫反應過程中,吸附態(tài)的氫原子H*是整個反應的中間產(chǎn)物,其自由能ΔGH*的高低直接影響三個子反應過程的相對反應速率的大小。而氫原子在不同晶面上的吸附自由能與金屬材料的成分及晶面取向等表面特性密切相關。另外,氫離子H+作為反應物也會直接影響析氫反應速率的大小。通過分析吸附態(tài)氫原子在晶體表面的自由能ΔGH*及溶液中氫離子的濃度(pH值)對三個子反應速率的影響,建立了三種不同析氫反應機制下析氫反應的交換電流密度表達式,明確了析氫反應速率與表面特性及溶液pH之間的聯(lián)系,進而建立腐蝕過程中的析氫反應計算模型。通過模型計算得到的三種不同機制下析氫反應的交換電流密度與文獻中已經(jīng)報道的不同純金屬的測量值符合很好。該工作發(fā)表于ActaMaterialia, 183(2020):377-389。
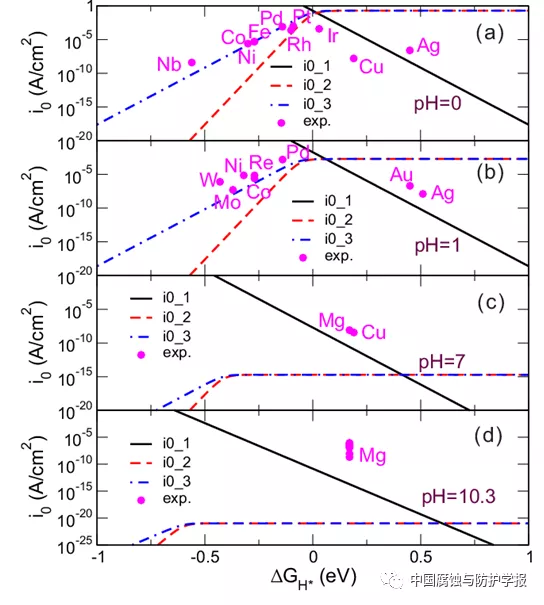
圖3 陰極析氫反應模型計算得到的三種反應機制在不同pH溶液中析氫反應的交換電流密度與吸附態(tài)氫原子的自由能ΔGH*之間的關系曲線,并與不同純金屬的實驗測量值之間進行對比。
結(jié)合陽極溶解與陰極析氫反應的微觀模型可以研究材料的電化學腐蝕行為,為研究材料耐蝕性計算模擬和行為預測提供了理論工具。1)利用模型可以研究純金屬一系列晶面的本征電化學腐蝕行為;2)對于多晶的金屬材料,可以利用計算模型并結(jié)合混合電位理論,將不同晶面進行陰極屬性與陽極相屬性的分類;3)可以計算研究合金元素對合金電化學腐蝕中陽極溶解及陰極析氫反應速率的影響,從而篩選出能夠提高合金耐蝕性的設計方案;4) 利用模型還可以研究金屬表面缺陷及組織結(jié)構(gòu)等對材料電化學腐蝕行為的影響。比如文獻中發(fā)現(xiàn)的實驗現(xiàn)象,無論是純鎂還是鎂合金在經(jīng)過變形處理后,晶粒內(nèi)部孿晶界增多,腐蝕速率會增大,但是內(nèi)在機制不是很清楚。通過構(gòu)建鎂合金中常見的三個孿晶界的結(jié)構(gòu)模型,并構(gòu)建表面存在孿晶界的結(jié)構(gòu)進行第一性原理計算,利用模型計算發(fā)現(xiàn)三個孿晶界會不同程度地增大純鎂的腐蝕速率(圖4所示)。分析其原因,主要是孿晶界的引入增大了表面能量密度。當材料表面存在不均勻的組織結(jié)構(gòu)或者缺陷時,完美表面與組織缺陷之間會由于腐蝕速率的不同形成微觀的電偶腐蝕,從而加速缺陷區(qū)域的腐蝕速率。該工作發(fā)表于Physical Review Materials,3 (2019) : 053806。
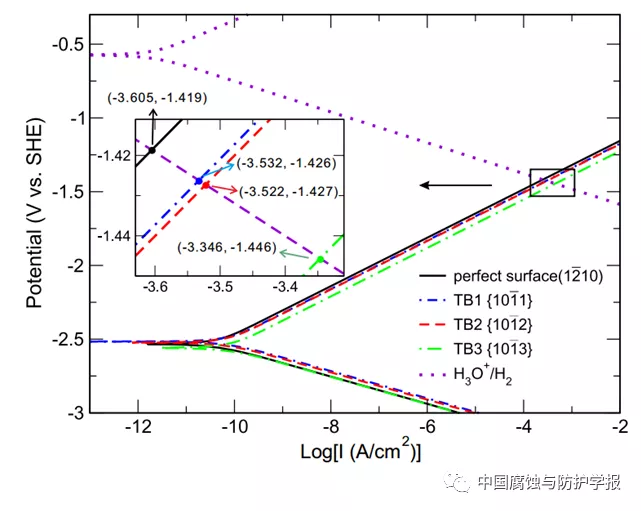
圖4純鎂金屬的完美表面與包含孿晶界表面之間極化曲線的對比。三個孿晶界的引入不同程度地增大了表面的腐蝕電流密度,降低了腐蝕電位。
免責聲明:本網(wǎng)站所轉(zhuǎn)載的文字、圖片與視頻資料版權(quán)歸原創(chuàng)作者所有,如果涉及侵權(quán),請第一時間聯(lián)系本網(wǎng)刪除。

官方微信
《中國腐蝕與防護網(wǎng)電子期刊》征訂啟事
- 投稿聯(lián)系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護網(wǎng)官方QQ群:140808414





