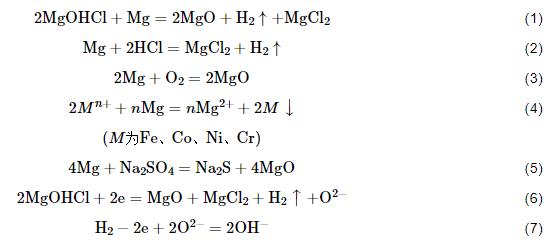摘要
通過電化學方法結合浸泡腐蝕測試考察了金屬Mg對MgCl2-NaCl-KCl (MNKC) 熔鹽的凈化和腐蝕抑制作用。結果表明,金屬Mg的加入量在500 μg·g-1以上時,316H不銹鋼在600 ℃ MNKC熔鹽中的腐蝕電位Ecorr<-0.80 V vs NiCl2/Ni,腐蝕電流密度Icorr<25 μA/cm2,線性極化電阻Rp>800 Ω·cm2,熔鹽對316H不銹鋼的腐蝕得到顯著抑制。并對金屬Mg對MNKC熔鹽的凈化和腐蝕抑制機理進行了探討。
關鍵詞: 氯化物熔鹽; 腐蝕控制; 316H不銹鋼; 聚光太陽能發電站 (CSP)
Abstract
The effect of Mg on purification of molten salts MgCl2-NaCl-KCl (MNKC) and corrosion behavior of 316H stainless steel in MNKC molten salts were investigated by means of immersion test and electrochemical means. Results indicated that the corrosion of 316H stainless steel in MNKC molten salts at 600 ℃ was well inhibited when the addition amount of Mg exceeds 500 μg·g-1, correspondingly, 316H stainless steel presents the free corrosion potential of Ecorr<-0.80 V vs NiCl2/Ni, corrosion current density of Icorr<25 μA/cm2, and linear polarization resistance of Rp>800 Ω·cm2. The purification and corrosion inhibition mechanism of Mg for the MNKC molten salts were discussed simultaneously.
Keywords: chloride molten salt; corrosion mitigation; 316H stainless steel; concentrated solar power (CSP)
左勇, 曹明鵬, 申淼, 楊新梅。 MgCl2-NaCl-KCl熔鹽體系中金屬Mg對316H不銹鋼的緩蝕性能研究[J]. 中國腐蝕與防護學報, 2021, 41(1): 80-86 doi:10.11902/1005.4537.2020.012
ZUO Yong, CAO Mingpeng, SHEN Miao, YANG Xinmei. Effect of Mg on Corrosion of 316H Stainless Steel in Molten Salts MgCl2-NaCl-KCl[J]. Journal of Chinese Society for Corrosion and Protection, 2021, 41(1): 80-86 doi:10.11902/1005.4537.2020.012
由堿金屬或堿土金屬氯鹽混合組成的氯化物熔鹽具有穩定性好、熱容及熱導率高、工作溫度范圍寬等特點,是極具競爭力的太陽能集熱候選介質[1]。研究者們已從熔鹽物性[2-4]、熱循環穩定性[5]、材料相容性[6]、綜合經濟性[7]等角度對不同組成的氯化物熔鹽開展了大量的研究工作,篩選出綜合性能優異的氯化物熔鹽體系。其中,MgCl2-NaCl-KCl熔鹽 (摩爾分數為45.4%-33.0%-21.6%,MNKC代表該熔鹽體系) 以其較低的熔點 (385 ℃)[7,8]、較高的熱容 (1.180 J·g-1·K-1)[7]、較低的成本 (325/t,4.95/kWh)[7]吸引了眾多研究者的注意[7-9]。其中,低熔點在工程上具有重要意義,一方面可提高熔鹽介質的工作溫度范圍,另一方面可以降低熔鹽管道發生凍堵的可能性,提高集熱系統整體的可靠性。
熔鹽材料相容性問題是研究者們關注最多的問題之一[10],也是基于熔鹽介質的太陽能集熱系統能否成功的核心問題之一[11]。盡管氯鹽對各類高溫合金的本征腐蝕很低,甚至低于氟鹽對金屬的本征腐蝕[12],然而由于水、氧等雜質不可避免的存在氯化物熔鹽中[13],在高溫下帶來的腐蝕實際是非常嚴重的,特別是在環境中氧分壓控制不好的條件下[14]。即使在惰性氣氛下,由氯鹽中雜質驅動引起的腐蝕仍不容忽視[15]。熔鹽雜質的存在甚至被認為是引起氯鹽或氟鹽腐蝕加劇的最重要原因[16]。因此,熔鹽凈化是熔鹽腐蝕控制的重要手段。
熔鹽電位是決定熔鹽腐蝕性的一個重要參數[17]。熔鹽電位由熔鹽自身的組成、雜質及所處的環境共同決定。通過凈化熔鹽、添加氧化還原緩沖離子對、或控制熔鹽覆蓋氣的組成可以降低熔鹽電位,從而達到腐蝕控制的目的[17]。另外,通過熔鹽電位結合熔鹽氧酸堿度 (E-pO2?圖) 可以預測金屬的穩定區、鈍化區及腐蝕區,為熔鹽腐蝕控制提供理論依據[18]。
金屬Mg在氯化物熔鹽中具有一定的溶解度[19],可與熔鹽中的鎂離子形成具有電位控制作用的電極電對。有研究[20,21]表明,金屬Mg在含鎂鹽的熔鹽中可能以Mg+、Mg2+或Mg22+等形式溶解。這一現象為采用金屬Mg作為MNKC熔鹽體系的緩蝕劑提供了理論基礎。首先,金屬Mg的引入可以除去熔鹽中的各類氧化性雜質 (如過渡金屬離子、溶解O2或Cl2、水及水解產物HCl、Mg(OH)Cl等),對熔鹽起到凈化效果。另外,溶解的金屬Mg可以與Mg2+形成具有電位調節能力的氧化還原離子對,大幅降低熔鹽電位,從而達到抑制金屬材料的腐蝕的目的。已有文獻采用金屬Mg控制含鎂氯鹽的腐蝕并取得不錯的效果。文獻[22,23]發現向MgCl2-KCl(32-68,mol%) 熔鹽中加入1.15% (摩爾分數) 金屬Mg,可以大幅降低該氯鹽對Haynes 230合金的腐蝕速率,使其腐蝕速率低于15 μm/a,滿足DOE SunShot項目30 a設計使用壽命的目標要求。
盡管金屬Mg對含鎂氯鹽有很好的腐蝕抑制效果,但由于金屬Mg在高溫下具有較高的蒸汽壓 (330 Pa/650 ℃)[24],長時間運行會有較高的損耗。另外,環境中微量的水、氧雜質也會不斷消耗溶解Mg致使其含量下降,Mg的腐蝕抑制效果也會降低。因此,如何對含鎂氯鹽體系金屬Mg的緩蝕效果進行在線監測顯得尤為必要。本文通過電化學方法結合浸泡腐蝕測試考察了金屬Mg對MNKC熔鹽的凈化及腐蝕抑制作用,對比了不同鎂金屬添加量下316H不銹鋼在MNKC熔鹽中的腐蝕,并對實驗結果及相關機理進行了討論。
1 實驗方法
MNKC熔鹽的制備:考慮到MgCl2具有較強的揮發性,實驗中將稱取的196 g (45.4%) MgCl2置于剛玉坩堝底部,將混合好的87.4 g (33.0%) NaCl與73.0 g (21.6%) KCl覆蓋在MgCl2上面,350 ℃烘干脫水過夜,隨后升溫至680 ℃并保溫10 h,隨后程序控制12 h降至室溫,得到白色晶體形態的MNKC鹽。所采用的氯鹽原料均為分析純無水氯鹽。熔鹽的稱量、裝料、烘干、熔融及后續的電化學測試及浸泡腐蝕測試均在帶自凈化功能的氬氣手套箱及與之相連的井式爐中進行。手套箱內氬氣氣氛中的水、氧指標低于2×10-6。經過稱量發現,在此條件下兩次制備MNKC熔鹽收率分別為98.5%和98.9%。
分別稱取10 g NiCl2,22 g MgCl2,9.8 g NaCl,8.2 g KCl,均勻混合,配制成20% (質量分數) NiCl2-MNKC混合鹽。將上述混合鹽填充至定制的高純熱壓氮化硼管 (?8 mm×50 mm,壁厚δ1 mm,底部有0.5 mm刻槽便于離子導通) 中制成Ni/NiCl2參比電極。每支參比電極管填充0.7 g左右的上述混合鹽。封裝完畢后置于坩堝中預熔融活化。實際測試發現其穩定性和靈敏性良好,置于熔鹽中5 min內即可達到穩定工作狀態,使用壽命經測試可達50 h以上。使用過程中定期通過循環伏安法對參比電極的穩定性進行標定,即通過觀察MNKC熔鹽電化學窗口的漂移觀測參比電極電位是否發生改變,整個使用壽命期間參比電極電位漂移不超過5 mV。文中電位值如無特殊說明均為相對該Ni/NiCl2參比電極的電位值。
實驗測試中使用?1 mm的鎢金屬工作電極材料純度高于99%。腐蝕測試采用的316H不銹鋼材料 (?1 mm金屬絲或20 mm×7 mm×2 mm金屬片) 的主要組成為Fe (基),C 0.09%,Si≤1%,Mn≤2%,Cr 17%,Ni 12%,Mo 2.5%。所使用的金屬鎂粉、鎂棒 (φ8 mm) 純度高于99%,鎂粉粒徑為75~150 μm。實驗中使用的其它試劑如無水氯化亞鉻均為分析純試劑。
電化學測試在AutoLab 302N型電化學工作站上完成。三電極體系,研究電極為待測金屬材料,輔助電極為石墨棒,參比電極為Ni/NiCl2。穩態極化曲線測試時掃描電位范圍從低于開路電位0.15 V到高于開路電位0.15 V,掃描速率為5 mV/s,電極浸入熔鹽平衡5 min后開始測量。電化學測試前,金屬電極均依次經過38,18和11 μm碳化硅砂紙打磨后進行測試,以保證不同測試中金屬電極的表面狀態處于相近狀態。測試重復3次以上,直至獲得重現性較好的極化曲線,然后根據曲線讀取腐蝕電位并計算腐蝕電流密度和線性極化電阻。循環伏安測試中工作電極為鎢絲,其它測試條件與上述極化曲線相同。浸泡腐蝕實驗在電化學測試同一裝置中進行,316H不銹鋼片 (20 mm×7 mm×2 mm) 經分級打磨、除油、清洗后于MNKC熔鹽中浸泡100 h。完成浸泡后取出清洗、制樣打磨后通過掃描電鏡 (SEM LEO,1530VP) 觀察截面微觀形貌。實驗中金屬鎂粉經稱量后通過特制的不銹鋼長頸漏斗直接加入熔鹽,攪拌后保溫30 min,再進行相關測試。
2 結果與討論
2.1 鎂粉對MNKC熔鹽的凈化效果
由于無水氯化鎂具有較強的吸潮特性,MNKC熔鹽在配制、熔融過程中所吸收的水會與氯鹽發生水解反應,生成腐蝕性較強的MgOHCl和HCl,其中前者能穩定的存在于熔鹽體系[6],并對金屬造成較大的腐蝕危害。金屬Mg作為強還原劑對熔鹽中的水解產物、溶解氧、過渡金屬離子、硫酸根離子等均有良好的去除效果 (見式 (1)~(5))。特別是水解產物和溶解氧,常規分析方法 (如ICP-OES、離子色譜等) 不便測量,但是對熔鹽的腐蝕性往往是決定性的。
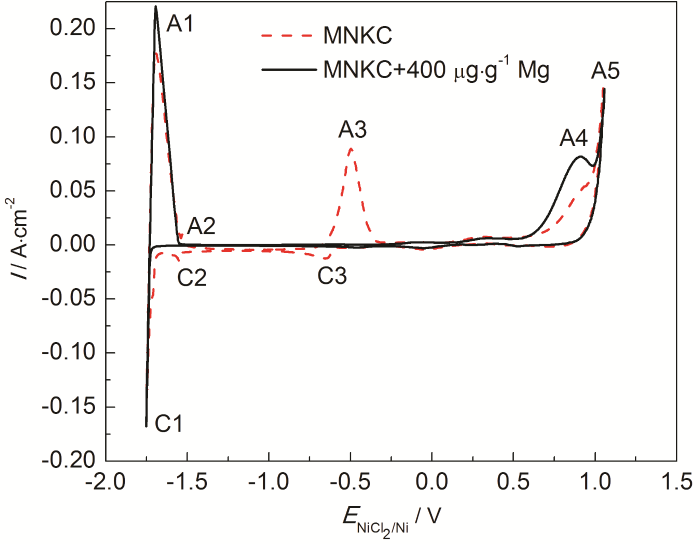
圖1為添加金屬Mg前后MNKC熔鹽循環伏安曲線對比。從圖中可以看到,未添加金屬Mg的熔鹽體系循環伏安曲線上有5處比較明顯的氧化峰 (A1至A5) 和3處對應的還原峰 (C1至C3),其中A1/C1峰歸為Mg的氧化和還原峰 (-1.75 V vs NiCl2/Ni),A5歸為氯氣的析出 (1.05 V vs NiCl2/Ni),A2/C2、A3/C3及A4峰由熔鹽雜質造成。添加400 μg·g-1金屬Mg的熔鹽體系循環伏安曲線中A2/C2及A3/C3峰均消失,其中消失的A3/C3峰對應于水解產物MgOHCl的還原和氧化 (式 (6) 和 (7))[25],而A2/C2對應雜質金屬離子。因此,通過循環伏安圖可以非常直觀地看到金屬Mg對這兩類雜質的凈化效果。值得注意的是添加金屬Mg以后,A4氧化峰有增強的趨勢,根據文獻中O在惰性電極上的析出電位[26]分析A4對應熔鹽中O2-的氧化峰。因此,金屬Mg對熔鹽中O2-的脫除沒有效果。添加金屬Mg后O2-氧化峰增強的原因可能是Mg與水解產物MgOHCl反應后釋放出部分自由O2-導致的。
圖1 鎢電極在600 ℃ MNKC熔鹽體系中的循環伏安曲線
除了上述循環伏安曲線外,熔鹽電位也可作為衡量熔鹽氧化性雜質去除效果的一個重要參考指標。熔鹽電位并不是一個嚴格的物理化學概念,可以理解為熔鹽氧化還原的水平。在以氧化物為主的熔鹽體系可采用“氧勢”的概念表示熔鹽電位,而在氟鹽體系可以采用“氟勢”的概念表示,Olander等[17]對此有專門論述。當熔鹽中氧化性雜質含量較高時,熔鹽具有較高的熔鹽電位,而當氧化性雜質降低時,熔鹽電位隨之降低。熔鹽電位通常不便直接測定,但可以通過添加氧化還原電極電對對熔鹽電位進行調控[17]。例如,根據Nernst方程可以很方便地計算MNKC熔鹽中溶解Mg對熔鹽電位的調控作用:
式中,E0*為表觀標準電極電位,由圖1循環伏安曲線Mg析出電位可以認為E0*為-1.75 V vs NiCl2/Ni,XMg2+為MNKC體系MgCl2摩爾分數,XMg為溶解金屬Mg的摩爾分數,R為理想氣體狀態常數,F為法拉第常數,n為轉移電子數2。根據上式計算MNKC熔鹽中分別溶解1、10、100、1000 μg·g-1金屬Mg時的熔鹽電位分別為-1.305、-1.391、-1.478、-1.565 V vs NiCl2/Ni。因此,在溶解有金屬Mg的MNKC熔鹽體系可以通過分析熔鹽中Mg的濃度來計算熔鹽電位。實際的熔鹽回路中,直接對熔鹽取樣分析是比較困難的。通過電化學探針在線進行電位測量,可反映熔鹽電位的變化情況。
根據混合電位理論,金屬 (含合金) 的腐蝕電位是熔鹽與金屬材料反應耦合形成的混合電位,主要由熔鹽電位、金屬材料組成及表面狀態共同決定。因此,通過測量確定組成和表面狀態的金屬腐蝕電位可以反映熔鹽電位的高低。圖2給出了316H不銹鋼在MNKC熔鹽體系隨金屬Mg添加量增加時的腐蝕電位變化曲線,從圖中可以看到,隨著Mg添加量的增加,腐蝕電位由-0.64 V逐漸降低至-1.14 V,根據混合電位理論可以推斷熔鹽電位從由氧化性雜質控制逐漸轉向由溶解Mg與MgCl2形成的Mg2+/Mg電對控制,這種轉變對熔鹽腐蝕的抑制極為重要。綜上所述,金屬Mg的添加不僅能去除MNKC熔鹽體系中的氧化性雜質,而且溶解的金屬Mg可以與MgCl2形成電位很低的氧化還原電極電對并實現對熔鹽電位的控制。
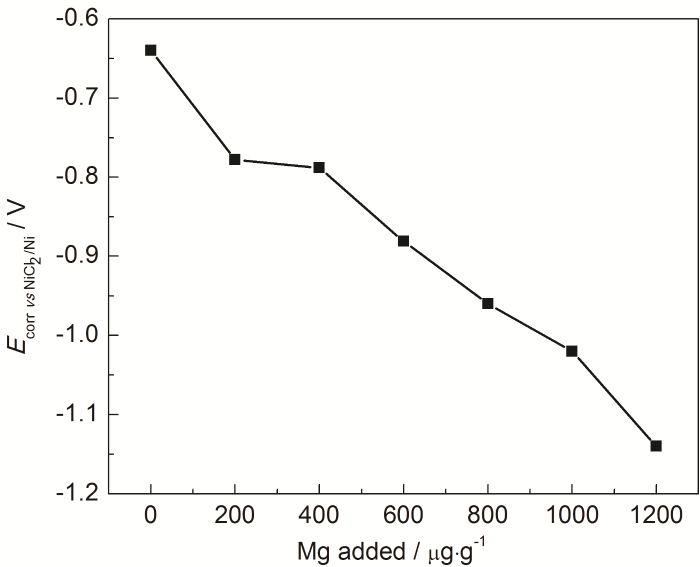
圖2 316H不銹鋼在600 ℃ MNKC熔鹽體系的腐蝕電位隨Mg添加量的變化曲線
2.2 金屬Mg對MNKC熔鹽腐蝕特性的影響
為了進一步量化Mg的添加量對MNKC熔鹽腐蝕特性的影響,本文測定316H不銹鋼在不同Mg添加量MNKC熔鹽中的穩態極化曲線 (圖3),并通過Tafel外延法計算了316H不銹鋼的腐蝕電流密度 (圖4),同時也給出了相應的線性極化電阻 (圖5)。從圖4可以看到,在未添加鎂粉的MNKC熔鹽中,316H不銹鋼的腐蝕電流密度為1670 μA/cm2,向MNKC熔鹽中添加200 μg·g-1金屬鎂粉以后,316H在MNKC熔鹽中的腐蝕電流密度大幅下降約2個數量級至50.2 μA/cm2,隨著Mg添加量的增加,腐蝕電流密度繼續小幅下降直至添加量為800 μg·g-1時達到最低點11.5 μA/cm2,隨后小幅增加。而圖5的線性極化電阻曲線則呈現相應的先升高隨后小幅下降的趨勢。從整體趨勢看,當Mg添加量高于500 μg·g-1時,316H不銹鋼在MNKC熔鹽中測得的腐蝕電位低于-0.80 V (圖2),腐蝕電流密度低于25 μA/cm2,而線性極化電阻高于800 Ω·cm2,腐蝕特征指標遠優于未添加Mg的數據,表明其處于很好的腐蝕抑制狀態。
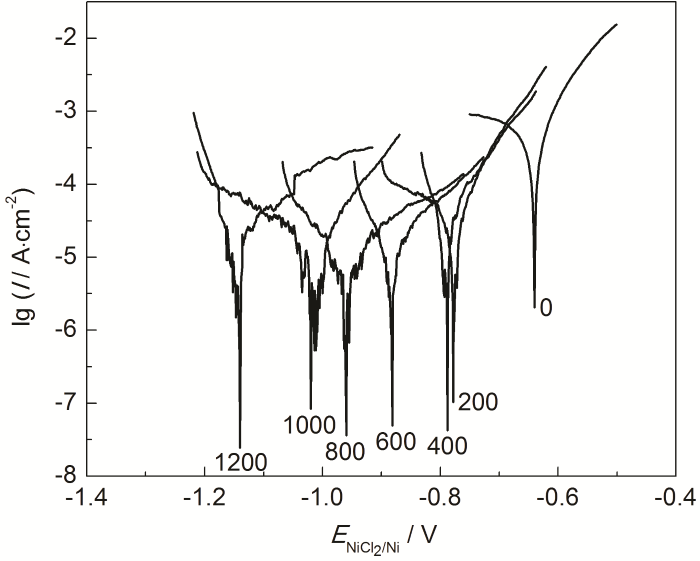
圖3 600 ℃下316H不銹鋼在MNKC-Mg (0~1200 μg·g-1) 熔鹽體系的極化曲線
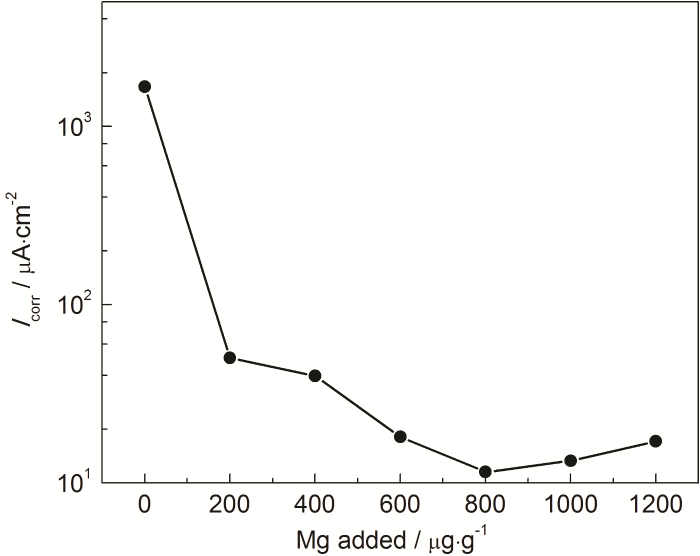
圖4 600 ℃下316H不銹鋼在MNKC熔鹽體系中的腐蝕電流密度隨Mg添加量的變化曲線
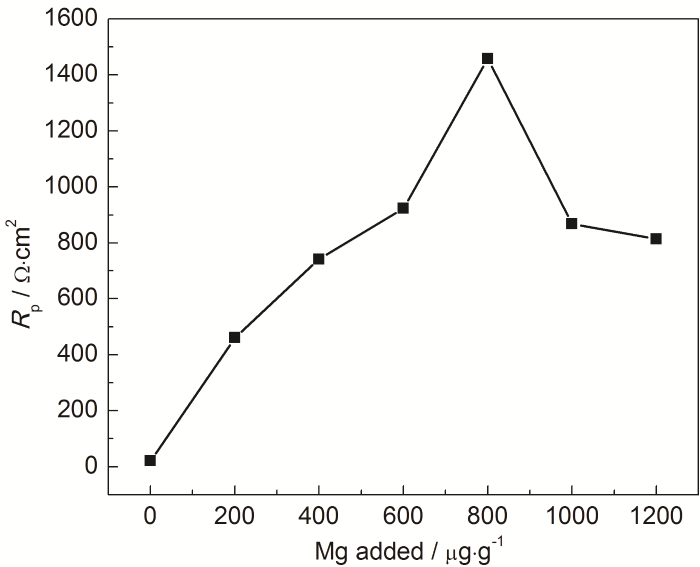
圖5 600 ℃下316H不銹鋼在MNKC熔鹽體系中的線性極化電阻隨Mg添加量的變化曲線
值得關注的特殊現象是,當金屬Mg添加量高于800 μg·g-1時測得的腐蝕電流密度有小幅上揚,或極化電阻有一定程度的降低,分析認為這并不意味著316H不銹鋼腐蝕的增加,而可能是熔鹽中溶解金屬Mg濃度的增加導致其參與到腐蝕反應中來。即在較低的腐蝕電位下 (如-0.96 V以下),溶解金屬Mg在腐蝕電極上的氧化逐漸替代316H不銹鋼中Cr的氧化腐蝕。此時,通過316H不銹鋼電極測得的腐蝕電流密度應遠高于316H不銹鋼的真實腐蝕速率。鑒于此種情形下通過極化曲線測得腐蝕參數指標仍處在較低水平 (Icorr<25 μA/cm2,Rp>800 Ω·cm2),因此我們仍可以通過該方法來監測316H不銹鋼在該體系中的腐蝕速率。例如,當測得316H不銹鋼在MNKC-Mg體系中的腐蝕電位高于-0.80 V且腐蝕電流密度高于25 μA/cm2或極化電阻低于800 Ω·cm2,我們可以向體系中添加適量金屬Mg,直到各項監測指標滿足我們的預期值。這組特征指標 (即Ecorr<-0.80 V,Icorr<25 μA/cm2,Rp>800 Ω·cm2) 可以作為316H不銹鋼在MNKC熔鹽體系腐蝕監測和調控的臨界點。
2.3 MNKC-Cr(II) 熔鹽體系循環伏安研究
由于316不銹鋼鈍化膜在氯鹽中不能長期穩定存在,316不銹鋼在熔鹽體系的腐蝕機理主要是Cr的流失[27]。為了進一步闡明金屬Mg和熔鹽電位對熔鹽腐蝕抑制的機理,對MNKC-Cr(II) 體系的循環伏安行為進行了研究。實驗前先采用金屬鎂棒與MNKC熔鹽接觸平衡以去除雜質,然后加入質量分數0.2%的CrCl2,考察了Cr的各種物種在MNKC熔鹽體系的氧化還原行為。由Martinez等[28]對氯鹽體系Cr電化學行為研究可知Cr(II) 在含氧氯鹽中存在自由Cr2+、Cr2O2+以及CrO 3種形式,并與熔鹽中的O2-保持平衡。上文已經提到,金屬Mg并不能去除MNKC熔鹽中的O2-,因此所研究的MNKC-Cr(II) 體系必然也含有Cr2+、Cr2O2+以及CrO 3種形式的Cr(II) 物種。通過文獻[28]所給出的各種氧化還原反應的標準電極電勢,結合本文MNKC-Cr(II) 體系的實際特點 (如以Cr(II) 為主且存在多種形式),將圖6中各氧化還原峰的歸屬列于表1。其中A3峰對應3種Cr(II) 物種氧化為Cr2O3的疊加峰。由于A3反應的產物Cr2O3為不溶物,因此反應的可逆性較差,與C3還原峰相對弱小的表現相符。
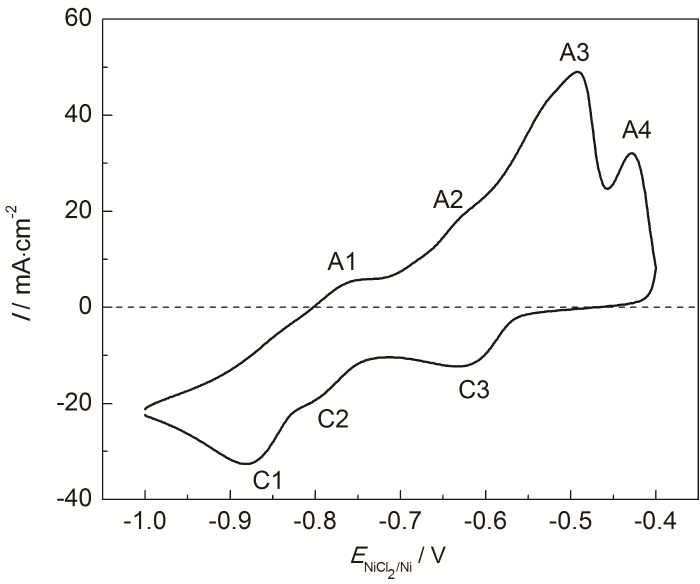
圖6 鎢電極在600 ℃的MNKC-0.2%CrCl2熔鹽體系中的循環伏安曲線
表1 循環伏安曲線氧化還原峰歸屬匯總
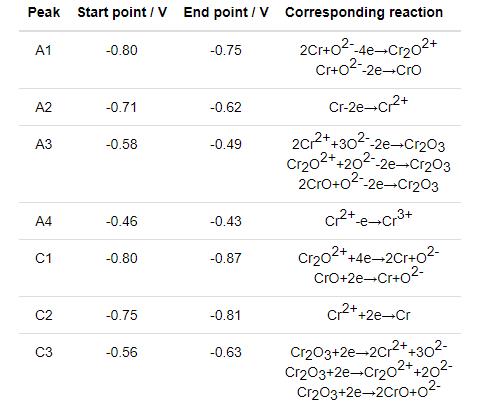
與金屬腐蝕行為相關的兩個氧化峰是A1和A2,分別對應金屬Cr氧化為Cr2O2+(或CrO) 和Cr2+。從圖6和表1的結果可以看到,A1峰的起始電位在-0.80 V,A2峰的起始電位在-0.71 V。即由于O2-的存在,金屬Cr的氧化起始電位由-0.71 V降低至-0.80 V。這一結論對316H不銹鋼的腐蝕控制非常關鍵。因此,欲抑制316H不銹鋼的氧化腐蝕,其在熔鹽中的腐蝕電位應控制在-0.80 V以下,這與上文極化曲線測試的結果相吻合。即腐蝕電位高于-0.80 V,316H不銹鋼中的金屬Cr在含有O2-的MNKC熔鹽體系有氧化為Cr2O2+(或CrO) 的趨勢,而低于這一電位則呈現Cr2O2+(或CrO) 還原為金屬Cr的趨勢。這也解釋了極化曲線測試在腐蝕電位降低至-0.96 V及以下時,隨著Mg添加量的增加,腐蝕電流密度有所增加的原因 (圖3和4)。此時從腐蝕電位向陽極極化時 (即-0.96→-0.81 V),電極上的主要反應是溶解Mg的氧化而非316H不銹鋼電極中金屬Cr的氧化。因此,在熔鹽腐蝕監測中,我們不能只看腐蝕電流密度或極化電阻的大小,而應結合腐蝕電位以及電極上發生的反應進行綜合分析,從而判斷體系的真實腐蝕情況。
2.4 MNKC熔鹽體系浸泡腐蝕
通過以上腐蝕電化學的相關測試表明,向MNKC熔鹽中加入500 μg·g-1以上的金屬Mg可以有效控制316H不銹鋼的腐蝕,相應的腐蝕控制判據為Ecorr<-0.80 V,Icorr<25 μA/cm2,Rp>800 Ω·cm2。為進一步證實這一判斷,在MNKC熔鹽體系開展了316H不銹鋼浸泡腐蝕測試。在添加500 μg·g-1金屬Mg的MNKC熔鹽中浸泡100 h,316H不銹鋼樣片未見可觀測的失重或增重現象,微觀截面照片未見Cr流失導致的晶間腐蝕現象 (圖7)。而相同條件下,316H不銹鋼在未添加金屬Mg的MNKC溶液中浸泡100 h后失重0.18%,樣品截面照片顯示發生了Cr流失造成的晶間腐蝕,腐蝕深度達30 μm (圖8)。這一對比測試表明添加的500 μg·g-1金屬Mg對MNKC體系316H不銹鋼的腐蝕抑制作用非常顯著。

圖7 600 ℃下MNKC-500 μg·g-1 Mg體系浸泡100 h后316H不銹鋼截面SEM像

圖8 600 ℃下MNKC體系浸泡100 h后316H不銹鋼截面SEM像
此外,500 μg·g-1金屬Mg添加量對應的腐蝕電流密度 (25 μA/cm2) 轉換為316H不銹鋼100 h腐蝕深度約為12 μm,而在該體系實際浸泡100 h后并未發現Cr流失 (圖7)。這也從側面證實了Ecorr<-0.80 V時所測得的Icorr遠高于316H不銹鋼真實腐蝕速率的判斷。
3 結論
金屬鎂對MgCl2-NaCl-KCl(MNKC) 熔鹽具有良好的凈化和電位控制效果。316H不銹鋼在不同鎂添加量的MNKC熔鹽體系的穩態極化曲線測試表明,當鎂添加量高于500 μg·g-1時,MNKC熔鹽對316H不銹鋼的腐蝕作用基本可以忽略,相應的腐蝕特征參數Ecorr<-0.80 V vs NiCl2/Ni,Icorr<25 μA/cm2,Rp>800 Ω·cm2可以作為腐蝕監測與控制的判據。當鎂的添加量高于800 μg·g-1且316H不銹鋼Ecorr<-0.96 V vs NiCl2/Ni時,采用極化曲線測量得到的腐蝕電流密度或極化電阻主要由溶解鎂在電極上的反應所產生的,316H不銹鋼自身腐蝕反應的貢獻基本可以忽略,且由于此時測得的總的腐蝕速率仍在較低水平 (Icorr<25 μA/cm2,Rp>800 Ω·cm2),因此即使在較高鎂含量下,穩態極化曲線法仍可作為MNKC-Mg熔鹽體系腐蝕監測手段,并仍可將Ecorr<-0.80 V vs NiCl2/Ni,Icorr<25 μA/cm2,Rp>800 Ω·cm2作為腐蝕控制或干預的目標。
參考文獻
1 Myers P D, Goswami D Y. Thermal energy storage using chloride salts and their eutectics [J]. Appl. Therm. Eng., 2016, 109: 889
2 Xu X K, Wang X X, Li P W, et al. Experimental test of properties of KCl-MgCl2 eutectic molten salt for heat transfer and thermal storage fluid in concentrated solar power systems [J]. J. Sol. Energy Eng., 2018, 140: 051011
3 Xu X K, Dehghani G, Ning J X, et al. Basic properties of eutectic chloride salts NaCl-KCl-ZnCl2 and NaCl-KCl-MgCl2 as HTFs and thermal storage media measured using simultaneous DSC-TGA [J]. Sol. Energy, 2018, 162: 431
4 Li Y Y, Xu X K, Wang X X, et al. Survey and evaluation of equations for thermophysical properties of binary/ternary eutectic salts from NaCl, KCl, MgCl2, CaCl2, ZnCl2 for heat transfer and thermal storage fluids in CSP [J]. Sol. Energy, 2017, 152: 57
5 Hu B H, Ding J, Wei X L, et al. Test of thermal physics and analysis on thermal stability of high temperature molten salt [J]. Inorgan. Chem. Ind., 2010, 42(1): 22
5 胡寶華, 丁靜, 魏小蘭等. 高溫熔鹽的熱物性測試及熱穩定性分析 [J]. 無機鹽工業, 2010, 42(1): 22
6 Ding W J, Bonk A, Bauer T. Corrosion behavior of metallic alloys in molten chloride salts for thermal energy storage in concentrated solar power plants: A review [J]. Front. Chem. Sci. Eng., 2018, 12: 564
7 Mohan G, Venkataraman M, Gomez-Vidal J, et al. Thermo-economic analysis of high-temperature sensible thermal storage with different ternary eutectic alkali and alkaline earth metal chlorides [J]. Sol. Energy, 2018, 176: 350
8 Pelton A D, Chartrand P. Thermodynamic evaluation and optimization of the LiCl-NaCl-KCl-RbCl-CsCl-MgCl2-CaCl2 system using the modified quasi-chemical model [J]. Metall. Mater. Trans., 2001, 32A: 1361
9 Sun L P, Wu Y T, Ma C F. Experimental study on optimization of molten salt for solar high temperature heat storage [J]. Acta Energ. Sol. Sin., 2008, 29: 1092
9 孫李平, 吳玉庭, 馬重芳. 太陽能高溫蓄熱熔融鹽優選的實驗研究 [J]. 太陽能學報, 2008, 29: 1092
10 Patel N S, Pavlík V, Bo?a M. High-temperature corrosion behavior of superalloys in molten salts: A review [J]. Crit. Rev. Solid State Mater. Sci., 2017, 42: 83
11 Sun H, Su X Z, Zhang P, et al. Research status and progress of molten salts corrosion for concentrated solar thermal power [J]. Corros. Sci. Prot. Technol., 2017, 29: 282
11 孫華, 蘇興治, 張鵬等. 聚焦太陽能熱發電用熔鹽腐蝕研究現狀與展望 [J]. 腐蝕科學與防護技術, 2017, 29: 282
12 Vignarooban K, Pugazhendhi P, Tucker C, et al. Corrosion resistance of Hastelloys in molten metal-chloride heat-transfer fluids for concentrating solar power applications [J]. Sol. Energy, 2014, 103: 62
13 Vindstad J E, Mediaas H, ?stvold T. Hydrolysis of MgCl2-containing melts [J]. Acta Chem. Scand., 1997, 51: 1192
14 Tzvetkoff T, Kolchakov J. Mechanism of growth, composition and structure of oxide films formed on ferrous alloys in molten salt electrolytes-a review [J]. Mater. Chem. Phys., 2004, 87: 201
15 Ding W J, Shi H, Xiu Y L, et al. Hot corrosion behavior of commercial alloys in thermal energy storage material of molten MgCl2/KCl/NaCl under inert atmosphere [J]. Sol. Energy Mater. Sol. Cells, 2018, 184: 22
16 Raiman S S, Lee S. Aggregation and data analysis of corrosion studies in molten chloride and fluoride salts [J]. J. Nucl. Mater., 2018, 511: 523
17 Olander D. Redox condition in molten fluoride salts-Definition and control [J]. J. Nucl. Mater., 2002, 300: 270
18 Zeng C L, Zhang J Q, Wu W T. Electrochemistry of corrosion in molten salts [J]. Corros. Sci. Prot. Technol., 1992, 4: 16
18 曾潮流, 張鑒清, 吳維. 熔鹽腐蝕電化學 [J]. 腐蝕科學與防護技術, 1992, 4: 16
19 Tian H Q, Du L C, Huang C L, et al. Enhanced specific heat capacity of binary chloride salt by dissolving magnesium for high-temperature thermal energy storage and transfer [J]. J. Mater. Chem., 2017, 5A: 14811
20 Jasien P G, Dykstra C E. An ab initio study of the stability and electronic structure of univalent magnesium salts [J]. Chem. Phys. Lett., 1984, 106: 276
21 Krumpelt M, Fischer J, Johnson I. Reaction of magnesium metal with magnesium chloride [J]. J. Phys. Chem., 1968, 72: 506
22 Garcia-Diaz B L, Olson L, Martinez-Rodriguez M, et al. High temperature electrochemical engineering and clean energy systems [J]. J. S. C. Acad. Sci., 2016, 14: 11
23 Mehrabadi B A T, Weidner J W, Garcia-Diaz B, et al. Modeling the effect of cathodic protection on superalloys inside high temperature molten salt systems [J]. J. Electrochem. Soc., 2017, 164: C171
24 Zhang M J, Li J D, Guo Q F. Recovery of magnesium from rejected magnesium alloy by vacuum sublimation process-magnesium alloy treating technology [J]. Light Met., 2006, (2): 48
24 張明杰, 李繼東, 郭清富. 真空升華法從廢鎂合金中回收鎂—鎂合金無害化處理技術 [J]. 輕金屬, 2006, (2): 48
25 Ding W J, Bonk A, Gussone J, et al. Electrochemical measurement of corrosive impurities in molten chlorides for thermal energy storage [J]. J. Energy Storage, 2018, 15: 408
26 Wang D H, Xiao W. Inert anode development for high-temperature molten salts [A].
26 Lantelme F, Groult H. Molten Salts Chemistry [M]. Oxford: Elsevier, 2013: 171
27 Sun H, Wang J Q, Li Z J, et al. Corrosion behavior of 316SS and Ni-based alloys in a ternary NaCl-KCl-MgCl2 molten salt [J]. Sol. Energy, 2018, 171: 320
28 Martínez A M, Castrillejo Y, B?rresen B, et al. Chemical and electrochemical behaviour of chromium in molten chlorides [J]. J. Electroanal. Chem., 2000, 493: 1
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。
相關文章
無相關信息

官方微信
《中國腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護網官方QQ群:140808414
點擊排行
PPT新聞
“海洋金屬”——鈦合金在艦船的
點擊數:7214
腐蝕與“海上絲綢之路”
點擊數:5808