摘 要:高溫金屬防護涂層在先進航空發動機上有著廣泛應用,其通過生成表面保護性氧化膜為發動機熱端部件提供保護,以提高熱端部件的抗高溫氧化腐蝕能力,延長熱端部件的服役壽命。微量活性元素由于能降低涂層材料的高溫氧化速率,提高涂層表面氧化膜的粘附性而被廣泛用于高溫防護涂層的改性上,特別是用于超高溫(≥1200 ℃)金屬涂層潛在應用材料NiAl 的改性上。但是截至目前,由于活性元素效應的影響因素復雜,相關作用模型并不完善,人們對活性元素效應的微觀作用機理還存在較大的爭論。從活性元素促進元素的選擇性氧化、降低氧化膜生長速率和提高氧化膜粘附性等角度出發,綜述了活性元素改性在高溫金屬防護涂層領域的研究進展,特別是針對以氧化鋁形成合金為代表的金屬防護涂層材料。重點分析了活性元素改性對氧化膜微觀結構、生長機制、界面孔洞、內應力等的影響以及活性元素與雜質元素(如C 和S)之間的交互作用。最后,對今后的研究工作進行了展望,希望在原子尺度進行更深入、更細致的研究,為超高溫金屬防護涂層的發展提供理論指導。
關鍵詞:高溫金屬防護涂層;氧化鋁形成合金;高溫氧化;活性元素效應;作用機理
提高關鍵熱端部件用鎳基高溫合金的承溫能力對于發展高推重比先進航空發動機至關重要。然而,目前研制的高溫合金已接近其承溫極限,僅僅通過合金設計難以滿足高溫及惡劣環境下的應用需求,因此表面涂覆高溫防護涂層十分必要。高溫防護涂層技術作為先進航空發動機的關鍵技術之一,可進一步降低發動機熱端部件的表面溫度,對提高發動機熱端部件的抗高溫氧化腐蝕性能,延長熱端部件服役壽命發揮著重要作用。目前,高溫防護涂層,尤其是高溫金屬防護涂層,已經在航空航天、石油化工、船舶、能源等領域得到了廣泛應用[1-2]。
眾所周知,涂層表面生成保護性氧化膜是金屬防護涂層為基體提供保護性的關鍵,其中,α-Al2O3 是比較典型的保護性氧化膜,它可以在1000 ℃以上起到良好的保護作用。通常將高溫下表面能夠形成完整、致密Al2O3 的合金稱為氧化鋁形成合金,如NiCrAl、FeCrAl、CoCrAl 等,它們是高溫金屬防護涂層的常用材料。為了提高這些合金表面氧化膜的抗剝落性能,通常在氧化鋁形成合金中添加Y、Hf 等活性元素,形成如NiCrAlY、FeCrAlY、CoCrAlY 等合金。另外,隨著高性能航空發動機的發展,熱端部件工作溫度不斷提高,對涂層高溫防護性能也提出了更高的要求。對金屬涂層而言,迫切需要發展超高溫、長壽命、抗氧化的涂層材料。而NiAl 金屬間化合物被認為是極具前景的超高溫金屬涂層材料,但是其循環氧化壽命不高,氧化膜容易剝落[3-9]。研究發現,活性元素改性可以顯著改善合金及涂層的抗高溫氧化腐蝕性能,降低氧化膜生長速率,提高氧化膜的粘附性[10-16],因此引起了人們極大的關注。近年來,研究人員針對活性元素改性進行了大量的研究。雖然取得了顯著成果,但活性元素的微觀作用機理還存在較大的爭議,相關基礎研究還有待進一步突破。因此本文以具有代表性的高溫金屬防護涂層材料——氧化鋁形成合金(如NiAl)為例,綜述了國內外活性元素改性在高溫金屬防護涂層領域的研究進展,重點介紹了活性元素效應及其作用機理的最新成果,希望對后續的研究起到借鑒和指導作用。
1 活性元素效應
活性元素(Reactive element, RE)是指氧親和元素,包括所有的稀土元素(Sc、Y 和La 系元素)以及Hf、Zr、Ti 等。活性元素在高溫氧化方面的作用最早由Pfeil[17]發現,之后人們針對這一現象進行了大量研究。Whittle 和Stringer[18]總結已有的研究成果,于1980 年首次提出“活性元素效應”這一概念,并將活性元素效應總結為以下幾點(最初主要針對氧化鉻形成合金,后來發現同樣適用于氧化鋁形成合金): 1)促進氧化膜形成元素的選擇性氧化;2)改變氧化膜生長機制;3)抑制氧化膜/合金界面孔洞的形成;4)降低氧化膜生長速率,提高氧化膜的粘附性。其中,1)、2)、3)涉及的效應歸根結底表現在對氧化膜生長速率和粘附性的影響上,因此,此后有關活性元素作用機理的研究主要集中在闡明活性元素如何降低氧化膜生長速率和提高氧化膜的粘附性上。
針對活性元素的作用機理,研究者已經提出了多種作用模型,包括氧化物“釘扎”模型[19-20]、“硫效應”模型[21-22]和動力學偏聚模型[23]等。隨后,各種先進的分析表征技術的發展應用(如二次離子質譜(SIMS)、場發射掃描透射電子顯微鏡(FEG-STEM)等)為這些模型提供了實驗數據上的支撐,促進了人們對活性元素效應的理解。然而,隨著研究范圍的進一步擴大,人們發現,活性元素的作用效果復雜多變,受到活性元素種類、添加量、添加方式、服役溫度、基體相組成等諸多因素的影響,已經建立的模型都存在一定的局限性,通常只能在特定環境下解釋某種活性元素的作用效果。比如動力學偏聚模型,一般用于解釋氧化鋁體系中活性元素對氧化膜生長速率的影響,而對氧化鉻體系中的活性元素效應難以給出合理的解釋。由此可見,活性元素對合金高溫氧化行為的影響十分復雜,明確活性元素的微觀作用機制、建立統一的活性元素作用模型仍然是當前研究的熱點。
2 活性元素對選擇性氧化的影響
大量研究結果表明,氧化鋁形成合金中添加活性元素(及其氧化物),可以促進氧化膜形成元素Al的選擇性氧化[24-25],這樣一方面降低了形成保護性氧化膜所需的臨界Al 含量,另一方面促進了保護性氧化膜的快速形成,減少了合金基體中的內氧化物形成。然而,近年來的研究發現,不同于活性元素的其他效應,選擇性氧化效應的前提是要合金晶粒發生細化。Pint 等[26]在改性Fe-Al 合金的研究中發現,合金晶粒尺寸不變,即使添加活性元素也不會促進Al 的選擇性氧化,而通過摻雜使得合金晶粒發生明顯細化時,形成保護性氧化膜所需的臨界Al 含量也隨之顯著降低。此外,一些表面改性技術(如添加活性元素氧化物、活性元素離子注入等)沒有顯著改善合金的顯微結構,因而也不會促進Al 的選擇性氧化[24]。由此可見,活性元素促進選擇性氧化與合金晶粒尺寸的細化有關,而非添加活性元素產生的化學效應。關于活性元素與氧化膜晶粒尺寸之間的關系,早期研究認為,高溫下活性元素氧化物的形成提供了成膜元素氧化的形核位點,促進了細晶氧化膜的形成[27]。但是,不僅是活性元素,其他第二相顆粒或表面缺陷活性元素離子在氧化膜晶界偏聚是影響氧化膜內元素傳輸機制,進而影響氧化膜生長機制及降低氧化膜生長速率的關鍵。Pint 等[10,23]針對活性元素改性FeCrAl 和NiAl 等合金的氧化過程進行了大量的研究,在已有研究成果的基礎上提出了“動力學偏聚”理論。該理論認為,氧化過程中活性元素離子在氧化膜內并非靜態,而是傾向于在氧化學勢梯度的作用下,向氧化膜/合金界面以及氧化膜晶界偏聚,并沿氧化膜晶界向外擴散。因此氧化一定時間后,活性元素氧化物將在氧化膜表面形核、長大(如圖2)[23],這一結果已被實驗證實[38-40]。由于活性元素離子與金屬陽離子有相同的擴散路徑,且離子尺寸更大、擴散更慢,也會產生類似的“形核效應”。在隨后的氧化過程中,這種細晶結構就主要依賴于活性元素所產生的“溶質拖曳”效應。該效應認為,添加了活性元素(包括活性元素氧化物)的合金,氧化過程中活性元素離子會在氧化膜晶界偏聚,可以釘扎晶界,阻礙晶界遷移,從而抑制晶粒長大,細化晶粒,同時產生更多的亞晶界,為Al 提供更多短路擴散的通道[10,28-29],促進保護性氧化膜的快速形成。
3 活性元素對氧化膜微觀結構及生長速率的影響
1984 年,Ramanarayanan 等[30]利用帶X 射線能譜的透射電子顯微鏡(TEM-EDXA)觀察到活性元素在氧化膜晶界偏聚,之后人們針對這一現象進行了大量研究。國內外研究者利用高分辨掃描透射電子顯微鏡(HR-STEM)、二次離子質譜(SIMS)、電子能量損失譜(EELS)等先進的表征技術手段,在多種合金體系中均檢測到活性元素在氧化膜晶界以及氧化膜/合金界面的偏聚[31-36](如圖1),并證明了活性元素只能以離子形式偏聚于氧化膜晶界,而非第二相顆粒[37]。
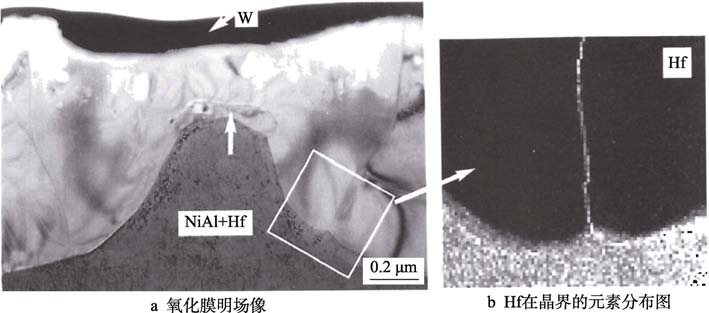
圖1 Hf 改性NiAl 合金(1100 ℃氧化100 h)后的氧化膜截面TEM 圖[36]
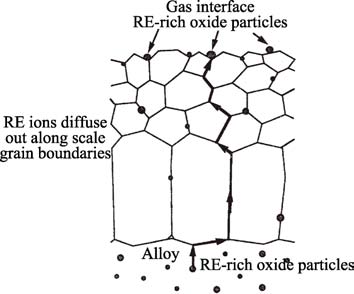
圖2 動力學偏聚理論示意圖[23]
因而可以有效抑制金屬陽離子的外擴散。與此相反,O 的吸附位點及擴散路徑與之完全不同,因此活性元素對O 的內擴散影響不大[41]。在活性元素的作用下,Al2O3 膜的生長機制由Al 向外和O 向內擴散同時進行轉變為以O 向內擴散為主,這導致氧化膜微觀結構從等軸晶向柱狀晶的轉變[15,42](如圖3 所示)以及氧化膜生長速率的降低[43-44]。
氧化膜微觀結構的改變與氧化膜生長機制密切相關。未改性合金Al2O3 膜的生長以O 向內和Al 向外雙向擴散為主,新的氧化物在氧化膜晶界形核,除向外生長成為脊外,同時橫向生長,最終形成等軸晶。而活性元素改性合金,表面氧化膜轉變為外層等軸晶加內層柱狀晶的雙層結構。這是由于活性元素離子晶界偏聚直接抑制了Al 離子的外擴散,使氧化膜生長以O 離子向內擴散為主,其橫向生長受到抑制,形成柱狀晶。

圖3 活性元素改性β-NiAl 合金(1200 ℃循環氧化100 h)后的氧化膜斷口形貌[15]
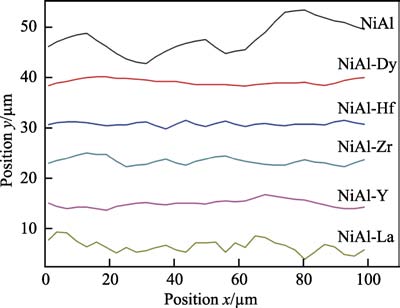
除氧化膜微觀結構外,活性元素改性對氧化膜生長速率也有顯著影響。相比于其他摻雜元素(如Y、Zr 等),NiAl、FeAl 等合金中摻雜Hf,可以更為顯著地降低Al2O3 膜生長速率,拋物線速率常數降低可達10 倍左右[12,45]。研究發現,氧化膜生長速率與摻雜活性元素的外擴散行為密切相關。一般認為,離子半徑較小的活性元素(如Ti 等),在氧化膜晶界擴散較快,對Al 離子的阻擋效應較弱[46];而離子半徑較大的活性元素(如Hf、Zr、Y 等),由于沿氧化膜晶界擴散較慢,可以更有效地阻礙Al 離子的外擴散過程,降低氧化膜生長速率[11-12],但也有反常現象。郭洪波等[15]對比了幾種活性元素改性NiAl 的高溫循環氧化行為,如圖4 所示,摻雜離子半徑最大的La 反而加速了合金氧化,氧化膜生長速率甚至高于未改性NiAl 合金,而離子半徑較小的Hf、Zr,其改性的合金氧化增重卻比半徑較大的Dy、Y 改性的合金氧化增重要小。由此可見,氧化膜生長速率與活性元素離子半徑之間的關系不能簡單地用動力學偏聚理論解釋,活性元素離子對Al 離子的阻礙作用除簡單的物理阻擋作用外,必然存在某種化學交互作用。因此,Pint 等[47]提出“有效離子半徑”的概念,將活性元素離子對Al 離子電子結構、擴散激活能等可能的影響考慮在內,用以描述“阻擋效應”的強度。利用這一概念可以很好地解釋不同活性元素對NiAl 合金氧化膜生長速率影響程度的不同。但是截至目前,活性元素離子對Al 離子的化學阻擋效應還沒有明確的解釋。
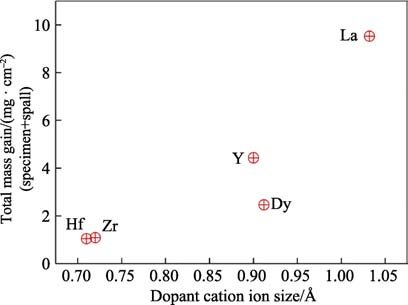
圖4 活性元素改性β-NiAl 合金1200 ℃循環氧化
4 活性元素對氧化膜粘附性的影響
針對活性元素效應,另外一個被廣泛關注的問題就是對氧化膜粘附性的改善。目前的研究認為,高溫氧化過程中,活性元素改善Al2O3 膜粘附性的機制主要有以下幾個方面[48-50]:1)抑制氧化膜/合金界面孔洞的形核與長大;2)在氧化膜/合金界面形成氧化物栓,提高氧化膜與合金接觸面積;3)緩解氧化膜褶皺;4)直接參與氧化膜/合金界面成鍵,提高界面鍵合能力。其中,1)是研究者認識較深入的一種活性元素作用機制,2)、3)的作用機制尚存在較大爭議。下面針對這4 種活性元素對氧化膜粘附性的改善機制進行詳細介紹。
氧化膜/合金界面孔洞的形成降低了氧化膜與合金基體的有效接觸面積,導致氧化膜極易剝落。研究人員針對界面孔洞的形成機理進行了比較系統的研究[51-53],目前提出的比較有代表性的模型,如空位沉積模型,認為高溫氧化過程中,由于氧化和元素擴散,氧化膜/合金界面產生大量的陽離子空位(柯肯達爾空位),這些空位不斷地在界面沉積長大,最終形成較大的孔洞。在氧化鋁形成合金中,活性元素改性可以有效抑制界面孔洞的形成,提高氧化膜的粘附性,相關結果在Whittle 和Stringer 的綜述以及其他人的研究中都有提及[18,54-55]。關于活性元素的作用機理,空位沉積模型認為合金中活性元素形成的氧化物可以作為空位沉積源,減少界面處空位的聚集和孔洞的形成,從而提高氧化膜的結合強度。另外也有研究指出,活性元素離子在界面的偏聚抑制了陽離子的外擴散,通過改變合金基體中元素的擴散速率,弱化了柯肯達爾效應,從而抑制了空位沉積所導致的界面孔洞的形核[52]。除空位沉積模型外,越來越多的研究表明,雜質元素(如S 等)對氧化膜的粘附性有顯著的負作用,而空位沉積模型無法解釋這種雜質元素對氧化膜粘附性的作用。俄歇電子能譜(AES)表明[56],S 傾向于偏聚在氧化膜/合金界面,包括結合緊密的界面以及界面處孔洞表面。這種雜質元素的界面偏聚削弱了界面強度,促進了界面孔洞的生長,最終導致氧化膜的快速剝落[22]。Hou、Pint 和Jiang 等[52-53,57-58]通過大量研究證明了這一結果,他們結合第一性原理計算,發現S 的存在確實會削弱氧化膜/合金界面的結合強度,并通過降低界面孔洞的形核能,促進孔洞的生長。添加活性元素后,界面S 等雜質元素的偏聚可以得到顯著改善,界面孔洞隨之大大減少。Lees 等[59]據此提出了活性元素的“硫效應”模型。該模型認為,活性元素能夠與S 形成穩定的硫化物,并將S 釘扎在合金內部,避免了S 在界面的偏聚和由此產生的有害作用。但是也有研究指出,RE-S 化合物的存在并非是改善氧化膜粘附性的必要條件,經氧化物彌散強化(ODS)的FeCrAl 合金中并未發現S 被活性元素捕獲的現象,但表面氧化膜同樣表現出良好的粘附性[23]。因此,研究者提出,除活性元素對S 的釘扎作用外,活性元素離子向氧化膜/合金界面的偏聚,會占據S的偏聚位置,減小S 向界面偏聚的驅動力,從而改善雜質元素S 的界面偏聚情況[41,57],抑制界面孔洞的形成,提高氧化膜粘附性。然而,近來的研究表明,即使合金中不含S 等雜質,氧化膜仍然容易剝落[60],這表明S 的偏聚并不一定是引起氧化膜剝落的直接原因。因此,有關硫效應的研究還有待進一步深入。除界面孔洞因素外,界面氧化物栓的形成也是影響氧化膜粘附性的重要因素。早在20 世紀70 年代,英國利物浦大學的Allam 等[19,20,61]發現在氧化鋁形成合金中添加活性元素,高溫氧化時這些活性元素會在氧化膜/合金界面處形成氧化物栓,并深入合金基體中,對氧化膜起到“釘扎”作用,從而顯著提高氧化膜抗剝落的能力,據此提出了氧化物“釘扎”模型。該模型認為在氧化初期,由于活性元素本身與氧親和力大,合金中析出的活性元素也會快速參與氧化形成富活性元素的復合氧化物,這些氧化物是O 的快速擴散通道。隨著氧化的進行,復合氧化物快速深入合金中,當活性元素析出物消耗殆盡時,沿著復合氧化物擴散進入的O 會與周圍合金發生反應,生成Al2O3,最終形成以活性元素氧化物為“核”。Al2O3 為“殼”的氧化物栓,對氧化膜/合金界面進行釘扎,提高氧化膜粘附性。但是氧化物“釘扎”模型目前仍存在較大爭議,因為有研究發現,經氧化物彌散強化(ODS)的氧化鋁形成合金氧化時,雖然沒有形成氧化物栓,卻同樣表現出優異的抗氧化性[62],表明氧化物“釘扎”效應并非是改善氧化膜粘附性的必要條件。而且研究認為,“釘扎”的有效性取決于氧化物栓的大小和分布,粗大的氧化物栓反而會引起應力集中,成為裂紋源,加速氧化膜的剝落[12]。因此,研究如何有效控制氧化物栓的形成,保證合適的形貌和密度,以利于提高氧化膜抗剝落性能將是一個重要方向。
除以上作用外,活性元素改性還可以緩解氧化膜的褶皺,從而提高氧化膜的粘附性。氧化膜褶皺的產生一般是由氧化膜內累積的殘余應力導致,包括氧化膜/合金界面的熱不匹配應力、氧化膜生長應力以及相變應力等[63-64]。褶皺一旦產生,很容易造成氧化膜內裂紋的萌生和擴展以及氧化膜/合金界面的分離。一些數值模擬研究認為,提高粘結層的屈服強度可以有效減小氧化膜的屈曲變形,延長熱障涂層體系的服役壽命[65-66]。然而,粘結層屈服強度或者說抗蠕變性能的提高往往是以犧牲抗氧化性能為代價,使粘結層難以滿足高溫應用的需求。而活性元素改性可以很好地解決這一問題。郭洪波等[15,67]針對活性元素改性NiAl 合金進行了系統的研究,發現活性元素改性可以有效緩解氧化膜褶皺情況(如圖5 所示),同時保證合金的抗高溫循環氧化性能。他們認為活性元素改性可以降低氧化膜的生長速率,延緩θ-Al2O3 向α-Al2O3 的相轉變,從而緩解氧化膜內應力的累積,抑制氧化膜褶皺的產生[68]。另一方面,活性元素易氧化形成氧化物,并彌散分布在氧化膜內,細化晶粒,可以有效改善氧化膜的力學性能,也有利于緩解氧化膜褶皺的產生[44]。此外,有研究認為,提高活性元素與雜質元素C 的比例可以改善氧化膜的褶皺情況。這是由于界面雜質元素C 的偏聚會加劇氧化膜褶皺,加入活性元素形成穩定碳化物,可以將C 固定在合金內部,從而緩解氧化膜褶皺,提高氧化膜的抗剝落性能[69]。目前,研究者對引起氧化膜褶皺的殘余應力產生原因認識不統一,無法確定熱不匹配應力、氧化膜生長應力、相變應力等各自所占的殘余應力比重,而且對雜質元素C 影響氧化膜褶皺的作用機理尚不明確,因此活性元素在改善氧化膜褶皺方面的作用也有待深入。
圖5 活性元素改性β-NiAl 合金1200 ℃循環氧化15 h 后的氧化膜褶皺曲線[15]
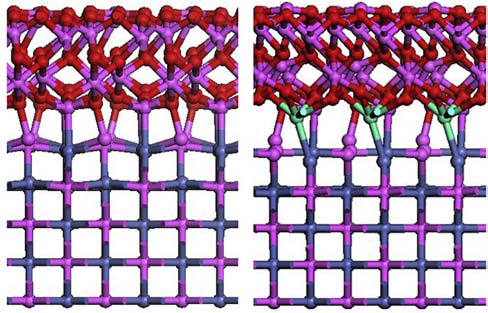
隨著計算模擬方法在活性元素改性研究上的應用,近些年來,研究者認為活性元素在氧化膜/合金界面偏聚的同時,也會直接參與界面的成鍵,從而提高界面鍵合能力。例如,郭洪波等[70-71]采用第一性原理計算,發現活性元素Dy 在Al2O3/NiAl 合金界面直接參與了成鍵,每個Dy 形成了1 個Dy─Ni 金屬鍵和4 個Dy—O 離子鍵(如圖6 所示),相比未改性的Al2O3/NiAl 界面,成鍵數量和鍵強均明顯增加,因此界面鍵合得到強化,氧化膜粘附性得到改善。當然,這一點還需要有效的實驗證據證明。
5 結語
新一代高推重比航空發動機對發展超高溫、長壽命金屬防護涂層提出了迫切要求,開發1200 ℃以上、長時間抗高溫氧化的金屬防護涂層材料成為當前亟須解決的關鍵問題。微量活性元素改性對于促進保護性氧化膜形成元素的選擇性氧化、降低氧化膜生長速率、提高氧化膜粘附性具有顯著的效果,引起了國內外學者的廣泛關注。研究人員在大量實驗的基礎上,針對活性元素的作用機理提出了多種模型,但這些模型均存在一定的局限性,目前對于活性元素的作用機理還存在很大的爭議。
因此,為了更好地理解活性元素效應并加以應用,必須從原子尺度上進行更深入的研究。比如:闡明活性元素與合金基體元素、微觀缺陷等的交互作用機制;結合高分辨電鏡、第一性原理計算等,揭示活性元素對氧化膜形核生長、氧化膜/合金界面微觀結構的影響機理等。通過研究,需要建立統一、普遍適用的活性元素作用模型以及活性元素選擇依據,為發展超高溫金屬防護涂層提供關鍵理論支撐。
參考文獻:
[1]王心悅, 辛麗, 韋華, 等. 高溫防護涂層研究進展[J]. 腐蝕科學與防護技術, 2013, 25(3): 175-183.
WANG Xin-yue, XIN Li, WEI Hua, et al. Progress of high-temperature protective coatings[J]. Corrosion scie-nce and protection technology, 2013, 25(3): 175-183.
[2]郭洪波, 宮聲凱, 徐惠彬. 先進航空發動機熱障涂層技術研究進展[J]. 中國材料進展, 2009, 28(9): 18-26.
GUO Hong-bo, GONG Sheng-kai, XU Hui-bin. Progress in thermal barrier coatings for advanced aeroengines[J]. Materials China, 2009, 28(9): 18-26.
[3]MIRACLE D B. The physical and mechanical properties of NiAl[J]. Acta metallurgica et materialia, 1993, 41(3): 649-684.
[4]SIVAKUMAR R, MORDIKE B L. High temperature coatings for gas turbine blades: A review[J]. Surface and coatings technology, 1989, 37(2): 139-160.
[5]HAYNES J A, PINT B A, ZHANG Y, et al. Comparison of the cyclic oxidation behavior of β-NiAl, β-NiPtAl and γ-γ′ NiPtAl coatings on various superalloys[J]. Surface and coatings technology, 2007, 202(4): 730-734.
[6]HAMADI S, BACOS M P, POULAIN M, et al. Oxidation of a Zr-doped NiAl bondcoat thermochemically deposited on a nickel-based superalloy[J]. High temperature technology, 2009, 26(2): 195-198.
[7]XIE L, DORFMAN M R, CIPITRIA A, et al. Properties and performance of high-purity thermal barrier coatings [J]. Journal of thermal spray technology, 2007, 16(5/6): 804-808.
[8]PADTURE N P, GELL M, JORDAN E H. Thermal barrier coatings for gas-turbine engine applications[J]. Science, 2002, 296(5566): 280-284.
[9]NAUMENKO D, PILLAI R, CHYRKIN A, et al. Over-view on recent developments of bondcoats for plasma- sprayed thermal barrier coatings[J]. Journal of thermal spray technology, 2017, 26(8): 1743-1757.
[10]PINT B, GARRATT-REED A, HOBBS L. The reactive element effect in commercial ODS FeCrAI alloys[J]. Materials at high temperatures, 1995, 13(1): 3-16.
[11]PINT B A. Optimization of reactive-element additions to improve oxidation performance of alumina-forming alloys[J]. Journal of the American Ceramic Society, 2003, 86(4): 686-695.
[12]PINT B A. Progress in understanding the reactive element effect since the Whittle and Stringer literature review [C]// Proc John Stringer Symposium on High Temperature Corrosion. USA: ASM International Materials Park, Ohio, 2003: 9-19.
[13]HOU P Y. The reactive element effect-past, present and future[C]//Materials science forum. Switzerland: Trans Tech Publications, 2011: 39-44.
[14]SONG P, NAUMENKO D, VASSEN R, et al. Effect of oxygen content in NiCoCrAlY bondcoat on the lifetimes of EB-PVD and APS thermal barrier coatings[J]. Surface and coatings technology, 2013, 221: 207-213.
[15]LI D Q, GUO H B, WANG D, et al. Cyclic oxidation of β-NiAl with various reactive element dopants at 1200 ℃[J]. Corrosion science, 2013, 66: 125-135.
[16]PINT B A, HAYNES J A, BESMANN T M. Effect of Hf and Y alloy additions on aluminide coating performance [J]. Surface and coatings technology, 2010, 204(20): 3287-3293.
[17]PFEIL L B. Improvement in heat-resisting alloys: UK, 459848[P]. 1937-01-11.
[18]WHITTLE D P, STRINGER J. Improvements in high temperature oxidation resistance by additions of reactive elements or oxide dispersions[J]. Philosophical transac-tions of the Royal Society of London, 1980, 295(1413): 309-329.
[19]ALLAM I M, WHITTLE D P, STRINGER J. The oxi-dation behavior of CoCrAl systems containing active element additions[J]. Oxidation of metals, 1978, 12(1): 35-66.
[20]ALLAM I M, WHITTLE D P, STRINGER J. Improve-ments in oxidation resistance by dispersed oxide add-ition: Al2O3-forming alloys[J]. Oxidation of metals, 1979, 13 (4): 381-401.
21]FUNKENBUSCH A, SMEGGIL J, BORNSTEIN N. Reactive element-sulfur interaction and oxide scale adherence [J]. Metallurgical transactions A, 1985, 16(6): 1164-1166.
[22]LEES D G. On the reasons for the effects of dispersions of stable oxides and additions of reactive elements on the adhesion and growth-mechanisms of chromia and alumina scales-the "sulfur effect"[J]. Oxidation of metals, 1987, 27(1/2): 75-81.
[23]PINT B A. Experimental observations in support of the dynamic-segregation theory to explain the reactive-ele-ment effect[J]. Oxidation of metals, 1996, 45(1/2): 1-37.
[24]HOU P, STRINGER J. The effect of reactive element additions on the selective oxidation, growth and adhesion of chromia scales[J]. Materials science and engineering: A, 1995, 202(1/2): 1-10.
[25]HOU P, STRINGER J. The influence of ion-implanted yttrium on the selective oxidation of chromium in Co- 25wt.% Cr[J]. Oxidation of metals, 1988, 29(1/2): 45-73.
[26]PINT B, LEIBOWITZ J, DEVAN J. The effect of an oxide dispersion on the critical Al content in Fe-Al alloys [J]. Oxidation of metals, 1999, 51(1/2): 181-197.
[27]STRINGER J, WILCOX B A, JAFFEE R I. The high- temperature oxidation of nickel-20 wt.% chromium alloys containing dispersed oxide phases[J]. Oxidation of metals, 1972, 5(1): 11-47.
[28]GUO H B, WANG X Y, JI L I, et al. Effects of Dy on cyc-lic oxidation resistance of NiAl alloy[J]. Transactions of Nonferrous Metals Society of China, 2009, 19(5): 1185- 1189.
[29]NANNI P, STODDART C T H, HONDROS E D. Grain boundary segregation and sintering in alumina[J]. Materials chemistry, 1976, 1(4): 297-320.
[30]RAMANARAYANAN T, RAGHAVAN M, PETKOVIC-LUTON R. The characteristics of alumina scales formed on Fe-based yttria-dispersed alloys[J]. Journal of the Ele-ctrochemical Society, 1984, 131(4): 923-931.
[31]PINT B A, MORE K L. Characterization of alumina interfaces in TBC systems[J]. Journal of materials science, 2009, 44(7): 1676-1686.
[32]CHEN Y M, REED R C, MARQUIS E A. Interfacial sol-ute segregation in the thermally grown oxide of thermal barrier coating structures[J]. Oxidation of metals, 2014, 82(5/6): 457-467.
[33]SWAD?BA R, SWAD?BA L, WIEDERMANN J, et al. Characterization of alumina scales grown on a 2nd generation single crystal Ni superalloy during isothermal oxidation at 1050, 1100 and 1150 °C[J]. Oxidation of metals, 2014, 82(3/4): 195-208.
[34]UNOCIC K A, PINT B A. Oxidation behavior of co- doped NiCrAl alloys in dry and wet air[J]. Surface and coatings technology, 2013, 237: 8-15.
[35]UNOCIC K A, PINT B A. Effect of water vapor on thermally grown alumina scales on bond coatings[J]. Surface and coatings technology, 2013, 215: 30-38.
[36]PINT B A, MORE K L, WRIGHT I G, et al. Charac-terization of thermally cycled alumina scales[J]. Materials at high temperatures, 2000, 17(1): 165-171.
[37]PINT B A, GARRATT-REED A J, HOBBS L W. Possible role of the oxygen potential gradient in enhancing diffusion of foreign ions on α-Al2O3 grain boundaries[J]. Journal of the American Ceramic Society, 1998, 81(2): 305- 314.
[38]PINT B A, ALEXANDER K B. Grain boundary segre-gation of cation dopants in α-Al2O3 scales[J]. Journal of the electrochemical society, 1998, 145(6): 1819-1829.
[39]GUO H B, LI D Q, ZHENG L, et al. Effect of co-doping of two reactive elements on alumina scale growth of β- NiAl at 1200 ℃[J]. Corrosion science, 2014, 88: 197-208.
[40]LI C, SONG P, KHAN A, et al. Influence of water vapour on the HfO2 distribution within the oxide layer on CoNiCrAlHf alloys[J]. Journal of alloys and compounds, 2018, 739: 690-699.
[41]MARINO K A, CARTER E A. Atomic-scale insight and design principles for turbine engine thermal barrier coa-tings from theory[J]. Proceedings of the national aca-demy of sciences of the United States of America, 2011, 108 (14): 5480-5487.
[42]GALMARINI S, ASCHAUER U, BOWEN P, et al. Ato-mistic simulation of Y-doped α-alumina interfaces[J]. Journal of the American Ceramic Society, 2008, 91(11): 3643-3651.
[43]HE J, ZHANG Z, PENG H, et al. The role of Dy and Hf doping on oxidation behavior of two-phase (γ′+β) Ni-Al alloys[J]. Corrosion science, 2015, 98: 699-707.
[44]GUO H B, WANG D, PENG H, et al. Effect of Sm, Gd, Yb, Sc and Nd as reactive elements on oxidation beha-viour of β-NiAl at 1200 ℃[J]. Corrosion science, 2014, 78: 369-377.
[45]PINT B A. The role of chemical composition on the oxidation performance of aluminide coatings[J]. Surface and coatings technology, 2004, 188: 71-78.
[46]PINT B A, UNOCIC K A. Ionic segregation on grain boundaries in thermally grown alumina scales[J]. Materials at high temperatures, 2012, 29(3): 257-263.
[47]PINT B A, MORE K, TORTORELLI P, et al. Optimizing the imperfect oxidation performance of iron aluminides [C]//Materials science forum. Switzerland: Trans Tech Publications, 2001: 411-418.
[48]HOU P Y, PRIIMAK K. Interfacial segregation, pore formation, and scale adhesion on NiAl alloys[J]. Oxidation of metals, 2005, 63(1/2): 113-130.
[49]TOLPYGO V K, CLARKE D R. Surface rumpling of a (Ni,Pt) Al bond coat induced by cyclic oxidation[J]. Acta materialia, 2000, 48(13): 3283-3293.
[50]PINT B A, WRIGHT I G, LEE W Y, et al. Substrate and bond coat compositions: Factors affecting alumina scale adhesion[J]. Materials science and engineering: A, 1998, 245(2): 201-211.
[51]TIEN J K, PETTIT F S. Mechanism of oxide adherence on Fe-25Cr-4Al (Y or Sc) alloys[J]. Metallurgical trans-actions, 1972, 3(6): 1587-1599.
[52]PINT B A. On the formation of interfacial and internal voids in α-Al2O3 scales[J]. Oxidation of metals, 1997, 48(3): 303-328.
[53]GESMUNDO F, HOU P Y. Analysis of pore formation at oxide-alloy interfaces—II: Theoretical treatment of va-cancy condensation for immobile interfaces[J]. Oxidation of metals, 2003, 59(1/2): 63-81.
[54]NAUMENKO D, PINT B A, QUADAKKERS W J. Current thoughts on reactive element effects in alumina- forming systems: In memory of John Stringer[J]. Oxid-ation of metals, 2016, 86(1/2): 1-43.
[55]GUO H B, ZHANG T, WANG S X, et al. Effect of Dy on oxide scale adhesion of NiAl coatings at 1200 ℃[J]. Corrosion science, 2011, 53(6): 2228-2232.
[56]HOU P Y, STRINGER J. Oxide scale adhesion and impurity segregation at the scale/metal interface[J]. Oxi-dation of metals, 1992, 38(5/6): 323-345.
[57]HOU P Y. Segregation phenomena at thermally grown Al2O3/alloy interfaces[J]. Annual review of materials research, 2008, 38(38): 275-298.
[58]JIANG Y, SMITH J R, EVANS A G. First principles assessment of metal/oxide interface adhesion[J]. Applied physics letters, 2008, 92(14): 245414.
[59]HOU P Y. Segregation behavior at TGO/bondcoat inter-faces[J]. Journal of materials science, 2009, 44(7): 1711- 1725.
[60]HOU P Y, IZUMI T, GLEESON B. Sulfur segregation at Al2O3/γ-Νi+γ′-Ni3Al interfaces: Effects of Pt, Cr and Hf additions[J]. Oxidation of metals, 2009, 72(1/2): 109-124.
[61]MENNICKE C, HE M Y, CLARKE D R, et al. The role of secondary oxide inclusions ("pegs") on the spalling resistance of oxide films[J]. Acta materialia, 2000, 48(11): 2941-2949.
[62]PINT B A, HOBBS L W. The oxidation behavior of Y2O3- dispersed β-NiAl[J]. Oxidation of metals, 2004, 61(3/4): 273-292.
[63]TOLPYGO V K, CLARKE D R. On the rumpling mec-hanism in nickel-aluminide coatings: Part I: An experi-mental assessment[J]. Acta materialia, 2004, 52(17): 5115- 5127.
[64]PENNEFATHER R C, BOONE D H. Mechanical deg-radation of coating systems in high-temperature cyclic oxidation[J]. Surface and coatings technology, 1995, 76: 47-52.
[65]KARLSSON A M, EVANS A G. A numerical model for the cyclic instability of thermally grown oxides in thermal barrier systems[J]. Acta materialia, 2001, 49(10): 1793- 1804.
[66]KARLSSON A M, LEVI C G, EVANS A G. A model study of displacement instabilities during cyclic oxidation [J]. Acta materialia, 2002, 50(6): 1263-1273.
[67]GUO H B, WANG X Y, GONG S K. Effects of Dy on the microstructure and spallation failure of the alumina scales grown on NiAl[J]. International journal of modern physics B, 2010, 24(15/16): 3149-3154.
[68]YANG L Y, ZHENG L, GUO H B. The residual stress of oxide scales grown on Ni-Al alloys doped with minor Dy and Y[J]. Corrosion science, 2016, 112: 542-551.
[69]PINT B A, SCHNEIBEL J H. The effect of carbon and reactive element dopants on oxidation lifetime of FeAl[J]. Scripta materialia, 2005, 52(12): 1199-1204.
[70]ZHANG Z, ZHANG R F, LEGUT D, et al. Pinning effect of reactive elements on adhesion energy and adhesive strength of incoherent Al2O3/NiAl interface[J]. Physical chemistry chemical physics, 2016, 18(33): 22864-22873.
[71]ZHANG T, GUO H B, GONG S K, et al. Effects of Dy on the adherence of Al2O3/NiAl interface: A combined first- principles and experimental studies[J]. Corrosion science, 2013, 66(1): 59-66.
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 腐蝕與防護網官方QQ群:140808414