摘要
硫酸鹽還原菌 (SRB) 是一類廣泛存在于自然環(huán)境中可以利用硫酸鹽類物質(zhì)作為呼吸代謝電子受體的厭氧類微生物,是造成金屬腐蝕破壞和設(shè)備故障的主要原因之一,已經(jīng)成為一個(gè)重要的研究課題。由于微生物活動(dòng)的復(fù)雜性,生物膜內(nèi)SRB與金屬表面的相互作用缺乏深入的研究,其誘導(dǎo)腐蝕機(jī)理和腐蝕過(guò)程尚不清楚,難以進(jìn)行有效的腐蝕預(yù)測(cè)。基于此,本文從SRB生物膜的呼吸代謝角度介紹了其誘導(dǎo)金屬腐蝕的研究進(jìn)展。介紹了SRB的生態(tài)特征和厭氧呼吸過(guò)程,重點(diǎn)綜述了SRB腐蝕機(jī)理,包括陰極去極化、代謝產(chǎn)物腐蝕、濃差電池作用和胞外電子傳遞等理論,最后簡(jiǎn)要介紹了微生物腐蝕 (MIC) 研究的方法與技術(shù)手段。
關(guān)鍵詞: 微生物腐蝕 ; 硫酸鹽還原菌 ; 腐蝕機(jī)理
腐蝕問(wèn)題涉及各行各業(yè),已經(jīng)對(duì)人類的生活環(huán)境和經(jīng)濟(jì)發(fā)展產(chǎn)生了嚴(yán)重的危害。根據(jù)《中國(guó)腐蝕成本》調(diào)查結(jié)果,2014年我國(guó)腐蝕成本超過(guò)2.1萬(wàn)億元人民幣,占當(dāng)年我國(guó)國(guó)內(nèi)生產(chǎn)總值 (GDP) 的3.34%[1],腐蝕防護(hù)已越來(lái)越被各行業(yè)各部門(mén)所重視。腐蝕防護(hù)關(guān)系到國(guó)家經(jīng)濟(jì)發(fā)展、自然環(huán)境保護(hù)和人民健康安全,腐蝕問(wèn)題在國(guó)家經(jīng)濟(jì)社會(huì)發(fā)展過(guò)程中已經(jīng)成為不容忽略的關(guān)鍵問(wèn)題[2-4]。
微生物腐蝕 (MIC) 是指金屬或非金屬表面因微生物的生命活動(dòng)而受到的腐蝕破壞。MIC是油氣管道、能源電力等許多行業(yè)中導(dǎo)致設(shè)施腐蝕失效,甚至造成重大經(jīng)濟(jì)損失的一類重要腐蝕[3,4],大約20%或更高的腐蝕損失是由微生物或其代謝活動(dòng)引起的[5]。微生物在環(huán)境中與材料表面相互作用較為復(fù)雜,尚無(wú)標(biāo)準(zhǔn)的腐蝕模型對(duì)其進(jìn)行預(yù)測(cè)和評(píng)估[6]。
硫酸鹽還原菌 (SRB) 屬于原核微生物,它們可以利用硫酸鹽作為末端電子受體進(jìn)行呼吸代謝 (異化硫酸鹽還原)。SRB不僅局限于細(xì)菌,研究認(rèn)為一些古菌也具有硫酸鹽還原功能[7]。目前已經(jīng)進(jìn)行了數(shù)十種SRB的研究,包括Desulfovibrio,Desulfomicrobium,Desulfobacter和Desulfotomaculum等,有些SRB甚至能夠進(jìn)行有氧呼吸,但這個(gè)過(guò)程不能維持生長(zhǎng)[8],SRB不僅是缺氧環(huán)境中發(fā)生MIC的重要原因,其代謝過(guò)程在全球硫循環(huán)中也起到重要作用,具有重要的生態(tài)功能。
研究SRB腐蝕微生物的生理代謝過(guò)程,并揭示其對(duì)海洋工程材料的腐蝕機(jī)理,對(duì)微生物腐蝕防護(hù)研究有重要參考價(jià)值[9-11]。本文介紹了SRB的生態(tài)特征和其厭氧呼吸過(guò)程,然后介紹了SRB在材料表面生物膜的形成過(guò)程,綜述了SRB腐蝕機(jī)理,從經(jīng)典的陰極去極化理論到胞外電子傳遞理論,最后簡(jiǎn)要介紹了MIC研究的方法與技術(shù)手段。
1 SRB的生態(tài)和生理特征
1.1 SRB的生態(tài)特征
SRB廣泛分布在土壤、海水、河水、沉積物等自然環(huán)境以及地下管道油氣井、港口等設(shè)施材料生物膜中,最適宜的生長(zhǎng)為pH6~9,溫度為20~30 ℃,生長(zhǎng)所需的氧化還原電位 (OPR) 一般不高于-150 mV,它們對(duì)生長(zhǎng)所需的環(huán)境有較強(qiáng)的適應(yīng)性,某些SRB可以在50~60 ℃的高溫下存活,同時(shí)一些高鹽生態(tài)環(huán)境中也能檢測(cè)到它們的存在[12]。H2S對(duì)SRB的生長(zhǎng)存在較大影響,一般認(rèn)為濃度達(dá)到16 mmol/L就會(huì)對(duì)其生長(zhǎng)產(chǎn)生明顯抑制效果[13]。在含有硫酸鹽的缺氧環(huán)境中,SRB通過(guò)獲取電子將硫酸鹽還原為H2S而獲得生長(zhǎng)所需的能量,該電子通常來(lái)源于有機(jī)物質(zhì)或分子氫的利用,分子氫是土壤、沉積物和其他缺氧環(huán)境中的常見(jiàn)發(fā)酵產(chǎn)物[14]。
通過(guò)研究不同地區(qū)的土壤SRB分布規(guī)律,顯示土壤中SRB的含量為10~1800 cell·g-1,土壤類型、溫度、氣候狀況和地理位置等因素都影響著SRB含量的分布[15],緯度較高、年平均溫度較低的地區(qū)也不利于SRB的生長(zhǎng)繁殖[16]。在海洋環(huán)境中,SRB廣泛存在于各個(gè)區(qū)域,主要分布在表層海水;隨著深度增加,SRB含量呈指數(shù)減少。例如,在加利福利亞太平洋表層海水中,SRB可達(dá)106 cell·g-1;而在780 m水深處,SRB含量銳減到103 cell·g-1。在近岸港灣、沿岸地區(qū)和污水處理廠附近SRB含量較高。據(jù)調(diào)查,中國(guó)山東乳山灣表層海水SRB含量為103~106 cell·g-1,在膠州灣潮間帶和沿岸區(qū)更可高達(dá)107 cell·g-1。SRB含量還呈現(xiàn)一定的季節(jié)變化趨勢(shì)[17]。2007~2008年對(duì)象山港海域的表層海水、上層海水和沉積物進(jìn)行取樣,分析SRB豐度的時(shí)空分布特征及主要影響因素,其結(jié)果顯示水樣及沉積物中SRB的變化范圍為30~2300 cells·mL-1,且沉積物中的SRB含量最高,其豐度與環(huán)境關(guān)系較大,并且呈現(xiàn)出不均勻的狀態(tài),人類活動(dòng)對(duì)于SRB的分布有明顯影響[14]。隨著研究的深入,結(jié)果顯示SRB的分布也與有機(jī)質(zhì)污染、營(yíng)養(yǎng)鹽 (NO2-—N、NH4+—N)、pH及溫度等因素有關(guān)[18]。SRB生態(tài)分布特征為實(shí)際環(huán)境中微生物的分布和代謝研究提供了重要指導(dǎo)。本課題組[19-21]研究了實(shí)際海洋環(huán)境中金屬材料表面微生物群落的附著情況,結(jié)果表明不同海域生物群落有較大差異,對(duì)于三亞和廈門(mén)海域優(yōu)勢(shì)屬為Bacillus和Vibrio;不同金屬材料附著的生物群落也有顯著差異,碳鋼銹層中硫酸鹽還原微生物為主要腐蝕微生物,由外銹層到內(nèi)銹層的優(yōu)勢(shì)菌屬分別為Desulfotomaculum、Desulfonatronum和Desulfovibiro。
1.2 SRB的厭氧呼吸
SRB在有機(jī)物的降解過(guò)程中以硫酸鹽 (SO42-) 作為末端電子受體還原產(chǎn)生H2S和CO2,因此,SRB在S和C的生物地球化學(xué)循環(huán)中起到重要作用,如圖1所示[22]。SRB將SO42-還原為H2S后,化能異養(yǎng)微生物可以將這些H2S氧化為單質(zhì)硫 (S0),并繼續(xù)氧化為SO42-;同時(shí),大氣中的H2S也可以通過(guò)氧化和大氣沉淀作用形成硫酸鹽,繼而形成的SO42-又再次被SRB利用還原為H2S;SRB細(xì)胞通過(guò)有機(jī)硫的脫硫基分解作用也釋放出H2S,整個(gè)過(guò)程構(gòu)成了SRB的硫循環(huán)系統(tǒng)。在碳循環(huán)中,SRB通過(guò)利用有機(jī)酸等有機(jī)物作為硫酸鹽還原過(guò)程中的電子供體而產(chǎn)生CO2,進(jìn)入全球碳循環(huán),CO2又可以通過(guò)光合作用和固碳微生物轉(zhuǎn)化為碳水化合物,這些復(fù)雜的碳水化合物又通過(guò)發(fā)酵微生物進(jìn)一步轉(zhuǎn)化為簡(jiǎn)單的有機(jī)物,從而繼續(xù)被SRB利用[6]。
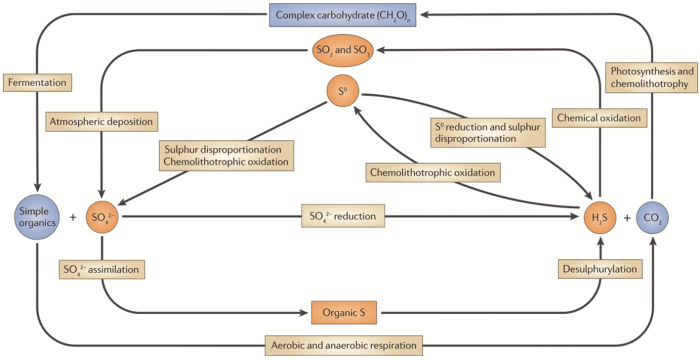
圖1 SRB參與的碳循環(huán)和硫循環(huán)示意圖[22]
在生物硫循環(huán)過(guò)程中,SRB的厭氧呼吸過(guò)程如圖2所示[22]。有機(jī)化合物 (如乳酸) 氧化產(chǎn)生的H+通過(guò)SRB內(nèi)活性Ech (Escherichia coli hydrogenase 3) 和COO (CO-dependent) 兩種酶循環(huán)到SRB胞質(zhì)。在胞質(zhì)中,H2被氫化酶重新氧化為質(zhì)子和電子,質(zhì)子為SRB提供了生長(zhǎng)所必需的ATP,電子將傳遞到C型細(xì)胞色素 (cytochrome c3),然后繼續(xù)傳遞到醌還原酶 (Qrc),再傳遞到與醌作用的膜結(jié)合氧化還原酶 (Qmo),最后傳遞到硫酸鹽還原的腺苷磷酸 (APS) 還原酶。同時(shí),電子還通過(guò)未知的機(jī)制傳遞到異化亞硫酸鹽還原酶 (Dsr),隨后傳遞到亞硫酸鹽 (SO32-) 還原酶。通過(guò)這一系列途徑,SRB能夠獲得足夠的電子將SO42-完全還原為H2S。同時(shí),胞質(zhì)中的乳酸會(huì)被分解為丙酮酸,進(jìn)一步分解為甲酸,在甲酸脫氫酶 (Fdh) 的作用下最終分解為H+、CO2和電子,甲酸分解產(chǎn)生的電子和H2分解產(chǎn)生的電子在胞質(zhì)內(nèi)具有相同的傳遞路徑[23]。電子傳遞過(guò)程在能量學(xué)角度上也是完全可行的[24]。
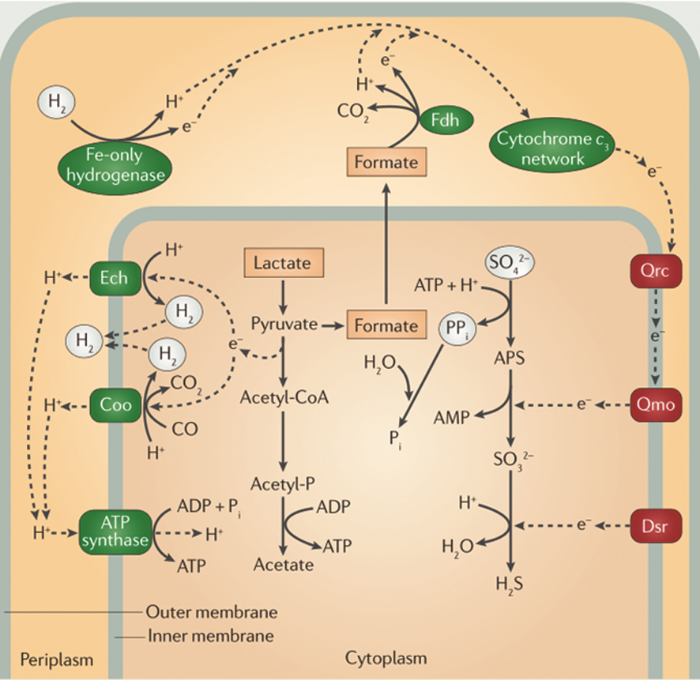
圖2 SRB的厭氧呼吸過(guò)程[22]
SRB將S和C的生物化學(xué)循環(huán)結(jié)合在一起,其不僅能夠?qū)⑷樗帷⒈帷⒑?jiǎn)單芳香族化合物 (苯或苯酚) 作為碳源,甚至能夠利用氨基酸或高分子鏈脂肪酸為其生長(zhǎng)代謝提供能量,某些SRB還可以將硝酸鹽或分子氫作為替代的呼吸底物[25]。因此,對(duì)SRB的生態(tài)和厭氧呼吸代謝過(guò)程進(jìn)行研究,對(duì)于控制微生物活動(dòng)和進(jìn)一步發(fā)展生物技術(shù)在環(huán)境修復(fù)、生物污染、能源生產(chǎn)、廢水處理和礦物回收等方面有重要意義。
2 SRB的附著和生物膜的形成
微生物在環(huán)境中可以以多種方式與材料表面相互作用,這使得MIC系統(tǒng)較為復(fù)雜,難以用標(biāo)準(zhǔn)的腐蝕模型評(píng)估預(yù)測(cè)。生物膜的形成使細(xì)菌能夠與材料表面密切接觸,并形成了與本體溶液不同的微環(huán)境,包括膜內(nèi)pH、溶解氧、有機(jī)和無(wú)機(jī)離子等[26]。在各種環(huán)境中,微生物90%以上是以生物膜的形式存在,附著微生物群落的組成很可能是由生物膜的調(diào)節(jié)和材料表面的相互作用決定的。生物膜內(nèi)包括細(xì)胞及其分泌的胞外聚合物 (EPS),其中EPS是由多糖、脂質(zhì)、核酸、蛋白質(zhì)等有機(jī)和無(wú)機(jī)物構(gòu)成,具有一定的強(qiáng)度和黏性,在金屬表面有較強(qiáng)的附著性,EPS含有的不同大分子物質(zhì)在其粘附于材料表面后,為活性酶和氧化還原活性酶的產(chǎn)生提供了理想條件[27]。生物膜在材料表面起到屏障作用,一方面阻止溶液物質(zhì)向金屬表面擴(kuò)散,另一方面阻止膜內(nèi)物質(zhì)向溶液擴(kuò)散,但是具體阻礙方式有待研究。圖3為SRB生物膜在金屬表面化學(xué)復(fù)雜性的示意圖及其在MIC中的影響。圖中,M為基體金屬,M2+為金屬離子,e-為電子。生物膜內(nèi)SRB大量聚集,其代謝產(chǎn)生了大量H+、SO42-和NO3-,然而生物膜阻礙膜內(nèi)外物質(zhì)的流通方式尚不明確[28]。
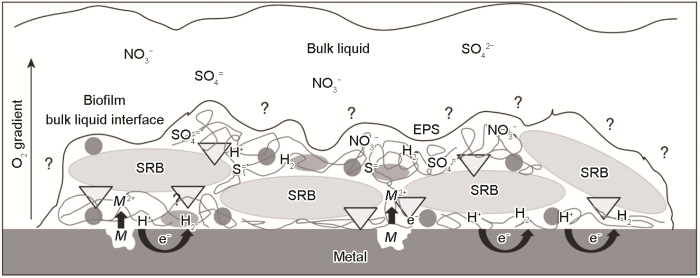
圖3 SRB生物膜在金屬表面化學(xué)復(fù)雜性的示意圖及其在MIC中的影響[7]
生物膜是精細(xì)的三維結(jié)構(gòu),在具有強(qiáng)大剪切力的系統(tǒng)中,生物膜只有數(shù)微米厚;而在液壓壓力較小的區(qū)域,生物膜的厚度可以達(dá)到厘米級(jí)。在天然海水中,生物膜的厚度為50~150 μm[29]。生物膜的形成和增長(zhǎng)過(guò)程可以分為6個(gè)階段:(1) 在金屬表面形成吸附膜;(2) 浮游微生物在吸附膜的吸引下遷移到材料表面;(3) 浮游微生物附著在材料表面的活性部位,轉(zhuǎn)化為固著微生物;(4) 固著微生物生長(zhǎng)并產(chǎn)生代謝產(chǎn)物,形成生物膜;(5) 隨著代謝產(chǎn)物和固著微生物的增加,形成成熟穩(wěn)定的生物膜;(6) 隨著時(shí)間的推移,生物膜的穩(wěn)定性降低,部分生物膜脫落,形成異質(zhì)生物膜[30]。
研究[31-33]表明,生物膜形成的不同時(shí)期對(duì)腐蝕的影響也不同,最終不穩(wěn)定生物膜脫落形成的異質(zhì)生物膜會(huì)引起材料的局部腐蝕,加速腐蝕速率。當(dāng)材料表面出現(xiàn)異質(zhì)生物膜時(shí),生物膜中致密部位會(huì)阻止O2的擴(kuò)散,生物膜中的好氧細(xì)菌也會(huì)消耗生物膜內(nèi)的O2,這兩種效應(yīng)共同作用下會(huì)產(chǎn)生低氧濃度的區(qū)域,這些區(qū)域成為材料腐蝕的陽(yáng)極。同時(shí),具有較低密度的生物膜或沒(méi)有生物膜的部位具有較高的氧濃度,成為陰極,在材料表面形成氧濃差電池,引起局部腐蝕。微生物膜的組成和形成過(guò)程是一個(gè)很復(fù)雜的生物化學(xué)過(guò)程,同時(shí)環(huán)境因素對(duì)生物膜的形成過(guò)程影響很大,膜內(nèi)微生物種群間的相互作用也極為復(fù)雜,實(shí)驗(yàn)室條件下還不能模擬出自然環(huán)境下形成的生物膜[34]。
3 SRB腐蝕研究進(jìn)展
3.1 氫化酶陰極去極化理論
1934年von Wolzogen等[35]提出了氫化酶陰極去極化理論,陰極去極化理論將這種金屬破壞歸因于陰極氫的微生物消耗。在沒(méi)有氧的條件下,金屬腐蝕的陰極反應(yīng)是H+的逸出,但由于H+的過(guò)電位太高,腐蝕電池本身難于供給這樣的電位,因而陰極被一層H2所覆蓋,使得金屬腐蝕中止。在SRB存在情況下,其能夠從金屬表面除去H2,從而使腐蝕過(guò)程繼續(xù)。之后,Booth等[36]證明Desulfovidrio vulgaris可以使低碳鋼表面的陰極區(qū)域去極化,利用陰極極化的氫還原硫酸鹽,促進(jìn)鋼的腐蝕,為陰極去極化理論奠定了基礎(chǔ)。
該理論提出后,眾多研究者深入研究,并在不斷的探索中完善了陰極去極化理論。Muyzer等[37]基于氫化酶陰極去極化理論建立MIC模型,如圖4所示。SRB在金屬表面吸附后利用體內(nèi)的氫化酶將SO42-還原成H2S,同時(shí)將金屬表面陰極上生成的H除去,局部分壓降低,并且通過(guò)這種“去極化”作用使得Fe溶解,反應(yīng)如 (1)~(7) 式:
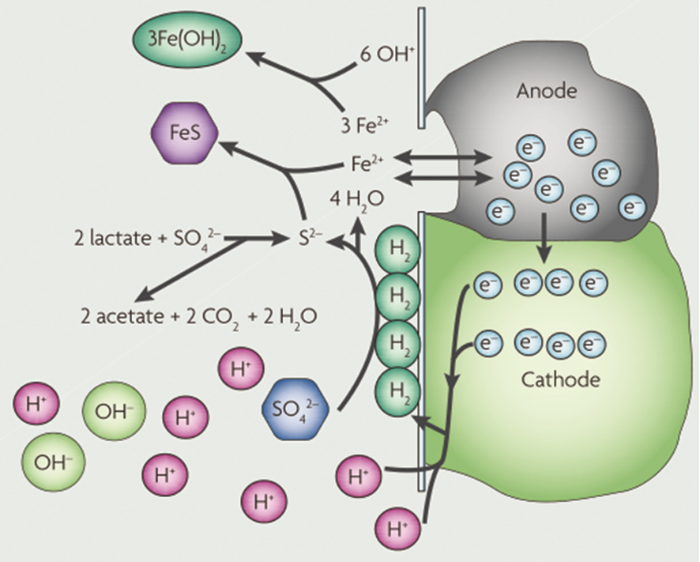
圖4 氫化酶陰極去極化機(jī)理圖[36]
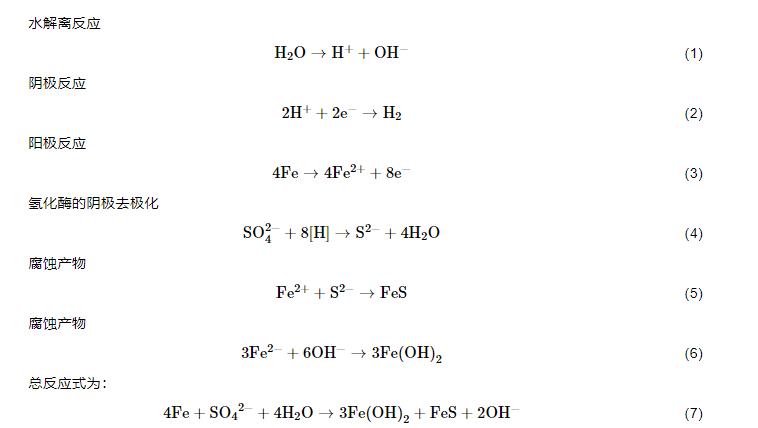
近幾年,陰極去極化理論不斷完善。大多數(shù)研究者認(rèn)為擴(kuò)散溶解的H2進(jìn)入SRB細(xì)胞后,最終到達(dá)細(xì)胞質(zhì)膜,在氫化酶的生物催化作用下被利用,膜結(jié)合的氫化酶和多血紅細(xì)胞色素通過(guò)黃素氧化還原蛋白 (或其他電子載體) 將電子傳遞到APS,使細(xì)胞質(zhì)中的硫酸鹽還原。實(shí)驗(yàn)室封閉環(huán)境模擬SRB腐蝕行為的研究顯示,隨著金屬材料腐蝕時(shí)間的延長(zhǎng),其腐蝕速率和EPS中蛋白質(zhì)數(shù)量顯著增加,這可能與SRB細(xì)胞內(nèi)的氫化酶有關(guān),材料表面溶解的Fe增加了氫化酶的合成,更多的氫化酶合成增加了細(xì)菌的代謝活性,從而加速腐蝕[38],da Silva等[39]的研究也有相似結(jié)果。通過(guò)計(jì)時(shí)安培法和循環(huán)伏安法研究D. desulfuricans 27774對(duì)不銹鋼和石墨電極表面生物膜的電活性影響,結(jié)果顯示,氫化酶與不銹鋼和石墨表面存在電子通道,可以進(jìn)行直接電子轉(zhuǎn)移,推測(cè)電子通道也可以讓營(yíng)養(yǎng)物質(zhì)和O2擴(kuò)散,形成濃度梯度[40],Yu等[10]研究表明,實(shí)驗(yàn)室石墨電極表面形成SRB能夠催化氫的氧化還原,推測(cè)氫化酶在電子傳遞過(guò)程中具有重要作用。Cu2+和Ag+對(duì)Desulfovibrio sp.細(xì)菌的影響研究表明,表面生物膜元素成分分析表明S峰值很高,這可能是在氫化酶的作用下形成了非均勻的FeS腐蝕產(chǎn)物膜,對(duì)材料起到一定保護(hù)作用[41]。同時(shí),研究者根據(jù)陰極去極化理論研發(fā)了一套點(diǎn)蝕預(yù)測(cè)系統(tǒng),利用計(jì)算機(jī)仿真研究SRB的腐蝕過(guò)程[42]。
氫化酶還同時(shí)起到了能量調(diào)節(jié)的作用。當(dāng)碳源缺乏時(shí),氫化酶可以增強(qiáng)SRB的還原硫酸鹽能力;當(dāng)碳源不可用時(shí),氫化酶可以促進(jìn)SRB直接獲取電子,這些代謝途徑研究對(duì)MIC的認(rèn)識(shí)有重要意義。在未來(lái)研究中,深入認(rèn)識(shí)氫化酶在MIC中的作用對(duì)于生物能源和生物技術(shù)的利用也具有重要意義[43,44]。
3.2 代謝產(chǎn)物腐蝕理論
微生物分泌的腐蝕性代謝物質(zhì)引起的MIC可以稱為代謝產(chǎn)物腐蝕 (M-MIC),如圖5所示[45]。腐蝕性代謝物質(zhì)包括H+、有機(jī)酸和硫化物等氧化劑。研究[46]表明,生物膜中產(chǎn)酸菌 (APB) 分泌的有機(jī)酸、SRB排出的H2S均能加速腐蝕。M-MIC本質(zhì)是一個(gè)電化學(xué)腐蝕過(guò)程,F(xiàn)e氧化和H+還原是兩個(gè)可分離的電極反應(yīng)。除了SRB和APB等細(xì)菌外,真菌 (如黑曲霉) 也會(huì)分泌酸性代謝物,從而引起M-MIC。
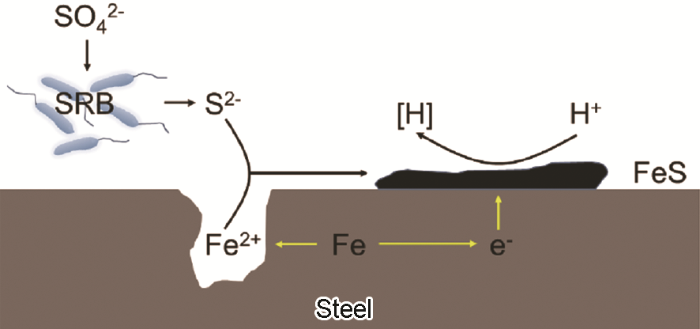
圖5 FeS代謝產(chǎn)物腐蝕機(jī)理圖[45]
SRB對(duì)銅合金的腐蝕研究結(jié)果顯示,由于硫酸鹽還原電位低于Cu+/Cu和Cu2+/Cu電位,Cu不能給SRB的硫酸鹽還原過(guò)程提供足夠的能量,因此SRB對(duì)Cu的腐蝕是由SRB代謝產(chǎn)生的硫化物引起,直接證明了銅合金腐蝕是由M-MIC造成的[47]。同時(shí),通過(guò)控制溶液環(huán)境中硫化物含量也證明了D. vulgaris對(duì)Cu的腐蝕方式為M-MIC[48]。研究者改變培養(yǎng)體系中SRB代謝產(chǎn)生的H2S含量,研究H2S對(duì)SRB生長(zhǎng)代謝和碳鋼腐蝕的影響。結(jié)果顯示,培養(yǎng)體系中氣體剩余體積越大,SRB代謝產(chǎn)生的H2S越多,溶液中溶解的H2S更少,浮游細(xì)菌和材料表面附著細(xì)菌的數(shù)量均增加,導(dǎo)致MIC更嚴(yán)重[49]。
介質(zhì)中Fe2+和Fe3+濃度是影響M-MIC的一個(gè)重要因素,研究人員開(kāi)展了大量工作研究Fe2+對(duì)SRB和FeS薄膜影響[50]。劉宏芳等[51]研究表明,介質(zhì)中不同濃度的Fe2+在碳鋼表面形成的FeS腐蝕產(chǎn)物膜不同,對(duì)碳鋼的腐蝕影響差異較大。更多的研究[52]表明,低碳鋼的腐蝕速率與溶液介質(zhì)中的Fe2+濃度成正比,F(xiàn)e2+的存在改變了FeS膜的類型,F(xiàn)e2+含量的增加會(huì)導(dǎo)致FeS膜的斷裂,從而增加腐蝕速率。關(guān)于Fe2+和Fe3+對(duì)SRB腐蝕的影響,人們提出了許多猜測(cè),包括Fe/FeS引起電偶腐蝕、陰極去極化影響、氫化酶調(diào)節(jié)和FeS薄膜物理性質(zhì)的變化。Fe2+和Fe3+在SRB細(xì)胞內(nèi)起到什么作用以及對(duì)FeS膜的形成有什么影響還需要進(jìn)一步研究。
H2S的含量對(duì)SRB代謝產(chǎn)物也有重要影響。生物膜中SRB的數(shù)量可以達(dá)到108 cell·cm-2,其產(chǎn)生的腐蝕性H2S會(huì)引起膜內(nèi)局部pH降低,造成嚴(yán)重局部腐蝕[53],同時(shí),SRB代謝產(chǎn)生的硫化物會(huì)減弱金屬鍵在材料表面的結(jié)合力,導(dǎo)致金屬的陽(yáng)極溶解速率增加[54]。Desulfovibrio sp.細(xì)菌對(duì)316L不銹鋼的腐蝕研究結(jié)果表明,該細(xì)菌能有效利用H2,但在給定電位下316L自腐蝕電位和腐蝕電流密度不變,材料表面沉積的FeS對(duì)陰極反應(yīng)沒(méi)有明顯的催化作用,因此H2消耗不是微生物腐蝕的決定性因素,而FeS作為一種半導(dǎo)體薄膜會(huì)影響電子從金屬移動(dòng)到細(xì)胞,在厭氧腐蝕中發(fā)揮著重要作用[55]。Iverson[56]綜述了厭氧腐蝕機(jī)理,認(rèn)為材料腐蝕速率與Fe2+和H2S有關(guān),F(xiàn)e2+和H2S反應(yīng)使基體表面形成鐵硫化合物的薄膜,從而使細(xì)菌與基體表面不直接接觸,其腐蝕速率增加。
生物膜中M-MIC過(guò)程會(huì)產(chǎn)生少量的H2,這部分H2被認(rèn)為是含有氫化酶微生物的能量來(lái)源,目前尚不清楚M-MIC過(guò)程產(chǎn)生的代謝產(chǎn)物是不是其他微生物的能量來(lái)源,未來(lái)還需要進(jìn)一步進(jìn)行相關(guān)實(shí)驗(yàn)論證。
3.3 濃差電池作用理論
1958年,Starkey[57]首先提出濃差電池理論,即金屬材料表面被腐蝕產(chǎn)物或者其它污垢覆蓋時(shí),在材料表面與介質(zhì)的界面處會(huì)形成濃差電池。1964年,King等[58]研究表明,F(xiàn)eS沉積在材料表面形成的濃差電池是金屬腐蝕的原因。
之后的研究進(jìn)一步表明濃差電池的形成與生物膜的結(jié)構(gòu)和形成有關(guān)[59]。材料在海洋和油氣環(huán)境下形成的生物膜,膜內(nèi)含有大量的好氧菌,好氧菌在生物膜內(nèi)分布不均勻,通過(guò)呼吸作用消耗了生物膜內(nèi)的O2,使得這些區(qū)域O2濃度較低成為陽(yáng)極區(qū),而生物膜密度較小或沒(méi)有生物膜覆蓋的區(qū)域具有較高的氧濃度成為陰極區(qū)。由于氧濃度差異而引起的局部腐蝕過(guò)程稱為氧濃差電池,如圖6所示[6]。Skovhus等[9]綜述了油氣管道MIC機(jī)理,生物膜內(nèi)固體有機(jī)和無(wú)機(jī)顆粒沉降在管道表面時(shí)會(huì)形成不同電偶電位區(qū)域,引起濃差電池腐蝕。因此,生物膜的研究對(duì)于濃差電池的作用機(jī)理認(rèn)識(shí)至關(guān)重要。
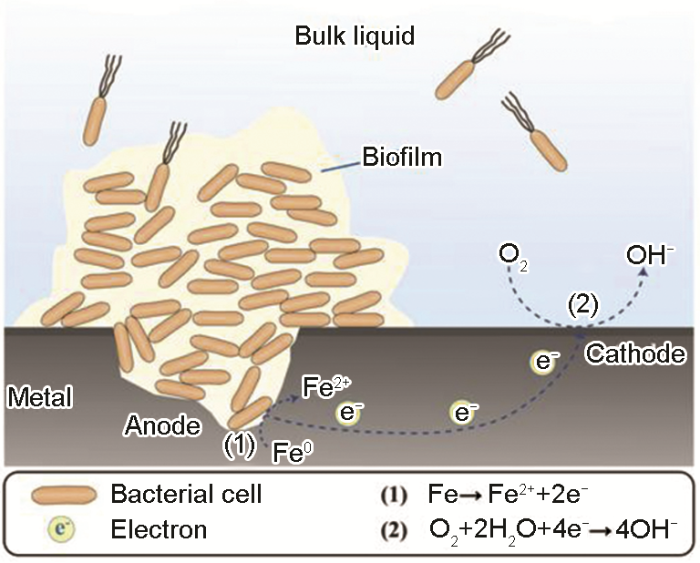
圖6 生物膜內(nèi)氧濃差電池點(diǎn)腐蝕機(jī)理圖[6]
近幾年,研究人員在MIC方面進(jìn)行了大量研究工作,濃差電池作用機(jī)理也較為完善。研究者[60]進(jìn)行了低合金鋼在海水中的氧濃差電池腐蝕行為研究,將低合金鋼的耐蝕性分為3類,之后進(jìn)一步研究了低合金鋼中不同元素形成的氧濃差電池差異。對(duì)潿洲油田套管斷裂事件的原因分析,認(rèn)為該事件是由于隔水管泄漏,使得套管與海水直接接觸,在海平面處形成了宏觀氧濃差電池導(dǎo)致套管腐蝕斷裂失效[61]。通過(guò)電化學(xué)和表面分析方法研究SRB對(duì)鋼的腐蝕影響,可見(jiàn)隨著培養(yǎng)時(shí)間的增加,SRB的腐蝕電位升高,由于溶液中形成了FeS,培養(yǎng)基顏色由灰色變?yōu)楹谏撛赟RB中的腐蝕速率增加,可能是因?yàn)槠潢帢O反應(yīng)速率增加使硫酸鹽還原為硫化物的速率增快從而形成了濃差電池[62]。Moon等[63]在之后的研究進(jìn)一步表明,SRB存在下的陰極反應(yīng)加速的同時(shí)也提高了陽(yáng)極反應(yīng)速率和腐蝕速率,SRB生物膜內(nèi)形成了氧濃差電池,并引起了嚴(yán)重的點(diǎn)蝕。
3.4 胞外電子傳遞理論
研究[64-66]表明,微生物能直接從金屬表面獲取電子,加速金屬的溶解。Dinh等[67]以金屬Fe作為唯一電子供體從海洋中分離培養(yǎng)得到一株新型腐蝕性SRB,通過(guò)測(cè)量其產(chǎn)生的硫化物、CH4、H2等代謝產(chǎn)物,顯示能夠直接從金屬Fe中獲得電子的新型SRB比傳統(tǒng)的SRB硫酸鹽還原得更快。經(jīng)典的陰極去極化理論明顯不能解釋這類細(xì)菌的腐蝕行為,細(xì)胞外電子傳遞 (EET) 理論的提出,很好地解釋了這類細(xì)菌的腐蝕機(jī)理[68,69]。胞外電子傳遞依賴于生物膜的形成,電子與離子不同,電子不能在液體中獨(dú)立存在,而生物膜內(nèi)電子載體較多,更有利于浮游細(xì)菌的利用。近年來(lái)許多研究者研究了SRB和硝酸鹽還原菌 (NRB) 在MIC中的跨膜電子傳遞機(jī)理,進(jìn)一步完善了該理論[7]。
胞外電子傳遞有兩種方式,如圖7所示[69],包括直接電子傳遞 (DET) 和電子載體電子傳遞 (MET)。直接電子傳遞包括兩種方式:(1) 依賴于外膜結(jié)合的氧化還原活性蛋白與基體導(dǎo)體表面直接接觸,如C型細(xì)胞色素;(2) 依賴于導(dǎo)電菌毛 (導(dǎo)電納米線) 與導(dǎo)體表面接觸。電子載體電子傳遞需要利用可溶性電子載體物質(zhì),如H+/H2、核黃素和黃素腺嘌呤二核苷酸 (FAD) 等氧化還原活性物質(zhì)。對(duì)于MIC中的胞外電子傳遞,電子通過(guò)DET或MET兩種方式傳遞到與細(xì)胞外膜結(jié)合的氧化還原蛋白處,電子進(jìn)入細(xì)胞后,細(xì)胞內(nèi)的電子傳輸鏈 (ETC) 通過(guò)一系列的氧化還原反應(yīng)將電子傳遞到細(xì)胞質(zhì)中的末端電子受體[70],即SRB厭氧呼吸中的硫酸鹽。對(duì)于細(xì)菌,ETC也依賴于各種與細(xì)胞質(zhì)膜結(jié)合的氧化還原活性物質(zhì),如細(xì)胞色素和核黃素類,研究表明這類氧化還原活性物質(zhì)作為電子媒介會(huì)加速碳鋼和不銹鋼的SRB腐蝕[68]。
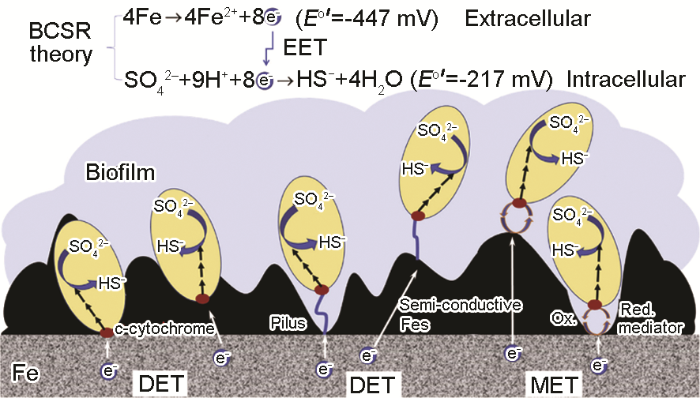
圖7 SRB 從金屬到細(xì)胞表面電子傳遞的3種方法[69]
依賴于外膜結(jié)合的氧化還原活性蛋白進(jìn)行的DET已經(jīng)成為了研究熱點(diǎn)。對(duì)D. Corrodens strain IS4典型腐蝕SRB的研究表明,從電極上獲取電子并不局限于鐵作為微生物代謝的唯一電子供體,細(xì)菌也能夠在石墨和摻雜鍺的陰極上獲取電子,同時(shí)通過(guò)紅外光譜電化學(xué)方法,認(rèn)為C型細(xì)胞色素是與外膜相關(guān)的氧化還原活性成分并且直接參與IS4細(xì)菌從基體表面直接獲取電子[8],具有這種功能的微生物可以稱為電營(yíng)養(yǎng)微生物[19]。但是,氧化還原活性蛋白對(duì)電子的吸收也存在爭(zhēng)議。研究者對(duì)SRB存在下管線鋼涂層的電化學(xué)腐蝕研究表明,必須具有足夠的負(fù)電荷SRB自身蛋白才能直接攝取電子[71]。未來(lái)應(yīng)用生物學(xué)等技術(shù)手段分離具有氧化還原活性成分的細(xì)菌細(xì)胞外膜,進(jìn)行功能分析,將有助于研究外膜細(xì)胞色素在整個(gè)DET過(guò)程中的作用,從而具體描述電子通過(guò)氧化還原活性蛋白在整個(gè)細(xì)胞中的傳遞過(guò)程。
依賴于導(dǎo)電菌毛 (納米線) 進(jìn)行的DET也已進(jìn)行了大量研究[69]。研究者[72]認(rèn)為在沒(méi)有有機(jī)碳源的培養(yǎng)基中,SRB細(xì)胞表面會(huì)出現(xiàn)大量菌毛附著在Fe表面,而在培養(yǎng)基中加入有機(jī)碳培養(yǎng)源,則未觀察到這些菌毛[73],進(jìn)一步研究顯示SRB細(xì)胞利用這些菌毛從碳鋼表面直接獲取電子進(jìn)行硫酸鹽還原從而在碳源缺乏環(huán)境中存活。Reguera等[74]的研究也顯示Geobacter sulfurreducens細(xì)菌菌毛缺失的突變體不能還原鐵 (III) 氧化物,但能吸附在鐵氧化物表面,電子探針原子力顯微鏡也顯示該菌毛具有良好的導(dǎo)電性。這些研究表明,SRB細(xì)胞的菌毛可以作為生物納米線,將電子從細(xì)胞表面轉(zhuǎn)移到鐵 (III) 氧化物表面。除了作為電子轉(zhuǎn)移通道,菌毛還可以參與其他電子轉(zhuǎn)移反應(yīng),例如,單個(gè)SRB的菌毛經(jīng)常交織在一起從而增加菌毛間細(xì)胞電子轉(zhuǎn)移的可能性[75]。該理論為獨(dú)特的細(xì)胞表面和細(xì)胞間相互作用提出了新的解釋,也為新型導(dǎo)電材料的研究提供了可能性。通過(guò)進(jìn)一步理論研究,這類細(xì)菌制造的納米線在納米電子和基因修飾方面將有很大的應(yīng)用前景。
研究者對(duì)MET方式進(jìn)行的胞外電子傳遞進(jìn)行了初步探究[6]。核黃素和黃素腺嘌呤二核苷酸 (FAD) 兩種電子傳遞介質(zhì)對(duì)Pseudomonas aeruginosa生物膜和碳鋼的腐蝕影響研究表明,兩種電子傳遞介質(zhì)對(duì)碳鋼腐蝕有明顯的促進(jìn)作用且碳鋼表面點(diǎn)蝕坑更深,而溶液中浮游細(xì)菌沒(méi)有太大變化[76]。Zhang等[77]用同樣方法證明電子傳遞介質(zhì)會(huì)增加304不銹鋼的點(diǎn)蝕和失重。目前對(duì)電子載體傳遞機(jī)理的研究仍相對(duì)較少,電子傳遞介質(zhì)在整個(gè)電子轉(zhuǎn)移過(guò)程中的作用還需要進(jìn)一步研究。
胞外電子傳遞相關(guān)基因研究,可以闡明電子傳遞在MIC中的重要性。Huang等[78]對(duì)P. aeruginosa內(nèi)合成內(nèi)源性電子介質(zhì)吩嗪-1-甲酰胺的PhzH基因進(jìn)行敲除,結(jié)果證明,PhzH的缺失降低了2205雙相不銹鋼的腐蝕速率,而在敲除的P. aeruginosa中恢復(fù)了該基因,腐蝕速率基本恢復(fù)。從分子和遺傳水平上闡明SRB中的胞外電子傳遞的機(jī)制,有助于證明EET和MIC的相互關(guān)系,還需要進(jìn)一步的研究和更多的證據(jù)。
胞外電子傳遞機(jī)理的研究對(duì)腐蝕保護(hù)應(yīng)用有重要意義[14]。通常使用外加電流陰極保護(hù) (ICCP) 作為一種常用的抑制微生物腐蝕的方法,但電營(yíng)養(yǎng)微生物存在時(shí),該方法的使用會(huì)為微生物代謝提供電子,促進(jìn)Desulfovibrio這類SRB和其他電營(yíng)養(yǎng)微生物在陰極保護(hù)設(shè)施周?chē)敝炒x,造成ICCP系統(tǒng)失效,使材料設(shè)施暴露在富含硫化物的沉積物和腐蝕性微生物群落中。已有研究[79,80]顯示,SRB存在下,在0.85 V (vs SCE) 陰極保護(hù)電位 (CP) 下,EQ70高強(qiáng)度鋼的腐蝕速率高于無(wú)CP的,而在-1.05 V (vs SCE) 下,EQ70的腐蝕速率低于無(wú)CP的,SRB在0.85 V (vs SCE) 時(shí)代謝活性增強(qiáng)很可能是由極化電極的直接電子傳遞引起。
隨著MIC研究的進(jìn)展,研究人員[9,81]進(jìn)一步提出了生物催化陰極硫酸鹽還原 (BCSR) 理論,從生物能量學(xué)和生物電化學(xué)的角度進(jìn)一步地解釋了MIC的作用機(jī)理[81,82]。對(duì)于SRB引起的MIC,乳酸等脂肪酸通常作為其生長(zhǎng)的有機(jī)碳源和電子供體,硫酸鹽作為末端電子受體完成氧化還原反應(yīng)過(guò)程。在BCSR理論中,當(dāng)SRB在鐵表面形成生物膜時(shí),由于受到擴(kuò)散和頂層生物膜對(duì)碳源消耗的限制,碳源很難到達(dá)貼近金屬表面的SRB生物膜,靠近金屬表面的固著SRB基本沒(méi)有能夠利用的碳源,此時(shí)饑餓的SRB將使用易被腐蝕的金屬 (如Fe) 作為電子供體從而獲取其生長(zhǎng)代謝所需的能量。圖8為有機(jī)碳-硫酸鹽還原和以Fe為電子供體的BCSR之間的差異[83]。因此,BCSR理論回答了當(dāng)生物膜中碳源缺乏時(shí),微生物腐蝕金屬的目的是從這個(gè)過(guò)程中獲得能量來(lái)維持它們的生長(zhǎng)代謝。
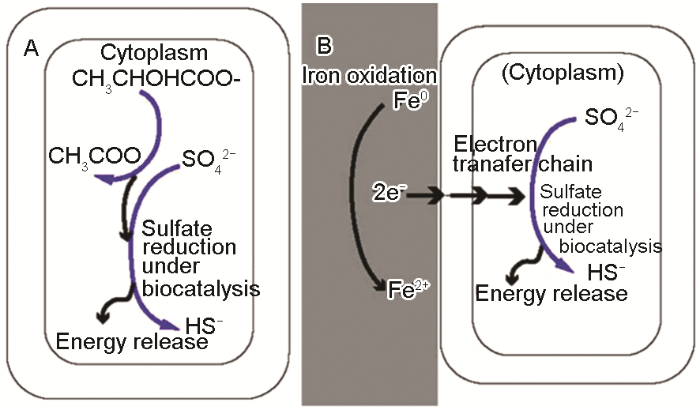
圖8 有機(jī)碳-硫酸鹽反應(yīng)和BCSR中SRB以鐵為電子供體的腐蝕示意圖[83]
當(dāng)Fe被SRB腐蝕時(shí),SRB外部發(fā)生金屬鐵的氧化,而硫酸鹽還原發(fā)生在SRB內(nèi)部。因此,F(xiàn)e氧化釋放出的電子將穿過(guò)SRB的細(xì)胞壁,最終達(dá)到其細(xì)胞質(zhì)內(nèi)發(fā)生硫酸鹽還原反應(yīng)的位置。細(xì)胞外電子傳遞到細(xì)胞內(nèi)部方式為胞外電子傳遞,包括DET和MET機(jī)制。該理論很好地解釋了微生物為什么和怎樣腐蝕金屬,是研究MIC的新方法和思路。未來(lái)還需要進(jìn)一步跟蹤電子在細(xì)胞內(nèi)外的傳遞途徑,進(jìn)一步解釋腐蝕產(chǎn)物的形成過(guò)程和變化原因。
4 MIC研究方法與技術(shù)手段
MIC涉及材料 (冶金)、微生物和電化學(xué)多學(xué)科交叉,需要運(yùn)用到電化學(xué)方法、表面分析方法、微生物學(xué)和分子生物學(xué)等多種技術(shù)手段進(jìn)行研究。
由于生物腐蝕基本上是一個(gè)電化學(xué)過(guò)程,生物膜的三維結(jié)構(gòu)和其化學(xué)成分都會(huì)隨著時(shí)間而改變,因此電化學(xué)方法常被應(yīng)用于微生物腐蝕的監(jiān)測(cè)和機(jī)理研究[84-86]。研究[87]表明傳統(tǒng)電化學(xué)技術(shù) (包括動(dòng)電位極化曲線法、LPR和EIS) 由于外部施加的電場(chǎng)會(huì)導(dǎo)致部分細(xì)菌的損傷和死亡,減低微生物活性。Zhao等[87]比較了Pseudomonas aeruginosa存在下不同電化學(xué)技術(shù)對(duì)2205不銹鋼連續(xù)腐蝕監(jiān)測(cè)后生物膜的影響情況,認(rèn)為EIS和LPR監(jiān)測(cè)會(huì)抑制細(xì)菌生長(zhǎng)并顯著降低生物膜厚度和腐蝕性,導(dǎo)致腐蝕速率和點(diǎn)蝕坑深度明顯降低。而新型電化學(xué)技術(shù)——電化學(xué)噪聲法不需要對(duì)體系施加劇烈擾動(dòng),不會(huì)對(duì)微生物的生長(zhǎng)繁殖產(chǎn)生干擾,對(duì)生物膜的影響和材料腐蝕影響很小,從而獲得最接近的腐蝕速率和點(diǎn)蝕坑深度。新型電化學(xué)技術(shù)包括微區(qū)電化學(xué)法、掃描電化學(xué)顯微鏡技術(shù)、電化學(xué)噪聲法等。Zhou等[88]使用電化學(xué)噪聲法研究了Pseudomonas aeruginosa在2205不銹鋼表面的點(diǎn)蝕瞬時(shí)形成過(guò)程,證明了細(xì)胞外電子傳遞機(jī)理。因此,新型電化學(xué)技術(shù)可以對(duì)亞穩(wěn)態(tài)點(diǎn)蝕、穩(wěn)態(tài)點(diǎn)蝕和離子溶解等過(guò)程進(jìn)行快速、小時(shí)間尺度的原位表征分析,在不影響微生物活性的同時(shí),可以獲得更多的電化學(xué)反應(yīng)界面動(dòng)力學(xué)信息,對(duì)于MIC研究有很重要的幫助。
表面分析技術(shù)是腐蝕研究的重要方法,對(duì)微生物腐蝕研究具有重要意義。表面分析技術(shù)包括掃描電鏡-能譜儀 (SEM-EDS)、原子力顯微鏡 (AFM)、X射線光電子能譜分析 (XPS)、飛行時(shí)間二次離子質(zhì)譜 (ToF-SIMS) 和激光掃描共聚焦顯微鏡 (CLSM) 等。每一種表面分析技術(shù)都有其獨(dú)特的優(yōu)點(diǎn)和局限性,對(duì)樣品的處理也各不相同,只有充分認(rèn)識(shí)每一種分析技術(shù),才能更好地發(fā)揮其優(yōu)點(diǎn)。已經(jīng)有大量文獻(xiàn)進(jìn)行了微生物對(duì)材料表界面的研究[89-91],對(duì)微生物產(chǎn)生的代謝產(chǎn)物或生物分子 (如酶、糖等) 進(jìn)行了定性和定量的研究分析,這對(duì)微生物腐蝕機(jī)理的認(rèn)識(shí)起到了關(guān)鍵作用。隨著腐蝕研究的深入,對(duì)表面分析技術(shù)的精度等各方面要求也更高。El Menjra等[92]利用ToF-SIMS技術(shù)研究了Fe表面生成鐵硫化物的來(lái)源,通過(guò)計(jì)算鐵硫化層中硫同位素的分餾值,可以區(qū)分生物和非生物形成的硫化物,有助于更好地研究含硫環(huán)境中鐵表面非生物或生物形成的鐵硫化物過(guò)程及其相互作用。多種表面分析技術(shù)的結(jié)合使用也是未來(lái)腐蝕研究發(fā)展的趨勢(shì),Li等[93]采用聚焦離子束掃描電子顯微鏡 (FIB-SEM) 研究了SRB在生物膜中的分布情況和基體表面點(diǎn)蝕的縱向元素分布,研究表明生物膜具有一定的陰離子選擇性并提出了MIC點(diǎn)蝕機(jī)理。因此,更加精確的原位表面分析技術(shù)對(duì)MIC研究有重要意義。
微生物學(xué)或生物化學(xué)方法是MIC研究的基礎(chǔ)。微生物的培養(yǎng)對(duì)MIC研究十分重要,培養(yǎng)基的選擇改良對(duì)體系微生物的生長(zhǎng)代謝有較大影響。世界上現(xiàn)有的大約95%的微生物還不能培養(yǎng)。此外,不同微生物的培養(yǎng)時(shí)間不同,從24 h到幾周不等,具體取決于樣品的種類和體系配比[94,95]。因此,進(jìn)行微生物腐蝕研究時(shí)對(duì)于微生物的選擇與培養(yǎng)應(yīng)該十分重視。
分子生物學(xué)方法是MIC研究的新趨勢(shì)。隨著分子生物學(xué)技術(shù)的發(fā)展普及和研究成本的降低,生物腐蝕研究中對(duì)微生物群落的DNA/RNA/蛋白質(zhì)的研究開(kāi)始增加。分子生物學(xué)不受培養(yǎng)的限制,可以通過(guò)保守的核糖體基因 (16S rDNA或23S rDNA) 研究微生物群落對(duì)腐蝕的影響,可以通過(guò)RNA或蛋白質(zhì)研究微生物的代謝活性,也可以通過(guò)研究生物腐蝕過(guò)程相關(guān)的功能基因 (如APS還原酶基因apsA) 從而研究電子在細(xì)胞內(nèi)傳遞途徑[96-98]。Smith等[50]開(kāi)展了近岸低海水腐蝕區(qū)的SRB腐蝕行為研究,采用宏基因組方法研究了細(xì)菌體內(nèi)硫循環(huán)過(guò)程。Palacios等[99]采用16S sRNA方法研究了Sporomusa和Methanosarcina兩種細(xì)菌共存下的電子傳遞機(jī)制。因此,分子微生物學(xué)的研究方法可能會(huì)成為未來(lái)微生物腐蝕機(jī)理研究的熱點(diǎn)。
在進(jìn)行MIC研究時(shí)必須注意樣品的采集和保存過(guò)程;進(jìn)行SRB腐蝕研究時(shí),一些測(cè)試要求樣品在低溫甚至在缺氧環(huán)境中保存,以防止某些化合物表面在環(huán)境中氧化。MIC是一門(mén)交叉學(xué)科,多種研究手段的交叉使用也是為了更好地研究腐蝕,但是這對(duì)研究者也極具挑戰(zhàn)[100-102]。
5 總結(jié)
微生物腐蝕研究已經(jīng)有100多年歷史,針對(duì)SRB腐蝕機(jī)理也進(jìn)行了多年研究,采用電化學(xué)、材料學(xué)和微生物學(xué)的方法,已提出了陰極去極化等多種經(jīng)典的腐蝕機(jī)理,近年來(lái)由于微區(qū)電化學(xué)和分子生物學(xué)等方法引入MIC研究中,從生物能量學(xué)和生物電化學(xué)角度提出了胞外電子傳遞理論。當(dāng)溶液環(huán)境中有充足的碳源 (如乳酸) 時(shí),SRB優(yōu)先利用有機(jī)物質(zhì)作為電子供體,而由于受到擴(kuò)散和頂層生物膜對(duì)碳源消耗限制,碳源很難到達(dá)貼近金屬表面的SRB生物膜,易被腐蝕的金屬 (例如Fe) 成為唯一電子供體,此時(shí)金屬表面SRB會(huì)通過(guò)胞外電子傳遞方式獲得金屬電子。胞外電子傳遞方式包括氧化還原活性蛋白、細(xì)菌納米線和可溶性電子載體3種方式,從而引起金屬材料腐蝕。未來(lái)還需要進(jìn)一步跟蹤電子在細(xì)胞內(nèi)外的傳遞路徑,通過(guò)基因工程等方法抑制某些特定基因或蛋白酶的表達(dá),探究腐蝕過(guò)程中的電子傳遞載體,并結(jié)合多種研究方法以進(jìn)一步研究SRB腐蝕機(jī)理。
參考文獻(xiàn)
1 Hou B R, et al. The Cost of Corrosion in China [M]. Beijing: Science Press, 2017
1 侯保榮等. 中國(guó)腐蝕成本 [M]. 北京: 科學(xué)出版社, 2017
2 Bhandari J, Khan F, Abbassi R, et al. Modelling of pitting corrosion in marine and offshore steel structures-A technical review [J]. J. Loss Prevent. Proc. Ind., 2015, 37: 39
3 Luo P, Zhang Y N, Cai P P, et al. Analysis and countermeasures of natural gas transmission pipeline internal corrosion accidents [J]. Total Corros. Control, 2010, 24(6): 16
3 羅鵬, 張一玲, 蔡陪陪等. 長(zhǎng)輸天然氣管道內(nèi)腐蝕事故調(diào)查分析與對(duì)策 [J]. 全面腐蝕控制, 2010, 24(6): 16
4 Hou B R, Zhang D, Wang P. Marine corrosion and protection: Current status and prospect [J]. Bull. Chin. Acad. Sci., 2016, 31: 1326
4 侯保榮, 張盾, 王鵬. 海洋腐蝕防護(hù)的現(xiàn)狀與未來(lái) [J]. 中國(guó)科學(xué)院院刊, 2016, 31: 1326
5 Yin Y S, Dong L H, Liu T, et al. Microbial Adhesion Corrosion of Marine Materials [M]. Beijing: Science Press, 2012
5 尹衍升, 董麗華, 劉濤等. 海洋材料的微生物附著腐蝕 [M]. 北京: 科學(xué)出版社, 2012
6 Jia R, Unsal T, Xu D K, et al. Microbiologically influenced corrosion and current mitigation strategies: A state of the art review [J]. Int. Biodeterior. Biodegrad., 2019, 137: 42
7 Dall'Agnol L T, Moura J J. Sulphate reducing bacteria (SRB) and biocorrosion [A].
7 Liengen T, Basséguy R, Féron D, et al. Understanding Biocorrosion: Fundamentals and Applications [M]. Oxford: Woodhead Publishing, 2014: 121
8 Beese-Vasbender P F, Nayak S, Erbe A, et al. Electrochemical characterization of direct electron uptake in electrical microbially influenced corrosion of iron by the lithoautotrophic SRB Desulfopila corrodens strain IS4 [J]. Electrochim. Acta, 2015, 167: 321
9 Xia J, Xu D K, Nan L, et al. Study on mechanisms of microbiologically influenced corrision of metal from the perspective of bio-electrochemistry and bio-energetics [J]. China J. Mater. Res., 2016, 30: 161
9 夏進(jìn), 徐大可, 南黎等. 從生物能量學(xué)和生物電化學(xué)角度研究金屬微生物腐蝕的機(jī)理 [J]. 材料研究學(xué)報(bào), 2016, 30: 161
10 Yu L, Duan J, Du X, et al. Accelerated anaerobic corrosion of electroactive sulfate-reducing bacteria by electrochemical impedance spectroscopy and chronoamperometry [J]. Electrochem. Commun., 2013, 26: 101
11 Zhang Y M, Zheng Z X, Duan J Z. Relationship between hydrocarbon degradation and biocorrosionin marine environment [J]. Surf. Technol., 2019, 48(7): 211
11 張一夢(mèng), 鄭澤旭, 段繼周. 海洋中石油烴類降解與微生物腐蝕關(guān)系研究 [J]. 表面技術(shù), 2019, 48(7): 211
12 Zhang X L, Chen Z X, Liu H H, et al. Effect of environment factors on the growth of sulfate-reducing bacteria [J]. J. Chin. Soc. Corros. Prot., 2000, 20: 224
12 張小里, 陳志昕, 劉海洪等. 環(huán)境因素對(duì)硫酸鹽還原菌生長(zhǎng)的影響 [J]. 中國(guó)腐蝕與防護(hù)學(xué)報(bào), 2000, 20: 224
13 Stott J F D, Herbert B N. The effect of pressure and temperature on sulphate-reducing bacteria and the action of biocides in oilfield water injection systems [J]. J. Appl. Bacteriol., 1986, 61: 57
14 Dec W, Mosia?ek M, Socha R P, et al. The effect of sulphate-reducing bacteria biofilm on passivity and development of pitting on 2205 duplex stainless steel [J]. Electrochim. Acta, 2016, 212: 225
15 Jiang B, Gong A J, Li X G, et al. The distribution laws of sulfate-reducing bacteria in eight soil corrosion test stations in China [J]. Chem. Bioeng., 2008, 25(4): 54
15 蔣波, 弓愛(ài)君, 李曉剛等. 硫酸鹽還原菌在8個(gè)土壤試驗(yàn)站中的分布規(guī)律研究 [J]. 化學(xué)與生物工程, 2008, 25(4): 54
16 Wang H L, Yang J F. Spatiotemporal distribution of sulfate-reducing bacteria in Xiangshan Bay and related affecting factors [J]. Chin. J. Ecol., 2011, 30: 2857
16 王海麗, 楊季芳. 象山港海域硫酸鹽還原菌的時(shí)空分布及其影響因素 [J]. 生態(tài)學(xué)雜志, 2011, 30: 2857
17 Chen H W. Economic importance of marine sulfate-reducing bacteria and their activities [J]. J. Oceanogr. Huanghai Bohai Seas, 1998, 16(4): 65
17 陳皓文. 海洋硫酸鹽還原菌及其活動(dòng)的經(jīng)濟(jì)重要性 [J]. 黃渤海海洋學(xué)報(bào), 1998, 16(4): 65
18 Schoeffler M, Gaudin A L, Ramel F, et al. Growth of an anaerobic sulfate-reducing bacterium sustained by oxygen respiratory energy conservation after O2-driven experimental evolution [J]. Environ. Microbiol., 2019, 21: 360
19 Duan J Z, Wu S R, Zhang X J, et al. Corrosion of carbon steel influenced by anaerobic biofilm in natural seawater [J]. Electrochim. Acta, 2008, 54: 22
20 Li X H, Xiao H, Zhang W J, et al. Analysis of cultivable aerobic bacterial community composition and screening for facultative sulfate-reducing bacteria in marine corrosive steel [J]. J. Oceanol. Limnol., 2019, 37: 600
21 Zhang Y M, Ma Y, Duan J Z, et al. Analysis of marine microbial communities colonizing various metallic materials and rust layers [J]. Biofouling, 2019, 35: 429
22 Zhou J H, He Q, Hemme C L, et al. How sulphate-reducing microorganisms cope with stress: lessons from systems biology [J]. Nat. Rev. Microbiol., 2011, 9: 452
23 Liu Y, Bond D R. Long‐distance electron transfer by G. sulfurreducens biofilms results in accumulation of reduced c-type cytochromes [J]. ChemSusChem, 2012, 5: 1047
24 Kato S. Microbial extracellular electron transfer and its relevance to iron corrosion [J]. Microb. Biotechnol., 2016, 9(2): 141
25 Da Silva J J R F, Williams R J P. The Biological Chemistry of the Elements: The Inorganic Chemistry of Life [M]. 2nd Ed. Oxford: Oxford University Press, 2001
26 Liu H W, Xu D K, Wu Y N, et al. Research progress in corrosion of steels induced by sulfate reducing bacteria [J]. Corros. Sci. Prot. Technol., 2015, 27: 409
26 劉宏偉, 徐大可, 吳亞楠等. 微生物生物膜下的鋼鐵材料腐蝕研究進(jìn)展 [J]. 腐蝕科學(xué)與防護(hù)技術(shù), 2015, 27: 409
27 Liu H W, Fu C Y, Gu T Y, et al. Corrosion behavior of carbon steel in the presence of sulfate reducing bacteria and iron oxidizing bacteria cultured in oilfield produced water [J]. Corros. Sci., 2015, 100: 484
28 Flemming H C, Neu T R, Wozniak D J. The EPS matrix: The “house of biofilm cells” [J]. J. Bacteriol., 2007, 189: 7945
29 Jia R, Yang D Q, Xu D K, et al. Anaerobic corrosion of 304 stainless steel caused by the Pseudomonas aeruginosa biofilm [J]. Front. Microbiol., 2017, 8: 2335
30 Duan J Z, Liu C, Liu H L, et al. Research progress of biofouling and its control technology in marine underwater facilities [J]. Mar. Sci., 2020, 44(8): 162
30 段繼周, 劉超, 劉會(huì)蓮等. 海洋水下設(shè)施生物污損及其控制技術(shù)研究進(jìn)展 [J]. 海洋科學(xué), 2020, 44(8): 162
31 Zhuang L, Tang Z Y, Ma J L, et al. Enhanced anaerobic biodegradation of benzoate under sulfate-reducing conditions with conductive iron-oxides in sediment of Pearl river estuary [J]. Front. Microbiol., 2019, 10: 374
32 Chen Y, Gu G D, Zhu G, et al. Separation of oilfield sulfate reducing bacteria identification and growth characteristics research [J]. Chem. Eng., 2015, 29(5): 50
32 陳穎, 谷國(guó)棟, 朱葛等. 油田硫酸鹽還原菌的分離鑒定及生長(zhǎng)特性研究 [J]. 化學(xué)工程師, 2015, 29(5): 50
33 Xing M N, Wei Y F, Zhou Y, et al. Radical-mediated C-S bond cleavage in C2 sulfonate degradation by anaerobic bacteria [J]. Nat. Commun., 2019, 10: 1609
34 Little B, Ray R. A perspective on corrosion inhibition by biofilms [J]. Corrosion, 2002, 58: 424
35 von Wolzogen K C A H, van der Vlugt I S. The graphitization of cast iron as an electrochemical process in anaerobic soils [J]. Water, 1934, 18: 147
36 Booth G H, Tiller A K. Cathodic characteristics of mild steel in suspensions of sulphate-reducing bacteria [J]. Corros. Sci., 1968, 8: 583
37 Muyzer G, Stams A J M. The ecology and biotechnology of sulphate-reducing bacteria [J]. Nat. Rev. Microbiol., 2008, 6: 441
38 Alkan A, Gümü? S, Atapek ? H, et al. A case study of a stress corrosion cracking failure in an AA5083 mold material used for curing rubber compounds [J]. Prot. Met. Phys. Chem. Surf., 2016, 52: 1100
39 da Silva M L B, Soares H M, Furigo A, et al. Effects of nitrate injection on microbial enhanced oil recovery and oilfield reservoir souring [J]. Appl. Biochem. Biotechnol., 2014, 174: 1810
40 Cordas C M, Guerra L T, Xavier C, et al. Electroactive biofilms of sulphate reducing bacteria [J]. Electrochim. Acta, 2008, 54: 29
41 Unsal T, Ilhan-Sungur E, Arkan S, et al. Effects of Ag and Cu ions on the microbial corrosion of 316L stainless steel in the presence of Desulfovibrio sp. [J]. Bioelectrochemistry, 2016, 110: 91
42 Xu D K, Li Y C, Gu T Y. Mechanistic modeling of biocorrosion caused by biofilms of sulfate reducing bacteria and acid producing bacteria [J]. Bioelectrochemistry, 2016, 110: 52
43 Moradi M, Duan J Z, Du X Q. Investigation of the effect of 4, 5-dichloro-2-n-octyl-4-isothiazolin-3-one inhibition on the corrosion of carbon steel in Bacillus sp. inoculated artificial seawater [J]. Corros. Sci., 2013, 69: 338
44 Wu T Q, Yan M C, Yu L B, et al. Stress corrosion of pipeline steel under disbonded coating in a SRB-containing environment [J]. Corros. Sci., 2019, 157: 518
45 Voordouw G, Niviere V, Ferris F G, et al. Distribution of hydrogenase genes in Desulfovibrio spp. and their use in identification of species from the oil field environment [J]. Appl. Environ. Microbiol., 1990, 56: 3748
46 Enning D, Garrelfs J. Corrosion of iron by sulfate-reducing bacteria: new views of an old problem [J]. Appl. Environ. Microbiol., 2014, 80: 1226
47 Fu W J, Li Y C, Xu D K, et al. Comparing two different types of anaerobic copper biocorrosion by sulfate- and nitrate-reducing bacteria [J]. Mater. Perform., 2014, 53: 66
48 Dou W W, Jia R, Jin P, et al. Investigation of the mechanism and characteristics of copper corrosion by sulfate reducing bacteria [J]. Corros. Sci., 2018, 144: 237
49 Jia R, Tan J L, Jin P, et al. Effects of biogenic H2S on the microbiologically influenced corrosion of C1018 carbon steel by sulfate reducing Desulfovibrio vulgaris biofilm [J]. Corros. Sci., 2018, 130: 1
50 Smith M, Bardiau M, Brennan R, et al. Accelerated low water corrosion: The microbial sulfur cycle in microcosm [J]. NPJ Mater. Degrad., 2019, 3: 37
51 Liu H F, Dong Z H, Xu L M. The influence of Fe2+ on the microbiological corrosion of carbon steel [J]. Corros. Prot., 1998, 19: 210
51 劉宏芳, 董澤華, 許立銘. Fe2+對(duì)碳鋼的微生物腐蝕作用的影響 [J]. 腐蝕與防護(hù), 1998, 19: 210
52 King J K, Harmon S M, Fu T T, et al. Mercury removal, methylmercury formation, and sulfate-reducing bacteria profiles in wetland mesocosms [J]. Chemosphere, 2002, 46: 859
53 De Romero M, Duque Z, Rodríguez L, et al. A study of microbiologically induced corrosion by sulfate-reducing bacteria on carbon steel using hydrogen permeation [J]. Corrosion, 2005, 61: 68
54 Dumlu F A, Aydin T, Odabasoglu F, et al. Anti-inflammatory and antioxidant properties of jervine, a sterodial alkaloid from rhizomes of Veratrum album [J]. Phytomedicine, 2019, 55: 191
55 Venzlaff H, Enning D, Srinivasan J, et al. Accelerated cathodic reaction in microbial corrosion of iron due to direct electron uptake by sulfate-reducing bacteria [J]. Corros. Sci., 2013, 66: 88
56 Iverson W P. Research on the mechanisms of anaerobic corrosion [J]. Int. Biodeterior. Biodegrad., 2001, 47: 63
57 Starkey R L. The general physiology of the sulfate-reducing bacteria in relation to corrosion [J]. Prod. Month., 1958, 22: 12
58 King R A, Miller J D A. Corrosion by the sulphate-reducing bacteria [J]. Nature, 1971, 233: 491
59 Ye Q. Microbiologically influenced corrosion in oilfield flooding water [D]. Wuhan: Huazhong University of Science & Technology, 2013
59 葉琴. 污水介質(zhì)中的微生物腐蝕 [D]. 武漢: 華中科技大學(xué), 2013
60 Guo J N, Huang Y M, Lin L J, et al. The study of the oxygen concentration cell corrosion of low alloy steel in sea water [J]. J. Chin. Soc. Corros. Prot., 1982, 2: 59
60 郭津年, 黃亞敏, 林連進(jìn)等. 低合金鋼在海水中氧濃差腐蝕的研究 [J]. 中國(guó)腐蝕與防護(hù)學(xué)報(bào), 1982, 2: 59
61 Ge R G. Failure analysis of marine casing [J]. Total Corros. Control, 2011, 25(7): 45
61 戈仁剛. 海洋油井套管斷裂原因分析 [J]. 全面腐蝕控制, 2011, 25(7): 45
62 Moon K M, Lee M H, Kim K J, et al. An electrochemical study on the microbiological influenced corrosion of steels sulfate-reducing bacteria [J]. Sci. & Tech., 2002, 11(1): 67
63 Moon K M, Cho H R, Lee M H, et al. Electrochemical analysis of the microbiologically influenced corrosion of steels by sulfate-reducing bacteria [J]. Met. Mater. Int., 2007, 13: 211
64 Al-Saadi S, Singh Raman R K. A long aliphatic chain functional silane for corrosion and microbial corrosion resistance of steel [J]. Prog. Organ. Coat., 2019, 127: 27
65 Shamsuddin R A, Bakar M H A, Daud W R W, et al. Can electrochemically active biofilm protect stainless steel used as electrodes in bioelectrochemical systems in a similar way as galvanic corrosion protection? [J]. Int. J. Hydrogen Energy, 2019, 44: 30512
66 Rasheed P A, Jabbar K A, Rasool K, et al. Controlling the biocorrosion of sulfate-reducing bacteria (SRB) on carbon steel using ZnO/chitosan nanocomposite as an eco-friendly biocide [J]. Corros. Sci., 2019, 148: 397
67 Dinh H T, Kuever J, Mu?mann M, et al. Iron corrosion by novel anaerobic microorganisms [J]. Nature, 2004, 427: 829
68 Tang H Y, Holmes D E, Ueki T, et al. Iron corrosion via direct metal-microbe electron transfer [J]. Mbio, 2019, 10(3): e00303-19
69 Gu T Y, Ru J, Unsal T, et al. Toward a better understanding of microbiologically influenced corrosion caused by sulfate reducing bacteria [J]. J. Mater. Sci. Technol., 2019, 35: 631
70 Jiang Y, Zeng R J. Bidirectional extracellular electron transfers of electrode-biofilm: Mechanism and application [J]. Bioresour. Technol., 2019, 271: 439
71 Enning D, Venzlaff H, Garrelfs J, et al. Marine sulfate-reducing bacteria cause serious corrosion of iron under electroconductive biogenic mineral crust [J]. Environ. Microbiol., 2012, 14: 1772
72 Li Y C, Xu D K, Chen C F, et al. Anaerobic microbiologically influenced corrosion mechanisms interpreted using bioenergetics and bioelectrochemistry: a review [J]. J. Mater. Sci. Technol., 2018, 34: 1713
73 Sherar B W A, Power I M, Keech P G, et al. Characterizing the effect of carbon steel exposure in sulfide containing solutions to microbially induced corrosion [J]. Corros. Sci., 2011, 53: 955
74 Reguera G, McCarthy K D, Mehta T, et al. Extracellular electron transfer via microbial nanowires [J]. Nature, 2005, 435: 1098
75 Shi L, Dong H L, Reguera G, et al. Extracellular electron transfer mechanisms between microorganisms and minerals [J]. Nat. Rev. Microbiol., 2016, 14: 651
76 Jia R, Yang D Q, Xu D K, et al. Electron transfer mediators accelerated the microbiologically influence corrosion against carbon steel by nitrate reducing Pseudomonas aeruginosa biofilm [J]. Bioelectrochemistry, 2017, 118: 38
77 Zhang P Y, Xu D K, Li Y C, et al. Electron mediators accelerate the microbiologically influenced corrosion of 304 stainless steel by the Desulfovibrio vulgaris biofilm [J]. Bioelectrochemistry, 2015, 101: 14
78 Huang Y, Zhou E Z, Jiang C Y, et al. Endogenous phenazine-1-carboxamide encoding gene PhzH regulated the extracellular electron transfer in biocorrosion of stainless steel by marine Pseudomonas aeruginosa [J]. Electrochem. Commun., 2018, 94: 9
79 Guan F, Zhai X F, Duan J Z, et al. Influence of sulfate-reducing bacteria on the corrosion behavior of high strength steel EQ70 under cathodic polarization [J]. PLoS ONE, 2016, 11: e0162315
80 Guan F. Research on the corrosion mechanism of sulfate-reducing bacteria under cathodic protection [D]. Qingdao: Institute of Oceanology, Chinese Academy of Sciences, 2017
80 管方. 陰極保護(hù)下硫酸鹽還原菌腐蝕機(jī)理研究 [D]. 青島: 中國(guó)科學(xué)院大學(xué) (中國(guó)科學(xué)院海洋研究所), 2017
81 Gu T Y, Zhao K, Nesic S. A practical mechanistic model for MIC based on a biocatalytic cathodic sulfate reduction (BCSR) theory [A]. Corrosion 2009 [C]. Atlanta, 2009: 09390
82 Xu D K, Gu T Y. Carbon source starvation triggered more aggressive corrosion against carbon steel by the Desulfovibrio vulgaris biofilm [J]. Int. Biodeterior. Biodegrad., 2014, 91: 74
83 Li Y F, Ning C Y. Latest research progress of marine microbiological corrosion and bio-fouling, and new approaches of marine anti-corrosion and anti-fouling [J]. Bioact. Mater., 2019, 4: 189
84 Xie F, Li X, Wang D, et al. Synergistic effect of sulphate-reducing bacteria and external tensile stress on the corrosion behaviour of X80 pipeline steel in neutral soil environment [J]. Eng. Fail. Anal., 2018, 91: 382
85 Xie F, Wang X F, Wang D, et al. Effect of strain rate and sulfate reducing bacteria on stress corrosion cracking behaviour of X70 pipeline steel in simulated sea mud solution [J]. Eng. Fail. Anal., 2019, 100: 245
86 Jia R, Wang D, Jin P, et al. Effects of ferrous ion concentration on microbiologically influenced corrosion of carbon steel by sulfate reducing bacterium Desulfovibrio vulgaris [J]. Corros. Sci., 2019, 153: 127
87 Zhao Y, Zhou E Z, Liu Y Z, et al. Comparison of different electrochemical techniques for continuous monitoring of the microbiologically influenced corrosion of 2205 duplex stainless steel by marine Pseudomonas aeruginosa biofilm [J]. Corros. Sci., 2017, 126: 142
88 Zhou E Z, Li H B, Yang C T, et al. Accelerated corrosion of 2304 duplex stainless steel by marine Pseudomonas aeruginosa biofilm [J]. Int. Biodeterior. Biodegrad., 2018, 127: 1
89 Yuan S J, Pehkonen S O. AFM study of microbial colonization and its deleterious effect on 304 stainless steel by Pseudomonas NCIMB 2021 and Desulfovibrio desulfuricans in simulated seawater [J]. Corros. Sci., 2009, 51: 1372
90 Xu P, Ren H Y, Wang C Z, et al. Research progress on mixture microbial corrosion and analytical method on metal surface [J]. Surf. Technol., 2019, 48: 216
90 許萍, 任恒陽(yáng), 汪長(zhǎng)征等. 金屬表面混合微生物腐蝕及分析方法研究進(jìn)展 [J]. 表面技術(shù), 2019, 48: 216
91 Skovhus T L, Eckert R B, Rodrigues E. Management and control of microbiologically influenced corrosion (MIC) in the oil and gas industry-Overview and a North Sea case study [J]. J. Biotechnol., 2017, 256: 31
92 El Menjra A I, Seyeux A, Mercier D, et al. ToF-SIMS analysis of abiotic and biotic iron sulfide layers formed in aqueous conditions on iron surfaces [J]. Appl. Surf. Sci., 2019, 484: 876
93 Li Y C, Feng S Q, Liu H M, et al. Bacterial distribution in SRB biofilm affects MIC pitting of carbon steel studied using FIB-SEM [J]. Corros. Sci., 2020, 167: 108512
94 Javaherdashti R. Impact of sulphate-reducing bacteria on the performance of engineering materials [J]. Appl. Microbiol. Biotechnol., 2011, 91: 1507
95 Videla H A, Herrera L K. Microbiologically influenced corrosion: looking to the future [J]. Int. Microbiol., 2005, 8: 169
96 Davidova I A, Duncan K E, Perez-Ibarra B M, et al. Involvement of thermophilic archaea in the biocorrosion of oil pipelines [J]. Environ. Microbiol., 2012, 14: 1762
97 Suflita J M, Aktas D F, Oldham A L, et al. Molecular tools to track bacteria responsible for fuel deterioration and microbiologically influenced corrosion [J]. Biofouling, 2012, 28: 1003
98 Beech I B, Sunner J A, Hiraoka K. Microbe-surface interactions in biofouling and biocorrosion processes [J]. Int. Microbiol., 2005, 8: 157
99 Palacios P A, Snoeyenbos-West O, L?scher C R, et al. Baltic sea methanogens compete with acetogens for electrons from metallic iron [J]. ISME J., 2019, 13: 3011
100 Zhai X F, Guan F, Wang N, et al. Preparation of DCOIT composited Zn-Ni alloy antibacterial coatings and sulfate-reducing bacterial corrosion resistance [J]. Surf. Technol., 2019, 48(7): 247
100 翟曉凡, 管方, 王楠等. DCOIT復(fù)合Zn-Ni合金抗菌鍍層的制備及其耐SRB腐蝕性能研究 [J]. 表面技術(shù), 2019, 48(7): 247
101 Liu H W, Cheng Y F. Mechanism of microbiologically influenced corrosion of X52 pipeline steel in a wet soil containing sulfate-reduced bacteria [J]. Electrochim. Acta, 2017, 253: 368
102 Bradley A S, Leavitt W D, Johnston D T. Revisiting the dissimilatory sulfate reduction pathway [J]. Geobiology, 2011, 9: 446
免責(zé)聲明:本網(wǎng)站所轉(zhuǎn)載的文字、圖片與視頻資料版權(quán)歸原創(chuàng)作者所有,如果涉及侵權(quán),請(qǐng)第一時(shí)間聯(lián)系本網(wǎng)刪除。

官方微信
《腐蝕與防護(hù)網(wǎng)電子期刊》征訂啟事
- 投稿聯(lián)系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 腐蝕與防護(hù)網(wǎng)官方QQ群:140808414





