大型原油儲罐是石油石化工業的重要裝備,然而腐蝕問題一直是威脅儲罐安全運行的關鍵因素。盡管原油含水率一般都小于0.5%,但是原油在存儲過程中存在“水沉油浮”現象,最終罐底被沉積水浸沒,為儲罐底板的腐蝕創造了電解質環境。沉積水中的Cl-濃度高、同時存在微生物、含有少量的溶解O2和H2S/CO2,因此腐蝕性較強,最快甚至不到1 a就導致儲罐底板腐蝕失效。研究表明,微生物腐蝕是儲罐底板腐蝕的主要原因,通常表現為嚴重的局部點蝕穿孔,而點蝕坑周圍材料的腐蝕往往很輕微[1]。
微生物腐蝕 (MIC) 是指因微生物的生命活動導致材料發生或加速腐蝕的現象[2,3]。金屬材料在發生MIC時主要以局部腐蝕,尤其以點蝕為主。目前在油氣生產領域中,研究MIC主要以硫酸鹽還原菌 (SRB)[4-6]、腐生菌 (TGB)[7,8]和鐵細菌 (FB)[9,10]為主,其中尤以SRB為甚。迄今,國內外研究者對于SRB導致金屬材料發生腐蝕的機理解釋主要有陰極去極化理論[11-13]、陽極加速理論[14,15]和直接電子傳遞理論[16-18]。陰極去極化理論認為由于微生物活動形成的生物膜使得金屬材料表面產生陽極區,當環境中含有SRB時,SRB不僅會降低金屬材料表面陰極反應中H結合生成H2的活化能,而且還可以利用金屬陰極區產生的氫還原硫酸鹽,由此加速陰極反應速度,進而加速金屬的腐蝕。陽極加速理論在陰極去極化理論的基礎上還考慮了SRB對陽極反應的影響,SRB還原硫酸鹽會產生大量的H2S和其他有機酸,這些代謝產物附著在金屬表面會與Fe2+相結合,加速Fe2+離開金屬基體表面,從而加速金屬腐蝕。直接電子傳遞理論認為在一系列酶促反應作用下,附著在金屬表面的SRB可以通過跨膜電子傳遞直接從金屬中獲得電子從而加速金屬的陽極溶解。
原油儲罐受自然環境影響明顯,導致儲罐內部的溫度會存在一定波動,在這種工況條件下微生物的腐蝕變化規律對于評估儲罐底板的腐蝕程度具有重要的參考價值。本文采用儲罐底部沉積水,測試了不同溫度下罐底板鋼的微生物腐蝕導致的均勻速率和點蝕速率變化規律,結合沉積水中的微生物種屬分析,探討了溫度對微生物腐蝕影響機制。
1 實驗方法
實驗水樣為白沙灣儲油庫罐底水,水溶液中含 (mg/L):Cl- 42637,HCO3- 2.43,SO42- 55,Na+ 15600,Ca2+ 1021,K+ 326,Mg2+ 730,細菌濃度104~105個/mL。
采用16S rRNA基因測序分析微生物的豐度。高通量測序文庫的構建和基于Illumina MiSeq平臺的測序由 GENEWIZ 公司完成。使用 Qubit 2.0 Fluorometer檢測DNA樣品的濃度,使用 MetaVx?文庫構建試劑盒構建測序文庫。
以30~50 ng DNA為模板,使用PCR引物擴增原核生物16S rDNA上包括V3及V4的2個高度可變區。采用包含"CCTACGGRRBGCASCAGKVRVGAAT”序列的上游引物和包含" GGACTACNVGGGTWTCTAATCC"序列的下游引物擴增V3和V4區。另外,通過PCR向16S rDNA的PCR產物末端加上帶有Index的接頭,以便進行NGS測序。
使用Agilent 2100生物分析儀檢測文庫質量,并且通過Qubit2.0 Fluorometer檢測文庫濃度。DNA文庫混合后,按Illumina MiSeq儀器使用說明書進行PE250/300雙端測序,由MiSeq自帶的MiSeq Control Software (MCS) 讀取序列信息。
試樣為罐底板用鋼Q235A,其化學成分 (質量分數,%) 為:C 0.15,Si 0.25,Mn 0.50,S 0.015,P 0.01,Cr 0.25,Ni 0.15,余量為Fe。將板材加工成100 mm×30 mm×10 mm的試片,并用砂紙將試片逐級打磨至800目,并用酒精和丙酮進行清洗后備用。
實驗前在無菌箱內采用紫外線對試樣和容器滅菌1 h,然后將試片水平放在底部固定有兩根玻璃棒的500 mL廣口瓶內,試片不與瓶底部接觸。隨后注入罐底水,再用橡膠塞密封廣口瓶。考慮到實際工況下罐底微生物菌落會形成局部厭氧環境,采用高純氮氣通過橡膠塞上的玻璃導管通入廣口瓶內除氧2 h,然后密封玻璃導管。所有縫隙處涂抹704膠密封。操作均在無菌箱內操作。最后將廣口瓶放入烘箱內,分別在25、35、45、55、65和85 ℃下腐蝕7 d。
腐蝕結束后,取出試片,利用KYKY-6900掃描電鏡 (SEM) 觀察腐蝕產物形貌,利用OXFORD-Ultim Max能譜儀 (EDS) 分析元素組成。去除腐蝕產物后,測量腐蝕失重,計算均勻腐蝕速率。通過Olympus OLS5000-SAF激光共聚焦顯微鏡 (CLSM) 測量試樣表面點蝕坑深度,計算均勻腐蝕速率。
2 結果與討論
2.1 罐底板腐蝕特征
通過清罐檢查罐底板腐蝕狀況可見,原油儲罐底板主要是以局部腐蝕為主,有部分焊縫發生了明顯的溝槽腐蝕,周圍分布著較多的圓形點蝕坑 (圖1a);在罐底板中部局部腐蝕坑并不多,但出現一個直徑大約為80 mm的蝕坑,深度幾乎快貫穿板厚 (圖1b)。在未發生局部腐蝕的區域,均勻腐蝕非常輕微,材料表面光滑平整,說明金屬腐蝕損失很少。

圖1 罐底板微生物腐蝕形貌
觀察罐底板點蝕坑形貌可以發現,點蝕坑都具有口大底小的特征。通常閉塞電池機制可以解釋點蝕坑快速發展的原因,即,由于腐蝕產物在點蝕坑的開口處堆積,最終導致點蝕坑內出現自催化酸化和濃差腐蝕電偶,結果點蝕坑內發生快速溶解,通常會形成口小底大的形貌特征,這也是含氧環境下點蝕坑的普遍特征。而罐底板的微生物菌落會團簇狀生長,其代謝的酸性產物會導致生物膜下的基底金屬快速腐蝕,因此罐底板的口大底小的點蝕形貌與微生物腐蝕的特征相吻合。
2.2 罐底水中微生物分析
罐底水微生物的豐度16S rRNA基因測序分析結果顯示出水樣中微生物種群分屬4個門,即Thermotogae (熱袍菌門)、Proteobacteria (變形菌門)、Bacteroidetes (擬桿菌門) 以及Firmicutes (厚壁菌門),具體含有20個屬,見圖2。主要菌屬的微生物含量以及特性整理后見表1。
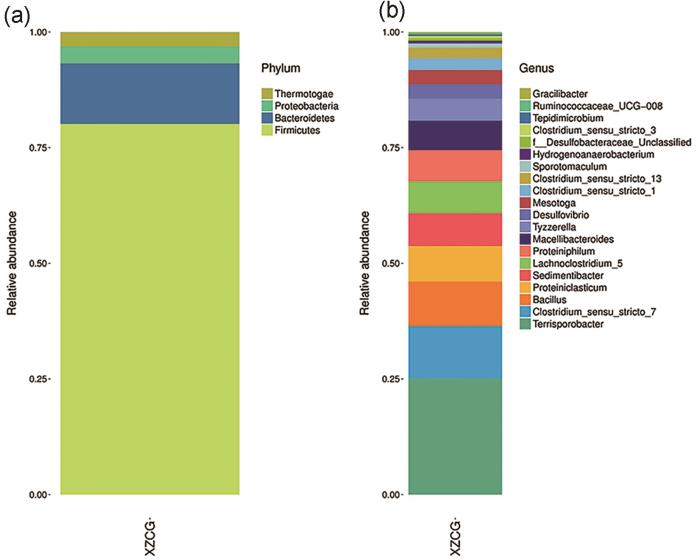
圖2 罐底水微生物的豐度16S rRNA基因測序分析
表1 罐底水微生物豐度與特性
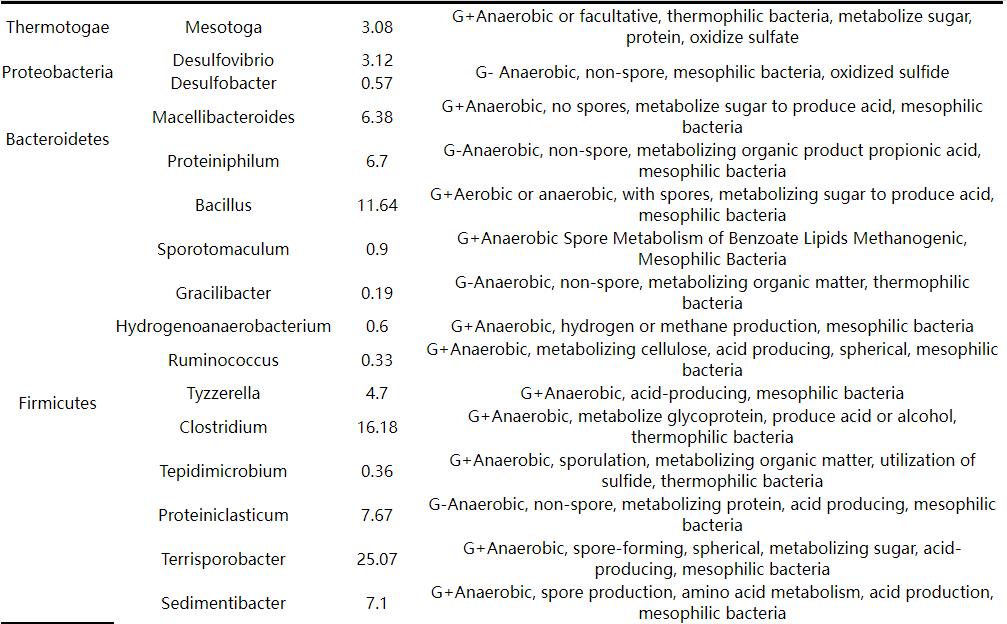
分析檢測結果可見Proteobacteria中的Desulfovibrio (脫硫弧菌屬) 和Desulfobacter (脫硫桿菌屬) 屬于SRB,總含量接近于4%。這類菌屬于嗜溫菌,其最適宜的生長溫度在30~40 ℃。Thermotogae中的Mesotoga菌屬雖然是異養細菌,在厭氧環境中也能氧化硫酸鹽,而且是嗜熱菌,最適宜生長溫度60~70 ℃[19]。Firmicutes中的Tepidimicrobium菌屬也能利用硫化物進行生理活動,也屬于嗜熱菌[20]。
細菌種群中屬于Bacteroidetes和Firmicutes的細菌種類和含量最多,均是異養微生物,代謝產物產生酸,通常會將這類菌屬歸類為腐生菌 (TGB)。其中除了Bacillus (芽孢桿菌屬) 是好氧細菌外,其余均為厭氧菌。另外,腐生菌中的Clostridium (梭菌屬) 屬于嗜熱菌[21],含量達到16.18%,在罐底水中也是優勢菌群。
微生物種群特性表明罐底水中不僅含有的豐富的SRB、TGB,而且在室溫和高溫下均有適合生長的微生物菌種。另外,罐底水中的菌群絕大多數是厭氧菌,說明罐底沉積物中的微生物是在厭氧環境下生存,而且SRB和TGB形成了共生體系。通常,SRB可以利用TGB代謝形成的有機酸作為電子供體進行生理代謝[22],因此,這種共生模式有助于微生物菌群增殖,最終對金屬材料造成更嚴重的腐蝕。
2.3 溫度對罐底水微生物腐蝕影響
不同溫度的沉積水浸泡后,罐底板的均勻腐蝕速率和最大點蝕坑深度變化規律如圖3所示。在25~85 ℃溫度范圍內,均勻腐蝕速率呈現先升后降的變化規律,其中在65 ℃達到最大值,溫度超過85 ℃以后均勻腐蝕速率迅速降低,但均勻腐蝕速率整體并不高,屬于輕微腐蝕范圍 (圖3a)。與均勻腐蝕速率類似,局部腐蝕速率也呈現先增大后減小的變化規律,峰值出現在30~40 ℃之間,點蝕坑深度接近15 μm,點蝕速率達到0.8 mm/a;在50~70 ℃之間也有10 μm左右,點蝕速率仍然超過0.5 mm/a,同樣當溫度超過85 ℃以后,點蝕速率也迅速降低。整體來說,從圖3b可以看出30~70 ℃是點蝕快速發生的溫度區間。
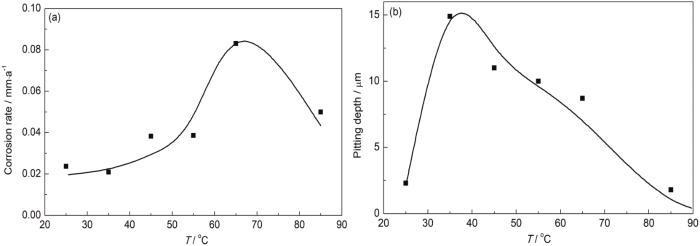
圖3 溫度對罐底板微生物腐蝕影響規律
觀察不同溫度下罐底板微生物腐蝕后的形貌可見,25 ℃下微生物膜均勻覆蓋在試樣表面,局部有團簇狀菌落生長 (圖4a);35 ℃時的生物膜最顯著,試樣表面布滿桿狀的細菌,而且也形成了較大的菌落團簇 (圖4c);當溫度升高到65 ℃以后,試樣表面的均勻腐蝕程度明顯加重,能顯現出晶界的特征,而生物菌落則相對減少 (圖4e);當溫度進一步升高到85 ℃以后,試樣表面的微生物菌落團簇相對減少。

圖4 罐底板微生物腐蝕后的表面形貌
去除生物膜以后觀察試樣表面的點蝕坑特征可見,25 ℃時點蝕坑深度雖然較小,但密度較高 (圖4b),溫度升高以后,點蝕坑的密度逐步降低 (圖4d和f)。觀察點蝕坑內部特征可見,腐蝕過程都是沿著固定的晶粒向內進行,相鄰的晶粒的晶界清晰可見,能觀察到相鄰晶粒比較平整的晶面 (圖5)。

圖5 35 ℃下腐蝕以后點蝕坑內部形貌
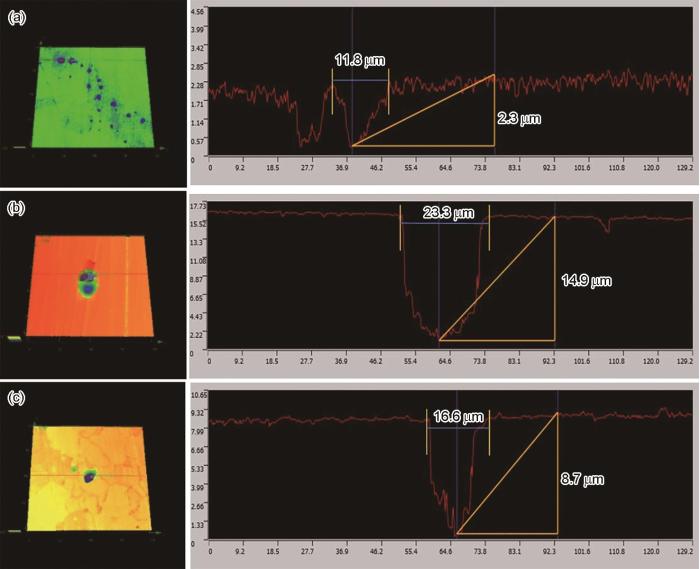
進一步利用激光共聚焦顯微鏡測量點蝕坑輪廓特征。可見,25 ℃條件下腐蝕生成的點蝕坑雖然深度較淺,但點蝕坑的直徑比較大,呈淺碟狀,計算直徑與深度的比值為5.1 (圖6a);35 ℃時的比值為1.6,65 ℃時為1.9 (圖6b和c)。
圖6 不同溫度腐蝕后最大點蝕坑輪廓形貌
點蝕通常由直徑非常微小的蝕坑發展起來,然后才逐漸擴大,一般尺寸小于1 μm的點蝕坑看成是亞穩態蝕坑。從圖6點蝕坑的發展過程來看,反映出初期時的點蝕坑直徑可能就比較大,這應該與微生物菌落團簇生長有關,先是微生物形成一定尺度的菌落,然后是菌落下逐步發生局部腐蝕,因此點蝕的萌生主要還是由于團簇狀的菌落導致的。
溫度直接影響硫酸鹽還原菌的代謝活性和生長速度。根據SRB適宜生長溫度的不同,可將其分為嗜溫型,嗜熱型及嗜冷型SRB。嗜冷型SRB的適宜生長溫度范圍為10~18 ℃[23,24]。嗜中溫型SRB的最適宜生長溫度為37±1 ℃[25],高于45℃停止生長。嗜熱SRB的生長溫度范圍在50~70 ℃,最佳生長溫度為65 ℃,在80 ℃或更高溫度下仍可以生存。附著在鋼鐵表面的SRB可以耐受更高溫度[26-28]。Liu等[29]研究從渤海油田分離得到的嗜熱SRB菌株在不同溫度下對碳鋼腐蝕的影響,可見60 ℃碳鋼的腐蝕速率是37 ℃時的2.2倍,表明嗜熱硫酸鹽還原菌的代謝活性對適宜生長溫度的依賴性。溫度太低太高均會抑制SRB的生長代謝活動。
罐底板的微生物主要是嗜溫和嗜熱菌,因此,從無論是均勻腐蝕速率還是點蝕速率在25 ℃時都不高,說明25 ℃以下罐底水中的微生物不活躍。均勻腐蝕速率在65 ℃達到峰值說明微生物在這一溫度也有較高的代謝活性,微生物代謝出來的酸性產物在高溫下與金屬基體會有較快的反應速率,當溫度升高到85 ℃以后,微生物活性大大降低,此時雖然溫度有利于腐蝕速率加快,但由于代謝產物較少,因此均勻腐蝕速率也降低。
從點蝕坑的特征情況來看,可以推測點蝕坑的發展主要與菌落的生長有關。相比較而言,嗜溫的硫酸鹽還原菌和腐生菌的數量最多,因此,35 ℃就是嗜溫菌的最有利生長溫度,因此在這個溫度下菌落最發達,代謝產物在生物膜下產生的的局部酸性對局部金屬造成快速腐蝕。其次,按照生物催化陰極硫酸鹽還原機理[30,31],由于SRB可直接從金屬獲取電子作為能量來源,因此在菌落下的金屬基體為上部的菌群提供電子,因此,菌落下方的金屬會發生快速腐蝕。
由于點蝕的發展與菌落的相關性更大,因此,溫度升高到65 ℃時,主要是嗜溫菌生長,但其數量要小于嗜溫菌,因此在試樣表面的菌落不夠發達,這從試樣表面的掃描電鏡也能看出來 (圖4e),因此點蝕坑深度和密度都降低。當超過85 ℃以后,絕大部分的微生物的活動受到抑制,因此點蝕也迅速減小。
3 結論
(1) 大型原油儲罐的罐底水中微生物種群含有嗜溫和嗜熱的SRB和TGB,它們在室溫到60~70 ℃范圍內均能生長。
(2) 罐底板鋼的微生物腐蝕的均勻腐蝕速率在65 ℃時達到峰值,但均勻腐蝕總體屬于輕微腐蝕。而點蝕速率在35 ℃時達到峰值,為0.8 mm/a,屬于嚴重腐蝕;65 ℃時也有較高的點蝕速率,溫度超過65 ℃以后點蝕速率迅速降低。30~70 ℃是點蝕快速發生的溫度區間,溫度對罐底板鋼微生物腐蝕的影響與微生物種類耐溫性有關。
(3) 罐底板微生物腐蝕形成的點蝕坑與菌落的團簇生長有關,微生物先是在金屬表面形成團簇狀的菌落,然后代謝過程中使得菌落下的金屬發生快速點蝕。
參考文獻
[1] Liu S, Wang J, Cheng H H, et al. Corrosion mechanism and protective measures of inner wall baseplate of large crude oil storage tank [J]. Surf. Technol., 2017, 46(11): 47
[1] (劉栓, 王娟, 程紅紅 等. 大型原油儲罐內壁底板腐蝕機理及防護措施 [J]. 表面技術, 2017, 46(11): 47)
[2] Javaherdashti R. Microbiologically influenced corrosion (MIC) [A]. Microbiologically Influenced Corrosion: An Engineering Insight [M]. Cham: Springer, 2017: 31
[3] Shi X B, Yang C G, Yan W, et al. Microbiologically influenced corrosion of pipeline steels [J]. J. Chin. Soc. Corros. Prot., 2019, 39: 9
[3] (史顯波, 楊春光, 嚴偉 等. 管線鋼的微生物腐蝕 [J]. 中國腐蝕與防護學報, 2019, 39: 9)
[4] Zhang F, Wang H T, He Y J, et al. Case analysis of microbial corrosion in product oil pipeline [J]. J. Chin. Soc. Corros. Prot., 2021, 41: 795
[4] (張斐, 王海濤, 何勇君 等. 成品油輸送管道微生物腐蝕案例分析 [J]. 中國腐蝕與防護學報, 2021, 41: 795)
[5] Shi J Y, Tao G F, Lu Y Q, et al. Study on the microbiological corrosion behavior of X65 pipeline steel by SRB and IB [J]. Oil Gas Field Surf. Eng., 2021, 40(8): 12
[5] (史晶瑩, 陶桂鳳, 盧永強 等. SRB和IB對X65管線鋼的微生物腐蝕行為研究 [J]. 油氣田地面工程, 2021, 40(8): 12)
[6] Ma G, Gu Y H, Zhao J. Research progress on sulfate-reducing bacteria induced corrosion of steels [J]. J. Chin. Soc. Corros. Prot., 2021, 41: 289
[6] (馬剛, 顧艷紅, 趙杰. 硫酸鹽還原菌對鋼材腐蝕行為的研究進展 [J]. 中國腐蝕與防護學報, 2021, 41: 289)
[7] Zhang R Y, Zhao G A, Shi D Y, et al. Experimental study on microbiologically influenced corrosion of natural gas gathering pipelines [J]. Mater. Prot., 2019, 52(11): 38
[7] (張仁勇, 趙國安, 施岱艷 等. 天然氣集輸管道的微生物腐蝕試驗研究 [J]. 材料保護, 2019, 52(11): 38)
[8] Jiang X, Fan J Z, Qu D R, et al. Corrosion failure analysis on an underground pipeline for a gas gathering station [J]. Corros. Sci. Prot. Technol., 2019, 31: 320
[8] (蔣秀, 范舉忠, 屈定榮 等. 某集氣站埋地管道腐蝕失效原因分析 [J]. 腐蝕科學與防護技術, 2019, 31: 320)
[9] Wang K T, Chen F, Li H, et al. Corrosion behavior of L245 pipeline steel in shale gas fracturing produced water containing iron Bacteria [J]. J. Chin. Soc. Corros. Prot., 2021, 41: 248
[9] (王坤泰, 陳馥, 李環 等. 鐵細菌對L245鋼腐蝕行為的影響研究 [J]. 中國腐蝕與防護學報, 2021, 41: 248)
[10] Chen X Y, Zhao Q H, Guo P. Discussion on the causes of gas field corrosion and anti-corrosion measures [J]. Total Corros. Control, 2020, 34(9): 95
[10] (陳曉宇, 趙啟宏, 郭樸. 關于氣田腐蝕原因及防腐措施探究 [J]. 全面腐蝕控制, 2020, 34(9): 95)
[11] Xu D, Li Y, Gu T. A synergistic D-tyrosine and tetrakis hydroxy‐methyl phosphonium sulfate biocide combination for the mitigation of an SRB biofilm [J]. World J. Microbiol. Biotechnol., 2012, 28: 3067
doi: 10.1007/s11274-012-1116-0
[12] Cord-Ruwisch R, Widdel F. Corroding iron as a hydrogen source for sulphate reduction in growing cultures of sulphate-reducing bacteria [J]. Appl. Microbiol. Biotechnol., 1986, 25: 169
doi: 10.1007/BF00938942
[13] Matias P M, Pereira I A C, Soares C M, et al. Sulphate respiration from hydrogen in Desulfovibrio bacteria: a structural biology overview [J]. Prog. Biophys. Mol. Biol., 2005, 89: 292
doi: 10.1016/j.pbiomolbio.2004.11.003
[14] Antony P J, Raman R K S, Mohanram R, et al. Influence of thermal aging on sulfate-reducing bacteria (SRB)-influenced corrosion behaviour of 2205 duplex stainless steel [J]. Corros. Sci., 2008, 50: 1858
doi: 10.1016/j.corsci.2008.03.009
[15] Hardy J A, Bown J L. The corrosion of mild steel by biogenic sulfide films exposed to air [J]. Corrosion, 1984, 40: 650
doi: 10.5006/1.3593903
[16] Duan J Z, Wu S R, Zhang X J, et al. Corrosion of carbon steel influenced by anaerobic biofilm in natural seawater [J]. Electrochim. Acta, 2008, 54: 22
doi: 10.1016/j.electacta.2008.04.085
[17] Li H B, Xu D K, Li Y C, et al. Extracellular electron transfer is a bottleneck in the microbiologically influenced corrosion of C1018 carbon steel by the biofilm of sulfate-reducing bacterium Desulfovibrio vulgaris [J]. PLoS One, 2015, 10(8): e0136183
doi: 10.1371/journal.pone.0136183
[18] Sherar B W A, Power I M, Keech P G, et al. Characterizing the effect of carbon steel exposure in sulfide containing solutions to microbially induced corrosion [J]. Corros. Sci., 2011, 53: 955
doi: 10.1016/j.corsci.2010.11.027
[19] Fadhlaoui K, Ben Hania W, Armougom F, et al. Obligate sugar oxidation in Mesotoga spp., phylum Thermotogae, in the presence of either elemental sulfur or hydrogenotrophic sulfate‐reducers as electron acceptor [J]. Environ. Microbiol., 2018, 20: 281
doi: 10.1111/1462-2920.13995 pmid: 29124868
[20] Whitman W B. Bergey's Manual of Systematics of Archaea and Bacteria [M]. Hoboken, New Jersey: Wiley, 2015: 1
[21] Du C, Webb C. Cellular systems [A]. Murray M Y. Comprehensive Biotechnology [M]. 2nd ed. Burlington, VT: Academic Press, 2011: 11
[22] Muyzer G, Stams A J M. The ecology and biotechnology of sulphate-reducing bacteria [J]. Nat. Rev. Microbiol., 2008, 6: 441
doi: 10.1038/nrmicro1892
[23] Isaksen M F, Jorgensen B B. Adaptation of psychrophilic and psychrotrophic sulfate-reducing bacteria to permanently cold marine environments [J]. Appl. Environ. Microbiol., 1996, 62: 408
doi: 10.1128/aem.62.2.408-414.1996
[24] Knoblauch C, J?rgensen B B, Harder J. Community size and metabolic rates of psychrophilic sulfate-reducing bacteria in arctic marine sediments [J]. Appl. Environ. Microbiol., 1999, 65: 4230
doi: 10.1128/AEM.65.9.4230-4233.1999
[25] Li J Y, Huang W B, Wang X L, et al. Research on screening and physiological characteristics of sulfate reducing bacteria [J]. Anhui Agric. Sci., 2010, 38: 16092
[25] (李俊葉, 黃偉波, 王筱蘭 等. 硫酸鹽還原菌的篩選及生理特性研究 [J]. 安徽農業科學, 2010, 38: 16092)
[26] Henry E A, Devereux R, Maki J S, et al. Characterization of a new thermophilic sulfate-reducing bacterium [J]. Arch. Microbiol., 1994, 161: 62
pmid: 11541228
[27] Chen M Y. The growth and the sulfur metabolisms of thermophilic sulfate-reducing bacteria at different temperatures [J]. Guangdong Chem. Ind., 2016, 43(3): 31
[27] (陳鳴淵. 嗜熱硫酸鹽還原菌在不同溫度下的生長及其硫代謝 [J]. 廣東化工, 2016, 43(3): 31)
[28] Liu H F, Liu T. Growth characteristics of thermophile sulfate-reducing bacteria and its effect on carbon steel [J]. J. Chin. Soc. Corros. Prot., 2009, 29(2): 93
[28] (劉宏芳, 劉濤. 嗜熱硫酸鹽還原菌生長特征及其對碳鋼腐蝕的影響 [J]. 中國腐蝕與防護學報, 2009, 29(2): 93)
[29] Liu T, Liu H, Hu Y, et al. Growth characteristics of thermophile sulfate-reducing bacteria and its effect on carbon steel [J]. Mater. Corros., 2009, 60: 218
doi: 10.1002/maco.200805063
[30] Lin J, Zhu G W, Sun C, et al. A review of microbiologically influenced corrosion of metals [J]. Corros. Sci. Prot. Technol., 2001, 13(5): 279
[30] (林建, 朱國文, 孫成 等. 金屬的微生物腐蝕 [J]. 腐蝕科學與防護技術, 2001, 13(5): 279)
[31] Gu T Y, Zhao K L, Nesic S. A new mechanistic model for mic based on a biocatalytic cathodic sulfate reduction theory [A]. Corrosion 2009 [C]. Atlanta, Georgia, 2009
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 腐蝕與防護網官方QQ群:140808414