摘要
鎂合金是最輕的工程結構材料,其溶解特性、腐蝕機理以及防護措施等方面已被廣泛研究,而鎂合金腐蝕測試方法和技術則是這些研究的重要基礎。由于鎂合金的溶解過程存在負差數效應,導致其測試技術和分析方法與其他金屬存在差異。本文綜述了國內外關于鎂合金腐蝕測試方法與技術的研究進展,介紹了鎂合金測試的通用技術與特色技術,分析了各種測試技術的適用條件和應用案例,重點對比了腐蝕速率測試方法,期望為鎂合金腐蝕測試方法與技術的選擇提供支撐,避免因不當測試帶來的錯誤分析和結論。
關鍵詞: 鎂合金 ; 測試方法 ; 電化學技術
鎂合金被稱為“21世紀新型綠色材料”,可作為結構材料、電極材料、植入材料和犧牲陽極材料[1, 2],應用前景廣闊。由于高化學活性和疏松表面膜,鎂合金極易發生溶解,因此鎂合金設計過程必須考慮其溶解特性,這時鎂合金的腐蝕評價方法和技術成為這些研究的重要基礎。
與碳鋼、不銹鋼相比,鎂合金溶解過程存在負差數效應,即鎂合金陽極極化時實際的溶解速度“異常”地高于Faraday定律計算值,且析氫速率隨著陽極極化電位或電流密度升高而增大的“反常”現象,這將影響鎂合金腐蝕測試和分析方法的選擇[3, 4],例如,在動電位曲線測試時,鎂合金極化曲線的陽極支只代表了流經外電路的電子,而鎂合金表面析氫反應消耗掉的電子卻未被表征。這些特殊情況極易被研究者忽略,因此十分有必要對鎂合金研究方法加以注意和選擇,同時避免測試方法對鎂合金溶解特性評估的準確性和科學性產生影響。
隨著腐蝕測試裝置和微區電化學技術的發展,鎂合金溶解特性被不同儀器或方法表征,但由于鎂合金表面因析氫反應產生的氫氣泡附著極易導致儀器測試產生假信號,因此不能將用于碳鋼等材料測試的方法簡單的移植應用。同時,新的儀器和測試方法也給鎂合金溶解過程帶來了新的發現,這有利于推進鎂合金溶解過程的深入研究。另外,一些簡單的測試儀器和測試方法也被開發出來用于鎂合金腐蝕性能的測試,這將為鎂合金的研究帶來方便。
本文系統歸納總結了目前國內外關于鎂合金腐蝕測試方法和技術的研究進展,詳細分析了新技術新方法在鎂合金腐蝕測試技術中的應用案例及存在問題,期望為鎂合金腐蝕性能研究和測試技術發展提供指導。
1 測試方法分類
鎂合金化學活性較大,常溫常壓下極易與水發生反應,其溶解反應過程如下:
其中,陽極反應(2)實現了電極與溶液界面的電子轉移,Mg原子氧化形成Mg2+,并伴隨著電子釋放;陰極反應(3或4)以析氫反應為主,這是由于純Mg的腐蝕對氧氣并不敏感。
基于鎂合金的溶解反應過程,將其溶解測試技術分為本征測試技術和非本征測試技術。其中,本征測試技術是指檢測鎂合金溶解過程前后物質的變化,包括質量變化、溶液中物質變化、以及所產生的氣體。非本征測試技術是指檢測鎂合金溶解陰陽極過程中涉及電子的轉移,也稱電化學技術。表征金屬整體的電化學性質的技術,稱為宏觀電化學技術;當表征涉及金屬表面若干小的陽極區和陰極區的技術,稱為微區電化學技術。
2 本征測試技術
2.1 失重測試
失重測試是金屬腐蝕速率最簡單、常用的方法,通過測試固定實驗時間內樣品腐蝕測試前后質量變化,可以提供腐蝕表面形貌分析,但只能提供暴露期間的平均腐蝕速率,且這個速率通常會隨著時間而變化[5]。鎂合金腐蝕產物通常采取硝酸銀和鉻酸的混合溶液去除,但是可能因為清洗不足或過度清洗導致的腐蝕速率被低估或高估。失重測試所得高純Mg在濃的NaCl溶液中的本征腐蝕速率為0.3 mm/a[6]。上述方法測試主要用于鎂合金自腐蝕的腐蝕速率。為了測試電化學極化鎂合金的失重腐蝕速率,避免封裝材料和連接線去除等問題的困擾,Shi和Atrens[7]設計了未封裝的Mg電化學試樣。如圖1a所示,首先在立方體Mg樣品的側面鉆取一個內徑為1.70 mm的孔,然后將外徑為1.78 mm部分包裹聚四氟膠帶的裸銅線壓入Mg樣品側面的孔內,制備堅固機械接觸和良好電連接的電化學Mg試樣。聚四氟膠帶可以確保Mg樣品和銅導線之間沒有裂縫,從而電解液無法接觸到銅導線。測試裝置如圖1b所示,測試后Mg樣品可以從銅導線上取下,而不會對Mg帶來任何損失或增重。去除Mg腐蝕產物后,精確測量Mg試樣的質量損失。該方法已經被用于鎂合金負差數效應的理論研究之中,但樣品的8個角和12條棱邊都暴露在溶液中,它們的行為顯然不同于平面,而且底面、側面、頂面的暴露條件也略有不同,這些都會對腐蝕結果造成影響,結果分析時應加以區別。
圖1 極化條件下鎂合金樣品和電化學測試裝置[7]
2.2 析氫測試
析氫現象是鎂合金腐蝕過程的重要特征[8]。根據Mg腐蝕的化學反應(1)可知,溶解1 mol的Mg(24.3 g)就會產生1 mol的氫氣(22.4 L)。因此,析氫測試可作為Mg腐蝕速率評價的特征方法,可用于開路條件和陰陽極極化條件下確定Mg的瞬時腐蝕速率,研究Mg的腐蝕機理。
析氫測試分為體積法和質量法。體積法是用漏斗覆蓋在Mg試樣,并插入倒置的酸性滴定管中,隨后用洗耳球吸取一定體積的腐蝕溶液填入滴定管中。在測試過程中,腐蝕過程產生的氫氣積聚成氣泡逃離Mg表面并置換出滴定管中的溶液,最后通過不同時間滴定管中溶液體積的變化來表示氫氣析出量,進而求得析氫速率[9]。質量法是基于測量浸入式容器中氫氣累積產生的浮力。將Mg試樣懸掛在一個倒置的燒杯下面,燒杯完全浸入到測試溶液中,并通過光纖連接到精密天平上。電極表面產生的氫氣聚積到倒置燒杯內,通過浮力減少其質量。與天平相連的計算機可以自動記錄質量隨時間的變化[10]。
從析氫測試過程來看,該方法存在一些缺點:有些氫氣泡經常附著在漏斗壁和滴定管上;實驗前很少用氫氣預飽和電解液,這些都會導致析氫速率被低估。但是,盡管析氫測試有一些局限性,但是裝置簡單易于監測鎂合金的瞬時腐蝕速率[11],因此成為鎂合金腐蝕評價的常用方法。
2.3 溶液分析
通過腐蝕產物分析鎂合金的腐蝕過程,除了氫氣外還包括了溶液中的離子。根據Mg腐蝕的陽極反應過程(2)可知,隨著Mg溶解的進行,Mg2+量/濃度的變化可用來評價Mg的腐蝕速率。溶液中Mg2+濃度的測試是基于在腐蝕電解池之后連接的電感耦合等離子體發射光譜儀(ICP-OES)來實現[12]。不管是開路條件還是極化條件下,該方法都可以在腐蝕介質存在的情況下直接測量Mg的溶解速率。值得注意的是,由于Mg的腐蝕產物Mg(OH)2的溶解度較低,大部分的Mg2+可能仍儲存在沉淀的腐蝕產物中,因此Mg溶解產生Mg2+的量可能被低估。
另外,根據Mg腐蝕的陰極反應過程(4)可知,隨著水解離反應的進行,不斷釋放OH-導致溶液pH值升高,因此可以根據測量溶液pH值的相對增加量來表征Mg的整體腐蝕速率。化學滴定法可以用來評估Mg溶解的腐蝕速率,通過用適當的溶液滴定,使電解液的pH值在整個實驗過程中保持在一個固定值,維持恒定pH值所需滴定液的體積來評價所消耗的電荷量[13]。值得注意的是,Mg2+的水解可能會影響溶液的pH值,從而測量過程中引入誤差,盡管這對Mg溶解反應的影響相對較小。此外,隨著滴定實驗的進行,實時測量受到滴定所需實驗時間的限制,影響陰極反應動力學的評價。
3 宏觀電化學技術
電化學方法是評估金屬腐蝕的重要而快速的手段,用來表征金屬與溶液界面反應的動力學信息,探討腐蝕機理和耐蝕性能。目前對于鎂合金腐蝕的研究使用較多的電化學技術包括:極化曲線、電化學阻抗、恒電流/電位極化等[14],其中外推Tafel曲線所得腐蝕速率和電化學阻抗譜所得腐蝕速率也是表征鎂合金腐蝕的重要數據。
3.1 極化曲線
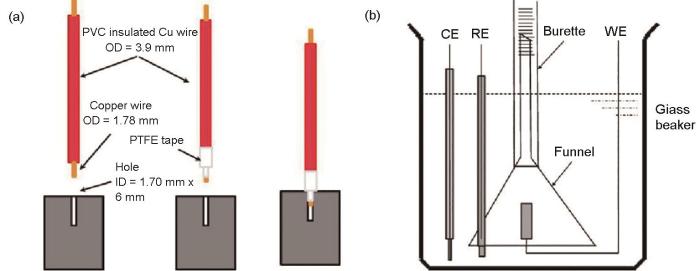
極化曲線是以固定速率在固定間隔內掃描電極的電位,獲得電極電位與極化電流或極化電流密度之間的關系圖譜,表征電極陽極和陰極的動力學信息。假設腐蝕過程是電化學控制的陽極和陰極半反應動力學,就可以從距離腐蝕電位足夠遠的電位,通過Tafel外推相交于腐蝕電流和腐蝕電位。如圖2所示,由于負差數效應的存在,Mg的陽極極化曲線并不表示真實的Mg氧化電流密度,只有將恒電位儀測量的凈陽極電流密度和陽極極化過程中析氫測量計算的電流密度相加才能代表真實的Mg氧化電流密度[15, 16]。陰極極化曲線是恒電位儀在陰極動電位極化過程中得到的電流密度。在測量Mg腐蝕速率的Tafel外推法中,一般采用極化曲線陰極分支的Tafel外推法估算腐蝕電流密度Icorr。這種陰極外推法只有在鎂合金的點蝕電位大于腐蝕電位時才有意義。
圖2 純鎂在飽和Mg(OH)2溶液中的動電位極化曲線[16]
極化曲線測量還可以在腐蝕電位下測定瞬時腐蝕速率[2],但要考慮到若干因素的影響:其一,陰陽極兩個半反應都是由電化學極化控制;其二,在陽極和陰極極化曲線中,劇烈的析氫反應和表面腐蝕產物膜都會產生歐姆電位降IR;其三,腐蝕膜影響鎂金屬暴露區域面積,即使在腐蝕電位附近,反應速率也可能依賴于表面膜的覆蓋度。基于這些原因,使用極化曲線的瞬時腐蝕速率測定時應謹慎使用,建議與其他電化學和非電化學技術聯合評估,如電化學阻抗譜(EIS)和析氫測試。事實上,對鎂合金而言,動態電位極化結果最有用的方面不是腐蝕速率的測定,而是代表陽極和陰極動力學分支的相對變化。這些變化與正確的腐蝕速率測定無關,但對于理解合金化的影響至關重要。
動電位極化提供了重要的動力學信息,是唯一可以揭示導致瞬時腐蝕速率的相對陽極和陰極貢獻的方法。然而,這種方法是短期的和破壞性的。因此,雖然動電位極化在理解腐蝕速率的機理上是不可缺少的,但它不能作為長期腐蝕速率的良好方法。
3.2 電化學阻抗譜
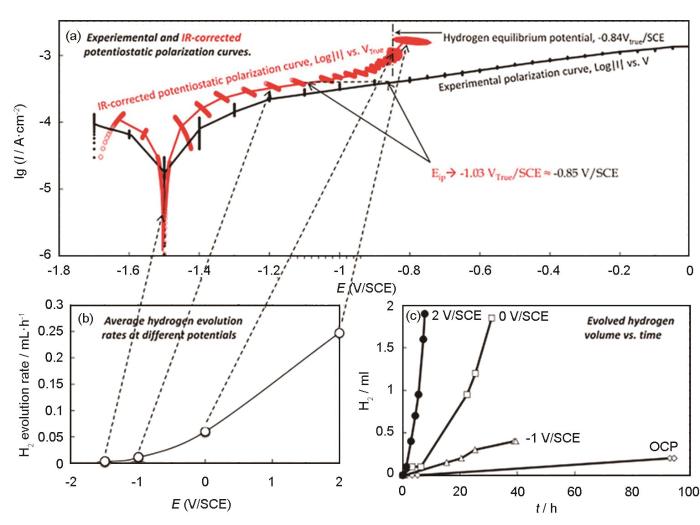
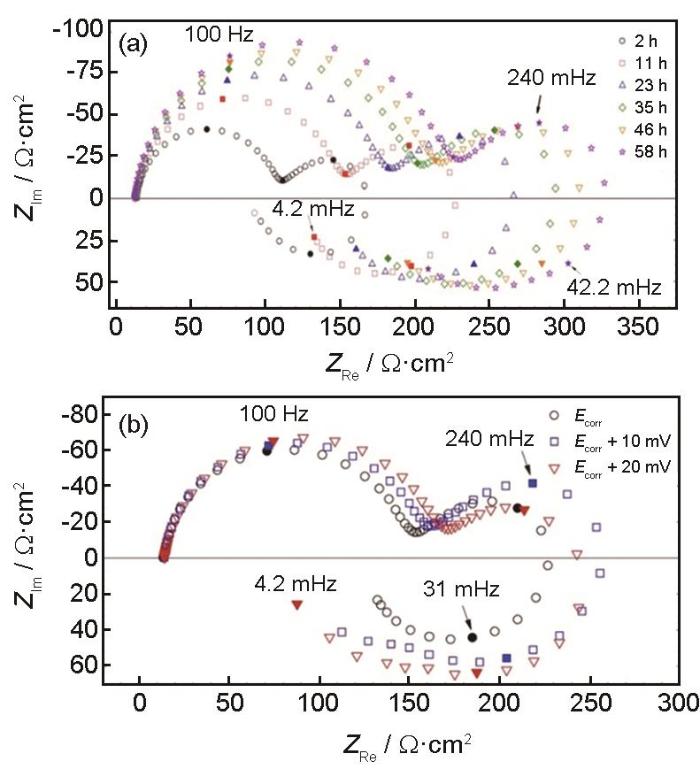
EIS是指在穩定體系中,給電極在不同頻率下施加一個小振幅(通常為5~10 mV)正弦電位擾動產生的響應。可見,EIS作為一種無損監檢測手段,可以長時間監測金屬的腐蝕行為。在實驗室應用中,電化學阻抗譜一般以Nyquist圖和Bode圖呈現,反映腐蝕系統的阻納頻譜特征。在阻抗譜圖分析時,經常采用等效電路圖來分析,即利用電阻、電容和電感等電子元件的串并聯形式。電化學阻抗譜經常被用來分析腐蝕過程中的反應步驟,包括非Faraday步驟和Faraday步驟。如圖3所示,一般Mg的電化學阻抗譜包括兩個容抗弧和一個感抗弧[17~19]。Song等[17]在開路和陰極極化條件下測試了鎂電極在稀NaCl和Na2SO4溶液中的EIS譜。結果分析認為,容抗弧主要由部分保護膜造成的;感抗弧與表面膜破裂處Mg+的濃度有關;陰極極化下,在低頻率范圍內感抗弧的消失可以解釋為鎂表面恢復了完整的表面膜的結果。
圖3 純鎂在0.1 mol/L Na2SO4溶液中不同時間和不同陽極極化條件下的阻抗圖[1]
3.3 恒電流/電位極化
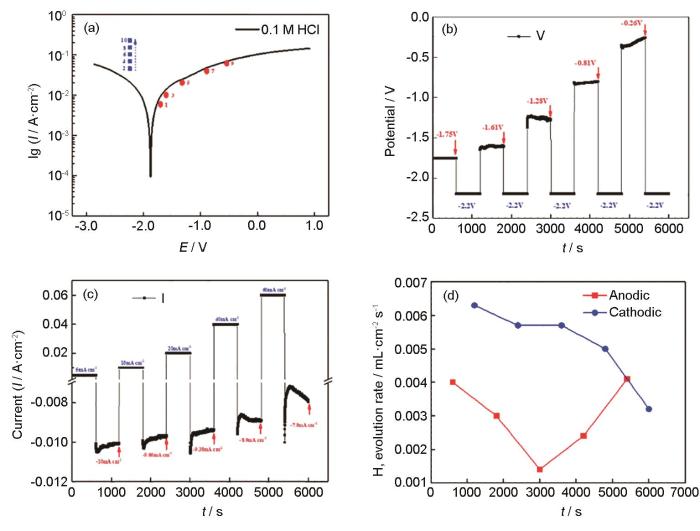
在鎂合金陽極析氫或負差數效應的研究中,恒電流/電位極化結合析氫測試時最常用的方法[15,20,21]。恒電流/電位極化是給樣品施加一個固定的電流密度/電位,測量腐蝕過程的電位/電流變化。當研究特定過程時,須使用恒電位極化測量,包括在鎂表面電沉積不同物種形成保護涂層,以及在陽極極化過程中研究析氫速率,即負差數效應。Birbilis等[20]研究了在0.1 mol/L NaCl溶液中陽極極化后的純Mg立即被陰極極化,表明與沒有陽極極化的純Mg相比,陽極極化后純Mg的陰極電流密度顯著增加,因此得出陽極極化導致產生的表面黑色腐蝕產物具有催化作用,增強了陰極析氫反應。如圖4所示,Huang等[21]研究了在0.1 mol/L的HCl溶液中Mg的交替陰陽極極化析氫行為,可見在恒電流陽極極化過程中測得的陽極析氫速率隨外加陽極電流密度的增大先減小后增大。緊接的恒電位陰極極化過程中測得的陰極析氫速率隨著外加陽極電流密度的增大而減小。上述結果可見,陽極極化后的Mg表面并沒有增強陰極析氫活性,陰極析氫和陰極電流都沒有增加。
圖4 在0.1 mol/L鹽酸溶液中鎂樣品的極化曲線及在恒電流陽極-恒電位陰極交替極化下的電位、電流密度和析氫速率[21]
在Mg的腐蝕過程中,氫氣作為陰極腐蝕產物將會產生并部分附著在Mg的表面,導致實驗過程中Mg的有效活化面積發生改變。在恒電位極化條件下,不管氫氣泡的存在與否,都會使Mg表面的每個點電位恒定不變。但是,在恒電流極化條件下,有無氣泡覆蓋的Mg表面區域的電流密度差別很大。
4 腐蝕速率的比較
Mg的腐蝕速率是Mg腐蝕研究的一項重要指標。目前主要應用的腐蝕速率測試方式分為失重速率、析氫速率、Tafel外推法估算腐蝕速率和阻抗譜計算Mg的腐蝕速率等[6]。上述溶液法較為復雜、影響較多,并沒有廣泛采用。
失重腐蝕速率是通過浸泡期間鎂合金的失重差來換算得到的,其具體計算公式為:
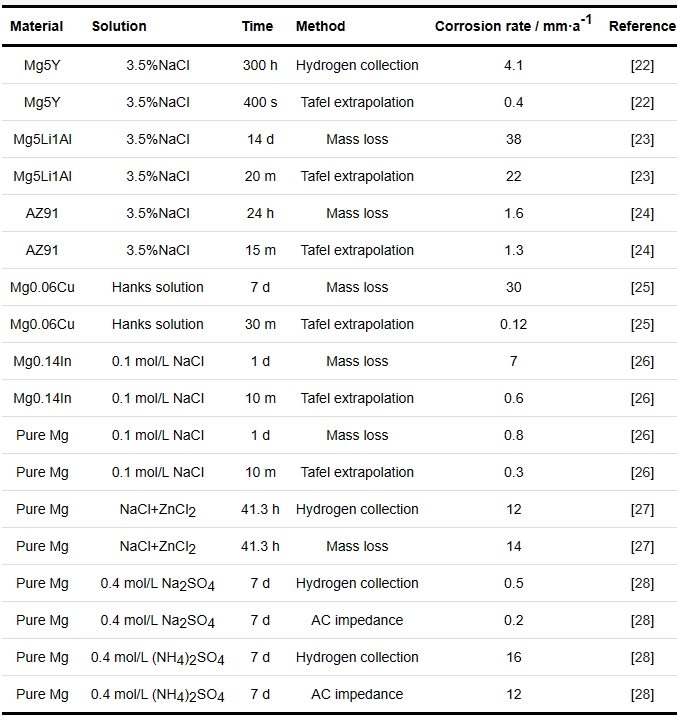
表1綜述了不同研究方法表征的鎂合金腐蝕速率。失重腐蝕速率與析氫腐蝕速率相差不大,而采用電化學方法測量的鎂合金腐蝕速率通常比失重法測量的速率低(通常相差數量級),其中原因包括了浸泡時間、陰極析氫、非Faraday部分。因此,采用電化學方法測量表征鎂合金的腐蝕速率不全面,還應測試失重速率或析氫速率表征鎂合金的腐蝕性能。另外,試樣浸入溶液后測量的腐蝕速率不能代表穩態腐蝕,初始腐蝕機制不能代表穩態腐蝕情況,應該根據腐蝕環境適當延長鎂合金在溶液中的浸泡時間,使鎂合金腐蝕穩定發展。
表1 不同鎂合金腐蝕速率的比較
5 微區電化學技術
在水環境中的自腐蝕或弱陽極極化時,鎂合金表面存在微納米范圍內的局部微電偶腐蝕,分布著陽極區域和陰極區域[29]。宏觀電化學技術可以確定在金屬表面發生的電極過程動力學,所測量電位和電流是整個電極表面的平均值。但是鎂合金與溶液的微區電化學信息無法獲得,恰恰這也是鎂合金腐蝕過程中最重要的研究部分。因此,宏觀電化學方法對于研究局部腐蝕等非均相電化學過程有很大的局限性。Song和Xu[30]利用自制針筒電解池(針尖的內徑為1 mm)研究了不同取向的Mg晶粒具有不同的電化學活性和腐蝕行為,表明基面在中性氯化物溶液或堿性Mg(OH)2飽和溶液中棱柱面和其他晶體面更耐腐蝕。
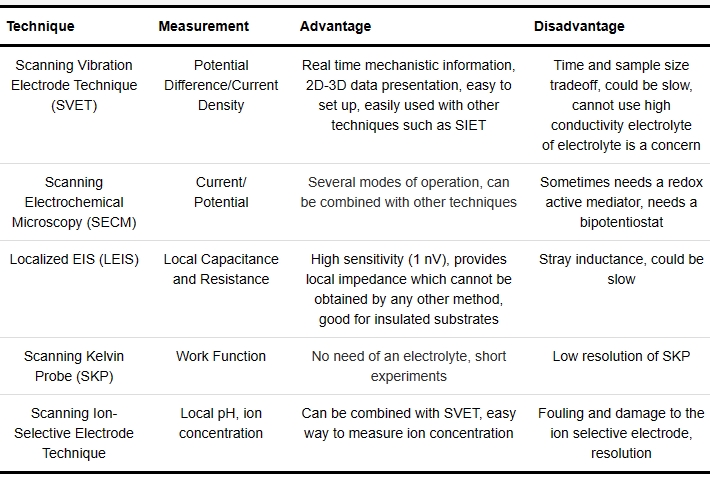
隨著電化學測試技術的發展,微區電化學技術使得在金屬/溶液界面上獲取微空間化學環境信息變得容易。目前,微區電化學技術主要有掃描振動電極技術(SVET)、掃描電化學顯微鏡技術(SECM)、局部電化學阻抗(LEIS)、掃描Kelvins探針(SKP)、掃描離子選擇電極技術(SIET)等[31]。表2為不同微區電化學技術的功能及其優缺點。
表2 微區電化學技術的特性和優缺點[4]
5.1 掃描振動電極技術
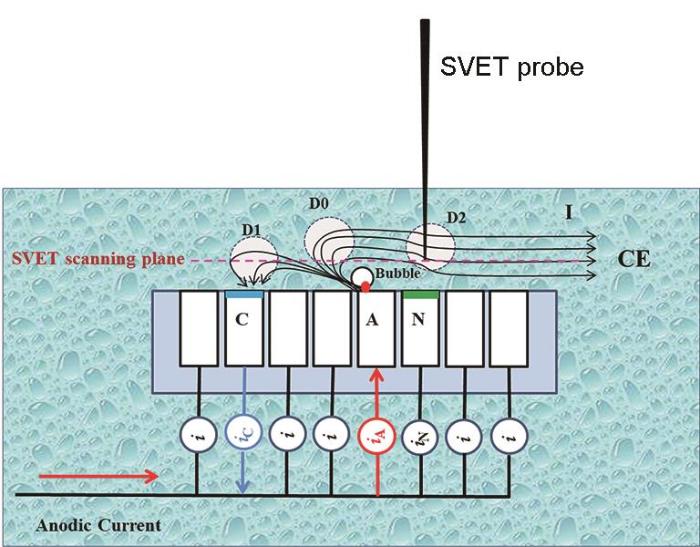
SVET是測量溶液中振動探針與腐蝕金屬之間的電位差,可視化展示金屬表面局部陰極和陽極反應的一種原位的電化學技術[32]。該技術在鎂合金微區電化學研究領域的應用最多,廣泛應用于鎂合金自腐蝕、負差數效應和電偶腐蝕的研究中。但是SVET用于腐蝕機理的測試還值得商榷。Williams等[33]研究表明在2 mol/L的NaCl溶液中SVET測試純Mg時Mg表面陰極區面積隨著極化時間(0~2 h)和外加陽極電流密度的增加而增加,而Huang等[29]通過SVET測試了鎂絲陣列電極研究表明純Mg隨著陽極電流增大,陰極電流逐漸減小直到消失。上述研究表明SVET技術的缺點,通常在電導率較高的溶液中變得不那么靈敏。只有那些高于儀器噪聲的信號才能被檢測并轉換為電流密度。此外,SVET在距離真實Mg表面一定距離處測量的電流密度或電勢分布可能在附著在Mg表面的氫氣泡處發生扭曲(如圖5所示)。
圖5 氣泡干擾SVET測試示意圖[29]
SVET在鎂合金電偶腐蝕研究中具有顯著的優勢,已經在Mg2Si與Al電偶、Mg-Mg2Ca電偶和Mg-MgZn2電偶得到應用[34,35]。Li等[34]利用SVET研究了金屬間化合物Mg2Si與Al電偶在不同pH值的0.01 mol/L NaCl溶液中的電偶腐蝕。研究表明,Mg2Si在酸性條件下作為陽極,隨著浸泡時間的延長,Mg2Si的陽極活性隨著金屬Al腐蝕的發生而降低。可見,SVET在鎂合金的電偶腐蝕研究中有明顯優勢,可以直觀表征出電偶之間的電流和電位之間的差別,且可以表征出各自之間電流和電位隨時間的變化。另外,由于Mg腐蝕總有氣泡的產生,對探針尖端的影響較大,因此該方法的適用條件上有所限制。
5.2 掃描電化學顯微鏡
SECM是一種利用超微探針電極表征浸泡在電解液中金屬表面非均勻電化學反應,建立表面形貌和表面反應活性之間的關系的掃描探針技術[36]。通常情況下,SECM需要在電解質溶液中加入氧化還原活性介質,檢測探針尖端活性物質電化學反應速率的空間變化。常見于檢測鎂合金表面膜的作用和變化來表征局部腐蝕,Liu等[37]在利用SECM監測了浸泡在NaCl溶液中的AM60和AMCe1鎂合金的電化學過程時研究表明,鎂合金的電化學行為受Cl-濃度和表面膜的影響,Cl-濃度增強了鎂合金局部腐蝕,導致活性點的快速產生和生長,促進表面膜的破裂和水化。另外,SECM技術可以通過極化超微電極,以固定電位來區分不同電化學活性物質,測量感興趣物種的氧化或還原所產生的電流,測量反應動力學和檢測某些特定物質。Zhang等[38]利用掃描電化學顯微鏡采用改進的SG/TC模式,通過生成的Mg+與鐵氰化鉀(K3[Fe(CN)6])反應來檢測Mg+的存在。表明Mg在+0.6 V陽極氧化120 s后,[Fe(CN)6]4-在超微碳纖維電極上的氧化電流明顯增加,證實了Mg+的存在。
5.3 微區電化學阻抗譜
LEIS利用微型探針在電解液中提供材料局部阻抗譜的技術,當探針靠近金屬表面,測量得到溶液中的局部電位差,進而求得局部電流密度。LEIS已經用于鎂合金局部腐蝕動力學的研究。Galicia等[39]通過LEIS和EIS研究了Na2SO4溶液中AZ91鎂合金的腐蝕行為。研究表明β相和α相的腐蝕機制都是由鎂的溶解控制,同時分析了導致測定β相的溶出慢于α相的局部動力學的信息。另外,LEIS適合于絕緣襯底(金屬涂層)的腐蝕測試研究,Calado等[40]采用LEIS測定了在0.005 mol/L的NaCl溶液中涂有自愈合涂層的鎂合金AZ31表面人工缺陷處的的導納情況,研究表面自愈合涂層的存在抑制了缺陷處導納的增加,具有抑制腐蝕的作用。目前來說,該技術不需要在溶液中添加任何氧化還原介質,避免其影響,但是測量速度慢、易出現雜散電感。
5.4 掃描Kelvin探針
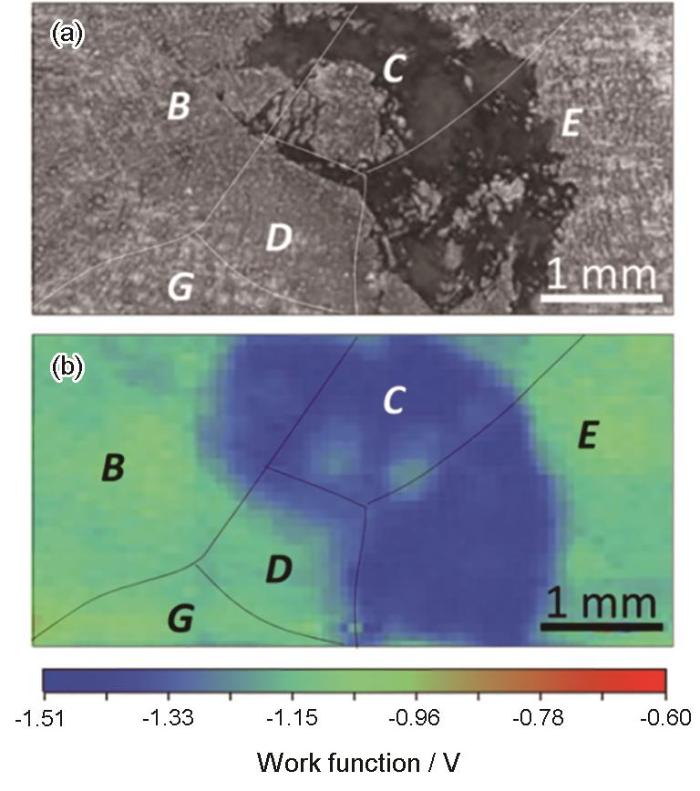
SKP是基于振動電容測試功函數的一種非破壞性、非接觸的技術,可以提供金屬表面的局部信息。SKP測量可以在真空、露天、潮濕的空氣中進行,也可以在表面滴一滴電解液。為了克服分辨率低的問題,開發了掃描Kelvin探針顯微鏡(SKPFM),其空間分辨率可達約0.1 μm,然而SKPFM測量更容易受到針尖與表面距離、表面形貌和針尖表面污垢/氧化所產生的人為因素的影響。如圖6所示,Song和Xu[30]利用SKP技術表征了在0.01 mol/L NaCl溶液中浸泡0.5 h后鎂表面腐蝕的位置,但該位置與實際光學圖片拍攝的發生腐蝕的并不完全一樣,認為表面薄膜的存在降低了SKP測量檢測襯底Mg伏特電位差的靈敏度。另外,該技術還用于測試異種金屬間的電偶腐蝕情況,Wu等[41]采用SKPFM測試了磁控檢測的純Mg和中間相Mg-28Al之間的電位差,結果顯示磁控濺射純鎂表面電勢的平均值與Mg-28Al表面電勢的平均值之間相差242 mV。
圖6 腐蝕后的鎂表面光學圖和SKP圖[32]
5.5 掃描離子選擇電極技術
SIET以非侵入性方式實時測量pH值和/或表面電解質特定離子物種的存在,可以用來研究化學和電化學反應機制,量化腐蝕過程動力學和擴散速率。該技術可以用于檢測pH值的變化或電極尖端的離子檢測。例如,可以根據Cl-分布法提供陰極區和陽極區,因為鎂合金腐蝕的陽極區的氯離子濃度總是高于陰極區。Mei等[42]利用SIET技術研究了有無pH緩沖液的模擬體液環境中鎂腐蝕行為。表明無pH緩沖液的體系中,由于表面膜的生成,Mg表面局部pH值相對較低;而含有pH緩沖液的體系中,Mg的腐蝕速率更快,導致pH值相對較高,且由于氫氣的產生使得pH測量出現了出現波動。Lamaka等[43]通過SIET技術成功應用在含氯化物水溶液中鎂合金表面的Mg2+和H+的局部活性掃描,測量了人工缺陷下腐蝕溶解的Mg2+的局部濃度和pH值變化。
6 結語與展望
耐蝕鎂合金和可溶鎂合金的陽極溶解測試、腐蝕機理探究、防護措施評價需要依托鎂合金的測試技術的發展與創新。不同的測試分析方法相互支撐,更好的理解鎂合金腐蝕與防護的本質,同時針對鎂合金溶解特性,需要合理選擇不同測試環境和測試技術,有助于提供真實準確的實驗數據,為鎂合金腐蝕科學研究提供技術保障。
(1) 鎂合金腐蝕速率的測量包括了失重法、析氫法、溶液法、極化曲線法以及阻抗法。失重法測量鎂合金腐蝕速率比電化學方法測量的腐蝕速率高,且相差幾個數量級。實際測試中失重法較為客觀,而不應僅依賴電化學方法測量的腐蝕速率。
(2) 與碳鋼、不銹鋼等金屬材料不同,由于負差數效應的存在,鎂合金腐蝕的測試技術與分析方法需要加以甄別,例如電化學測試與失重方法的結合使用,析氫測試、溶液測試等特殊測試技術;微區電化學技術中氣泡的影響;極化曲線陽極支和阻抗圖譜中動力學分析方法的注意事項等等。
(3) 微區電化學技術提供了局部尺度的電化學信息,更好地明晰鎂合金腐蝕機理,但是每種技術都具有各自優缺點,適用于不同測試環境。未來隨著測試技術的發展和改進,使得多種測試數據集中測試,實時準確同步反映腐蝕信息。同時,也應進一步發展腐蝕測試標準化工作,使得大家測試數據具有可比性,避免系統性誤差。
參考文獻
1 Huang J F, Song G L, Atrens A, et al. What activates the Mg surface-A comparison of Mg dissolution mechanisms [J]. J. Mater. Sci. Technol., 2020, 57: 204
doi: 10.1016/j.jmst.2020.03.060
2 Esmaily M, Svensson J E, Fajardo S, et al. Fundamentals and advances in magnesium alloy corrosion [J]. Prog. Mater. Sci., 2017, 89: 92
doi: 10.1016/j.pmatsci.2017.04.011
3 King A D, Birbilis N, Scully J R. Accurate electrochemical measurement of magnesium corrosion rates; A combined impedance, mass-loss and hydrogen collection study [J]. Electrochim. Acta, 2014, 121: 394
doi: 10.1016/j.electacta.2013.12.124
4 Jadhav N, Gelling V J. Review-The use of localized electrochemical techniques for corrosion studies [J]. J. Electrochem. Soc., 2019, 166: C3461
doi: 10.1149/2.0541911jes
5 Wang Z Q, Xu C X, Yang L J, et al. Microstructure and corrosion resistance of medical degradable Mg-2Y-1Zn-x Zr alloy [J]. J. Chin. Soc. Corros. Prot., 2022, 42: 113
5 王中琪, 許春香, 楊麗景 等. 醫用可降解Mg-2Y-1Zn-x Zr合金微觀組織和耐蝕性能研究[J]. 中國腐蝕與防護學報, 2022, 42: 113
doi: 10.11902/1005.4537.2021.014
6 Atrens A, Shi Z M, Mehreen S U, et al. Review of Mg alloy corrosion rates [J]. J. Magnes. Alloy., 2020, 8: 989
doi: 10.1016/j.jma.2020.08.002
7 Shi Z M, Atrens A. An innovative specimen configuration for the study of Mg corrosion [J]. Corros. Sci., 2011, 53: 226
doi: 10.1016/j.corsci.2010.09.016
8 Huang J F, Song G L. Hydrogen evolution, efficiency and exacerbated galvanic corrosion damage of magnesium alloy anode [J]. J. Mater. Eng., 2021, 49(12): 48
8 黃居峰, 宋光鈴. 鎂合金陽極的析氫、效率與電偶腐蝕放大效應 [J]. 材料工程, 2021, 49(12): 48
doi: 10.11868/j.issn.1001-4381.2021.000287
9 Song G L, Atrens A, StJohn D. An hydrogen evolution method for the estimation of the corrosion rate of magnesium alloys [A]. Hryn J N. Magnesium Technology [M]. Warrendale: TMS, 2001: 255
10 Fajardo S, Frankel G S. Gravimetric method for hydrogen evolution measurements on dissolving magnesium [J]. J. Electrochem. Soc., 2015, 162: C693
doi: 10.1149/2.0241514jes
11 Lü X, Deng K K, Wang C J, et al. Effect of SiCp size on microstructure and corrosion properties of cast AZ91 Mg-alloys [J]. J. Chin. Soc. Corros. Prot., 2023, 43: 135
11 呂 鑫, 鄧坤坤, 王翠菊 等. SiCp尺寸對鑄態AZ91鎂合金顯微組織與腐蝕性能的影響 [J]. 中國腐蝕與防護學報, 2023, 43: 135
12 wiatowska J, Volovitch P, Ogle K. The anodic dissolution of Mg in NaCl and Na2SO4 electrolytes by atomic emission spectroelectrochemistry [J]. Corros. Sci., 2010, 52: 2372
doi: 10.1016/j.corsci.2010.02.038
13 Rybalka K V. Determination of metal corrosion rate using the pH-metry by the method of compensating additives [J]. Russ. J. Electrochem., 2014, 50: 500
doi: 10.1134/S1023193514050085
14 Liu Z Q, He X X, Qi K, et al. Galvanic corrosion behavior for galvanic couple of AZ91D Mg-alloy/2002 Al-alloy in 0.5 mg/L NaCl solution [J]. J. Chin. Soc. Corros. Prot., 2022, 42: 1016
14 劉澤琪, 何瀟瀟, 祁 康 等. AZ91D鎂合金和2002鋁合金在0.5 mg/L NaCl溶液中的電偶腐蝕行為研究 [J]. 中國腐蝕與防護學報, 2022, 42: 1016
doi: 10.11902/1005.4537.2021.355
15 Fajardo S, Frankel G S. A kinetic model explaining the enhanced rates of hydrogen evolution on anodically polarized magnesium in aqueous environments [J]. Electrochem. Commun., 2017, 84: 36
doi: 10.1016/j.elecom.2017.10.001
16 Song G L, Unocic K A. The anodic surface film and hydrogen evolution on Mg [J]. Corros. Sci., 2015, 98: 758
doi: 10.1016/j.corsci.2015.05.047
17 Song G, Atrens A, St John D, et al. The anodic dissolution of magnesium in chloride and sulphate solutions [J]. Corros. Sci., 1997, 39: 1981
doi: 10.1016/S0010-938X(97)00090-5
18 Baril G, Galicia G, Deslouis C, et al. An impedance investigation of the mechanism of pure magnesium corrosion in sodium sulfate solutions [J]. J. Electrochem. Soc., 2007, 154: C108
doi: 10.1149/1.2401056
19 Gomes M P, Costa I, Pébère N, et al. On the corrosion mechanism of Mg investigated by electrochemical impedance spectroscopy [J]. Electrochim. Acta, 2019, 306: 61
doi: 10.1016/j.electacta.2019.03.080
20 Birbilis N, King A D, Thomas S, et al. Evidence for enhanced catalytic activity of magnesium arising from anodic dissolution [J]. Electrochim. Acta, 2014, 132: 277
doi: 10.1016/j.electacta.2014.03.133
21 Huang J F, Song G L, Zhu Y X, et al. The anodically polarized Mg surface products and accelerated hydrogen evolution [J]. J. Magnes. Alloy., 2023, 11: 230
doi: 10.1016/j.jma.2021.05.008
22 Liu X B, Shan D Y, Song Y W, et al. Influence of yttrium element on the corrosion behaviors of Mg-Y binary magnesium alloy [J]. J. Magnes. Alloy., 2017, 5: 26
doi: 10.1016/j.jma.2016.12.002
23 Xiang Q, Jiang B, Zhang Y X, et al. Effect of rolling-induced microstructure on corrosion behaviour of an as-extruded Mg-5Li-1Al alloy sheet [J]. Corros. Sci., 2017, 119(5): 14
doi: 10.1016/j.corsci.2017.02.009
24 Turan M E, Sun Y, Aydin F, et al. Effects of carbonaceous reinforcements on microstructure and corrosion properties of magnesium matrix composites [J]. Mater. Chem. Phys., 2018, 218: 182
doi: 10.1016/j.matchemphys.2018.07.050
25 Yan X D, Zhao M C, Yang Y, et al. Improvement of biodegradable and antibacterial properties by solution treatment and micro-arc oxidation (MAO) of a magnesium alloy with a trace of copper [J]. Corros. Sci., 2019, 156: 125
doi: 10.1016/j.corsci.2019.05.015
26 Gore P, Cain T W, Laird J, et al. Enrichment efficiency of noble alloying elements on magnesium and effect on hydrogen evolution [J]. Corros. Sci., 2019, 151: 206
doi: 10.1016/j.corsci.2019.02.026
27 Huang J F, Song G L, Wang Z M, et al. ZnThe2+ destabilized surface film and accelerated corrosion of magnesium [J]. J. Electrochem. Soc., 2020, 167: 161508
doi: 10.1149/1945-7111/abd002
28 Cao F Y, Zhao C, Song G L, et al. The corrosion of pure Mg accelerated by haze pollutant ammonium sulphate [J]. Corros. Sci., 2019, 150: 161
doi: 10.1016/j.corsci.2019.01.042
29 Huang J F, Song G L, Wang Z M, et al. The real current density distribution on Mg surface [J]. J. Electrochem. Soc., 2021, 168: 077505
30 Song G L, Xu Z Q. Crystal orientation and electrochemical corrosion of polycrystalline Mg [J]. Corros. Sci., 2012, 63: 100
doi: 10.1016/j.corsci.2012.05.019
31 Zhang P H, Pang K, Ding K K, et al. Research progress of scanning vibrating electrode technique in field of corrosion [J]. J. Chin. Soc. Corros. Prot., 2017, 37: 315
31 張彭輝, 逄 昆, 丁康康 等. 掃描振動電極技術在腐蝕領域的應用進展 [J]. 中國腐蝕與防護學報, 2017, 37: 315
doi: 10.11902/1005.4537.2016.115
32 Bastos A C, Quevedo M C, Karavai O V, et al. Review—on the application of the scanning vibrating electrode technique (SVET) to corrosion research [J]. J. Electrochem. Soc., 2017, 164: C973
doi: 10.1149/2.0431714jes
33 Williams G, Birbilis N, McMurray H N. The source of hydrogen evolved from a magnesium anode [J]. Electrochem. Commun., 2013, 36: 1
doi: 10.1016/j.elecom.2013.08.023
34 Li L L, Zhang B, Tian B, et al. SVET study of galvanic corrosion of Al/Mg2Si couple in aqueous solutions at different pH [J]. J. Electrochem. Soc., 2017, 164: C240
doi: 10.1149/2.0671706jes
35 Liu Y, Liu X, Zhang Z C, et al. Comparative, real-time in situ monitoring of galvanic corrosion in Mg-Mg2Ca and Mg-MgZn2 couples in Hank’s solution [J]. Corros. Sci., 2019, 161: 108185
doi: 10.1016/j.corsci.2019.108185
36 Hampel M, Schenderlein M, Schary C, et al. Efficient detection of localized corrosion processes on stainless steel by means of scanning electrochemical microscopy (SECM) using a multi-electrode approach [J]. Electrochem. Commun., 2019, 101: 52
doi: 10.1016/j.elecom.2019.02.019
37 Liu W J, Cao F H, Xia Y, et al. Localized corrosion of magnesium alloys in NaCl solutions explored by scanning electrochemical microscopy in feedback mode [J]. Electrochim. Acta, 2014, 132: 377
doi: 10.1016/j.electacta.2014.04.044
38 Zhang Q H, Liu P, Zhu Z J, et al. Electrochemical detection of univalent Mg cation: A possible explanation for the negative difference effect during Mg anodic dissolution [J]. J. Electroanal. Chem., 2021, 880: 114837
doi: 10.1016/j.jelechem.2020.114837
39 Galicia G, Pébère N, Tribollet B, et al. Local and global electrochemical impedances applied to the corrosion behaviour of an AZ91 magnesium alloy [J]. Corros. Sci., 2009, 51: 1789
doi: 10.1016/j.corsci.2009.05.005
40 Calado L M, Taryba M G, Carmezim M J, et al. Self-healing ceria-modified coating for corrosion protection of AZ31 magnesium alloy [J]. Corros. Sci., 2018, 142: 12
doi: 10.1016/j.corsci.2018.06.013
41 Wu P P, Song G L, Zhu Y X, et al. The corrosion of Al-supersaturated Mg matrix and the galvanic effect of secondary phase nanoparticles [J]. Corros. Sci., 2021, 184: 109410
doi: 10.1016/j.corsci.2021.109410
42 Mei D, Lamaka S V, Feiler C, et al. The effect of small-molecule bio-relevant organic components at low concentration on the corrosion of commercially pure Mg and Mg-0.8Ca alloy: An overall perspective [J]. Corros. Sci., 2019, 153: 258
doi: 10.1016/j.corsci.2019.03.039
43 Lamaka S V, Karavai O V, Bastos A C, et al. Monitoring local spatial distribution of Mg2+, pH and ionic currents [J]. Electrochem. Commun., 2008, 10: 259
doi: 10.1016/j.elecom.2007.12.003
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606
- 郵箱:fsfhzy666@163.com
- 腐蝕與防護網官方QQ群:140808414