鹽酸左氧氟沙星(LEV)作為氟喹諾酮類(FQS)藥物中應用最廣的一類抗生素,由于其在動物體內的代謝效率較低,很容易隨著代謝物進入水環境中,因此對生態環境以及人類健康生活產生了極大威脅。目前,人們已經采取了多種方法從水體中去除LEV[1-6]。在眾多的處理方法中,吸附法因其具有操作簡單,處理成本低,綠色環保等優勢,被認為是一種極具潛力的抗生素處理方法[7]。而今已有多種吸附材料被開發并用于LEV的去除[8-10]。然而,這些吸附材料往往存在制備成本高、降解程度低、易造成二次污染、不易回收等問題,限制了其廣泛應用[11-14]。因此,需要開發合適的吸附材料來去除水體中的LEV。
生物質氣凝膠是一種三維多孔固體網狀輕質材料,具有低密度、大比表面積、高孔隙率、簡單易得、易降解、無污染等優點[15]。目前已經作為吸附材料,被用于水體中抗生素污染物的處理。例如,Li等[16]設計并制備了一種由木質素(LN)、蒙脫土(MMT)和纖維素組成的生物質復合氣凝膠LN/MMT @cellulose,能夠有效吸附水中的環丙沙星、四環素和甲氧芐啶污染物。
明膠(Gel)是一類非常重要的天然生物高分子材料,自身無毒并且其分子結構中含有大量的—OH,—NH2,—COOH等官能團[17],這使得明膠易于凝膠化和功能化,因此,Gel很適合用來制備生物質氣凝膠[18]。然而,Gel的穩定性低、機械阻力小,常常需要加入骨架增強材料,幫助其成型。氧化石墨烯(GO)是一種具有高比表面積和豐富含氧官能團的二維碳材料[19],能夠對氣凝膠內部交聯結構起到支撐作用。如Kovtun等[20]分別選用嵌入和包覆的方法,制備了兩種類型的氧化石墨烯-殼聚糖-明膠復合氣凝膠,結果顯示,兩種復合氣凝膠對氧氟沙星和環丙沙星都表現出了較好吸附性能。然而,GO由于自身的高內聚力,使得其在溶液中分散性較差,阻礙了GO的潛在應用。因此,需要通過對GO進行化學改性以改善其性能[21]。
十二烷基二甲基芐基氯化銨(BKC)是應用最為廣泛的季銨鹽類陽離子表面活性劑之一[22-23],其結構中包含了完整的苯環結構以及親水性的氯化銨結構,能夠通過π-π相互作用以及靜電相互作用組裝在GO表面,對其進行非共價改性[24],促進GO片層進一步分離,并改善其分散性。聚多巴胺(PDA)是一種環保型生物高分子聚合物[25],在堿性條件下能夠在底物上形成黏附膜,幫助被包覆的底物更好地與骨架材料結合,有利于底物成為后續功能化材料的良好中間體。
基于此,本工作利用BKC對GO進行改性,選擇PDA進行包覆,并進一步與Gel進行復合,采用溶膠-凝膠法結合冷凍干燥技術制備了明膠/改性氧化石墨烯/聚多巴胺復合氣凝膠(GGB),探究了復合氣凝膠對LEV的吸附行為,并分析了吸附機理,為改性GO復合氣凝膠吸附抗生素提供借鑒。
1 實驗材料與方法
1.1 實驗材料
氧化石墨烯(GO)購自蘇州碳豐科技有限公司,明膠(Gel)購自上海阿拉丁生化科技股份有限公司,鹽酸多巴胺(DA)和十二烷基二甲基芐基氯化銨(BKC)購自潤有化學有限公司,鹽酸左氧氟沙星(LEV)購自天津大茂化學試劑廠,鹽酸(HCl,37%)購自常州武衛試劑廠,氫氧化鈉(NaOH)購自天津北聯精細化學品開發有限公司。實驗過程中所用到的水均為去離子水。
1.2 實驗方法
1.2.1 BKC改性GO的制備
對GO進行改性[26],具體改性方法如下:將0.04 g GO置于30 mL去離子水中超聲分散30 min得到GO分散液;再稱取0.08 g BKC置于30 mL去離子水中,在室溫條件下攪拌30 min,令其完全溶解;將GO分散液與BKC溶液混合,在25 ℃下攪拌2 h后抽濾,去離子水洗滌數次,在60 ℃的烘箱中烘干,得到BKC改性的GO粉末,記作GB。
1.2.2 明膠/改性氧化石墨烯/聚多巴胺復合氣凝膠(GGB)的制備
首先稱取上述制備的GB粉末0.04 g并置于10 mL去離子水中,再稱取0.5 g DA,并在DA粉末中加入10 mL pH值為8.5的NaOH溶液,攪拌至完全溶解。之后,將上述GB溶液與DA溶液混合,待反應完全后離心分離,得到PDA包覆GB的復合材料GBP。將GBP再分散到10 mL去離子水中,隨后將GBP與Gel溶液進行混合,在40 ℃下繼續攪拌1 h。最后,裝入孔板中靜置老化,在冰箱預凍24 h,再由冷凍干燥機(FD-1A-50)連續冷凍干燥12 h后,得到Gel/GB/PDA復合氣凝膠,并命名為GGB,其外觀如圖1所示,整個GGB制備流程如圖2所示。為進行相應的對比,參照上述實驗步驟,以未改性GO為原料,制備出Gel/GO/PDA復合氣凝膠,命名為GGO。
準確配制體積為50 mL、濃度為150 mg/L的LEV溶液,用0.1 mol/L HCl和0.1 mol/L NaOH調節LEV溶液的pH值,然后向調節好pH值的LEV溶液中加入復合氣凝膠GGB,并將其置于數顯全溫振蕩器(HZQ-1)中,25 ℃振蕩吸附,待吸附平衡后,移取少量LEV溶液,利用紫外可見分光光度計在294 nm處測得LEV溶液的吸光度,并通過標準曲線法計算吸附平衡后LEV溶液的濃度,進而計算復合氣凝膠GGB對LEV的吸附量和去除率。
吸附量計算公式:
2 結果與分析
2.1 復合氣凝膠的形貌和結構表征
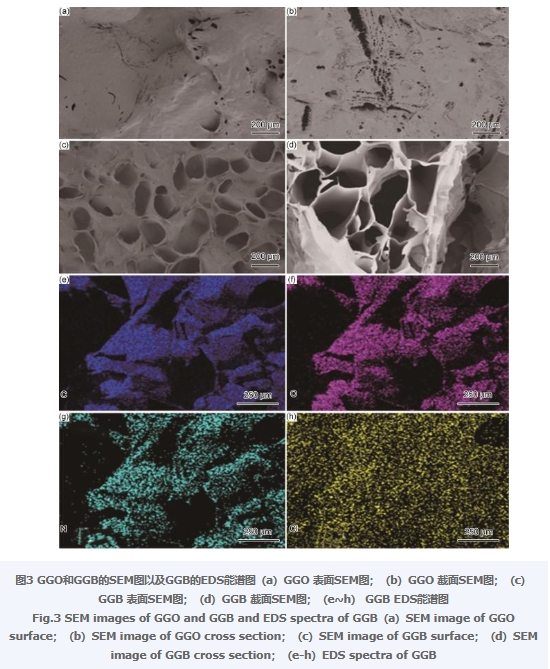
利用SEM(Gemini500)對制備出的兩種復合氣凝膠進行形貌表征,圖3為GGO,GGB的掃描電鏡圖以及GGB的EDS能譜圖。圖3(a),(b)分別為GGO的表面和截面圖,從圖3(a)中可以看到,GGO表面較為光滑,存在一些褶皺和少量細小的孔洞,整體呈現出了致密的結構,而從圖3(b)中也可以看出,GGO內部的結構和表面類似,同樣呈現出致密緊實的結構,并且GGO內部孔洞數量更為豐富,同時出現一些溝壑。圖3(c),(d)分別為GGB的表面和截面圖,從圖3(c)中可以看出,GGB的表面存在大量孔洞,呈蜂窩狀不規則排布,孔壁之間相互交聯錯落有致,孔道明顯。與GGO表面孔洞相比,GGB表面孔洞的孔徑明顯增大。這表明改性后的GO片層被進一步剝離,增大了其片層間距,并改善了GO分散性,避免了團聚的發生,使其能夠更好地作用于Gel網絡結構中進行支撐。從圖3(d)中同樣可以看出,GGB內部孔道豐富,材料整體呈現三維網狀多孔結構。從圖3(e)~(h)GGB的EDS能譜圖中可以看到,C,O,N,Cl元素在復合氣凝膠上均勻分布,說明GO被BKC成功改性,同時也表明復合氣凝膠GGB制備成功。
2.2 化學結構分析
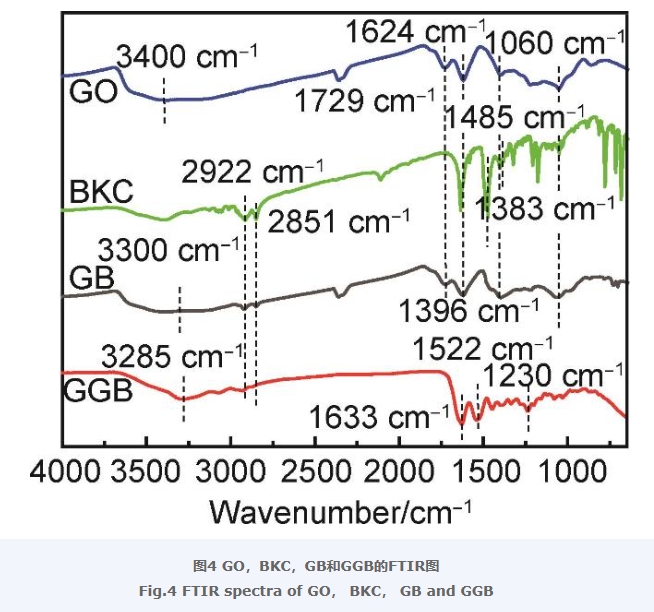
圖4為GO,BKC,GB以及GGB的傅里葉變換紅外光譜(FTIR,IR-21)。從圖中可以看出,GO在3400 cm-1處有一個明顯寬峰,屬于—OH的伸縮振動,除此之外,在1729,1624,1396,1060 cm-1的特征吸收峰分別屬于C=O,C=C,C—OH和C—O—C的伸縮振動,它們歸屬于GO中的各種含氧基團的特征吸收[27-28]。BKC在2922,2851 cm-1的特征吸收峰屬于典型的—CH3,—CH2—的伸縮振動,1485,1383 cm-1處的特征吸收峰歸屬于C—N鍵的伸縮振動[29-30]。在GB的紅外光譜中,—OH的伸縮振動出現在了3300 cm-1,吸收峰向低波數方向發生移動,這表明GO與BKC之間存在著氫鍵相互作用,這種作用使得電子云密度發生平均化,從而影響伸縮振動的頻率。此外,在2922,2851 cm-1處同樣出現了—CH3,—CH2—的伸縮振動,并且GO中的各含氧基團的特征吸收峰也能夠在GB的紅外光譜中找到相應歸屬,證明GO已經成功被BKC改性。GGB的紅外圖譜在3285 cm-1明顯可以看出N—H伸縮振動,2922,2851 cm-1出現了明顯的—CH3,—CH2—伸縮振動,1633,1522 cm-1處的吸收峰屬于C=O和C=C的伸縮振動,1230 cm-1處的特征吸收峰歸因于N—H的彎曲振動[31],上述特征峰的出現,證實了復合氣凝膠GGB制備成功。
2.3 復合氣凝膠的元素組成分析
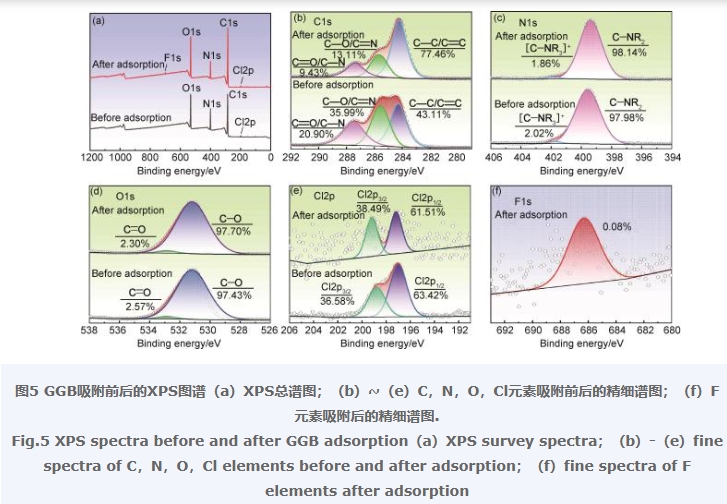
圖5是GGB吸附LEV前后的XPS(Thermo Scientific K-Alpha)全譜圖以及C,O,N,Cl,F各元素的高分辨率XPS光譜圖。從圖5(a)和圖5(f)中可以看出GGB吸附LEV后的XPS全譜圖上新出現了F1s的特征峰,且圖5(f)中F元素的出現證實了LEV已經被GGB成功吸附[32]。圖5(b)C1s XPS 譜圖中包含了C—C/C=C,C—O/C—N,C=O/C=N鍵,C—C/C=C的相對含量由GGB吸附LEV前的43.11%增加到吸附LEV后的77.46%,表明GGB與LEV之間存在著明顯的π-π相互作用。而C—O/C—N的相對含量也有由吸附LEV前的35.99%降低到吸附LEV后的13.11%,這可能是由于GGB與LEV之間發生的氫鍵相互作用。此外,從圖5(c)N1s可以看到,GGB吸附LEV后—N—的相對含量略有增加,也證明LEV的成功吸附,同時—N+的相對含量從吸附LEV前的2.02%降低到了吸附LEV后的1.86%,說明GGB與LEV之間存在著弱的靜電相互作用,類似的結論從圖5(d)O1s也可以得到。吸附前后Cl2p的變化如圖5(e)所示,結合能的變化表明了氯原子與羧基之間存在靜電相互作用。以上分析表明LEV主要通過π-π相互作用、氫鍵相互作用和靜電相互作用與GGB發生吸附。
2.4 接觸時間對吸附性能的影響
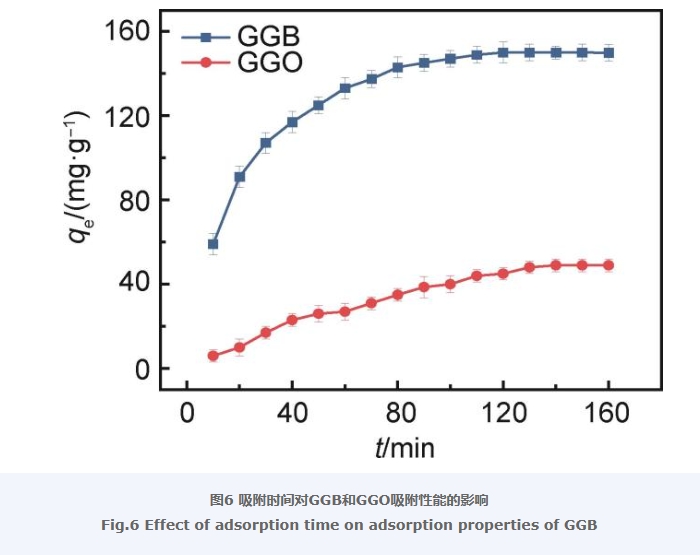
圖6為GGB和GGO在298 K下對抗生素LEV的吸附量與吸附時間的關系。從圖6中可以看出,GGB和GGO對于LEV的吸附平衡時間相差不大,都在120 min左右,但GGB對LEV的平衡吸附量明顯優于GGO,GGO對LEV的平衡吸附量只有49 mg/g,而GGB對LEV的平衡吸附量達到了150 mg/g,是GGO對LEV平衡吸附量的3倍有余。上述結果表明,經過BKC改性后的GO與Gel復合制備得到的氣凝膠能夠有效提升其對于LEV的吸附能力。此外,從圖6中也可以看出,GGB吸附LEV的前50 min吸附速率較快,而后續的50~110 min吸附速率變得緩慢,在120 min達到吸附平衡。而GGO吸附LEV基本保持勻速進行,在0~120 min的吸附過程中吸附速率變化不大。結合形貌的差別,分析原因可能是由于BKC通過靜電作用和π-π作用組裝在GO表面,有效阻止了GO片層之間的緊密的π堆疊,促進GO片層和Gel構成具有多孔結構的GGB,其表面大量的孔道,有助于對LEV吸附容量的提升。而GGO表面較為致密緊實,存在少量的空洞,使得其對于LEV吸附容量相對較差。
2.5 pH值對吸附性能的影響
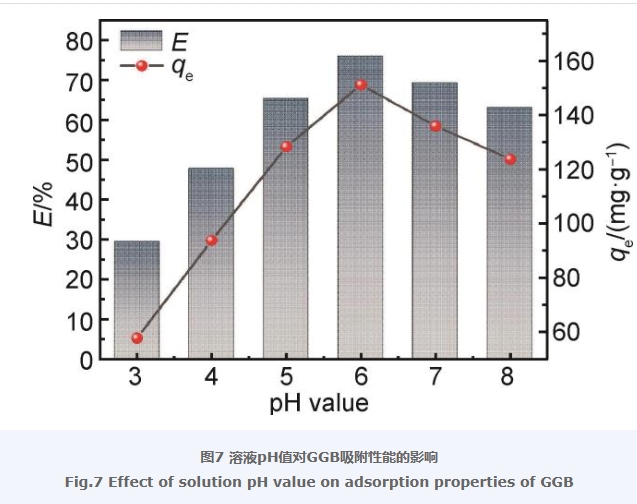
溶液的pH值對吸附具有重要影響,因為它能夠調控吸附劑與吸附質的表面電荷,從而影響二者之間的相互作用。溶液pH值對GGB吸附性能的影響如圖7所示。由圖7可以看出,在pH值從3增加到8的過程中,GGB對LEV的去除率和吸附量呈現先增加后減少的趨勢,當pH值為6時,GGB對LEV的去除率達到75.75%,為最佳條件,其平衡吸附量為150.80 mg/g。這可能是由于在pH值較低時,溶液中H+濃度較高,GGB表面的羥基、氨基等官能團受溶液中大量H+的影響,發生質子化,使GGB表面顯正電性,同時,在酸性條件下,LEV分子中叔胺基同樣被質子化,以陽離子形式存在的LEV與GGB的電性相同,兩者相互排斥,使得吸附量不高;隨著pH值繼續增加,H+濃度逐漸減小,GGB表面的相關官能團質子化作用降低,同時LEV分子中的叔胺基官能團,其質子化程度也同樣降低,LEV與GGB之間的電性相斥作用減弱,吸附量增加。此外,羥基、氨基等官能團由于受質子化作用的影響,也會減弱GGB與LEV分子之間氫鍵相互作用的發生,從而影響吸附量。當溶液pH值為6時,GGB與LEV分子靜電相斥作用最弱,吸附量達到最大值。隨著pH值的繼續增加,GGB結構中的羧基發生去質子化,GGB逐漸轉為負電性,同時LEV分子上的羧基也同樣電離出H+,GGB與LEV之間的靜電相斥作用又被增強,使得GGB對于LEV的吸附量降低。雖然GGB在pH值為7和8時,對于LEV的吸附量有所降低,但仍保持了一定的吸附能力,這也說明了GGB對LEV的吸附作用除了靜電作用外,還有π-π堆積作用、氫鍵作用等其他因素。綜合以上結果,后續實驗選定在上述最優pH值為6條件下進行。
2.6 初始溶液濃度對吸附性能的影響
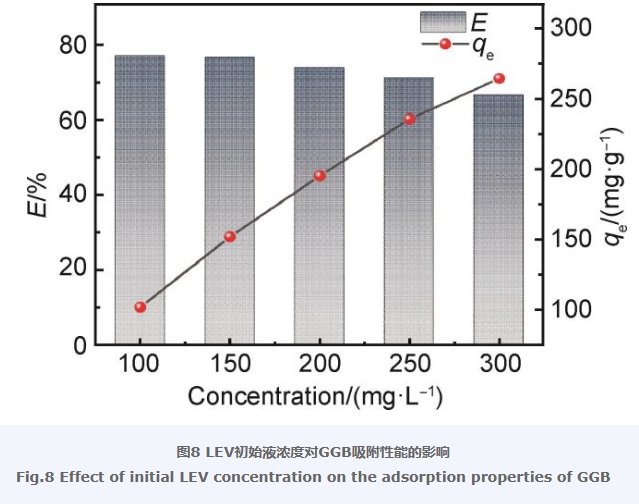
在其他參數不變的情況下,LEV初始液濃度對GGB吸附性能的影響如圖8所示。從圖8中可以看出,隨著LEV的初始濃度由100 mg/L逐步增加到300 mg/L,去除率從76.26%逐步下降到65.83%,而平衡吸附量從101.21 mg/g上升到262.14 mg/g。這是因為在GGB投加量保持不變的情況下,隨著溶液中LEV濃度的逐漸增大,吸附劑吸附LEV的量也隨之增加,但是因其吸附容量有限,使得過多的LEV無法與氣凝膠發生吸附,造成去除率下降。綜合考慮,選擇LEV溶液初始濃度為150 mg/L進行后續實驗,此濃度下的去除率為75.75%,平衡吸附量為150.80 mg/g。
2.7 吸附劑用量對吸附性能的影響
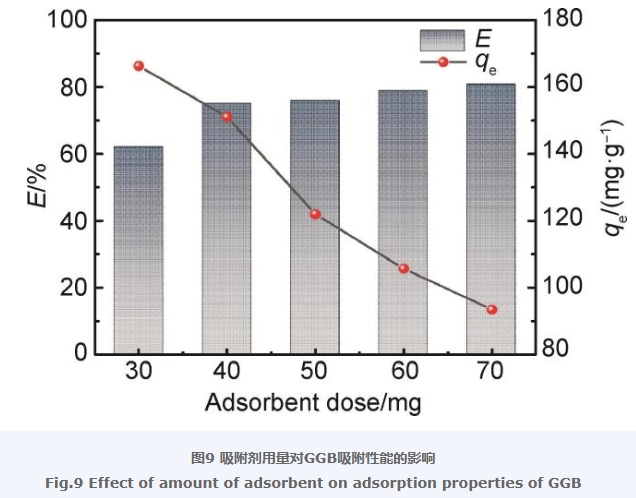
GGB用量對其吸附LEV性能的影響如圖9所示。從圖9中可以看出,吸附劑用量從30 mg增加到70 mg,GGB對LEV的去除率從61.91% 增加到了80.53%,但平衡吸附量從165.90 mg/g減少到了93.40 mg/g,這是由于隨著吸附劑用量的增多,與LEV接觸的位點也同樣增多,從而得到較高的去除率,但隨著吸附劑用量的增多,單位質量下的吸附劑上吸附LEV的量減少,使得平衡吸附量下降。因此綜合考慮,選擇40 mg的吸附劑投加量來進行后續的實驗。
2.8 溫度對吸附性能的影響
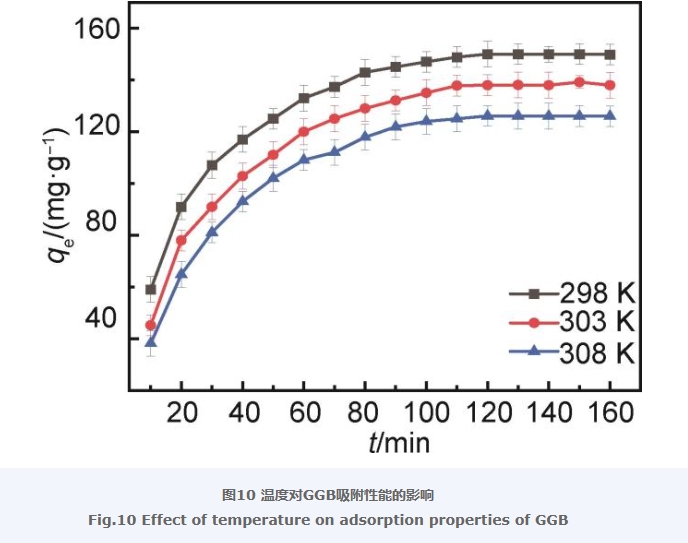
圖10顯示的是GGB在溫度分別為298,303,308 K時對LEV的吸附情況。由圖10可以看到,在298 K時GGB對LEV的平衡吸附量最大,達到了150 mg/g,并且隨著溫度逐漸升高至308 K,GGB對LEV的平衡吸附量從150 mg/g逐步降低至125 mg/g。結果表明,隨著溫度的升高,GGB對LEV的吸附量逐漸降低,并且吸附速率未發生明顯變化。
2.9 吸附動力學實驗研究
式中: Ki 是速率常數,mg/(g·min0.5); ci 是邊界層厚度。
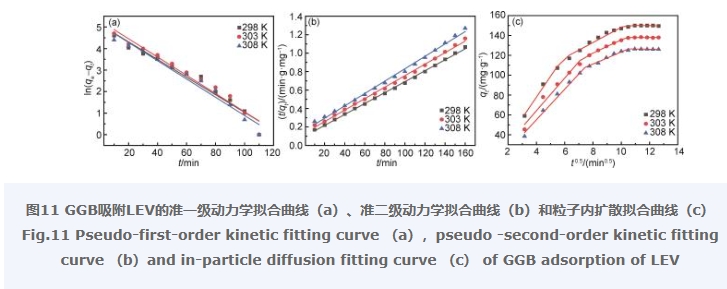
圖11為GGB對LEV吸附動力學擬合曲線,擬合得到對應模型的參數記錄于表1和表2。從表1數據可以看出,準二級動力學模型擬合得到的線性相關系數R 2(0.99)優于準一級動力學模型擬合得到的線性相關系數R 2(0.95~0.96),且準二級動力學模型擬合得到的平衡吸附量q e(298 K: 168.63 mg/g,303 K: 160.51 mg/g,308 K: 149.03 mg/g)數據與實驗得到的平衡吸附量q e(150 mg/g)更為接近。這表明GGB對LEV的吸附過程更加符合準二級動力學模型,吸附主要受化學吸附控制。
表1 GGB對LEV的吸附動力學擬合參數Table 1 Fitting parameters of LEV adsorption kinetics of GGB |
| T/K | Pseudo-first-order kinetic model | Pseudo-second-order kinetic model | ||||
|---|---|---|---|---|---|---|
| q e/(mg·g-1) | k 1/min-1 | R 2 | q e/(mg·g-1) | k 2/min-1 | R 2 | |
| 298 | 169.01 | 0.0409 | 0.954 | 168.63 | 0.00593 | 0.998 |
| 303 | 200.33 | 0.0424 | 0.958 | 160.51 | 0.00623 | 0.996 |
| 308 | 169.18 | 0.0424 | 0.963 | 149.03 | 0.00671 | 0.995 |
表2 GGB對LEV的粒子內擴散模型擬合參數Table 2 Fitting parameters of GGB for LEV intra particle diffusion model |
| T/K | K 1/(mg·g-1·min-0.5) | R |
K 2/(mg·g-1·min-0.5) | R |
K 3/(mg·g-1·min-0.5) | R |
|---|---|---|---|---|---|---|
| 298 | 20.97 | 0.975 | 7.639 | 0.948 | 0.217 | 0.309 |
| 303 | 16.42 | 0.969 | 6.702 | 0.993 | 0.066 | 0.035 |
| 308 | 15.36 | 0.982 | 6.155 | 0.922 | 0.196 | 0.994 |
為進一步討論其吸附速率,選用粒子內擴散模型進行擬合,結果如圖11(c)所示,擬合參數見表2,從圖11(c)和表2可以看出,GGB吸附LEV的過程大致可以分為三個階段。第一階段是邊界層擴散階段,曲線斜率較高,這是因為在吸附初期,氣凝膠表面有大量的—COOH,—OH和—NH2,為LEV提供了豐富的活性吸附位點,使得LEV能夠快速進入氣凝膠表面;第二階段是LEV擴散到吸附劑孔隙中的顆粒內擴散過程,擬合出的曲線沒有經過原點,這表明GGB與LEV之間還存在其他吸附機制的影響;第三階段是吸附與解吸平衡階段,氣凝膠的吸附位點被完全占據,吸附量趨于飽和。從粒子內擴散模型中可以看出,在整個吸附過程中,邊界層擴散和顆粒內擴散過程為主要控速步驟,說明了GGB吸附LEV的過程主要由這二者來共同控制。
2.10 吸附熱力學實驗研究
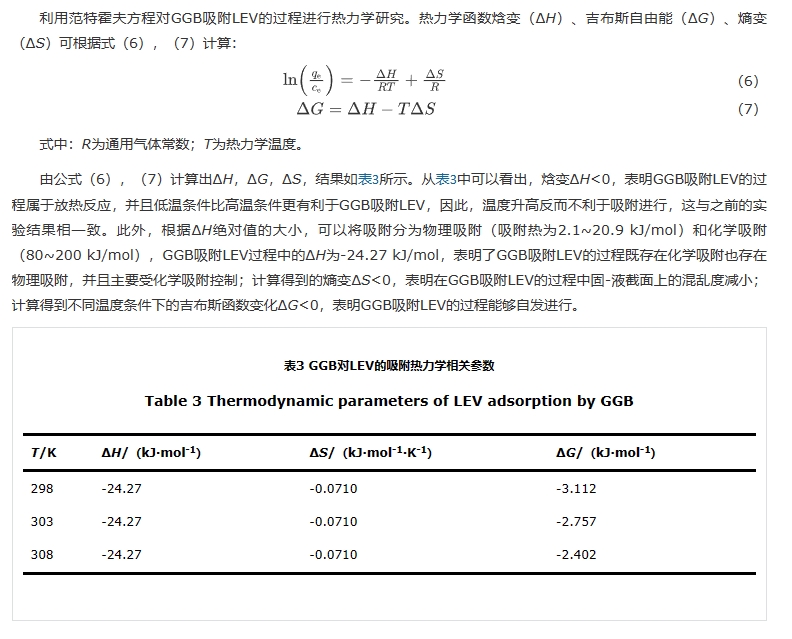
利用范特霍夫方程對GGB吸附LEV的過程進行熱力學研究。熱力學函數焓變(ΔH)、吉布斯自由能(ΔG)、熵變(ΔS)可根據式(6 ),(7 )計算:
2.11 吸附等溫實驗研究
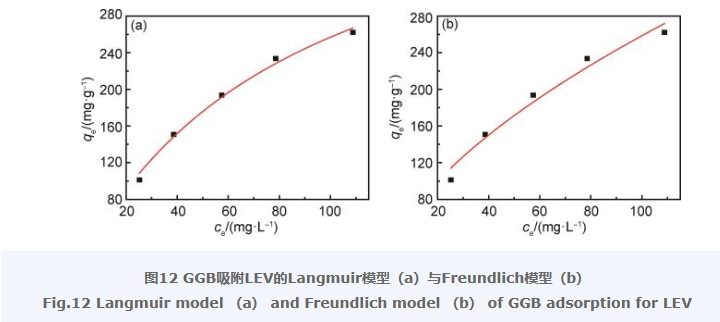
圖12是GGB吸附LEV的Langmuir和Freundlich等溫吸附擬合曲線,從圖12和表4的擬合參數可以看出,當溫度為298 K時,Langmuir等溫吸附模型擬合的相關系數R 2=0.990高于Freundlich等溫吸附模型擬合的相關性系數(R 2=0.965),此外,較低的R L值(0.460)也表明使用Langmuir等溫吸附模型進行模擬是有利的。基于以上分析,GGB吸附LEV的過程屬于單分子層吸附。通過Langmuir等溫吸附模型計算出GGB在298 K的溫度條件下對于LEV的理論最大吸附量能夠達到476.42 mg/g。表5中列出了近年來報道的LEV吸附材料[34-38],從表5中的數據可以發現,和其他吸附劑材料相比,本研究所制備的吸附劑對LEV具有更大的吸附容量。
| Langmuir model | Freundlich model | |||||
|---|---|---|---|---|---|---|
| q m/(mg·g-1) | k L | R 2 | R L | k F | n | R 2 |
| 476.42 | 0.0117 | 0.990 | 0.460 | 16.87 | 1.689 | 0.965 |
表5 不同吸附劑材料對LEV的最大吸附量比較Table 5 Comparison of adsorption properties of different adsorbents for LEV |
| Adsorbent | T/K | pH value | C 0/(mg·L-1) | q m/(mg·g-1) | Reference |
|---|---|---|---|---|---|
|
2-hydroxypropyl-β-cyclodextrin/ poly(acrylic acid)/poly (vinyl alcohol) nanofibrous membrane |
318 | 100 | 110 | [34] | |
| Rice husk biomass materials | 318 | 7 | 120 | [35] | |
| Biochar-supported manganese dioxide composite | 298 | 7.7 | 50 | 104.13 | [36] |
| MWCNTs/CoFe2O4 nanocomposites | 303 | 5 | 50 | 122 | [37] |
| Pithophora macroalgae biosorbent | 298 | 6.5 | 150 | 17.8 | [38] |
| GGB | 298 | 6 | 150 | 476.42 | This study |
2.12 復合氣凝膠吸附LEV的循環性能
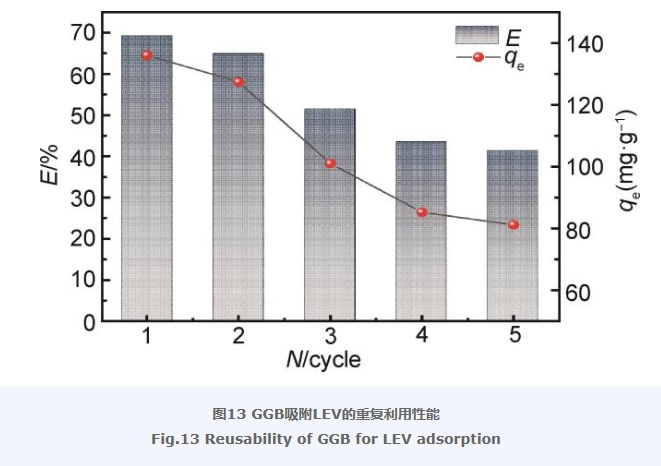
圖13顯示了GGB吸附LEV的重復利用性能。由圖13可知,當循環第一次時,LEV的去除率為69%,平衡吸附量為135.64 mg/g,之后每進行一次循環,LEV的去除率和平衡吸附量都相應地降低和減少,分析其中的原因可能是氣凝膠存在著脫附不完全的問題,表面活性劑改性的GO體現出兩親的特性,使得脫附變得困難,脫附不完全,因此,隨著循環次數的增多,GGB對LEV的吸附量也不斷降低。此外,在脫附過程中,部分氣凝膠的損失也會造成GGB對LEV吸附量的降低。從圖13中也可以看出,經過5次循環后GGB對LEV的平衡吸附量仍超過80 mg/g,相比其他吸附LEV的材料,GGB對于LEV的吸附效果依然具有一定的優勢[39]。
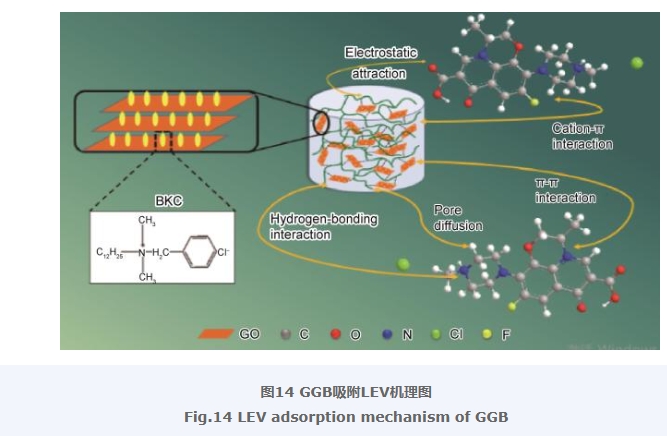
2.13 復合氣凝膠吸附LEV的機理分析
通過實驗結果推測了GGB吸附LEV的可能機理,如圖14所示。首先,由GGB的SEM分析可以看出,復合氣凝膠表現出優異的三維蜂窩狀多孔結構。因此,孔隙擴散作用是GGB吸附LEV發生的主要物理作用。其次,由pH對GGB吸附LEV的分析可以得出,受復合氣凝膠表面羥基、羧基、氨基等官能團的影響,LEV與GGB可以發生靜電相互作用。此外,GGB表面羥基,氨基等也能夠與LEV分子發生氫鍵相互作用,提升GGB對于LEV的吸附能力,相關的XPS分析也證明了氫鍵和靜電作用的存在。再次,由于氣凝膠體系中包含大量的π共軛結構(如GO的共軛結構、BKC的苯環結構、PDA的鄰苯二酚共軛結構),毫無疑問能夠與LEV結構中的芳香環形成有效的π-π相互作用。最后,陽離子-π鍵是一種較強的相互作用,可以發生在富電子的π體系和相鄰的陽離子之間。GGB結構中的π電子可以與LEV結構中的質子化氨基形成陽離子-π鍵。綜上所述,復合氣凝膠可能是通過靜電作用、氫鍵相互作用、π-π相互作用、陽離子-π相互作用以及孔隙擴散與LEV發生作用。
3 結論
(1)以表面活性劑十二烷基二甲基芐基氯化銨(BKC)為改性試劑,聚多巴胺(PDA)為包覆試劑,成功制備了一類明膠-改性氧化石墨烯-聚多巴胺復合氣凝膠(GGB),通過SEM,FTIR,XPS等表征分析表明,GO被BKC成功改性,GGB具有三維多孔網絡結構并且含有—OH,—COOH,—NH2等官能團。
(2)相對于復合未改性GO的復合氣凝膠GGO,GGB對于水體中鹽酸左氧氟沙星(LEV)的平衡吸附量明顯優于GGO,超過了GGO對LEV平衡吸附量的3倍。吸附實驗數據擬合符合準二級動力學模型和Langmuir吸附等溫模型,在298 K下擬合所得最大理論吸附量為476.42 mg/g,表明GGB吸附LEV的過程主要屬于受化學吸附過程控制的單分子層吸附。同時,吸附熱力學研究表明整個吸附過程是自發進行的放熱反應,并且經過5次循環,GGB對LEV的平衡吸附量仍超過了80 mg/g,表明該復合氣凝膠具有吸附處理水體中LEV的潛力。
(3)通過機理分析表明,復合氣凝膠GGB可能是通過靜電作用、氫鍵相互作用、π-π相互作用、陽離子-π相互作用以及孔隙擴散與抗生素LEV發生反應。
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。
相關文章
無相關信息

官方微信
《腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606
- 郵箱:fsfhzy666@163.com
- 腐蝕與防護網官方QQ群:140808414
點擊排行
PPT新聞
“海洋金屬”——鈦合金在艦船的
點擊數:10028
腐蝕與“海上絲綢之路”
點擊數:7814