不銹鋼在Nac1溶液中的“環狀”陽極極化曲線如圖3所示。
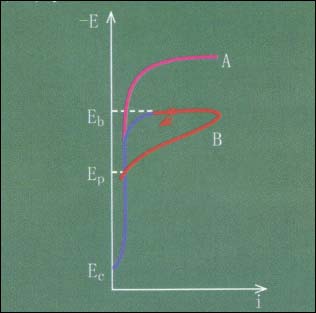
圖3 不銹鋼在Nacl溶液中的“環狀”陽極極化曲線
當溶液中不含C1ˉ時,不銹鋼的陽極極化曲線(EcA)中,穩定鈍化電位區間較寬。
如果溶液中含C1ˉ,當極化電位升至孔蝕電位Eb(又稱擊穿電位)時,陽極溶解電流開始顯著增大,不銹鋼表面產生小孔。當極化電流密度達到預定值后,電位立即以一定速度回掃(BEp),電流再次回到鈍態電流密度。此時,鈍化膜己重新修復好,再次回到鈍化狀態,Ep稱再鈍化電位或保護電位。
可見,氯離子對鈍化膜的破壞,只是出現在一定的電位范圍內。
當E>Eb時,金屬發生孔蝕;當Eb>E>Ep,金屬表面已有的蝕孔繼續生長,但不再產生新的蝕孔;當E<Ep,金屬處于鈍態。以此可以衡量不銹鋼鈍化狀態的穩定性以及耐各種介質侵蝕的性能。
但必須注意的是,用動電位法測量時,Ep值與掃描速度有關,而Eb值與回掃的電流密度值有關。所以,只有控制在相同的測試條件下,方可用此法相對比較不銹鋼的耐孔蝕能力和再鈍化能力。
氯離子破壞鈍化的機理
成相膜論者認為,由于氯離子半徑小,穿透力強,它最容易透過。膜申極小的孔隙與基體金屬相互作用形成可溶性化合物,導致局部腐蝕發生。
吸附論者認為,C1ˉ具有很強的可被金屬吸附的能力,而且溶液中的C1ˉ、溶解O2或OHˉ在Fe、Cr等金屬表面上存在著競爭吸附,原來被吸附的02可被C1ˉ排代,從而使原來耐蝕性好的鈍化膜(金屬—氧—羥水合絡合物)成為可溶性的絡合物(金屬—氧—羥—氯絡合物),使膜被破壞造成局部腐蝕。
過鈍化及其腐蝕
實踐證明,金屬獲得并維持鈍態可降低腐蝕。但利用鈍性時,必須嚴格注意防止過鈍化引起的腐蝕。
化學鈍化中,由于強氧化劑介質的作用,會使金屬進入過鈍化區,表面將形成可溶性或不穩定的化合物,腐蝕速度重新增大。例如18—8型不銹鋼在高濃度硝酸中會形成可溶的高價鉻的化合物,發生強烈的過鈍化腐蝕。
陽極鈍化中,當陽極(被保護設備)電位過高,偏離鈍化區進入過鈍化區時,同樣會出現過鈍化腐蝕。例如碳鋼在化肥工業的碳化生產液中陽極極化,當電位升高到0.8Ⅴ以上,也同樣進入了過鈍化區,此時鐵被氧化成更高價的,可溶性化合物,使腐蝕加劇。
鈍性的利用
金屬材料的合金化
金屬材料的耐蝕性提高,往往是通過合金化途徑,若將某些易鈍化的金屬,如Ti、A1等和鈍化性較弱的金屬組成固溶體合金時,可使鋼表面易形成鈍化膜,顯著提高了鋼的耐蝕性和其他性能。
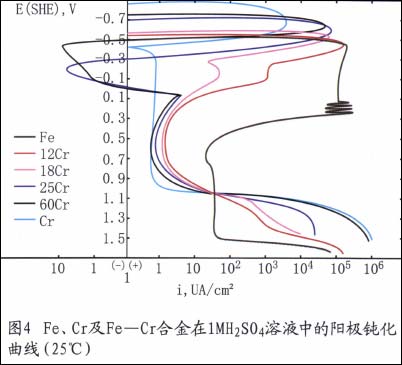
例如,鉻是不銹鋼獲得耐蝕性的最基本元素。在氧化性介質中,鉻能使鋼表面很快生成Cr203保護膜。這種膜一旦被破壞,會很快修復。在氧化性條仵下,隨鋼中含鉻量的升高,其耐蝕性愈好。如圖4所示。
鉬也是不銹鋼中主要的合金元素,通常添加2%~3%鉬時,鋼的表面形成富鉬氧化物膜。
鉬能有效地提高鋼的孔蝕電位,可抑制因氯離子侵入而產生的孔蝕。當鉬和鉻配合使用時,抗孔蝕效果更佳。
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。
-
標簽: 金屬應用鈍化

官方微信
《腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 腐蝕與防護網官方QQ群:140808414





