1. 摘要:
腐蝕電化學研究近些年進展相對較為緩慢。現(xiàn)有研究更多的是把腐蝕電化學作為腐蝕金屬或涂層在典型環(huán)境中腐蝕失效過程的評價工具,關注一些唯象參數(shù),如自腐蝕電流、極化電阻、電荷轉(zhuǎn)移電阻和噪聲電阻等,鮮有從電化學反應本身出發(fā),深入研究腐蝕金屬電極電化學反應動力學的報道,導致的后果是對腐蝕電化學反應難以深入認識,對電化學測試結(jié)果的分析容易流于形式。
腐蝕電化學反應本質(zhì)是多反應耦合(包括至少兩個電化學反應,以及后續(xù)化學反應)的非平衡反應,是電化學研究領域的難點,對腐蝕電化學反應歷程和動力學的深入研究有助于明確反應機制、認識腐蝕機理和發(fā)展非平衡電化學,具有重要的科學意義。本報告從腐蝕電化學基本方程出發(fā),明確基于混合電位理論的腐蝕動力學方程處理存在的若干簡化,及其合理性,結(jié)合現(xiàn)代電化學發(fā)展,創(chuàng)新性地提出應用掃描電化學顯微鏡腐蝕金屬電極探針產(chǎn)生 - 基底收集模式,定量分離全極化范圍下(線性極化區(qū)、弱極化區(qū)和塔菲爾區(qū))典型腐蝕金屬電極的表觀電流,明確陰陽極各自反應的準確電流,結(jié)合電荷轉(zhuǎn)移和傳質(zhì)定律基礎方程,建立 COMSOL 空間模型,解析獲得精確的反應動力學參數(shù)。通過對典型腐蝕金屬電極腐蝕電化學反應歷程和動力學參數(shù)的確定,重新審視經(jīng)典電化學阻抗譜、極化曲線和電化學噪聲方法與數(shù)據(jù),并指出其合理性與應用范圍,最終發(fā)展非平衡電化學。
關鍵詞:腐蝕電化學;非平衡;多反應耦合;動力學
2. 研究背景
對于多數(shù)金屬腐蝕過程,腐蝕電化學反應是腐蝕過程中最重要,也是最為復雜的化學反應[1] 。腐蝕研究從早期的形貌觀察、失(增)重法,逐漸演化用電化學方法監(jiān)測腐蝕過程,明確腐蝕機制。對于腐蝕反應而言,因非平衡和多反應耦合特征,很多電化學技術應用受限,在腐蝕中最重要也是被廣泛使用的技術通常有兩種:極化曲線和電化學阻抗譜。而電化學噪聲技術因數(shù)據(jù)解析困難,與腐蝕反應之間的物理化學圖像建立困難而應用受限。實際上,極化曲線和電化學阻抗譜在腐蝕體系的數(shù)據(jù)重復性欠佳[2] ,解析獲得的參數(shù),如極化電阻(R p )和電荷轉(zhuǎn)移電阻(R ct )等,與腐蝕電化學反應本征參數(shù)缺乏直接的聯(lián)系。腐蝕電化學反應通常為氧化性物種(如 O 2 ,H + )被還原和金屬被氧化形成離子過程,即:
陰極反應:O+ne - =R,陽極反應:M-ne - =M n+
對于陰極反應和陽極反應,我們先假設是基元電化學反應,則各自反應的Bulter-Volmer 表達式為[ 3] 。
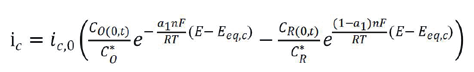 (1)
(1)
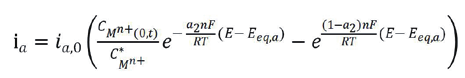 (2)
(2)
式中:下標中 a 和 c 代表陽極反應和陰極反應,下標 eq 代表平衡,O 表示氧化性物種,R 表示還原性物種,C (0,t) 表示 t 時刻表面濃度,上標 * 表示本體,i c,0 和 i a,0 分別為陰極反應和陽極反應的交換電流密度。顯然,這兩個獨立的電流表達式表明各自反應的物種濃度及其空間分布對電流大小有顯著影響。
對于腐蝕研究,對公式 1 和 2 做了如下重要假設:(1)腐蝕電極的自腐蝕電位與陰陽極反應的各自平衡電位差值較大,可以分別忽略陰極反應的陽極分支和陽極反應的陰極分支;(2)表面濃度與本體濃度近似相等,前提是動力學速率小且電位偏離各自平衡電位較小。此時,對于腐蝕發(fā)生的陰陽極反應分別簡化為:
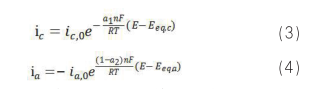
根據(jù) i corr 和 E corr 的物理意義,可知:
![]() (5)
(5)
則腐蝕電極的表觀電流與電位的關系為:
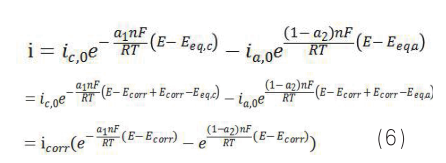


對于陽極反應的式 4,因為就是金屬自身的溶解,一般不認為存在擴散控制。通過此時的處理,不能獲得式 6 或者式 7 的腐蝕方程,i corr 和 E corr 的數(shù)值一般通過圖解法獲得[1] 。但是這個推導過程隱含了一個重要假設:即擴散層厚度一定,且濃度變化為線性關系。實際上擴散層內(nèi)厚度與測試時間有關,且濃度區(qū)間也非簡單線性,因此極限擴散電流也不是一定值。腐蝕研究一般通過電極電位與腐蝕電位的偏離程度來判斷是否是擴散控制,實際上需要考慮動力學因素。
對 O+ne - =R 的電化學反應,其電化學動力學基本方程應該具有如下基本形式:
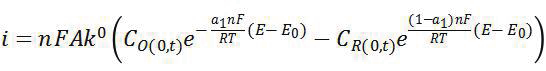
該式表明電化學反應的動力學基本參數(shù)是且僅是 k 0 ,a 和 E 0 ,不是 i 0 或者i corr (這兩個參數(shù)實際上包含物種濃度信息)。而在溶液中的傳質(zhì)過程,在忽略電遷移和強制對流的前提下,可用 Fick第一和第二定律描述,即表明濃度梯度需要考慮,擴散系數(shù)是重要的參數(shù)。對于腐蝕而言,腐蝕電化學需要確定的參數(shù)應該是陰極反應和陽極反應各自的標準速率常數(shù) k 0 ,傳遞系數(shù) a 和標準電極電位 E 0 ,而不是簡單默認 a 為 0.5,且用 i corr 作為腐蝕動力學參數(shù)。推導過程已經(jīng)表明 i corr 與各自陰陽極反應的交換電流、反應物種的濃度梯度、傳遞系數(shù)、各自的平衡電位以及自腐蝕電位等有關。腐蝕電化學的核心基礎方程對于深入認識腐蝕電化學行為特征具有重要作用,但是腐蝕電化學發(fā)展至今,需要再次審視腐蝕基本方程,并對其內(nèi)在科學問題進一步深入研究,特別是有關腐蝕電化學反應機制及其動力學的研究。
3. 腐蝕電化學動力學研究現(xiàn)狀
國內(nèi)外有關腐蝕反應動力學的研究多集中于腐蝕速率演化,以及環(huán)境因素的影響,對于普遍應用的極化曲線[5.6.7.8.9.10.11.12] 、電化學阻抗譜[9,10,12,13.14.15,]和電化學噪聲[15,16.17]等電化學技術中,更多的關注一些唯象參數(shù),如極化曲線中的自腐蝕電位、自腐蝕電流、陰陽極 Tafel 斜率、臨界點蝕溫度等;電化學阻抗譜中的電荷轉(zhuǎn)移電阻、膜電阻和雙電層電容等,而電化學噪聲技術則集中在時頻轉(zhuǎn)換分析,包括噪聲電阻、離散小波變換、快速傅里葉變換等。我們課題組在浙江大學期間也開展了大量有關極化曲線、電化學阻抗譜和電化學噪聲在腐蝕中的應用研究,如應用極化曲線和電化學阻抗譜評價稀土合金化鎂合金[18.19] ,鎂合金表面 Cu/Ni-P鍍層[20]和稀土轉(zhuǎn)化膜 + 微弧氧化膜[21]耐蝕性能及其隨時間演化等。而對于電化學噪聲,課題組自 2006 年發(fā)展小波變換時頻分析技術區(qū)分局部類型與強度[22] ,2012 年應用散粒噪聲理論研究鋅合金在干濕循環(huán)下腐蝕行為[23] ,然后于2013 年提出基于混沌理論量化亞穩(wěn)態(tài)孔蝕的特征參數(shù)最大 Lyapunov 指數(shù)[24] 。國外 McCafferty 于 2005 年的工作[25]闡述了極化曲線外推法在三種典型腐蝕體系(Fe 在鹽酸、氯化鈉溶液和 Ti 在沸騰硫酸溶液)獲得腐蝕速率的可靠性問題,并與其它技術互為驗證,提出了使用極化曲線外推法需要注意的內(nèi)容,包括活化控制、反應可知、Tafel 區(qū)顯著和均勻腐蝕等,但是實際上很多腐蝕體系或多或少不能滿足其中一條或多條,如不是活化控制,局部腐蝕等。對于具有氧化膜的鈦合金,Leygraf 報道了應用電化學阻抗譜研究鈍化膜的穩(wěn)定性,以及應用膜層分層結(jié)構(gòu)(外層疏松和內(nèi)層阻擋層)解釋電化學阻抗譜圖中的時間常數(shù)現(xiàn)象[26] ,Rajendran 也有類似工作 [27] 。Jiang 則考察極化曲線掃描速率對鈦合金自腐蝕電流判定的影響,并認為充放電電流導致了顯著的自腐蝕電流的偏差[28] ,而實際上,如果認可雙電層電容是固定值,則充放電電流僅是掃描速率的函數(shù)。掃描速率影響的偏差核心仍是對鈦合金表面狀態(tài)的改變繼而對反應動力學的影響。這些工作仍是局限于腐蝕表觀參數(shù),關注耐蝕性能的演化,并未從腐蝕電化學反應出發(fā),深入研究反應動力學。
對于腐蝕研究,極化曲線通常容易存在 Tafel 區(qū)不明顯,特別是陽極 Tafel分支,對于局部腐蝕嚴重金屬材料或者涂層體系,極化曲線重復性較差[2] 。電化學阻抗譜在腐蝕體系的理論與應用最大進展仍是由曹楚南先生提出的基于狀態(tài)變量原理的數(shù)學模型[29] , 并系統(tǒng)研究了典型腐蝕體系的電化學阻抗譜行為[30,31] 。曹先生基于電化學反應的數(shù)學模型有效克服了等效電路(仍是目前應用最廣泛的電化學阻抗譜分析方法)的諸多不足,如時間常數(shù)的歸屬,感抗的解釋與意義等,但是數(shù)學模型的建立與數(shù)據(jù)分析比較困難,導致數(shù)學模型的應用比較受限。電化學噪聲技術的發(fā)展更多的是體現(xiàn)在在線監(jiān)測方面,特別是現(xiàn)場腐蝕監(jiān)測,作為基礎研究,其最大的不足應該是各種特征參數(shù),如噪聲電阻、傅里葉變換結(jié)果功率譜密度(Powerspectral density)和小波變換結(jié)果能量分布譜圖(Energy distributionplot)等,與腐蝕行為或者腐蝕動力學之間的相關性相對較弱[32,33] ,數(shù)據(jù)挖掘與解釋陷入一定程度的困境。現(xiàn)在的腐蝕電化學更多的是作為一種腐蝕評價技術,關注腐蝕速率(Corrosion rate)或耐蝕性能(Corrosion resistance),鮮有從電化學反應本身出發(fā)探究腐蝕電化學反應動力學。
Kolotyrkin 早在上世紀六十年代就開始應用極化曲線技術評價陰離子對金屬陽極溶解行為的影響[34.35] ,但是經(jīng)典工作仍要到 1986 年,由 Bockris(國際著名電化學專家,著有《量子電化學》)報道的,利用旋轉(zhuǎn)環(huán)盤電極,結(jié)合極化曲線,研究中性溶液中鐵電極氧氣還原的途徑及其速率決定步驟,并比較裸鐵(bare iron)和鈍化鐵(passive iron)表面氧還原的區(qū)別,探討過氧化氫(H 2 O 2 )作為中間物種的反應途徑,并最終提出一個包含化學吸附為速率決定步驟的氧還原路徑[36] 。Bockris 的工作并沒有詳細闡述極化電流曲線中是否涉及 Fe 氧化的電流,也受限于旋轉(zhuǎn)環(huán)盤電極結(jié)構(gòu)導致的收集效率較低問題,以及并沒有報道準確的動力學速率常數(shù)等,而是用多步反應的 Tafel 斜率替代。國內(nèi)董俊華研究員應用穩(wěn)態(tài)極化曲線和電化學阻抗譜研究硫脲對鐵的緩蝕作用,并結(jié)合Tafel 斜率分析獲得電化學參數(shù)[37] 。吳維?研究員結(jié)合 pH 影響腐蝕電位與腐蝕電流數(shù)據(jù),并根據(jù)腐蝕反應方程推導了 A3 鋼在乙酸中可能的腐蝕機理[38] 。這些工作非常具有代表性,但受限于實驗條件與技術發(fā)展水平,具體的動力學參數(shù)很難在當時的環(huán)境下解析獲得,所以后續(xù)工作也受到限制。
4. 課題組工作
現(xiàn)代電化學發(fā)展已經(jīng)進入分子 / 原子階段,原位微區(qū)技術不斷出現(xiàn)與更新[39,40,41] 。如何結(jié)合現(xiàn)代電化學發(fā)展,從電化學反應出發(fā),深入認識腐蝕反應動力學特征及其參數(shù)的準確表征,仍是具有重要意義的研究工作,也相對于傳統(tǒng)腐蝕電化學研究方法,提供了認識反應機制的新可能。腐蝕電化學反應定量研究的首要前提是多耦合反應的定量分離,特別是在線性極化區(qū)和弱極化區(qū)的分離,因為通常電位掃描腐蝕電極獲得的電流是表觀電流,包含多個反應的電流疊加,其次是解析 Bulter-Volmer 和傳質(zhì)動力學方程。
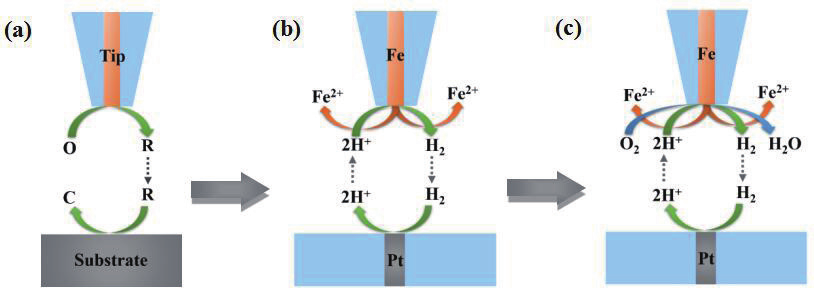
圖1. SECM的TG/SC模式用于Fe腐蝕反應分離的示意圖,其中(a)傳統(tǒng)TG/SC模式;(b)改進后的TG/SC模式用于
除氧溶液中Fe腐蝕反應分離;(c)改進后TG/SC模式用于含氧溶液中腐蝕反應分離。
在傳統(tǒng) TG/SC 模式中(圖 1a),探針在某一電位下發(fā)生O+ne - →R反應,控制基底電位將產(chǎn)生的 R 收集,并重新生成 O,然后擴散至探針電極上形成正反饋效應。圖 1b 是改進后的產(chǎn)生 - 收集模式用于除氧酸性溶液中 Fe 腐蝕耦合反應的分離,在 Fe 電極表面發(fā)生腐蝕時有兩個反應同時進行,即 2H + +2e -→ H 2 和 Fe → Fe 2+ +2e - ,因此測量得到的表觀電流中包含 Fe 氧化和質(zhì)子還原電流,通過設置Pt基底電極電位為某一值,使其表面只發(fā)生氫氣氧化反應,則基底上 H 2 氧化電流與探針 H + 還原電流大小相等,從而實現(xiàn) Fe 探針電極上兩個反應分離。圖 1c 是溶液中含氧條件下(自然狀態(tài))Fe 電極表面發(fā)生的腐蝕,此時除了 Fe 氧化和質(zhì)子還原外還包含氧氣還原過程:O 2 +4e - +4H + → 2H 2 O,同圖2b 一樣 Pt 基底電極上也只收集探針產(chǎn)生的 H 2 ,再結(jié)合除氧溶液中分離得到的Fe 氧化電流,可進一步將自然條件下 Fe腐蝕時表面上發(fā)生的三個電化學反應分離。

圖2. 典型(a)Fe探針超微電極(b)Pt基底超微電極的掃描電鏡圖
圖 2 為 Fe 探針電極和 Pt 基底電極的光學掃描電鏡圖。從圖中可以看出 Fe電極和 Pt 電極在拋光后呈圓盤狀,通過測量得到 Fe 電極半徑為 50μm,玻璃與金屬絲半徑比值(RG)為 3.7,Pt的半徑為 62.5μm,RG 為 10.8,在玻璃管密封前后 Fe 和 Pt 的直徑都沒有變化。Fe 探針電極是在激光拉制儀(p-2000)上制備,而 Pt 基底電極是商業(yè)PC-10 拉制儀上制備,從中可以看出,這兩種方法制備得到的電極較好的保存了金屬絲原來的表面結(jié)構(gòu)和尺寸。實驗中探針電極逼近基底電極時所采用的氧化還原電對為實驗室自制的三乙醇胺鐵(Fe(III)-TEA),由于 Fe 的電極電勢較負(E 0 Fe 2+ /Fe =-0.447 vs NHE),若采用二茂鐵甲醇(E 0 =0.44 vs NHE)或氯化六胺合釕(E 0 =0.05 vs NHE)這些常用的氧化還原電對,在逼近過程中 Fe 會發(fā)生反應,導致 Fe 表面在測試前發(fā)生明顯的變化。實驗中將 Fe 探針電極逼近至 Pt 基底電極 33μm 處。在探針和基底之間的距離確定后,將電解池中溶液換為 5mM HClO 4 +0.1M NaClO 4 ,并除氧 15min,對 Fe 探針電極進行線性掃描伏安法(LSV)測試。圖 3 為 Fe 探針電極和基底電極電流隨 Fe 電極電位變化的產(chǎn)生 / 收集曲線。從圖 3a 和 b 中可以看出,隨著探針電位的正移,析氫反應逐漸減弱,F(xiàn)e氧化開始發(fā)生,直至-0.4V vs NHE 時,基底電極上氫氣氧化電流趨向于 0,表明探針上析氫反應基本消失,F(xiàn)e探針電極上開始以Fe的氧化為主。通過陰極極化區(qū)探針和基底電流,確定探針電極的收集效率為 91.5%。
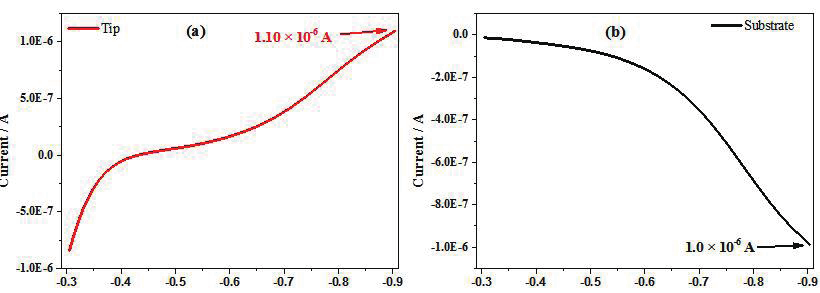
圖3. 在5 mM HClO 4 + 0.1 M NaClO 4 除氧溶液中,50μm Fe探針電極在62.5 μm Pt基底電極上的線性循環(huán)伏
安曲線,其中(a)探針電流(b)基底電流。探針電位掃描區(qū)間為從-0.9V 至 -0.3 V vs NHE,基底氧化
氫氣恒定電位為+0.3 V vs NHE,掃速為5 mV·s -1
圖 4a 中紅線為圖 3 中探針電流,黑線為對基底電流收集效率校正并取絕對值后的電流值,藍線為探針電流與校正后基底電流的差值即 Fe 的氧化電流。

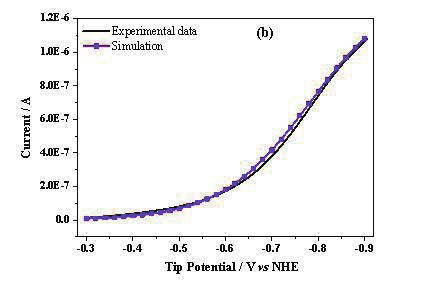
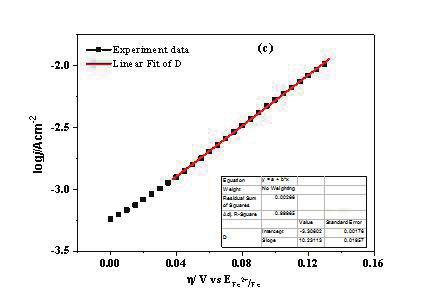
圖4.(a)對圖3中的數(shù)據(jù)進行進一步的處理,探針電流、基底電流和兩者電流差與探針電位之間的關系。紅線代表探針電流,黑線代表91.5%的收集效率校正后并取絕對值的基底電流,藍線是這兩者的差值。插圖是探針電流為0時的局部放大圖。(b)Fe電極表面的質(zhì)子還原電流與COMSOL的模擬曲線。(c)Fe氧化電流為j,則logj與Fe氧化過電勢η之間的關系(黑線),以及線性擬合(紅線)之間的關系。
從圖 5a 中可以看出在電位區(qū)間為 -0.55至 -0.9V vs NHE 時,探針電流與校正后的基底電流重合,表明 Fe 探針上主要是質(zhì)子的還原。在 -0.31 至 -0.36 Vvs NHE 時,基底電流為 0,則 Fe 電極上主要發(fā)生的是 Fe 的氧化。當探針電流為 0 時,F(xiàn)e 氧化電流與質(zhì)子還原電流大小相同為腐蝕電流,大小為 5.09×10 -8 A(電流歸一化后,自腐蝕電流密度為 6.48×10 -4 A/cm 2 ),此時電位為Fe 的腐蝕電位,為 -0.433 V vs NHE。

圖5. (a)酸性有氧體系中放入Fe電極表觀電流(紅線)和基底Pt收集電流(黑線);(b)有氧酸性環(huán)境下,
根據(jù)收集效率計算得到的Fe的析氫電流(黑線)、氧的還原電流(綠線)和Fe溶解電流(藍線)。
通過對質(zhì)子還原電流和 Fe 氧化電流進行 COMSOL 模擬和線性擬合,可以分別得到 Fe 腐蝕時析氫反應和 Fe 氧化反應的標準速率常數(shù) k 0 和傳遞系數(shù) α 分別為 9.2×10 -6 cm/s 和 0.27(圖 4b),2.5×10 -6 cm/s 和 0.7(圖 4c) [42] 。
Fe 發(fā)生腐蝕時通常有氧氣參與,因此課題組又進一步研究了在含氧酸性溶液中 Fe 的腐蝕行為[43] 。圖 5a 中探針電流上包含有質(zhì)子還原電流、氧還原電流和 Fe 氧化電流,而基底電極只發(fā)生氫氣的氧化反應,因此通過對基底電流進行收集效率校正后可得到探針上質(zhì)子還原電流,結(jié)合除氧條件下 Fe 氧化電流,可得到探針電極上的氧還原電流。從圖8b 中反常吸氧還原曲線(隨電位負移,O 2 還原電流下降)表明酸性溶液體系O 2 還原與質(zhì)子還原存在競爭關系,且與電位密切相關。圖 8b 中插圖為有氧體系中自腐蝕電位的放大部分,亦即自腐蝕電流和自腐蝕電位真正的物理化學圖像。表觀電流為 0 時,各自對應的 Fe溶解電流,質(zhì)子還原電流以及 O 2 還原電流均有準確數(shù)值,腐蝕所關注的電流大小是且應該就是 Fe 的溶解電流大小。
此外,在腐蝕電位附近,氧還原電流和質(zhì)子還原電流相差較小,表明在自腐蝕電位附近,氧還原反應與質(zhì)子還原反應同等重要,不能忽略。
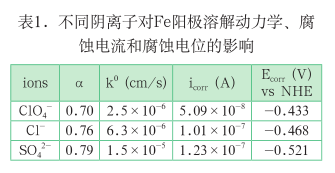
表 1 為改變?nèi)芤旱年庪x子分別為ClO 4 - ,Cl - 和 SO 4 2- 時,對應的 Fe 陽極溶解的傳遞系數(shù),表觀速率常數(shù)、自腐蝕電流和自腐蝕電位數(shù)據(jù)。結(jié)果清晰表明傳遞系數(shù)均顯著偏離 0.5,陰離子顯著改變表觀速率常數(shù),自腐蝕電流 SO 4 2-溶液中最大,ClO 4 - 溶液中最小,這些結(jié)果表明陽極溶解動力學過程不簡單是金屬失去電子的過程,陰離子的吸附作用等對金屬離子從金屬晶格中溶出具有重要影響,這一部分的理論分析正在結(jié)合第一性原理展開。
而對于 Cu 的陽極溶解與陰極還原反應的定量研究則涉及溶解過程的一價銅離子等。圖 6a 和 b 分別為探針電流和基底電流隨探針電位的變化,當探針開始掃描時,探針電極上只發(fā)生質(zhì)子還原反應,同樣基底電極上也只發(fā)生氫氣氧化反應,據(jù)此可得到基底電極對探針產(chǎn)生氫氣的收集效率為 83%。當探針電位在 -0.184 至 0.206V 之間時,探針電流和基底電流都趨向于 0,表明探針上既不發(fā)生質(zhì)子還原也不發(fā)生Cu氧化反應。
當電位高于 0.206V 時,探針上開始發(fā)生 Cu 氧化反應,而基底電流大小先增大后減小,在 0.452V 時達到最大值,此時基底電流為探針產(chǎn)生的 Cu + 發(fā)生氧化反應的電流,通過收集效率校正后,發(fā)現(xiàn)基底電流僅占到探針電流的4.9%,表明 Cu 氧化主要發(fā)生的是雙電子過程(生成 Cu 2+ 占到 95.1%),單電子過程只占到很小的比例。通過對圖 6 中得到的 Cu 表面質(zhì)子還原電流進行 COMSOL多物理場模擬,可得到 Cu 表面析氫反應標準速率常數(shù) k 0 H 和傳遞系數(shù) αH 分別 為 1.28×10 -4 cm/s 和 0.29。Cu 氧化為 Cu 2+ 的標準速率常數(shù) k 0 Cu2+ /Cu 和αCu 2+ /Cu 分 別 為 1.31×10 -4 cm/s 和0.76,而對于 Cu 氧化為中間態(tài) Cu + ,Cu + 的標準速率常數(shù) k 0 Cu+ /Cu 和 αCu + /Cu 分別為 5.69×10 -4 cm/s 和 0.42。

圖6?在除氧5mM?HClO 4 +0.1M?NaClO 4 溶液中,Cu探針電極線性伏安曲線,其中(a)Cu探針電流和(b)Pt基底電流隨探針電位的變化。圖(a)中插圖為質(zhì)子還原電流隨探針電位變化,圖(b)中插圖為Cu探針電極產(chǎn)生中間物在基底上氧化電流。
為了進一步研究含氧溶液中 Cu 腐蝕動力學,分別在自然條件和氧飽和條件下對 Cu 電極進行線性極化曲線測量。圖 7a 和 b 為自然條件下探針電流和基底電流隨探針電位的變化,圖 7c和 d 為氧飽和條件下探針電流和基底電流隨探針電位的變化。當 Cu 探針電極上電流為 0 時,自然條件下酸性溶液中 Cu 腐蝕電位(E corr )為 0.20V。從圖 7a 和 c 可以看出,在陰極極化區(qū),隨著氧濃度的增加,相同電位下質(zhì)子還原電流減小,表明部分質(zhì)子可能參與了氧還原反應過程。在陽極極化區(qū)(圖 7b 和 d),隨著氧濃度增加,Cu氧化電流逐漸增大,說明氧氣存在可以促進 Cu 氧化。在 0.250V 至 0.516V 電位區(qū)間,基底電極上也能檢測到探針產(chǎn)生的 Cu + ,按照收集效率校正后,在自然條件和氧飽和條件下,Cu 氧化為Cu + 的電流占總 Cu 氧化電流比值分別為1.3% 和 0.24%,與除氧條件下 4.9%相比,明顯降低。可能原因有兩個:一是溶液中氧氣與產(chǎn)生的 Cu + 發(fā)生反應,即 Cu + +H + +1/2O 2 → 1/2H 2 O 2 +Cu 2+ ;二 是 氧 氣 在 Cu 表 面 失 去 電 子 形 成(Cu)-(HO x )ads, 吸 附 的 (HOx) ads 可以 與 Cu + 反 應, 即 Cu(I)ads+(HOx)ads → Cu(II)+H 2 O(or H 2 O 2 )。
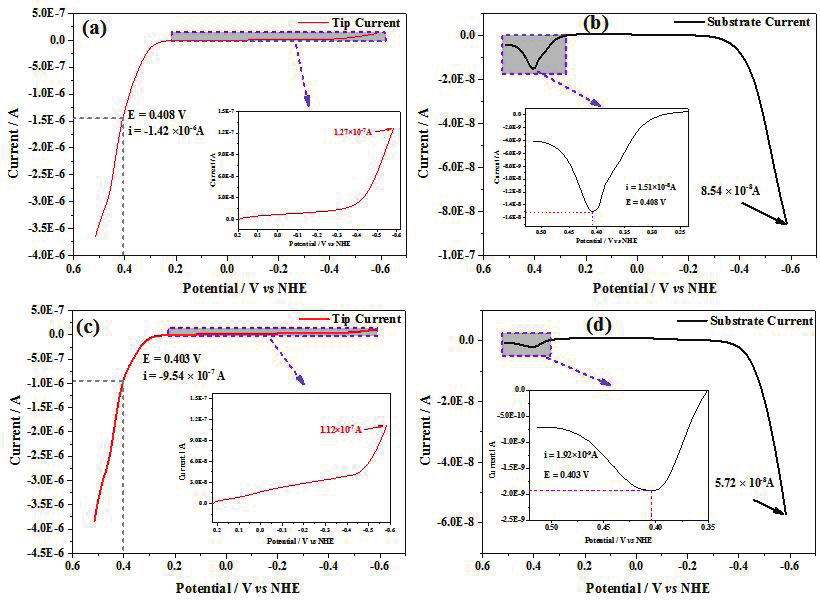
圖7 在5mM HClO 4 +0.1M NaClO 4 溶液中不同氧濃度下Cu探針電極線性伏安曲線,其中在自然條件(a)Cu探針電流和(b)Pt基底電流隨探針電位變化,在氧飽和條件下(c)Cu探針電流和(d)Pt基底電流隨探針電位變化。圖(a)和(c)中插圖為質(zhì)子還原電流隨探針電位變化,圖(b)和(d)為Cu氧化中間物氧化電流隨探針電位變化。
5. 結(jié)論
腐蝕反應是涉及異相電荷轉(zhuǎn)移和均相化學反應的耦合反應,且異相電化學反應包含陽極溶解反應和陰極還原反應,其動力學研究需要從電化學 - 化學反應本身出發(fā),揭示腐蝕與防護研究中的腐蝕電化學的反應歷程與機制,繼而推動和促進腐蝕與防護研究,發(fā)展非平衡電化學。
致謝
國家自然科學基金(51771174,51131005,51171172 和 50801056)、國 家 重 點 研 發(fā) 計 劃 子 任 務(2017YFB0702302)、浙江省自然科學基金杰出青年項目(LR16E010001)和自然環(huán)境腐蝕平臺資助。
參考文獻
[1] 曹楚南,腐蝕電化學原理,第三版,北京,化學工業(yè)出版社,2008
[2] L.R. Chang, F.H. Cao, J.S. Cai, W.J. Liu, J.J.Zheng, J.Q. Zhang, C.N. Cao, Polarization Behaviorof Magnesium Alloy AZ91D with Micro-Arc OxidationCoating in NaCl Solution. Acta Physico-ChimicaSinica, 28 (2012) 127-136.
[3] A.J. Bard, L.R. Faulkner, Electrochemicalmethods: Fundamentals and Applications, 2nd edition,New York, John Wiley & Sons. INC. 2000
[4] N. Perez, Electrochemistry and Corrosion Science,Boston, Kluwer Academic Publishers, 2004
[5] J.H. Liu, G. Rong, S. Cen, S.M. Li, H.B. Shi,K. Zhao, M. Yu, Dissolution Behavior of IntermetallicParticles in AA2297-T87 during Anodizing in Adipic-Sulfuric Acid, Journal of the Electrochemical Society.165 ((2018) C980-C990.
[6] X. Wu, Y.T. Sun, Y.Y. Liu, Y.Y. Yang,J. Li, Y.M. Jiang, The Critical Pitting ChlorideConcentration of Various Stainless Steels Measuredby an Electrochemical Method, Journal of theElectrochemical Society. 165 ((2018) C939-C949.
[7] X. Qiu, Microstructure, hardness and corrosionresistance of Al2CoCrCuFeNiTix high-entropy alloycoatings prepared by rapid solidification, Journal ofAlloys and Compounds. 735 (2018) 359-364.
[8] R.L. Liu, J.R. Scully, G. Williams, N. Birbilis,Reducing the corrosion rate of magnesium viamicroalloying additions of group 14 and 15 elements,Electrochimica Acta. 260 (2018) 184-195.
[9] Y.J. Qiang, S.T. Zhang, B.C. Tan, S.J. Chen,Evaluation of Ginkgo leaf extract as an eco-friendlycorrosion inhibitor of X70 steel in HCl solution,Corrosion Science. 133 (2018) 6-16.
[10] C.Q. Li, D.K. Xu, X.B. Chen, B.J. Wang,R.Z. Wu, E.H. Han, N. Birbilis, Composition andmicrostructure dependent corrosion behaviour of Mg-Lialloys, Electrochimica Acta. 260 (2018) 55-64.
[11] L.H. Yang, Y.X. Wan, Z.L. Qin, Q.J. Xu,Y.L. Min, Fabrication and corrosion resistance of agraphene-tin oxide composite film on aluminium alloy6061, Corrosion Science. 130 (2018) 85-94.
[12] Y.J. Qiang, S.T. Zhang, L. Guo, X.W. Zheng,B. Xiang, S.J. Chen, Experimental and theoreticalstudies of four allyl imidazolium-based ionic liquids asgreen inhibitors for copper corrosion in sulfuric acid,Corrosion Science. 119 (2017) 68-78.
[13] Y.B. Zhao, H.P. Liu, C.Y. Li, Y. Chen, S.Q.Li, R.C. Zeng, Z.L. Wang, Corrosion resistance andadhesion strength of a spin-assisted layer-by-layerassembled coating on AZ31 magnesium alloy, AppliedSurface Science. 434 (2018) 787-795.
[14] D.K. Xu, J. Xia, E.Z. Zhou, D.W. Zhang,H.B. Li, C.G. Yang, Q. Li, H. Lin, X.G. Li, K.Yang, Accelerated corrosion of 2205 duplex stainlesssteel caused by marine aerobic Pseudomonas aeruginosabiofilm, Bioelectrochemistry. 113 (2017) 1-8.
[15] A. Ehsani, M.G. Mahjani, M. Hosseini, R.Safari, R. Moshrefi, H.M. Shiri, Evaluation ofThymus vulgaris plant extract as an eco-friendlycorrosion inhibitor for stainless steel 304 in acidicsolution by means of electrochemical impedancespectroscopy, electrochemical noise analysis and densityfunctional theory, Journal of Colloid and InterfaceScience. 490 (2017) 444-451.
[16] M. Sakairi, R. Sasaki, A. Kaneko, Y. Seki,D. Nagasawa, Evaluation of metal cation effects ongalvanic corrosion behavior of the A5052 aluminumalloy in low chloride ion containing solutions byelectrochemical noise impedance, Electrochimica Acta.131 (2014) 123-129.
[17] F. Safizadeh, E. Ghali, Monitoring passivationof Cu-Sb and Cu-Pb anodes during electrorefiningemploying electrochemical noise analyses,Electrochimica Acta. 56 (2010) 93-101.
[18] W. Liu, F. Cao, L. Zhong, L. Zheng, B. Jia,Z. Zhang, J. Zhang, Influence of rare earth elementCe and La addition on corrosion behavior of AZ91magnesium alloy, Materials and Corrosion-WerkstoffeUnd Korrosion. 60 (2009) 795-803.
[19] W. Liu, F. Cao, A. Chen, L. Chang, J.Zhang, C. Cao, Corrosion behaviour of AM60magnesium alloys containing Ce or La underthin electrolyte layers. Part 1: Microstructuralcharacterization and electrochemical behaviour,Corrosion Science. 52 (2010) 627-638.
[20] S. Zhang, F. Cao, L. Chang, J. Zheng, Z.Zhang, J. Zhang, C. Cao, Electrodeposition of highcorrosion resistance Cu/Ni–P coating on AZ91Dmagnesium alloy, Applied Surface Science. 257 (2011)9213-9220.
[21] J.S. Cai, F.H. Cao, L.R. Chang, J.J. Zheng,J.Q. Zhang, C.N. Cao, The preparation andcorrosion behaviors of MAO coating on AZ91D withrare earth conversion precursor film, Applied SurfaceScience. 257 (2011) 3804-3811.
[22] F.H. Cao, Z. Zhang, J.X. Su, Y.Y. Shi, J.Q.Zhang, Electrochemical noise analysis of LY12-T3in EXCO solution by discrete wavelet transformtechnique, Electrochimica Acta. 51 (2006) 1359-1364.
[23] A.N. Chen, F.H. Cao, W.J. Liu, L.Y. Zheng,Z. Zhang, J.Q. Zhang, C.N. Cao, Shot noiseanalysis on corrosion behavior of zinc alloy (ZnAl4Cu1)under dry-wet cycles, Transactions of NonferrousMetals Society of China. 22 (2012) 228-240.
[24] A.N. Chen, F.H. Cao, X.N. Liao, W.J. Liu,L.Y. Zheng, J.Q. Zhang, C.A. Cao, Study ofpitting corrosion on mild steel during wet-dry cyclesby electrochemical noise analysis based on chaostheory, Corrosion Science. 66 (2013) 183-195.
[25] E. McCafferty, Validation of corrosion ratesmeasured by the Tafel extrapolation method, CorrosionScience. 47 (2005) 3202-3215.
[26] J. Pan, D. Thierry, C. Leygraf, Electrochemicalimpedance spectroscopy study of the passive oxide filmon titanium for implant application, ElectrochimicaActa. 41 (1996) 1143-1153.
[27] S. Tamilselvi, V. Raman, N. Rajendran,Corrosion behaviour of Ti-6Al-7Nb and Ti-6Al-4V ELI alloys in the simulated body fluid solution byelectrochemical impedance spectroscopy, ElectrochimicaActa. 52 (2006) 839-846.
[28] X.L. Zhang, Z.H. Jiang, Z.P. Yao, Y. Song,Z.D. Wu, Effects of scan rate on the potentiodynamicpolarization curve obtained to determine the Tafelslopes and corrosion current density, CorrosionScience. 51 (2009) 581-587.
[29] 曹楚南,張鑒清,電化學阻抗譜導論,北京,科學出版社,2002 年 7 月[30] C.N. Cao, On the impedance plane displays forirreversible electrode reactions based on the stabilityconditions of the steady-state—I. One state variablebesides electrode potential, Electrochimica Acta. 35(1990) 831-836.
[31] C.N. Cao, On the impedance plane displays forirreversible electrode reactions based on the stabilityconditions of the steady-state—II. Two state variablesbesides electrode potential, Electrochimica Acta. 35(1990) 837-844.
[32] Y.Y. Shi, Z. Zhang, F.H. Cao, J.Q. Zhang,Dimensional analysis applied to pitting corrosionmeasurements, Electrochimica Acta. 53 (2008) 2688-2698.
[33] Y. Xia, P. Liu, J.Q. Zhang, F.H. Cao,Corrosion Behavior of Weathering Steel Under ThinElectrolyte Layer at Different Relative Humidity,Journal of Materials Engineering and Performance. 27(2018) 202-218.
[34] Y.M. Kolotyrkin, Effect of anions on thekinetics of the dissolution of metals, Russian ChemicalReviews. 31 (1962) 160-167.
[35] J.M. Kolotyrkin, Effects of Anions on theDissolution Kinetics of Metals, Journal of theElectrochemical Society. 108 (1961) 209-216.
[36] V. Jovancicevic, J.O. Bockris, The Mechanismof Oxygen Reduction on Iron in Neutral Solutions,Journal of the Electrochemical Society. 133 (1986)1797-1807.
[37] 董俊華 , 宋光鈴 , 林海潮 , 曹楚南 , 硫酸中硫脲影響鐵腐蝕行為的機制 , 中國腐蝕與防護學報 . 16 (1996) 53-58.
[38] 高延敏 , 王紹明 , 徐永祥 , 吳維– , 文山 , A3 鋼在乙酸中的腐蝕行為和機理 , 腐蝕與防護 . 27 (2006) 11-13.
[39] A.J. Bard, F.R.F. Fan, D.T. Pierce, P.R.Unwin, D.O. Wipf, F.M. Zhou, Chemical Imagingof Surfaces with the Scanning ElectrochemicalMicroscope. Science. 254 (1991) 68-74.
[40] D. Polcari, P. Dauphin-Ducharme, J. Mauzeroll,Scanning Electrochemical Microscopy: A ComprehensiveReview of Experimental Parameters from 1989 to 2015.Chemical Reviews. 116 (2016) 13234-13278.
[41] C.G. Zoski, Review-Advances in ScanningElectrochemical Microscopy (SECM)。 Journal of theElectrochemical Society. 163 (2016) H3088-H3100.
[42] Q.H. Zhang, Z.N. Ye, Z.J. Zhu, X.Y. Liu,J.Q. Zhang, F.H. Cao, Separation and kinetic studyof iron corrosion in acidic solution via a modifiedtip generation/substrate collection mode by SECM,Corrosion Science. 139 (2018) 403-409.
[43] Q.H. Zhang, P. Liu, Z.J. Zhu, Z.N. Ye,J.Q. Zhang, F.H. Cao, X.G. Li, Quantitativeanalysis of the polarization behavior of iron in anaerated acidic solution using SECM, ElectrochemistryCommunications. 93 (2018) 143-147.
免責聲明:本網(wǎng)站所轉(zhuǎn)載的文字、圖片與視頻資料版權歸原創(chuàng)作者所有,如果涉及侵權,請第一時間聯(lián)系本網(wǎng)刪除。

官方微信
《腐蝕與防護網(wǎng)電子期刊》征訂啟事
- 投稿聯(lián)系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 腐蝕與防護網(wǎng)官方QQ群:140808414





