仇銀燕1,2,朱華1,林安1 ,汪的華1,*
1、武漢大學(xué)資源與環(huán)境科學(xué)學(xué)院,武漢 430072
2、中南林業(yè)科技大學(xué)林學(xué)院,長(zhǎng)沙 410004
* 聯(lián)系人Email:wangdh@whu.edu.cn
仇銀燕,中南林業(yè)科技大學(xué)林學(xué)院講師,碩士。1977年11月生于湖南省邵陽(yáng)市。2002年畢業(yè)于武漢大學(xué)環(huán)境科學(xué)專業(yè)。現(xiàn)主要從事環(huán)境科學(xué)的教學(xué)與研究工作,參與環(huán)境保護(hù)部公益項(xiàng)目研究1項(xiàng)。

仇銀燕
摘要:硅酸鹽、稀土金屬鹽和殼聚糖都是對(duì)環(huán)境友好的化合物,本文采用電化學(xué)方法研究了稀土鈰鹽與硅酸鹽、稀土鈰鹽與殼聚糖、稀土鈰鹽與硅酸鹽及殼聚糖組成的復(fù)合體系對(duì)鋅的鈍化作用及其防護(hù)性能。結(jié)果表明,硅酸鹽和稀土鈰鹽、稀土鈰鹽和殼聚糖的復(fù)合體系均能在鋅表面形成耐蝕性較好的鈍化膜,表現(xiàn)出緩蝕協(xié)同效應(yīng)。
關(guān)鍵詞:鍍鋅層;鈍化;協(xié)同緩蝕;殼聚糖;稀土
1 引言
鍍鋅是鋼鐵構(gòu)(零)件最重要的防護(hù)性鍍層之一,鍍后的鈍化處理是進(jìn)一步提高其耐蝕性的重要途徑。由于傳統(tǒng)的鉻酸鹽鈍化環(huán)境污染嚴(yán)重,其應(yīng)用受到嚴(yán)格的限制,環(huán)境友好的無(wú)鉻鈍化技術(shù)的研發(fā)非常緊迫[1-3]。硅酸鹽是沉淀型緩蝕劑,在溶液中,帶負(fù)電荷的SiO32-或SiO2膠團(tuán)與溶解下來(lái)的金屬離子結(jié)合形成保護(hù)膜覆蓋在金屬表面[4]。稀土金屬鹽通過(guò)在材料表面形成含稀土的氧化物和氫氧化物轉(zhuǎn)化膜,阻滯氧的擴(kuò)散和電子傳遞。[5-6殼聚糖則可能形成CS-Zn(Ⅱ)絡(luò)合物[7]。三者的成膜機(jī)理各不相同。目前,僅靠單一組分形成的鈍化膜或化學(xué)轉(zhuǎn)化膜的耐蝕性能均遠(yuǎn)遜于鉻酸鹽鈍化體系,發(fā)揮它們各自的長(zhǎng)處組成復(fù)合鈍化體系是探索高性能無(wú)鉻鈍化體系的方向。在本實(shí)驗(yàn)中,試圖將硅酸鹽、稀土鈰鹽和殼聚糖組成新的復(fù)合鈍化體系,探討它們對(duì)金屬鋅的協(xié)同緩蝕作用,以開(kāi)發(fā)環(huán)境友好的鈍化技術(shù)。
資助信息:本項(xiàng)目受到中國(guó)教育部新世紀(jì)優(yōu)秀人才支持計(jì)劃(NCET-08-0416)和中央高校自主科研項(xiàng)目資助。
2 實(shí)驗(yàn)
2.1 材料與試劑
0.1mol/L Ce(NO3)3,0.1mol/L Na2SiO3,3%NaCl溶液,粉狀殼聚糖(CS),D.D≥90%,用鹽酸(0.1mol/L)溶解CS配成溶液,30% H2O2。試液用二次蒸餾水配制。
2.2鋅電極的鈍化
本工作實(shí)驗(yàn)了三種典型的復(fù)合鈍化體系和工藝,作為比較,同時(shí)也進(jìn)行了三種單組分體系的鈍化實(shí)驗(yàn),具體操作如下所述。
Ce1:將鋅電極放入pH=4、約30℃的0.1mol/L的Ce(NO3)3 中4-5min,加入適量H2O2促進(jìn)成膜;將成膜的鋅電極再放入0.1mol/L Na2SiO3 中5min,溫度60-70℃。取出后,用蒸餾水沖洗,在60℃烘箱老化15min,常溫下冷卻。
Ce2:鈍化液:0.1mol/L Ce(NO3)3 35ml;0.05mol/L CS 1-5ml;H2O2少量;pH3-5,溫度約30℃。將鋅電極浸入5min。取出后,用蒸餾水沖洗,在60℃烘箱老化15min,常溫下冷卻。
Ce3:將鋅電極放入含0.067mol/L Ce(NO3)3和0.02mol/L CS的溶液中 4-5min,加入H2O2促進(jìn)成膜,溶液pH 3-4,溫度約30℃;將成膜的鋅電極再放入0.1mol/L Na2SiO3中5min,溫度60-70℃。取出后,用蒸餾水沖洗,在60℃烘箱老化30min,常溫下冷卻。
單一的鈰鹽鈍化:鈍化液:0.1 mol/L Ce(NO3)3溶液;H2O2少量;pH值3-4。溫度約30℃,將鋅電極放入,時(shí)間3-5min。鈍化后,用蒸餾水沖洗,在60℃烘箱老化15min,常溫下冷卻。
鉻酸鹽鈍化:鈍化液:Cr2O3 3-5 g/L;濃硫酸 0.6-0.9 ml/L;濃硝酸 0.4-0.7 ml/L。溫度為室溫,將鋅電極放入,時(shí)間30-60S。鈍化后,用蒸餾水沖洗,在60℃烘箱老化10-15min,常溫下冷卻。
硅酸鹽鈍化:鈍化液:Na2SiO3·9H2O 90g/L,硫酸適量,30%H2O2 100ml/L,pH2-4,室溫,時(shí)間1min。
2.3 電化學(xué)測(cè)量
電化學(xué)測(cè)量在30±2℃下進(jìn)行,電解液為中性的3%NaCl溶液。工作電極為純鋅,飽和甘汞(SCE)為參比電極,鉑片為輔助電極,交流阻抗測(cè)定的頻率范圍100k Hz-10m Hz,電位幅值5mV。測(cè)量?jī)x器為CHI660電化學(xué)工作站。
3 結(jié)果與討論
在中性NaCl 溶液中,鋅的腐蝕過(guò)程包括鋅的陽(yáng)極溶解和氧的陰極還原。
Zn → Zn2+ + 2e
O2 + 2H2O +4e → 4OH-
溶解的Zn2+和OH-生成Zn(OH)2沉淀在鋅的表面,并轉(zhuǎn)化為鋅的氧化物ZnO,形成鈍化膜,
Zn2++OH-→ Zn(OH)2→ZnO+H2O
有Cl-存在時(shí),氫氧化鋅與Cl-反應(yīng)生成可溶解的化合物Zn-Cl-OH,破壞鈍化膜導(dǎo)致腐蝕。
3.1 硅酸鹽與鈰鹽復(fù)合鈍化
鋅電極按Ce1配方和工藝進(jìn)行鈍化后,測(cè)量得到的交流阻抗譜示于圖1,為了比較,對(duì)未經(jīng)鈍化和經(jīng)鈰鹽、鉻酸鹽單組分鈍化后測(cè)得的結(jié)果一并列于圖1中。
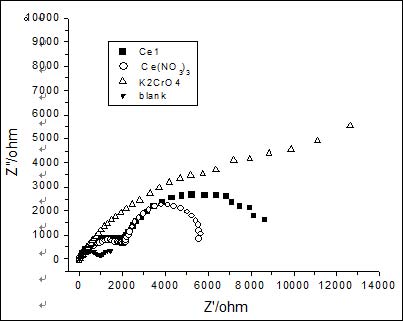
圖1 鉻酸鹽、鈰鹽、鈰硅復(fù)合鹽鈍化的鋅電極在3%NaCl溶液中的交流阻抗譜#p#副標(biāo)題#e#
鋅在含Na2SiO3溶液中,表面形成含鋅的氫氧化物和硅酸鹽膜[8],對(duì)鋅的陽(yáng)極和陰極過(guò)程都有抑制作用。鋅在含鈰鹽溶液中,陰極區(qū)氫和氧的還原導(dǎo)致局部pH升高,當(dāng)pH達(dá)一定值時(shí),鈰的氫氧化物或氧化物便沉積在鋅的表面,形成鈰的轉(zhuǎn)化膜[8]。
2Ce3+ + 6OH-→ 2Ce(OH)3 → Ce2O3 + 3 H2O
H2O2的加入,加速了成膜反應(yīng),部分Ce3+被氧化成Ce4+,使膜呈黃色,
2Ce3+ +H2O2 → 2Ce4+ + OH-
表面形成的少量 Zn[OH]與鈰的水合物或氫氧化物反應(yīng)而生成H+,使轉(zhuǎn)化膜中含有H+。在Na2SiO3溶液中,SiO32-與這些H+中和并沉積在鈰的氧化物膜的缺陷處起封閉作用,膜更穩(wěn)定。
成膜后的鋅電極在中性NaCl溶液測(cè)得的阻抗譜是雙容抗弧,一個(gè)與鈍化膜的的電阻、電容有關(guān),出現(xiàn)在高頻端,另一個(gè)與反應(yīng)電阻及雙電層電容有關(guān),出現(xiàn)在低頻端。而鉻酸鹽鈍化膜表現(xiàn)為單容抗弧特征。擬合的電路參數(shù)見(jiàn)表1。由表中數(shù)據(jù)可見(jiàn),稀土和硅酸鹽復(fù)合鈍化層電極反應(yīng)阻抗是單純稀土鹽鈍化的1.6倍,耐蝕性有很大的提高,但離鉻酸鹽鈍化還有較大的距離,需要進(jìn)一步優(yōu)化配方和工藝條件。
表1 自然腐蝕電位下阻抗譜的等效電路參數(shù)
| 鈍化體系 | Cf (μF) | n1 | Rf (kΩ) | Rt (kΩ) | Cd (μF) | n2 |
| Ce1 | 43.2 | 0.740 | 2.65 | 6.01 | 432.0 | 0.952 |
| Ce(NO3)3鈍化 | 15.9 | 0.659 | 2.48 | 3.70 | 203.4 | 0.980 |
| Blank | 37.4 | 0.740 | 0.98 | 0.91 | 6.21×103 | 0.756 |
| K2CrO4鈍化 | 18.8 | 248.0 | 0.607 |
3.2 稀土與殼聚糖復(fù)合鈍化
將0.1mol/L Ce(NO3)3和0.05mol/L 殼聚糖以不同體積比混合,分別對(duì)鋅電極進(jìn)行處理,測(cè)得成膜后的鋅在自然腐蝕電位下的阻抗譜如圖2。可見(jiàn),隨著混合液中殼聚糖的量不同,所形成的膜的耐蝕性也有差別。成膜后的鋅電極的阻抗譜也呈雙容抗弧特征,擬合后的電路參數(shù)列于表2。
當(dāng)Ce(NO3)3和殼聚糖以2:1的體積比混合,即濃度分別為0.07和0.017mol/L時(shí),具有最好的耐蝕效果,反應(yīng)電阻是單純鈰鹽中鈍化的2.9倍。稀土鈰為鑭系元素,含有未充滿的4f電子,殼聚糖的氨基和羥基都含有孤對(duì)電子,容易與稀土離子絡(luò)合。在金屬——溶液界面,除生成鈰的氧化物和氫氧化物膜外,殼聚糖分子也能吸附在表面,并與Zn2+、Ce3+形成絡(luò)合物,進(jìn)一步提高了膜的致密性,從而增加了膜的耐蝕性。
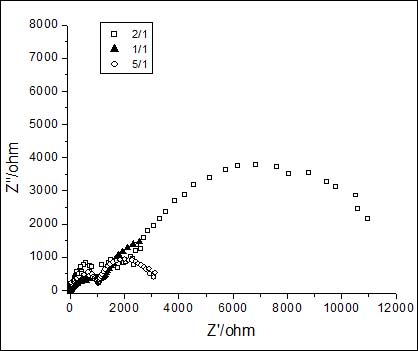
圖2 不同配比的鈰鹽與殼聚糖溶液中鈍化的鋅電極在3%NaCl溶液中的交流阻抗譜
表2 鈰鹽與殼聚糖復(fù)合液中鈍化處理后EIS圖譜的等效電路參數(shù)
| Ce/CS (體積比) |
Cf (μF) | n1 | Rf (kΩ) | Rt (kΩ) | Cd (μF) | n2 |
| 1:1 | 50.5 | 0.560 | 1.43 | 4.12 | 456.5 | 0.829 |
| 5:1 | 15.6 | 0.827 | 1.16 | 2.01 | 879.0 | 0.951 |
| 2:1 | 15.7 | 0.717 | 1.84 | 10.6 | 219.0 | 0.700 |
3.3 硅酸鹽、鈰鹽、殼聚糖三元復(fù)合鈍化體系研究
根據(jù)對(duì)SEM結(jié)果的觀察,三元復(fù)合鈍化后,鋅表面的轉(zhuǎn)化膜從外觀上與硅酸鹽和鈰鹽復(fù)合鈍化差不多,在稀土膜的表面均勻覆蓋著一層硅酸鹽沉淀;單純的鈰鹽轉(zhuǎn)化膜由厚度不均的基膜和附著其上的不同形狀和大小的微粒組成。從測(cè)得的交流阻抗譜看,反應(yīng)電阻與硅酸鹽和鈰鹽復(fù)合液鈍化相當(dāng),而小于鈰鹽和殼聚糖復(fù)合液,鈍化效果沒(méi)有明顯提高,需要進(jìn)一步優(yōu)化。
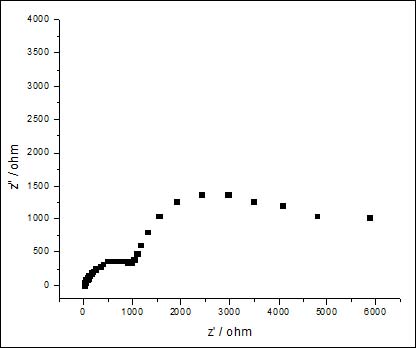
圖3 鈰鹽、硅酸鹽和殼聚糖復(fù)合液鈍化鋅電極在3%NaCl溶液中的交流阻抗譜
4 結(jié)論
鋅在硅酸鹽和鈰鹽復(fù)合液中形成的鈍化膜表現(xiàn)出了較好的耐蝕性,二者的復(fù)合優(yōu)于單組分鈍化;鈰鹽和殼聚糖復(fù)合液的鈍化,能提高膜的致密性,具有很好的耐蝕效果;對(duì)于鈰鹽、硅酸鹽和殼聚糖三元體系,與硅酸鹽和鈰鹽復(fù)合液鈍化效果差不多,有待進(jìn)一步深入研究。
參考文獻(xiàn)
[1] 陳錦虹,盧錦堂,許喬瑜等,鍍鋅層上有機(jī)物無(wú)鉻鈍化涂層的耐蝕性,材料保護(hù),2002,35(8):29-31.
Chen J H, Lu J T, Xu Q Y, Corrosion resistance of organic chromate-free passivation coating for galvanized steel [J]. Materials Protection. 2002, 35(8):29-31 (in Chinese)
[2] 劉艷榮,周婉秋,趙強(qiáng)等,鍍鋅板表面無(wú)鉻鈍化的研究進(jìn)展,電鍍與精飾,2010,32(4):22-26.
Liu Y R, Zhou W Q, Zhao Q, Advances on surface non-chromium passivation of galvanized steel plate [J], Plating & Finishing, 2010,32(4):22-26. (in Chinese)
[3] 章江洪,張英杰,閆磊等,鍍鋅產(chǎn)品無(wú)鉻鈍化技術(shù)研究進(jìn)展, 材料保護(hù), 2009, 42(3):49-57.
Zhang J H, Zhang Y J, Yan L, Progress in Research on Chromium-Free Passivation of Galvanized Wares [J], Materials Protection, 2009, 42(3):49-57 (in Chinese)
[4] 董鵬,張英杰,鋅鍍層硅酸鹽鈍化膜的耐腐蝕性能,材料保護(hù), 2010, 43(10):5-8.
Dong P, Zhang Y J, Corrosion resistance of silicate passivation film on electro-deposited zinc coating [J], Materials Protection, 2010, 43(10):5-8 (in Chinese)
[5] Bethenourt M, Botana F J, et al. Lanthanide compounds as environmentally friendly corrosion inhibitors of aluminium allors: a review. Corr. Sci., 1998, 40(11): 1803-1819.
[6] Arenas M A etal. Growth mechanisms of cerium layers on galvanized steel [J]. Electrochemical Acta, 2003, 48(24):3693-3698.
[7] Manov S, Lamazouere A M, Aries L, Electrochemical study of the corrosion behavior of zinc treated with a new organic chelating inhibitor. Corr. Sci., 2000, 42: 1235-1248.
[8] Aramaki K., The inhibition effects of chromate-free, anion inhibitors on corrosion of zinc in aerated 0.5M NaCl. Corr. Sci., 2001, 43(3): 591-604.
[9] Aramaki K., Treatment of zinc surface with cerium(III) nitrate to prevent zinc corrosion in aerated 0.5M NaCl. Corr. Sci., 2001, 43(11): 2201-2215.

官方微信
《中國(guó)腐蝕與防護(hù)網(wǎng)電子期刊》征訂啟事
- 投稿聯(lián)系:編輯部
- 電話:010-62313558-806
- 郵箱:fsfhzy666@163.com
- 中國(guó)腐蝕與防護(hù)網(wǎng)官方QQ群:140808414




