
所謂腐蝕
腐蝕是指材料與環境間發生的化學或電化學相互作用而導致材料功能受到損傷的現象。
腐蝕電池
在大多數情況下,當金屬被放置在水溶液中或潮濕的大氣環境中時,金屬表面會形成一種微電池,有時也稱腐蝕電池(其電極一般稱為陰、陽極)。
在陽極上發生氧化反應,使陽極發生溶解,在陰極上則發生還原反應,一般只起傳遞電子的作用。
形成原因
腐蝕電池的形成原因主要是由于金屬表面吸附了空氣中的水分,形成了一層水膜,因而使空氣中CO?、SO2和NO2等氣體溶解在這層水膜中,形成電解質溶液,而浸泡在這層溶液中的金屬又總是不純的,例如工業上用的鋼鐵,其實際上是合金材料,即除鐵之外,還含有石墨、滲碳體(Fe3C)以及一些其它的金屬和雜質,它們大多數沒有鐵元素活潑。這樣形成的腐蝕電池的陽極為鐵,而陰極為雜質,又由于鐵與雜質緊密接觸,使得腐蝕不斷進行。
發生腐蝕作用期間,來自金屬表面不同區域的電子在具有導電功能的氛圍中流動到其他區域,這是較為簡單的化學腐蝕。不同的電化學腐蝕對于材料所造成的影響也不盡相同。
可怕的腐蝕!!!
事實上,因為腐蝕而造成的經濟損失遠遠大于許多人的認知。據CC Technologies Laboratories Inc.在2001年做出的一項研究報道稱:僅在美國,腐蝕成本每年就高達2760億美元,其中,用于管理腐蝕的費用為1210億美元,而剩余的1550億美元是則對經濟造成的凈損失。公共事業,特別是水管和下水道系統受到的經濟損失最大,其次為機動車輛和運輸行業。
由于金屬腐蝕是一個持續的電化學過程,因此了解電化學反應的本質特性至關重要,這將有助于技術人員合理的抑制腐蝕并減少其對結構的影響。
今天我們就將先為大家介紹涉及腐蝕的三類化學反應
電化學反應
丹尼爾電池
陽極反應
什么是腐蝕電化學?
在水性環境和大氣環境中發生的腐蝕本質上是一種電化學反應,是由于電子在金屬表面和液體電解質溶液之間互相轉移而造成的,通常會導致基板材料性能的劣化。
腐蝕發生是因為金屬與氧氣、水和大氣中的其他物質發生電化學反應的傾向很大。在這種情況下,術語“陽極”用于表示真正腐蝕的金屬表面部分,而“陰極”則用于表示消耗由腐蝕反應產生的電子的金屬表面。
研究電化學反應腐蝕方面的早期先驅學者Ulick R. Evans說,腐蝕可以被理解為由于發生電化學反應而造成的破壞現象。因此,腐蝕電化學只是一種電化學反應,通過它人們可以更好的了解腐蝕的機理。
電化學反應
電化學反應被概述為涉及到電子轉移的反應。此外,這也是一個涉及氧化和還原的反應。
腐蝕一般由至少一個化學反應以及一個并不完全明顯的還原反應組成,不過這兩個反應經常會在一片金屬(例如鋅)中結合在一起發生,如下圖所示。
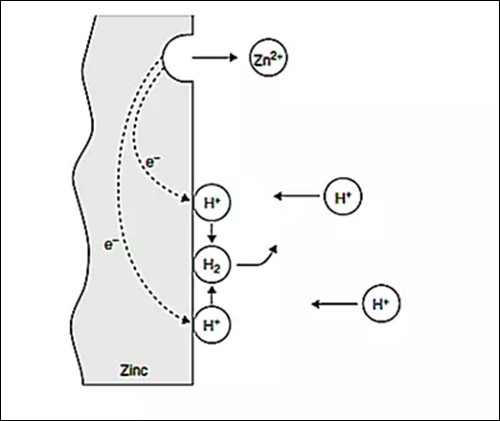
圖1:在無空氣鹽酸溶液中鋅腐蝕過程中發生的電化學反應
在圖1中,浸入到酸溶液中鋅片(Zn)正在經歷腐蝕。在其表面上的某一點,Zn失去電子轉變為Zn離子,這些電子穿過固體導電金屬到金屬表面上的其他區域,這些區域上的氫(H)離子通過得到電子被還原成氫氣,方程式如下:

這些方程式很好的闡釋了鋅片中電化學反應的特征。通過這樣一個反應,電子經歷了失去和得到兩個過程,伴隨而來的氧化反應與還原反應則一起發生。
![]()
因此,在電化學中,陽極和陰極反應同時發生并以相同的速率進行。但是,腐蝕現象僅在作為陽極的區域中發生。
丹尼爾電池和電化學腐蝕
1什么是丹尼爾電池
丹尼爾電池就是將Zn(鋅)置于ZnSO4(硫酸鋅)溶液中,將Cu(銅)置于CuSO4(硫酸銅)溶液中,并用鹽橋或離子膜等方法將兩種電解質溶液連接的一種原電池。該電池是最早一批具有高敏感性及可靠性的電池,支撐著19世紀許多的工業應用創新,例如電報等。
2丹尼爾電池的原理
丹尼爾電池的原理也屬于一種電化學反應,電子從腐蝕的鋅片上經過導電途徑(例如鹽橋等)轉移到銅上并形成電流(想進一步了解丹尼爾電池,可以參考一篇介紹Alexander電池的文章,因為該兩種電池具有類似的腐蝕機理。
鋅片比銅片更加容易失去電子,這也就意味著將鋅片和銅片置于其各自的電解質溶液中(硫酸鋅和硫酸銅)時,電子能夠從外界導電線發生轉移,其發生的電化學反應如下圖所示:
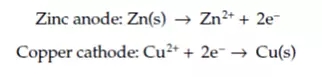
這兩種金屬之間的腐蝕電位差異通常會導致一種被稱為原電池腐蝕(galvanic腐蝕,為了紀念其發現者Luigi Galvani而命名)的情況。
這種情況在自然腐蝕電池中是非常常見的,尤其是當腐蝕電池處于電解質環境中時。液體氣氛如土壤,混凝土以及水的傳導通常都與金屬材料的腐蝕性相關。
下列等式中的描述方程對于每個丹尼爾電池配置都是有效的。該方程將鋅電極鑒定為陽極,而銅由于帶有正電荷而作為陰極。
![]()
陽極反應和腐蝕
現在我們詳細介紹一下發生腐蝕時(陽極反應)在陽極上將發生的情況。例如,鐵的腐蝕反應,該反應就涉及到將氫離子還原為氫氣這一過程,這與鋅在鹽酸中的電化學反應一致。
這種析氫反應通常會發生在各種金屬和酸性溶液組成的體系中,包括鹽酸、硫酸、高氯酸、氫氟酸、甲酸和其他酸等。鐵,鎳和鋁的單獨陽極反應如下圖所示:

我們可以通過觀察上述等式寫出腐蝕過程中發生的一般陽極反應:
![]()
也就是說,金屬“M”的腐蝕導致金屬“M”與價電荷為n+的離子發生化學反應,從而導致“n”電子被釋放。n的具體數值當然取決于金屬材料本身的性質。一般金屬,例如銀,是一價的,而多價鐵,鈦和鈾等金屬則具有高達+6的正電荷。
該方程式是根據許多情況總結出來的,幾乎適用于所有的金屬腐蝕反應。
今天的主角團就是以下三位
法拉第定律
陰極反應
表面積影響
法拉第定律和腐蝕電化學
如果由前面提及的陽極反應所產生的電流是已知的,則可以使用Michael Faraday發現的有效關系式將該電流轉換成類似的質量損失或腐蝕滲透率。
法拉第的電解實驗規律巧妙的將電化學反應中的電流與被反應元素的摩爾數進行了關聯。
假設這種反應中每個離子需要得到一個電子,就像電鍍銀或者銀的腐蝕情況一樣,可以表示為如下方程式:
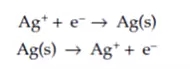
根據法拉第定律,與1摩爾銀發生反應將需要1摩爾的電子,或者說是一個阿伏伽德羅的電子數(6.022×1023)。1摩爾電子攜帶的電荷被定義為一法拉第(F)。1法拉第約等于96485C/(摩爾電子)。
將法拉第的主要參數與特定電化學反應中公認的化學計量學相結合,就可以得出以下等式:

其中,N代表摩爾數,△N代表摩爾數的變化值,n是每分子被反應物質的電子數,I代表總電流(安培,A),t則代表電化學反應的時間(秒,s)。
陰極反應
當氫(H)離子被還原時,正如前面所述,它們通常會與陰極表面的電子反應生成氫氣。在陰極表面的這種氫離子的還原可能會干擾酸性氫(H+)離子和形成堿的羥基(OH-)離子之間的平衡,使得該溶液在該區域中酸性較弱,或者呈現出更強的堿性。
在中性水中,一些金屬(例如鋁、鋅和鎂等)的陽極腐蝕會產生足夠的能量來直接對水進行電離,方程式如下圖所示:
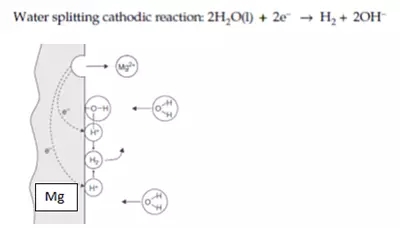
圖2:Mg在中性水中發生腐蝕時的電化學反應
氫離子濃度的變化或羥基(OH)離子濃度的增加可以通過測試體系的pH值來衡量,進而明確發生的是哪種陰極反應。在整個腐蝕過程中會發生許多陰極反應,主要包括以下這些:
氧氣還原就是其中一種常見的陰極反應,因為氧氣存在于大氣中以及暴露于環境的溶液中。
此外,雖然金屬離子還原和金屬沉積現象發生的不是很頻繁,但金屬離子還原和金屬沉積會引起非常嚴重的腐蝕問題,因此同樣需要注意。
所有的腐蝕反應僅僅是一個或多個上述陰極反應與陽極反應的組合。因此,在大多數情況下,無論是單獨的還是組合的,每種液體腐蝕的情況都可以歸納成上述那些方程式。
考慮到水或濕空氣容易對鋅金屬造成腐蝕,所以以鋅為例,通過將Zn發生腐蝕的氧化反應乘以2并將其與氧還原反應相加,可以得到以下等式:
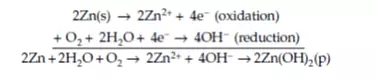
該反應的產物是Zn2+和OH-,這兩者會立即發生反應生成不溶的Zn(OH)2。同樣地,硫酸銅中的Zn的腐蝕方程式如下列等式所示,簡單而言就是Zn的氧化反應與涉及銅(II)離子的金屬沉積反應的總和:

在發生腐蝕反應過程中,有時可能會發生不止一次的氧化和還原反應。
例如在含有溶解氧的濃縮型鹽酸溶液中的Zn腐蝕,就可以進行兩次陰極反應。一個是氫離子的變化,另一個則是氧的還原反應。
由于存在兩種消耗電子的陰極反應,所以鋅的一般腐蝕速率將大大增加。因此,這種溶液通常比無空氣酸溶液更容易發生腐蝕現象,從酸性溶液中除去氧氣通常可以使這些溶液的腐蝕性降低。這也是在許多環境中降低腐蝕性的典型方法。產生的氧氣則可以通過化學或一些機械方式排出。
表面積的影響
一塊金屬材料發生腐蝕時,在陽極區域產生的電子會流過金屬在陰極區域發生反應,這些陰極區域暴露在同樣的環境中,這些環境有助于維持系統的整體電荷平衡。
在腐蝕表面上沒有電荷累積的事實對于理解大多數腐蝕過程和開發出相應減輕腐蝕的方法至關重要。然而,利用以下等式表示的陽極和陰極電流之間的電荷相等卻并不意味著這些電流的電流密度也是相等的:

通過獲取相對陽極(Sa)和陰極(Sc)的表面積(以及以mA/cm2為單位表示的相關電流密度ia和ic),該方程還可以利用電流密度表示為如下形式:
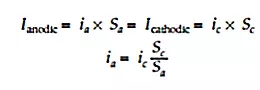
上述方程式中的表面積比(Sc / Sa)對點腐蝕和應力腐蝕開裂等幾種局部腐蝕具有重要的參考意義。此外,該值大小對于異種金屬的腐蝕發生也有很大的影響。
我們很容易知道,集中在金屬表面一小塊面積上的陽極電流大小將比在一塊更大面積區域上的電流值大得多。當Sc / Sa比值大于1時,這將是一個重要的陽極電流放大相關問題,當該比值小于1時,則是一個不利的因素。
當將兩個不同的金屬連接(這里是Cu和Fe)時,就可以看到電流密度不等的原因,如圖3中所示:
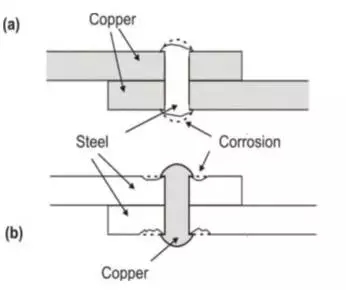
圖3
受不同金屬影響的區域
“a”表示銅板上的鋼鉚釘
“b”表示鋼板上的銅鉚釘
當鋼鉚釘是銅板上的一部分時,陰極銅板的腐蝕將很小,而小區域陽極鋼鉚釘的腐蝕程度將很高。另一方面,如果銅鉚釘接合鋼板,則銅的腐蝕性將會很高,而鋼板的腐蝕則不怎么明顯。
腐蝕預防
在這篇文章中,我們研究了導致許多材料/結構劣化的電化學腐蝕現象。只有充分了解電化學腐蝕的原因和機理,我們才可以更好的防止腐蝕,因此,腐蝕產品的制造商和使用者應該多加注意腐蝕背后的電化學機制。這將為工業上有效控制腐蝕現象的發生以及制備出具有高度抗腐蝕產品提供巨大的指導意義。
更多關于材料方面、材料腐蝕控制、材料科普等方面的國內外最新動態,我們網站會不斷更新。希望大家一直關注中國腐蝕與防護網http://www.ecorr.org
責任編輯:王元
投稿聯系:編輯部
電話:010-62313558-806
中國腐蝕與防護網官方 QQ群:140808414
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《中國腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護網官方QQ群:140808414





