根據中國海洋局公布的《2016 年中國海洋經濟統計公報》,2016 年全國海洋生產總值達到7 萬多億元,占國內生產總值的9.5%,航運業以及海洋相關產業已經成為當今經濟發展的重要支柱。海洋腐蝕是海洋工程面臨的重大難題,世界腐蝕組織(WorldCorrosion Organization,WCO)估計每年海洋腐蝕損失約為0.8 萬億美元,占到全球腐蝕總量(2.4 萬億美元)的1/3,高于所有自然災害損失的總和。
海洋腐蝕在造成大量經濟損失的同時,還會引起嚴重的人員安全與環境污染問題,英國曾報道“亞歷山大基定號”海洋平臺樁腿焊縫因海水腐蝕形成裂紋,在海浪的反復作用下裂紋不斷擴大,最終平臺傾倒并造成123 人遇難。美國海域發生過的最嚴重的油污染就是因為“深水地平線”鉆井平臺海底閥門受海水腐蝕而失效爆炸,導致3 個月內約400 萬桶原油泄漏入海。我國海洋腐蝕研究起步較晚,目前多數海洋工程結構物與載體處于欠防護狀態,腐蝕損失巨大且安全堪憂,海洋腐蝕已成為我國海洋經濟大發展中必須攻克的關鍵問題。
海洋環境下金屬材料的腐蝕包括電化學腐蝕和污損生物腐蝕,每年海洋金屬材料因腐蝕而造成的損失中,約有20%是由微生物腐蝕引起的。微生物在金屬表面的腐蝕還會與磨損、氣蝕、沖蝕等因素協同,導致材料表面快速剝落,使包括船舶與海洋平臺在內的海洋設施的可靠性面臨嚴重威脅。參與微生物腐蝕過程的包括真菌和藻類,以及各種類型的細菌。船舶船體、甲板、上層建筑、艙壁中大量使用的碳鋼,常用作海水管系、熱交換器、螺旋槳材料的銅合金以及在海洋平臺中廣泛應用的各種不銹鋼,都不同程度地受到各類微生物的腐蝕而失效。因此,研究海洋微生物對金屬材料的腐蝕機理,對提高船舶與海洋平臺的壽命,增強服役安全性和可靠性具有重要意義。
1 海洋環境下的微生物腐蝕
1.1 微生物腐蝕概述
微生物腐蝕(Microbiological Induced Corrosion,MIC)是指金屬或非金屬表面因微生物的生命活動而受到的腐蝕破壞。海洋中的微生物接觸到金屬表面,分泌出胞外多糖(Exopolysaccharides)與金屬表面粘附的有機物、無機物,甚至直接與金屬基體發生反應,進一步形成胞外聚合物( Extracellular PolymericSubstances,EPS),細菌與EPS 一起附著于金屬表面,形成生物膜。浸沒在海水中的金屬材料在數小時內就會覆蓋一層生物膜,這層膜由各種細菌和微藻類以及它們的代謝產物組成,是發生微生物腐蝕的先決條件。生物膜內部的pH 值、溶解氧(Dissolved Oxygen,DO)、離子濃度與有機物含量等都與海水中有很大差異。金屬材料與生物膜直接接觸,微生物的代謝活動控制著金屬表面電化學反應的類型與速率。
海洋中的微生物種類繁多,具有腐蝕能力的海洋細菌大多是鐵、硫等元素循環過程的參與者,并改變金屬表面的陰、陽極反應過程。根據細菌種類和代謝特點,可以將海洋中主要的腐蝕性細菌分為硫酸鹽還原菌(Sulfate-reducing bacteria,SRB)、鐵氧化細菌(Iron-oxidizing Bacteria,IOB)、鐵還原細菌(IronreducingBacteria,IRB)、產酸菌(Acid-producingBacteria,APB)與產粘液菌(Slime-producing Bacteria,SPB)等,其中SRB 被認為是主要的腐蝕菌種,由它引起的金屬材料腐蝕損失更是達到了微生物腐蝕損失的50%以上。
SRB 是在厭氧過程中占據主導地位的腐蝕菌種,有文獻報道SRB 在非嚴格厭氧的環境下也可存活,所以SRB 也被認為是一種兼性厭氧菌[7]。最常見的SRB 包括脫硫弧菌屬(Desulfovibrio sp.)與脫硫腸狀菌屬(Desulfotomaculum sp.),由于SRB 的作用,硫酸根離子被還原為S2-,進而在鐵基金屬表面留下典型的腐蝕產物FexS。SRB 是異養菌,可直接從金屬基體獲得電子以維持自身生命活動。IOB 能將亞鐵離子(Fe2+)氧化為鐵離子(Fe3+),并生成Fe(OH)3 沉淀,在金屬表面產生氧濃差電池,引起局部腐蝕。IRB與IOB 相反,它將Fe3+還原為Fe2+,并進一步破壞金屬表面的鈍化膜以造成腐蝕[8]。SPB 通常是好氧的異養菌,常見的有假單胞菌(Pseudomonadaceae)與芽孢桿菌(Bacillaceae),其中Pseudomonadaceae 可以利用烴類作為能量來源,新陳代謝產生有機酸,并因此影響金屬的腐蝕過程,生長旺盛時分泌大量的EPS并引起管路腐蝕、堵塞等問題。
1.2 船舶涉及的微生物腐蝕
嚴新平等將船舶摩擦分為外摩擦和內摩擦,MIC 與船舶的內、外摩擦均存在不同程度的協同作用。航行于海洋中的船體表面直接與海水接觸,會有大量污損生物附著。楊宗澄等[11]調查了船舶表面生物污損情況,發現某些散貨船的污損率可達到50%以上。多數船舶表面有防污漆保護,可以在一定程度上防止腐蝕。但大型污損生物,如藤壺等的長期附著,會破壞船殼表面的保護層,微生物迅速在船體表面破損處大量繁殖,使其表面產生脆弱的腐蝕產物層,受到海水沖刷時極易剝落,暴露出金屬基體,從而加劇船體的外摩擦損失。Zarasvand 等從船體底部存在點蝕與黑色腐蝕產物的典型銹蝕部位取樣分析,發現了大量SRB,其中多數為典型的腐蝕性菌屬Desulfovibrio sp.。
與船舶外部環境相比,內部環境擾動小,各種艙室內溫度范圍在10~40 ℃之間,燃油、潤滑油、艙內積水和生活污水的存在提供了豐富的營養物質,非常適合微生物生長。某些系統與艙室中,因含有油性污水、隔絕空氣、清理困難等因素,形成缺氧且營養富集的環境,為一些厭氧菌的生長提供了條件,成為微生物腐蝕的多發部位。因此,船舶內部的微生物腐蝕相較于船舶外部更加普遍和嚴重,燃油系統、潤滑系統、壓載系統、液貨艙以及各種液體管系都會發生不同程度的微生物腐蝕。
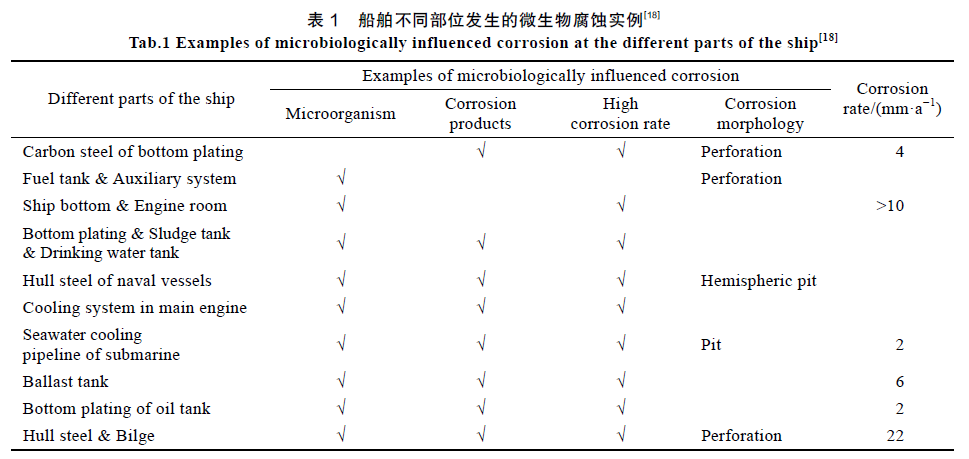
潤滑油中的微生物能腐蝕艙壁,并隨潤滑油被輸送至各摩擦副,加劇船舶主機各主要零部件、傳動元件、支撐元件等的腐蝕磨損。船舶發電機中常用潤滑脂作為潤滑劑,其中的腐蝕微生物加速潤滑脂變質失效,降低潤滑性能與部件壽命。海洋微生物直接與水潤滑尾軸承摩擦副相接觸,微生物腐蝕會對軸承材料的摩擦學性能產生影響。船舶油艙底部常出現一層水,有時水層可占據油艙容積的20%,水中的微生物對艙底不斷造成點蝕,形成局部缺陷,影響船舶的營運安全。有船舶曾發現碳鋼板的點蝕速率達到了2 mm/a,考慮到艙室板厚度普遍介于10~15 mm之間,這樣高的點蝕率造成了嚴重的安全隱患。有關調查顯示,超過65%的船舶壓載艙底部含有大量的沉積物,其中包含多種外來微生物,特別是厭氧菌與古生菌類(Archaea)可以在艙內缺氧環境下長期存活。陳德斌等報道了我國多艘艦艇艙底使用不到兩年就發生了多處腐蝕穿孔,經檢測后發現,艙底水中SRB數量是海水中的103~104 倍,蝕坑形貌多為階梯型圓錐體,且腐蝕產物呈黑色泥狀,有明顯異味,認為SRB 是造成嚴重穿孔的主要原因。王毅等總結了近年來發生在船舶各部位中的微生物腐蝕(見表1),表明船舶上各種系統及結構部件均受到微生物腐蝕的影響。
1.3 海洋平臺涉及的微生物腐蝕
海洋平臺作為相對獨立的系統在海洋環境下長期工作,根據其結構與功能可分為固定式、移動式與半固定式。海洋平臺的腐蝕按縱向環境特點分為5 個區域,分別是海洋大氣區、飛濺區、潮差區、全浸區與海泥區,微生物腐蝕主要存在于海洋大氣區、全浸區以及海泥區。海洋大氣區包括平臺上的水、油、氣管路以及動力系統和各種結構物,其環境與船舶內部環境相似,各種液體介質以及適宜的溫度給微生物腐蝕創造了條件。全浸區的污損生物附著在樁腿上,微生物腐蝕使其界面的耐摩擦磨損性能大大降低。同時,微生物還能改變金屬的腐蝕過程,引起局部腐蝕或穿孔,并在海流的沖刷作用下,導致腐蝕磨損加劇。海泥區由于深度大、海水中氧含量低,且海泥中存在H2S,厭氧菌特別是SRB 在腐蝕過程中占主導地位。
有關調查顯示,在油氣開采與運輸儲存過程中,輸油管路、海水系統、造水系統等多處均會受到微生物腐蝕。Korenblum 等[23]研究了海洋采油平臺海水注射系統中的微生物分布情況后發現,即使是經過滅菌處理的海水中依然存在包括SRB 在內的大量微生物,給海洋平臺帶來腐蝕加劇與石油酸化的威脅。一些近海港口或海岸由于污染造成了水質富營養化,Wiener 等[24]調查了污染水質中各物質的含量,發現有機碳、氮、氨以及有機硫化物的含量都很高,這種富營養化環境能促使微生物大量繁殖。
2 典型金屬材料的微生物腐蝕
海洋運輸船舶和海洋平臺都是為海洋開發服務的關鍵裝備。碳鋼、不銹鋼、銅合金是制造船舶和海洋平臺的幾種主要的金屬材料。海洋微生物的代謝產物與生物膜會直接改變浸水材料表/界面的介質環境,將原有的海水/金屬界面系統轉變為海水/表面膜層/金屬界面系統,加速金屬材料的腐蝕。因此,碳鋼、不銹鋼、銅合金在苛刻海洋環境下的微生物腐蝕直接影響著船舶與海洋平臺的可靠性與使用壽命。
2.1 碳鋼
碳鋼因較好的經濟性與優良的焊接性、強度等綜合性能,成為船舶上使用最廣泛的材料,船體、各層甲板、艙壁、艙底板、上層建筑以及各種船舶結構物等普遍使用碳鋼作為主要材料。一艘320 000 載重公噸位(DWT)的散貨船碳鋼用量可達到30 000 t 以上,100 000 DWT 級遠洋船舶中有約90%的鋼材是低碳鋼。船舶常用的低碳鋼(如Q235)及結構鋼AH32、DH32、AH36 和DH36 等,強度高,但耐微生物腐蝕的能力較差。
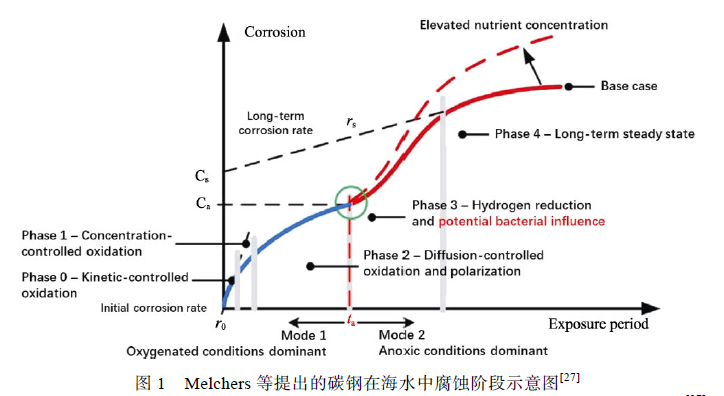
海水中碳鋼的腐蝕主要受到表面微環境中DO濃度、銹層厚度、EPS 理化性質、優勢菌種更替、生物膜微觀形態等因素控制。Melchers 等提出了一個模型,將碳鋼在海水中的腐蝕過程分為需氧階段(Mode1:oxygenated conditions dominant)與厭氧階段(Mode2:anoxic conditions dominant),如圖1 所示。在需氧階段,碳鋼的腐蝕速率取決于DO 的濃度高低,腐蝕產物累積并阻礙氧向碳鋼表面擴散,同時在需氧菌的耗氧作用下形成缺氧環境,腐蝕開始進入厭氧階段,微生物對碳鋼的腐蝕主要發生在這一階段。
Lanneluc 等將碳鋼試樣在法國西部La Rochelle海港深度為1 m 的海水中浸泡8 周后發現,碳鋼的腐蝕產物主要是鐵的氧化產物( Fe3O4 、α-FeOOH、γ-FeOOH),同時在銹層內部發現了極少量的FeS,但是并沒有發現SRB 存在于銹層中(可能是由于試驗周期較短,導致SRB 的數量過少),說明腐蝕初期(1~8 周)主要發生的是由氧擴散主導的純電化學腐蝕,但少量FeS 的出現表明厭氧菌已經開始影響腐蝕過程。根據Melchers 等提出的模型,此時碳鋼表面的腐蝕主要處在需氧階段,并開始向厭氧階段過渡,但在需氧階段并非沒有微生物參與碳鋼的腐蝕過程。Wu 等[29]研究了脫硫弧菌屬(Desulfovibriosp.)與假交替單胞菌屬(Pseudoalteromonas sp.)在天然海水中對低碳鋼Q235 的腐蝕,發現DO 濃度是影響微生物腐蝕的重要因素。需氧菌Pseudoalteromonassp.耗盡了海水中的DO,當海水中僅存在Desulfovibrio sp.時,不會導致微生物腐蝕,這是由于高濃度DO 抑制了SRB 的生命活動。需氧菌Pseudoalteromonassp.的出現消耗了海水中的DO 并形成低氧環境,為Desulfovibrio sp.的生命活動提供了基本條件,引發微生物腐蝕。這說明在需氧階段好氧菌阻礙DO 向碳鋼表面擴散,起到抑制腐蝕的作用,同時DO 耗盡使銹層內優勢菌種由需氧菌轉變為厭氧菌,碳鋼表面開始受到MIC 的影響。
微生物在不同生長階段與生存環境中分泌的EPS 并非完全相同,EPS 理化性質差異影響著微生物對碳鋼的腐蝕。董耀華等認為需鈉弧菌(Vibrionatriegens)在DH32 表面分泌的EPS 與金屬離子有絡合作用,從而加劇碳鋼的腐蝕。Dong 等提取了SRB 新陳代謝所產生的EPS,研究不同EPS 濃度對腐蝕的影響,發現低濃度的EPS 吸附在碳鋼的表面,阻礙氧氣與金屬表面的接觸,減緩了碳鋼的腐蝕;高濃度的EPS 中含有大量氨基酸與核苷酸等負電基團,對二價鐵離子(Fe2+)有明顯的螯合作用,加速了碳鋼表面的陽極溶解,使腐蝕更劇烈。Liu 等對比了不同生長時期IOB 的EPS 對低碳鋼Q235 的腐蝕情況,隨著IOB 的生長,EPS 的pH 值逐漸降低,腐蝕性增強,在碳鋼表面EPS 與腐蝕產物形成的層狀結構越來越疏松,碳鋼所受腐蝕也更嚴重,這解釋了為什么在Melchers 等提出的模型中,厭氧階段碳鋼腐蝕率高于需氧階段。隨著腐蝕產物不斷累積,碳鋼表面的離子濃度也會發生變化。Javed 等研究了鐵離子濃度對SRB 附著與腐蝕的影響,在試驗初期,鐵離子濃度差異對碳鋼表面的SRB 數量沒有明顯影響。隨著試驗進行至4~6 h,高鐵離子濃度使得碳鋼表面附著更多的SRB 且EPS 分泌量顯著增多,這是由于脫硫弧菌細胞膜外層的脂多糖(lipopolysaccharide,LPS)與環境中的鐵離子結合,促進了EPS 的分泌。
試驗28 天后,碳鋼腐蝕速率出現了巨大差異,高鐵離子濃度試驗組中,碳鋼的腐蝕速率超過70 μm/a,而對照組(無鐵離子)腐蝕速率僅有4 μm/a,兩組相差17 倍之多。上述研究表明,高鐵離子濃度能夠顯著促進SRB 的腐蝕,而碳鋼的MIC 過程中能夠產生大量的鐵離子,即微生物腐蝕產物又進一步加劇了碳鋼的MIC。碳鋼為鐵基金屬材料,在含有SRB 的介質中會生成鐵硫化物(FexS)與EPS 構成的復合生物膜。Xu 等認為碳鋼表面的生物膜是非均勻的異相結構,其內層由多裂紋的腐蝕產物構成。Dong 等發現FexS 嵌入在疏松多孔的生物膜內,對腐蝕過程中的電子轉移有良好的導通能力,使生物膜具備良好的電容特性。非均勻多孔異相生物膜使鐵基金屬表面存在濃度梯度,這種微環境差異造成表面各處金屬陽極曲線發生變化,產生“自催化效應”,并造成更多的點蝕。同時,疏松生物膜中的微孔結構在碳鋼MIC中起到關鍵作用,多孔生物膜下的碳鋼表面電流分布并不均勻,這是由于腐蝕性離子通過生物膜上的微孔直接與碳鋼基體接觸所致。目前這種微孔結構的形成機制尚不清楚,有學者認為微生物分泌的酶導致了生物膜疏松多孔,在對EPS 進行酶失活處理后,生物膜失去了多孔特性,但有研究表明,含有生物酶的EPS 同樣在碳鋼表面形成了致密的生物膜,還有學者認為,酶能夠利用葡萄糖產生H2O2,從而增大陰極電流密度。多種酶是微生物新陳代謝與金屬腐蝕過程中不可或缺的活性物質,如氫化酶對MIC 過程中的氫消耗有決定性的作用,從生物酶的角度闡釋腐蝕過程中的生物膜形態,為人們理解微生物腐蝕提供了一種新的思路。
實驗室中針對單一菌種對碳鋼的腐蝕已經進行了大量研究,但實際環境中微生物腐蝕通常是多種細菌聯合作用的結果。近年來隨著環保意識的提高,人們開始使用超低硫柴油(ultra low sulfur diesel,ULSD)作為船舶主機等大型動力裝置的主要燃料。但超低硫柴油的使用伴隨著更嚴重的局部腐蝕,船舶燃油柜、貨油艙與油液管道等甚至出現因嚴重點蝕而失效的現象。Aktas 等[39]研究了碳鋼在超低硫柴油使用環境下的微生物腐蝕,認為硫含量變化導致燃油對某些有降解能力的厭氧菌耐受程度降低,但這并沒有顯著影響碳鋼的腐蝕。而ULSD 中存在的某些SRB如解烷烴脫硫簇桿菌(Desulfoglaeba alkanexedens),對其他類型SRB 的生長有促進作用,加劇了SRB 的新陳代謝,使碳鋼受到更嚴重的局部腐蝕。菌種間具體的影響作用機制有待進一步研究。
2.2 不銹鋼
不銹鋼因良好的物理化學性能成為一種普遍采用的船舶與海洋工程材料。由于不銹鋼具有優良的耐空泡腐蝕與耐沖蝕性能,美國、英國等在20 世紀80年代開始將不銹鋼作為大型商船與高速艦船的螺旋槳材料,并取得了良好的效果。高速水翼艇的水翼要求材料強度高、韌性高與耐高速海水腐蝕性能好,雙相不銹鋼已成為水翼首選材料。特種運輸船舶,如液化天然氣運輸船與腐蝕性化學試劑運輸船中,不銹鋼常用于制造貨艙艙壁。艦船上各種接觸海水的重要部件,如通海閥、波紋管與變速槳的機械連接部分等大量使用不銹鋼材料。海洋油氣開采平臺在有H2S、硫酸氣與氯化物的復雜海水環境中工作,其結構部件也大多采用不銹鋼制造。
不銹鋼表面在海洋中附著了生物膜后不再直接與海水接觸,生物膜的微觀形態、成膜過程變化都對材料的腐蝕有著很大的影響。Sheng 等[40]對比了不同SRB 菌種在316 不銹鋼上的附著成膜情況后發現,脫硫脫硫弧菌(Desulfovibrio desulfuricans)在不銹鋼表面形成的生物膜具有疏松網狀的微觀結構,不斷地累積增厚,導致了更高的腐蝕速率。Cheng 等觀察到Vibrio natriegens 在不銹鋼表面的成膜過程與Desulfovibrio desulfuricans 有所不同,在成膜初期,因細菌生長繁殖,生物膜不斷增厚,隨后細菌數量下降,開始出現脫離現象(detachment phenomenon),同時形成具有疏松多孔結構的生物膜。這與碳鋼表面的非均勻異相多孔生物膜很相似。微生物代謝產物也會加速不銹鋼材料的腐蝕。Yuan 等對比了Desulfovibrio desulfuricans 代謝硫化物與無機硫化物對304 不銹鋼的腐蝕情況發現,代謝硫化物對材料表面的腐蝕性更強,腐蝕產物、代謝硫化物與細菌共同組成了致密且粗糙的生物膜,代謝硫化物對不銹鋼表面的氧化速度比無機硫化物更快。Chen 等對脫硫微桿菌(Desulfomicrobium sp.)的研究也得到了相似的結論,Desulfomicrobium sp.增大了不銹鋼表面的粗糙程度與腐蝕速率,而無機硫化物在不銹鋼表面形成的鐵硫化物層更加均一穩定,腐蝕速率更小。
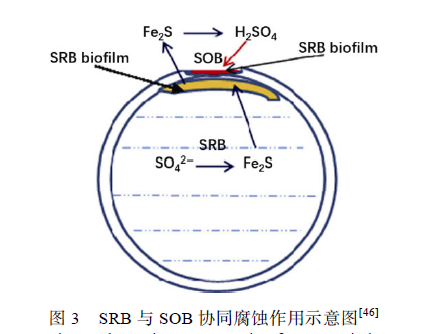
雙相不銹鋼(Duplex Stainless Steel,DSS)含有等量的奧氏體相(austenite(γ) phases)和鐵素體相(ferrite (α) phases),同時具備鐵素體不銹鋼與奧氏體不銹鋼的優點,并含有大量鈍化元素,如鉻(Cr)、鉬(Mo)與鎳(Ni),對Cl?腐蝕與硫化物腐蝕有著良好的抵抗能力。在過去幾十年中,雙相不銹鋼,特別是2205 雙相不銹鋼(2205 DSS)被廣泛應用在各種海洋工程結構物中,同時人們開始關注微生物對雙相不銹鋼造成的腐蝕。 Antony 等調查了Desulfovibrio desulfuricans對2205 DSS 的腐蝕情況發現,其表面同時受到了點蝕與縫隙腐蝕,縫隙腐蝕始于晶界處,并有選擇性地向奧氏體相擴展,鐵素體相所受腐蝕明顯小于奧氏體相,在雙相不銹鋼表面形成了兩種不同的微觀形貌,說明奧氏體對SRB 腐蝕更加敏感,這可能與奧氏體中較低的Cr 與Mo 元素含量有關。在構件的某些部位如材料的焊接處,由于微生物的作用,耐蝕性優良的雙相不銹鋼也會發生異常嚴重的腐蝕。Liang 等報道了液態烴冷卻器管路因腐蝕而失效的情況,在管內壁發現了較多點蝕,腐蝕產物中硫元素含量達到7.59%,說明海水中的SRB 直接參與了腐蝕過程。Liu等發現游艇上的2205 DSS 材料僅使用3 個月就在其焊接處出現了10 mm×60 mm 的異常蝕洞(如圖2所示),提出導致這一異常腐蝕現象的原因是SRB 與硫氧化菌(SOB)的協同作用(如圖3 所示)。海水中的厭氧菌SRB 在管道內壁形成生物膜并不斷腐蝕2205 DSS 奧氏體相,同時將海水中的硫酸鹽(SO4 2-)還原為Fe2S,蝕穿管壁后,海水中的需氧菌SOB 接觸到空氣,開始大量生長繁殖,SOB 又將SRB 的代謝產物Fe2S 氧化成有強烈腐蝕性的硫酸(H2SO4),在短時間內造成了異常嚴重的腐蝕現象。

微生物在不銹鋼表面的成膜情況與金屬材料的化學組分有關,Cr 與Mo 等元素使不銹鋼表面在海水中形成鈍化膜。不銹鋼與碳鋼雖同為鐵基材料,但二者在MIC 中的表面層結構有顯著差異。碳鋼基體直接與疏松多孔的生物膜接觸,相較于不銹鋼來說,碳鋼在微生物介質中的腐蝕速率要高得多。許多學者研究發現,不銹鋼在發生微生物腐蝕后,形成了一種具有雙層結構的表面膜,外層是由EPS 與腐蝕產物組成的生物膜,內層是鈍化膜,說明不銹鋼基體在MIC 過程中并不像碳鋼那樣直接與生物膜接觸。
同時,微生物的生命活動能夠改變不銹鋼鈍化膜的成分與結構,如SRB 的代謝產物H2S 能夠破壞鈍化膜,并產生鐵硫化物。Dec 等對比了Desulfovibriodesulfuricans 在2205 DSS 與超級奧氏體不銹鋼904L上的腐蝕情況發現,Desulfovibrio desulfuricans 在2205 DSS 表面的生物膜中含有大量EPS 與鐵離子形成的牢固的有機金屬鍵EPS—Fe,并加速不銹鋼的陽極溶解。生物膜中含有大量的二硫陰離子S2 2-,對2205DSS 鈍化膜有明顯的硫化作用。不銹鋼在海水中的抗蝕能力與Cr 元素含量密切相關,鈍化膜內的Cr 含量同樣受到微生物的影響。
Moradi 等研究了海洋菌假交替單胞菌(Pseudoalteromonassp.)在2205 DSS 上的腐蝕情況發現,生物膜中含有高濃度的Cl?,金屬表面鈍化膜內與蝕坑處表面Cr 含量降低,并隨微生物生長,Cr 的流失量越大。但是Yuan 與Seyeux 等[53,54]的實驗卻得到了不同的結果,不銹鋼受到微生物腐蝕后,其表面的鉻含量反而增大,XPS 的結果顯示,鈍化膜內Cr 的主要化合物由Cr2O3 變為Cr(OH)3,認為Cr(OH)3 的抗蝕能力低于Cr2O3 是造成點蝕增多的主要原因。這些結果分別從不同的角度解釋了不銹鋼的MIC,前者認為微生物使Cr 流失,從而降低了不銹鋼的抗蝕能力;后者則考慮了Cr 的化合物種類轉變對MIC 的促進作用。這進一步反映出不銹鋼相較于碳鋼在微生物的影響下有更加復雜的腐蝕機制,一方面,鈍化膜存在于生物膜與不銹鋼基體之間,使表面層結構更加復雜,研究微生物對鈍化膜的影響是理解不銹鋼MIC 的關鍵;另一方面,鈍化元素Cr 在MIC 過程中的含量變化一直存在爭議。此外Cr 的抗微生物腐蝕能力尚未有研究證實。MIC 本質上是微生物在特定環境中的一種生存策略,深入研究Cr 元素在微生物活動中的轉化過程,有助于從生物學的角度理解MIC 機理。
2.3 銅合金
早在19 世紀,銅合金就被應用于船舶與海洋工程領域,當時銅合金主要用作船體的保護層。在純銅中加入鎳元素可以顯著提高材料的力學性能、耐蝕性與延展性,因此銅鎳合金(又名白銅)在海洋工程領域備受青睞。在天然海水中,銅鎳合金表面會迅速地生成主要由銅、鎳的氧化物(Cu2O、Cu2(OH)3Cl、NiO、Ni(OH)2)構成的保護膜,這是銅鎳合金具有較高耐蝕性的主要原因。海水淡化冷凝管、海水管道、艦船外殼等都大量使用銅鎳合金作為主要材料。銅合金在海洋環境中具有良好的抗生物污損性能。Drach等選取了多種海洋工程領域常用的銅合金,在北大西洋海水中浸泡一年后發現,絕大多數試樣表面沒有出現宏觀的生物污損,抗大型生物附著率高達100%。
銅離子通過破壞某些微生物細胞膜與DNA 蛋白質,從而具有一定的廣譜抗菌作用。研究表明,在鐵基合金中加入Cu 可以提高材料的抗菌性能,從而起到抑制微生物的腐蝕作用。Li 等研究了含銅2205雙相不銹鋼(2205-3%Cu DSS)在有海洋細菌綠膿桿菌(Pseudomonas aeruginosa)人造海水中的腐蝕情況,與2205 DSS 相比,2205-3%Cu DSS 上的生物膜數量顯著降低,最大蝕坑深度也由4.83 μm 減小至1.53 μm。對鐵基金屬進行Cu 合金化功能改進后也發現,材料的生物膜貼附量與受點蝕程度明顯降低。
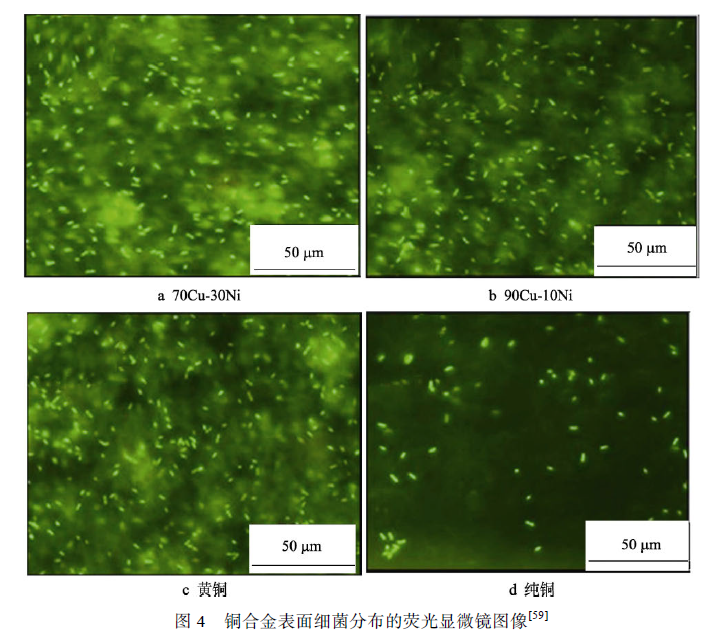
因為銅在鐵基合金中表現出良好的抗微生物腐蝕性能,那么以銅為主要基體元素的銅合金應該具備更加優良的抗菌與抗腐蝕能力,但大量的研究表明,銅合金在海洋微生物介質中的抗微生物貼附和抗蝕能力與含銅鐵基合金有很大的差異。Krishnan 等對比了多種金屬材料在海洋中微生物附著情況,發現銅合金表面的微生物數量雖少于不銹鋼與碳鋼,但銅離子的毒性并不能完全阻止微生物的生長,特別是革蘭氏陽性菌(Gram-positive bacteria)的數量居多,如圖4 所示,銅鎳合金與黃銅表面的微生物附著量明顯多于純銅。
Javed 等報道了銅鎳合金在SRB介質中的腐蝕僅次于碳鋼,90Cu10Ni 在SRB 溶液中最大點蝕率達到82 μm/a,是在無菌溶液中均勻腐蝕速率(5 μm/a)的近17 倍, 而70Cu30Ni 的最大點蝕率也達到43 μm/a,這不僅遠高于不銹鋼在SRB 中的腐蝕速率(~0.1 μm/a),還出現了隨著Cu 含量的增加,腐蝕反而加劇的現象。陳娟等觀察SRB 對銅鎳合金的腐蝕行為發現,在點蝕處Cu 的質量損失百分比僅是Ni 的1/4,在晶間腐蝕處Cu 的損失也遠小于Ni 與Sn,這可能是由于EPS 對Ni 與Sn 有更強的絡合作用,導致脫合金成分腐蝕,使銅鎳合金表面出現大量點蝕與晶間腐蝕。Chen 等[62]研究了SRB 對金屬銅的腐蝕發現,SRB 在Cu 表面能夠快速生長繁殖,形成多相疏松的生物膜(如圖5a 所示),在銅表面造成了明顯的點蝕(如圖5b 所示),分析腐蝕產物發現了大量的Cu2S。Sheng 等提出細菌EPS 與銅離子之間的絡合反應是腐蝕過程中的關鍵,EPS 中羥基團的氧原子能夠與環境中的游離態銅離子形成某種絡合物,降低環境中的銅離子濃度,使細菌在一定程度上免受銅離子的毒性作用。上述研究結果解釋了Krishnan 等發現的銅合金有較高微生物貼附量的現象,EPS 對Ni 與Sn 更加敏感,所以銅鎳合金表面微生物附著量高于純銅,而EPS 上的某些官能團,如羥基團中和了Cu 離子毒性,導致純銅表面仍然有微生物貼附。

銅合金與不銹鋼都屬于鈍化類金屬材料,微生物在其表面的生命活動會改變鈍化膜的物理化學狀態。微生物分泌的EPS 從形態上可分為緊密結合型胞外聚合物(Tightly bound EPS,TB-EPS)與松散結合型胞外聚合物(Loosely bound EPS,LB-EPS),TB-EPS直接包裹微生物細胞形成類似膠囊結構,LB-EPS 則游離于EPS 的外層,且多呈黏液狀。Bautista等提取了海洋假單胞菌(Pseudomonas)分泌的LB-EPS 并貼附在銅鎳合金表面,發現鈍化膜厚度明顯降低,認為LB-EPS 能阻礙Cl-與Cu 接觸,從而具有抑制腐蝕的效果。但僅從EPS 的角度去理解銅合金的MIC 是不全面的,因為在含有微生物的介質中,生物膜狀態遠比均勻貼附要復雜得多。Fu 等發現,SRB 新陳代謝所產生的硫化物具有強烈的腐蝕性,能使鈍化膜持續溶解,黑色腐蝕產物與EPS 以及微生物細胞共同組成具有疏松多孔特性的生物膜,這與碳鋼表面生物膜的不均勻異相結構非常相似。Tuba等認為,由于細菌對毒性離子(Cu2+)的天然反應,EPS 的含量增多,并與大量細菌以及腐蝕產物聚集在一起,所形成的生物膜面積變小但更厚,可能有助于微生物抵抗銅離子毒性。Huang 等觀察到銅合金表面的生物膜分布呈現出非連續的團聚現象,明顯區別于碳鋼與不銹鋼表面生物膜的連續分布,這證實了Tuba 與Sheng 對微生物抵抗Cu 毒性機制的猜測。雖然微生物分泌的EPS 能與Cu 發生某種絡合反應,但并未形成類似于鐵基金屬表面上的牢固有機金屬鍵(EPS—Fe),所以銅合金表面的生物膜更加疏松脆弱,導致鈍化膜被完全破壞,直至暴露基體金屬,造成局部腐蝕。表2 中對比了銅合金、碳鋼與不銹鋼在微生物介質中的腐蝕特征,銅合金鈍化膜在SRB 介質中受到很大程度的破壞,其中的氧化銅完全轉變為Cu2S,使鈍化膜失去對基體的保護能力,這也就解釋了為什么銅合金受到的微生物腐蝕遠比不銹鋼嚴重。

目前人們對Cu 的抗菌機理并無統一定論,僅提出了幾種可能的機制:1)銅離子直接接觸殺菌;2)催化作用殺菌;3)破壞細菌酶系統殺菌;4)凝固細菌蛋白質殺菌。從上述研究工作來看,微生物在對銅合金的腐蝕過程中,對Cu 的毒性有一定的抵御策略,Cu 不僅未起到明顯的抗菌效果,銅合金在海水中的抗腐蝕能力也因微生物附著而急劇降低[47,58-69]。對于銅合金與含銅鐵基合金在抗微生物腐蝕方面的較大差異值得深入研究,這不僅為Cu 的抗菌機制研究提供了一個新的視角,同時對如何增強材料的抗微生物腐蝕性能具有重要的指導意義。
3 微生物腐蝕機理研究進展
金屬材料的電化學腐蝕經過多年的研究,已經有比較透徹的機理解釋,微生物腐蝕的機理也吸引了眾多的學者去開展這方面的研究工作,陰極去極化理論和微生物電化學腐蝕理論是目前最主要的用于微生物腐蝕機理解釋的理論。
3.1 陰極去極化理論
陰極去極化理論是早期學者通過研究SRB 對碳鋼的腐蝕所提出的[71,72]。這個理論認為,微生物能通過消耗金屬表面在水中形成的氫,并降低局部分壓,起到去極化劑的作用,加速金屬陽極溶解,同時電化學意義上的陰極氫也能促進微生物的生長。SRB 附著在碳鋼表面后捕獲陰極上的吸附氫(Hads),在硫酸根離子(SO4 2 -)的還原過程中,Hads 被消耗(見式(1)),生成S2-,氫膜被破壞后無法阻止Fe2+由金屬基體向生物膜擴散,Fe2+與S2-生成FeS(見式(2)),沉淀在生物膜中,形成疏松多孔的表面層。
![]()
用陰極去極化理論解釋SRB 對碳鋼的腐蝕機理得到了眾多學者的支持,在碳鋼表面觀察到的不均勻異相生物膜以及對腐蝕產物的分析,都證實了陰極去極化理論的可行性。SRB 分泌的氫化酶在消耗氫的過程中起到關鍵的作用。Liu 等將生物膜進行處理,使酶失去活性,發現碳鋼表面的層狀結構變得緊密,腐蝕產物中的鐵硫化物含量顯著降低,說明氫化酶控制著S2-的生成。
然而僅用陰極去極化理論無法解釋所有的微生物腐蝕現象。按照陰極去極化理論,SRB 在沒有碳源作為電子供體的情況下,無法將海水中的SO4 2?還原為S2-,對碳鋼的腐蝕應該有所減輕,但Xu 等發現,SRB 在有機碳源匱乏的情況下,對碳鋼的腐蝕反而更加劇烈。當環境介質中缺乏90%的有機碳源時,脫硫弧菌(Desulfovibrio vulgaris)對碳鋼的平均點蝕深度達到7 μm,是碳源充足時的近兩倍。Chen 等進一步研究了SRB 在有機電子供體缺乏的條件下對碳鋼的腐蝕情況,隨著溶液中營養物質的不斷消耗,游離態細菌比例從實驗初期的(92±5)%逐漸下降至(6±4)%,游離態的SRB 轉而吸附在碳鋼表面,局部腐蝕也更加嚴重。另外,有研究表明,微生物活動能夠改變不銹鋼鈍化膜內的化合物成分與元素含量,并阻礙不銹鋼表面的保護層再生,因此不銹鋼的MIC機理更加復雜。
3.2 微生物電化學腐蝕理論
由于陰極去極化理論的局限性,學者們試圖從其他角度去理解MIC。有研究指出,微生物燃料電池(Microbial fuel cells,MFCs)中存在細胞外電子傳遞機制,微生物細胞可以通過生物納米導線、細胞膜功能蛋白、活性電子中介體等多種方式,將金屬基體元素的電子轉移至細胞內,作為生命活動的能量來源。
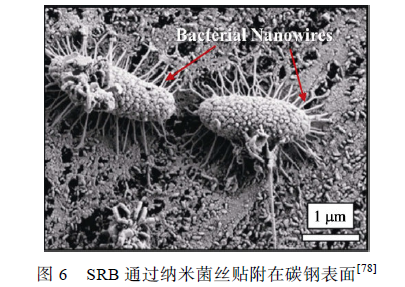
SRB 細菌胞體能分泌出多條與金屬表面緊密結合的納米菌絲(Bacterial nanowires),使細菌牢固地貼附在碳鋼表面,如圖6 所示。Yu 等證明了SRB 的電活性,認為SRB 可以從極化0.61 V(vs. SHE)的石墨電極中直接或間接地獲得電子。Guan 等發現0.85 V(vs. SCE)的極化電位更有利于SRB 生長,提出SRB 可以從此電位下的電極中獲得電子,促進金屬腐蝕。Xu 等提出了生物陰極催化硫酸鹽還原機理,認為SRB 可以通過納米菌絲或某些特異蛋白質直接利用金屬基體元素作為電子供體,這個過程就表現為微生物對金屬產生腐蝕作用。根據這個理論,微生物優先利用環境介質中的營養物質作為電子供體,隨著腐蝕產物和生物膜的累積增厚,環境中的有機碳源難以被生物膜底層的微生物捕獲,這時金屬基體元素如Fe 就成為唯一的電子供體。陽極反應為Fe失去電子被氧化為Fe2+(見式(3)),陰極反應為SO4 2-被還原為S2-(見式(4)),與陰極去極化理論中的陰極反應相似,不同的是生物陰極催化硫酸鹽還原理論認為陰極過程直接發生在微生物細胞內,傳統觀點中的物理陰極被發展為生物陰極。
![]()
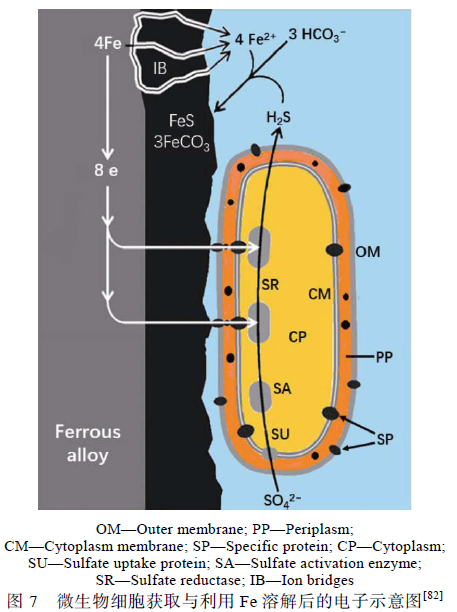
Venzlaff 與Enning 等[82,83]強調微生物電化學過程對金屬腐蝕的影響,提出了與陰極催化硫酸鹽還原機理相似的電化學微生物腐蝕理論,并給出了電子與各離子在微生物細胞內的轉移過程,見圖7。細胞外膜(OM)、外周胞質(PP)與細胞質膜(CM)上均存在特異蛋白質(SP),能夠將細菌胞外的電子傳遞至細胞質(CP)內,同時CM 上的硫酸鹽攝取蛋白質(SU)捕獲環境介質中的SO4 2 -,通過細胞質內的硫酸鹽活化酶(SA)與硫酸鹽還原酶(SR)利用金屬失去的電子將SO4 2-還原為H2S,Fe2+能通過生物膜上的離子橋(IB)與H2S 接觸生成腐蝕產物FeS。他們提出的離子橋(IB)結構與文獻[34]中報道的碳鋼表面生物膜微孔類似。Yu 等證實了SRB 的電子傳遞在碳鋼的腐蝕中起到重要作用,并為SRB 與碳鋼之間的電子傳遞提供了依據。Xu 與Chen 等的研究結果以及生物膜具有良好導電性的發現[35]也為微生物電化學腐蝕理論提供了有力證據。
陰極去極化理論可以被認為是微生物電化學腐蝕理論的一種特殊情況。當微生物能夠分泌氫化酶時,將利用金屬表面的H 作為電子供體,并起到陰極去極化的作用,但對于無法分泌氫化酶或無法直接利用環境中碳源的微生物來說,可以通過多種方式從金屬基體獲取電子,以支持生命活動。微生物電化學腐蝕理論將電化學與微生物能量學聯系在一起,具有開創性,使人們對MIC 有了全新的認識。但這個理論同樣存在缺陷,比如Cu 的SRB 腐蝕就很難用微生物電化學的機制去解釋。根據腐蝕熱力學,腐蝕發生的前提條件是氧化-還原反應的電化學親和勢A 為大于零的正值(見式(5))。
![]()
式中:A 為電化學親和勢;n 為電子化學計量系數;F 為法拉第常數,約為96 494 C;E02與E01 分別為陰極與陽極的平衡電位。
Cu 被分別氧化為Cu+與Cu2+的陽極反應中,相對飽和甘汞電極(vs. SHE)的標準電位分別為522 mV與345 mV,若將Cu 的兩種氧化反應作為SO4 2 -還原過程的陽極計算,得到了小于零的電化學親和勢,這與腐蝕熱力學的觀點相悖,說明微生物可能無法直接利用Cu 作為電子供體。Fu 等認為銅晶體(Cu(crystal))雖然無法參與微生物細胞內的陰極過程,但可以與新陳代謝產物S2-反應,生成硫化亞銅沉淀(Cu2S(crystal))(見式(6)),H 作為電子轉移載體出現,且最終生成氫氣(H2(g))。這說明Cu 在SRB 作用下的腐蝕過程,既不完全符合陰極去極化理論中消耗氫的觀點,又無法用微生物的電化學腐蝕來解釋。
![]()
從目前的研究來看,對Cu 的MIC 機理傾向于用微生物代謝產物具有較強腐蝕性來解釋,如SRB 產生的H2S,APB 與SPB 分泌的有機酸等。微生物腐蝕是一個復雜的過程,無論是陰極去極化理論或是近年來提出微生物電化學腐蝕理論,都不會在MIC 中單獨起作用,如硫還原地桿菌細胞外膜上有絲狀的菌毛蛋白(Geopili),能在細胞與金屬之間傳遞電子,脫氮硫桿菌無法直接利用金屬被氧化后的失去電子,但可以通過某種導電的納米顆粒將硫還原地桿菌獲取的電子轉移至細胞內以供生命活動,對金屬造成間接性的腐蝕。除了菌種間的協同與競爭作用,生物膜的附著狀態、微觀結構、膜內沉積的腐蝕產物以及表面微環境的差異,都能影響微生物對金屬的腐蝕,生存環境的改變也能導致同種微生物產生不同的腐蝕效果。
針對碳鋼、不銹鋼和銅合金這幾種最主要的海洋金屬材料,上述兩種理論都在一定程度上可以對他們的微生物腐蝕機理做出一些解釋。碳鋼、不銹鋼與銅合金的MIC 必定伴隨著金屬基體的溶解,根據上述理論,微生物主要通過以下幾種方式影響溶解過程:
1)改變金屬陽極失去電子的轉移過程與電子受體,微生物電化學腐蝕理論就是從這個角度闡釋了碳鋼的MIC 過程;2)破壞金屬表面原有的保護膜,碳鋼、不銹鋼與銅合金的MIC 中都體現出了微生物對保護膜的影響,陰極去極化理論認為SRB 消耗了碳鋼表面的氫膜,不銹鋼與銅合金的鈍化膜也受到了不同程度的破壞;3)腐蝕性新陳代謝產物加速金屬溶解,銅合金基體在SRB 海水中的局部腐蝕就主要受代謝產物H2S 的控制。然而,上述兩種理論還不能完整地對海洋材料的微生物腐蝕機理做出完全令人信服的解釋,這也充分說明了微生物腐蝕過程的復雜性,還亟需進一步開展這方面的研究,來繼續完善微生物腐蝕機理。
4 展望
海洋環境中金屬材料的微生物腐蝕研究越來越受到人們的關注,大量學者在微觀層面對微生物腐蝕機理進行了研究,提出了一些理論模型并試圖解釋金屬材料發生微生物腐蝕的過程,并取得了一定的研究成果。但海洋微生物腐蝕過程極其復雜,它不是一個簡單的電化學過程,其研究涉及到海洋科學、微生物學、界面化學、金屬材料等多個學科領域的交叉,而且目前的實驗技術手段還不足以完全掌握微生物腐蝕機理,加之復雜的海洋工況環境,仍有諸多問題值得研究與探討:
1)不同菌種間的協同作用機理研究。海洋環境中微生物種類繁多,對單一菌種的實驗研究難以反映出金屬材料在實際工況下的腐蝕,菌種間的相互作用機理、協同作用如何影響腐蝕過程,與單一菌種的腐蝕有何區別,這些將成為今后重要的研究方向。
2)非鐵基金屬的MIC 機理研究。針對鐵基金屬的MIC 已進行了大量研究,得到了具有代表性的幾種腐蝕理論,但這些理論無法完全解釋非鐵基金屬,如銅合金的MIC 腐蝕機理還沒有一個完整的機制理論,對此進行深入研究能進一步理解MIC 過程。
3)微生物對海洋耐蝕材料的影響。海洋耐蝕合金相較于一般的金屬材料具有更復雜的化學成分與金相結構,對海水腐蝕有良好的抵抗能力,但對微生物的耐蝕性如何,耐蝕元素如Cr 是如何影響微生物的成膜與腐蝕過程等,都有待進一步研究。
4)微生物腐蝕與摩擦磨損的協同作用。目前多數有關海洋環境下摩擦副摩擦磨損行為的研究未考慮微生物腐蝕的影響,兩者間的相互促進或抑制作用機理的研究對提高材料在海洋中的使用性能具有重要指導意義。
5)微生物與宏觀污損生物的協同作用。宏觀污損生物附著于金屬表面,加速材料的局部腐蝕,其下的銹層中往往存在微生物群落,宏觀污損生物與微生物的共存如何影響腐蝕,兩者間的協同機理尚不明確。
更多關于材料方面、材料腐蝕控制、材料科普等方面的國內外最新動態,我們網站會不斷更新。希望大家一直關注中國腐蝕與防護網http://www.ecorr.org
責任編輯:王元
《中國腐蝕與防護網電子期刊》征訂啟事
投稿聯系:編輯部
電話:010-62313558-806
郵箱:fsfhzy666@163.com
中國腐蝕與防護網官方 QQ群:140808414
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《中國腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62313558-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護網官方QQ群:140808414





