《豐金屬常溫分解水制氫反應原理探秘》:與南陽氫水車老總龐青年、董仕節教授商榷
李達剛
中國科學院蘭州化學物理研究所退體研究員
為什么現在發表此文,是因為近年來國內科技領域出現某些怪現象,例如有的研發項目稍有點研究進展,不顧產品產業化的經濟性和實際價值,就開始做產品做示范,其中不少人是為了騙到錢,達快速致富發財。而且在中國產業界有成果慌之時,就可能會變成為某些“能人”借科技創新允許失敗的名義走捷徑騙錢之實,令真正科研者氣憤!
2019年5月23日南陽青年汽車宣稱:“車輛只需加水就能行駛”引起輿論暴發,因為對鋁合金制氫原理不透明,產生巨大爭議。其間,歡呼鋁/水常溫制氫之催化劑功效神奇者不少;但質疑又產生了一個《水變油騙錢事件》呼聲更高。新華社和人民日報也都發聲,科技日報或因廠家保密也末言明此產氫原理,更令人疑慮重重。“南陽氫水車事件”到底是重大的科技進步?還是高級騙錢之術?一時難以斷定。因而許多人呼之: “以舉國之力搞個清清楚楚!”、呼喚中科院發聲等不絕于耳。如何判斷“南陽氫水車事件”?涉及科學向題還是須用科學事實回答才會有說服力。
其實對此問題中國早已有過研究,最先申報于中國發明專利,申請號:2007100168498,專利名稱:《豐金屬常溫分解水或重水制氫或氘的方法》,之后又發布于中國發明專利ZL 2011 10266145.2,對鋁合金制氫的應用及原理早己有說明。現公開“常溫分解水制氫反應機理”的發掘過程及中國笫一份有關“常溫分解水制氫”的發明專利獲得授權之經歷故事,就可以清清楚楚說明白“鋁合金水解制氫”的化學反應原理。能夠讓關心人士做出較準確的判斷,推動這場全國科技創新大討論更健康發展。
本文未章提出的幾點結論與南陽洛特斯新能源汽車公司負責人龐青年、專利發明人董仕節教授二位商榷。不妥之處請與指正。
(一)從《意外發現》到《原始創新》
介紹豐金屬常溫分解水制氫的原始發明過程。
一個意外的發現:1993年在中科院蘭州化學物理研究所改進SHOP法乙烯齊聚制α-烯時,用緩釋長效的還原劑金屬鋅(Zn)代替瞬間還原劑硼氫化鈉,組成由:中心金屬:NiCl2;膦配體:Ph2PCH2COONa;還原劑:Zn;溶劑:丁二醇HOCH2CH2CH2CH2OH構成四元體系,意外的發現生成大量的氫氣,而且在室溫的條件下就能產生氫氣。
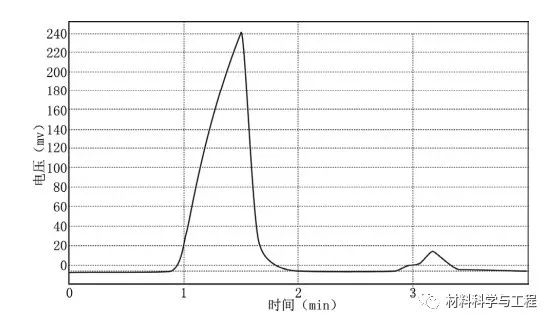
圖1.產物氫氣的毛細管氣相色譜分析圖
(二)查明氫的來源
在由鋅/有機膦/丁二醇/氯化鎳組成的四元體系中,只有丁二醇分子中含有活潑氫原子,為了確認氫來源于醇,考察了醇結構對產氫速率的影響,結果得出: 1)產氫速率與醇類的酸性呈順變關系,見表1。
2)與膦配體的存在與否無關的結果。
表1 醇類產氫速率與解離常數關系
產氫速率 甲醇>乙醇 =丁二醇 >丁醇 >異辛醇 >> 叔丁醇 解離常數pKa 15.5 16 16.8 18 19.2 產氫最低溫度℃ 10 15 15 30 70 不產氫
由上表可見,醇類溶劑產生氫氣的最低溫度與醇類的解離常數(pKa值)次序呈順變關系。也就是說甲醇的羥基中氫最易解離,(pKa值最低)產氫最容易,生成氫氣氣泡的初始溫度也最低(10℃);而叔丁醇的酸性最弱(pKa值最高),即它的羥基中氫最不易解離,在室溫下,甚至提高到70℃也無氫氣生成。 用二甲基亞砜代替醇類作溶劑,因它無羥基,無可解離的氫原子, 故不能產生氫。為氫氣來源于醇的羥基找到了證據。
(三)用水代替醇制氫成功
醇類可看做烷基水, 因烷基的給電子能力除甲基外通常小于氫的給電子能力,醇與水相比較,其羥基氫較不易解離,液態醇的氫離子濃度大約為十億分之一, 而液態水的氫離子濃度為千萬分之一。 水的pKa值為15.74, 與甲醇相當。據此, 提岀用水代替醇組成:鋅/水/氯化鎳三元新體系,進行常溫分解水制氫的試探。試驗結果表明:豐金屬(Al、Mn、Zn、Fe) / 金屬鹽類 / 水三元體系,在10-60℃常溫條件下即可產生氫氣。
(四)探索擴展
鹽類產氫速率次序可排列為:FeCl3 > CrCl3 >MgCl2> AlCl3 > NiCl2 > FeSO4 > CuSO4 > 》 NaCl。
其水合離子[M(H2O)6]3+的解離常數pKa值為:
Fe[(H2O)6]3+ [Cr(H2O)6]3+ [Al(H2O)6]3+ [Cu(H2O)6]2+ [Fe(H2O)6]2+ 2.2 3.9 4.9 8.0 8.3
比較以上兩個排列次序可見, 兩者似乎呈逆變關系, 也就是水解常數越小, H+離子越易解離, 產氫速率越高。Na+離子的pKa值大于14-15, 無水解能力。金屬種類的考察結果表明:非活潑金屬在該三元體系中的產氣能力大體與金屬的活潑次序一致。
非活潑金屬的活潑次序:鋁、錳、鋅、鉻、鉄、鈷、鎳、錫、鉛、氫、銅、銀、金實驗產氫次序:Mn > Zn > Al > Cr >Fe >Co> Ni > Sn。
其例外是金屬錳(Mn)的產氫性能大大優于排在前邊的金屬鋁(Al),更大大優于排在后邊的鋅(Zn)。查明,其原因是金屬鋁在生成氫氣的過程中,鋁表面同時生成氧化鋁保護膜;而金屬鋅表面同樣易生成堿式碳酸鋅保護膜所致。金屬活潑次序排列在氫原子之后的銅(Cu)與銀(Ag)、金(Au)不能在該三元體系中產生氫氣。
(五)《原始發現》的確認
本人檢索了近50年(1955年-2005年)美國化學文摘索引及世界專利索引,均未見由金屬鋅/醇/氯化鎳組成的三元體系,進一步擴展為非活潑金屬/醇(或水)/金屬鹽類組成的三元體系也未見到可在室溫下持續產生氫氣的報導。初步確認此乃原始發現。
新發現的這種產氫現象與現有制氫方法相比,具有:
1) 不需外加能源,室溫條件下即可產生氫氣。
2) 不必用強酸或強堿,無腐蝕。
3) 氫氣中無任何雜質,無須分離可得到純氫。
4) 對環境無污染。
若能將此發現轉化為技術發明,無疑將會為人類增添一種新的制氫方法。為了圓夢探索最終結果,2003年非典期間就在自家的車庫里進一步開展豐金屬常溫分解水制氫反應機理的研究。(見照片)

豐金屬常溫分解水制氫中國笫一發明人李達剛, 1936年生,中科院蘭州化物所退休研究員
(六)制氫原理探索----知識組合的創新
俗語云:“小雞不撒尿,總是有條道” ,要把這條道找出來。從三元體系中的金屬產氫能力與金屬活潑次序大體一致的規律,可知金屬Zn參與了還原氫質子的經典反應:
Zn + 2 H+ →Zn2+ + H2(g) 反應式<1>
反應式<1 >中的H+ 可來源於水自身的解離反應, 然而在Zn/H2O的二元體系下不能生成氫氣(H2 ), 是因為在標態下, 水的解離常數很小, 僅為1.08×10-14 , 故在室溫下不能產氫。那么,三元體系中的氫質子從那兒來的呢?從三元體系中鹽類的產氫能力與金屬離子水合物的水解反應常數呈逆變關系可知,該三元體系中發生了經典的水解反應:
[Fe(H2O)6]3+→ [Fe(H2O)5(OH)]2++ H+ PKa=3.05 反應式<2>
[Fe(H2O)5]2+→ [Fe(H2O)4(OH)2]+ + H+ PKa=3.26 反應式<3>
將反應式<1>與反應式<2>和反式<3>組合在同一個系統,即可將釋放岀來的H+離子還原為氣態氫(H2)。本文的偶然發現, 恰好將金屬還原和鹽類水解兩個經典反應組合在同一個系統,故可在常溫下產岀氣態氫(H2)。常溫制氫的總反應式可歸納為:
M3+ + xH2O ? [M ( H2O) x ]3+ [M ( H2O)x ] 3+
[ M ( H2O) x-2( OH )2]+ + 2H+
2H+ + m m2++ H2 (g)
M3++xH2O + m ?[ M ( H2O)x-2 (OH) 2]+ + m2++ H2(g) <總反應式1>
式中M3+:代表三價金屬離子; m:代表零價金屬。
(七) 抑制副反應
在鋅/水或甲醇/氯化鎳三元體系中,于室溫下產生氫氣的同時發現金屬鋅表面生成大量黑色沉積物,阻斷了制氫反應的進行。
詳情請點擊鏈接查看:《與南陽水氫發動機商榷:豐金屬常溫分解水制氫》
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《中國腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62313558-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護網官方QQ群:140808414





