海洋資源的開發利用需要大量海上設施設備,如用于海洋石油開采的鉆井平臺,海洋風力發電設備及跨海大橋等。目前,作為海上設備平臺使用的工程結構材料多為金屬材料,在惡劣的高腐蝕海洋環境中極易發生腐蝕。目前,在全浸泡環境中金屬材料的防腐蝕措施通常采用重防腐涂料聯合陰極保護作為主要的腐蝕防護手段。
然而,陰極保護會產生過剩的OH-使得涂層與金屬界面發生堿化,從而導致涂層陰極剝離。關于陰極剝離已有許多學者進行了研究。Bi等研究了低碳鋼表面涂層下陰極氧還原與陰極剝離的關系,認為氧的還原反應產生的界面堿化導致了涂層的剝離。Shi等使用局部掃描振動電極技術 (SVET) 研究了低碳鋼上缺陷環氧涂層防護作用,結果表明:施加陰極保護,涂層缺陷處形成的鈣質膜層有利于陰極保護過程。Eltai等認為陰極保護導致完好環氧清漆涂層的阻抗下降,涂層的吸水量由于陰極保護電位的提高而增加。李玉楠研究了陰極保護對破損有機涂層防護作用的影響,結果表明:完好涂層的-850 mV (vs Cu/CuSO4) 保護準則對破損涂層是不適用的,為了陰極保護能夠發揮正常的作用,應該將保護電位負移。張麗研究了外加電流陰極極化下環氧清漆及環氧富鋅涂層的失效行為,結果表明:對環氧清漆涂層施加-900 mV (vs SCE) 陰極保護后,增強了基材/涂層界面處的堿性環境,加速了涂層中交聯結構破壞,減弱了基材/涂層界面處的附著力,降低了涂層壽命。
本文主要研究不同陰極保護電位對破損環氧涂層下海洋平臺研制鋼的陰極保護效果及對破損的高附著化學鍵合防腐涂料防腐性能的影響及陰極剝離機理。
1 實驗方法
實驗中所用的金屬基體材料為海洋平臺研制鋼,其化學成分 (質量分數,%) 為:C 2.76,Mo 0.58,Si 0.24,Ni 2.61,Cr 0.79,Fe 92.48。鋼片的尺寸為50 mm×50 mm×3 mm,參照GB 13288-1991《涂裝前鋼材表面粗糙度等級的評定》中關于涂裝前鋼材的表面粗糙度等級相關規定,將試樣進行噴砂處理,再經丙酮超聲除油,無水乙醇除水,吹干,置于干燥器中備用。
本實驗所用的涂料是由哈爾濱工程大學研制的HGL-2化學鍵合防腐涂料底漆,使用前按A、B組分質量比3∶1混合攪勻,抽真空除去涂料中氣泡,靜置1 h后,均勻涂覆到備用鋼片上。25 ℃固化24 h后,60 ℃固化48 h。
采用Ф=3 mm的鉆孔器人為制造涂層缺陷,缺陷面積約占測試面積的0.6%。
采用PosiTector6000測厚儀測定涂層厚度,選取固化后涂層厚度為 (100±5) μm的試樣進行電化學阻抗譜 (EIS) 測試。
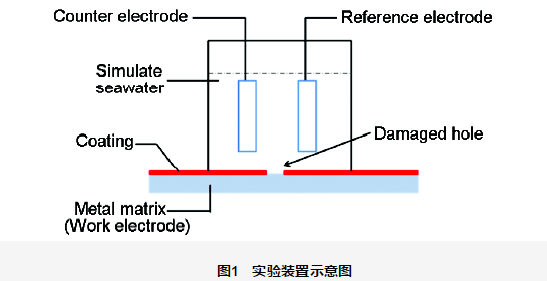
本實驗施加陰極保護的恒電位儀為IviumStat電化學工作站,參比電極為飽和甘汞電極,輔助陽極為自制的高純度石墨電極,有效實驗面積為11.34 cm2,破損面積約占測試面積的0.6%。實驗在室溫靜態模擬海水中進行,實驗裝置示意圖如圖1所示。本實驗采用人工海水溶液,溶液配方參照國標GB/T 7790-2008,NaCl:23 g/L,MgCl2·10H2O:9.8 g/L,Na2SO4·10H2O:8.9 g/L,CaCl2:1.2 g/L。
對于海洋工程而言,金屬材料所要求的陰極保護電位比穩態下自腐蝕電位至少低200 mV;對于涂覆有機涂層的保護體系,目前最常使用的電位規范是-850 mV (vs Cu/CuSO4),即-780 mV (vs SCE)。潘大偉等研究了-750~-950 mV (vs Ag/AgCl) 電位對于海洋高強鋼 裸鋼)的保護效果,結果表明最佳的陰極保護電位區間為-0.76~-0.94 V。眾所周知有機涂層本身具有防護效果,可以降低陰極保護電位;而-780 mV (vs SCE) 是完整涂層常用的保護電位,不是其最低的保護電位。本實驗所用的試樣是0.6%破損的有機涂層金屬體系,所以為了方便電位節點的設置 (本實驗以100 mV為梯度來設置保護電位) 以及參考海洋工程中有機涂層選擇的陰極保護電位,故而本文選擇了-750,-850,-950和-1050 mV (vs SCE) 對海洋平臺研制鋼在模擬海水中進行HGL-2化學鍵合防腐涂料與陰極保護聯合保護效果的研究。
施加了不同陰極保護電位的涂層耐腐蝕性能測試采用PGSTAT302電化學工作站進行EIS測試。測試選用三電極體系:施加陰極保護電位的試樣為工作電極,Pt片為輔助電極,飽和甘汞電極為參比電極 (SCE)。阻抗測試頻率范圍為105~10-2 Hz,擾動信號為10 mV,試樣測試面積為11.34 cm2,破損面積約占測試面積的0.6%。測試溶液為人工海水溶液。為了防止外界電磁信號的干擾,EIS測試在Faraday屏蔽籠里進行。測試得到的EIS數據均采用ZSimpWin軟件進行擬合。
采用JSM-6480型掃描電子顯微鏡 (SEM) 對涂層下的金屬基體進行表面微觀形貌觀察,采用SAM型X射線能譜儀 (EDS) 對金屬基體元素進行分析,并采用X'PertPro型X射線衍射儀 (XRD) 對金屬表面附著產物進行物相分析。根據國標GBT 16545-2015 金屬和合金的腐蝕 -腐蝕試樣上腐蝕產物的清除,采用浸泡法去除金屬表面的附著物。
2 結果與討論
2.1 宏觀腐蝕形貌
破損涂層施加不同陰極保護電位1056 h后,試樣的宏觀表面形貌如圖2所示。在開路電位 (未施加陰極保護) 下的試樣 (圖2a) 破損處發生了嚴重的腐蝕,涂層表面附著了大量的腐蝕產物,破損涂層周圍未見明顯鼓泡現象。施加陰極保護電位的試樣(圖2b~e),破損處的金屬腐蝕程度降低,表面無明顯銹蝕產生;但隨著陰極保護電位的增加,破損處白色沉積物增多,破損周圍的涂層發生鼓泡的程度增大。施加不同陰極保護電位1056 h后涂層鼓泡情況見表1。每個電位下均觀察4個平行試樣,鼓泡數目及鼓泡處距離破損邊緣的距離均為4個平行試樣的平均值。可見,施加不同陰極保護電位1056 h后,隨著電位的負移,涂層鼓泡數量增多,鼓泡處距離破損邊緣的距離變大。
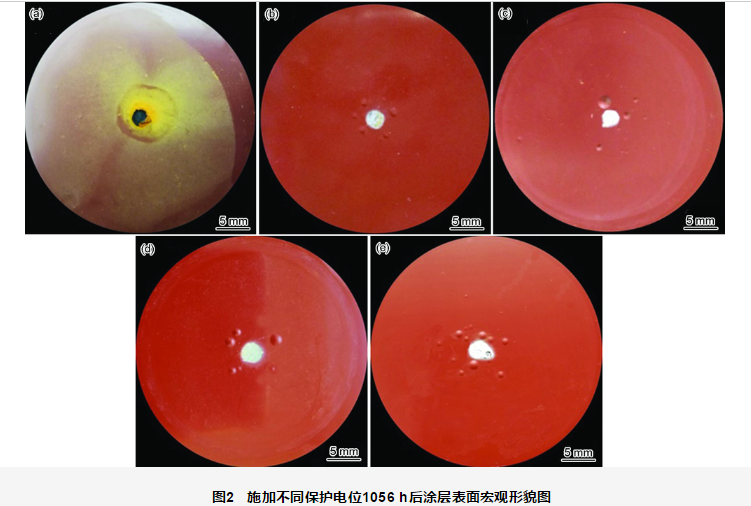
圖3為施加不同陰極保護電位后涂層陰極剝離形貌。每個電位下均觀察4個平行試樣,陰極剝離距離及剝離面積均為4個平行試樣的平均值。施加不同保護電位1056 h后涂層的剝離距離及剝離面積見表2。圖4為圖3c腐蝕處的局部放大圖,A處于未腐蝕區域,B處于圖中黑色腐蝕區域,A和B處的EDS分析結果見表3。

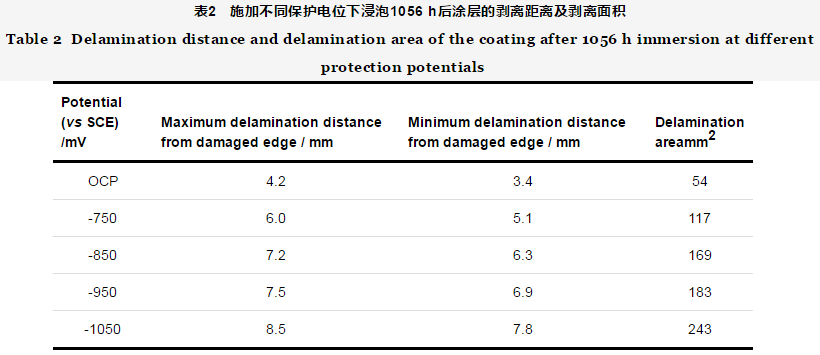
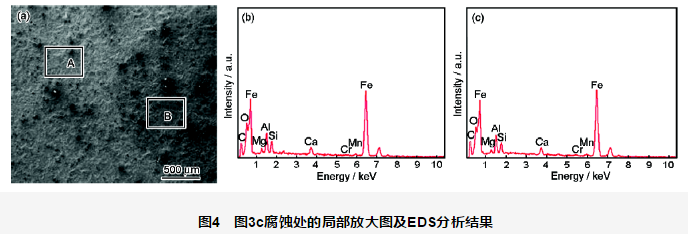
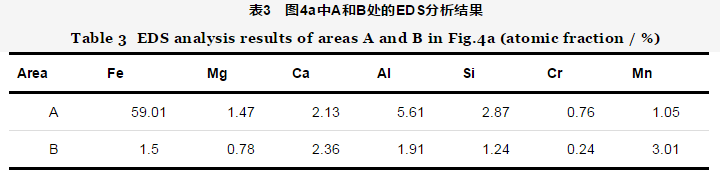
由圖3及表2可知,開路電位下的涂層陰極剝離面積最小,僅54 mm2,但破損處有明顯腐蝕發生。在-750 mV保護電位下,剝離面積增大 (增至117 mm2),破損處仍有腐蝕發生,說明此時處于欠保護狀態。-850 mV保護電位下,剝離面積進一步增大 (增至169 mm2),破損處未發生腐蝕,說明對破損處金屬基體保護效果較好。但在涂層鼓泡處,基體顏色較深,EDS結果 (圖4及表3) 顯示鼓泡區域O含量 (原子分數) 要略高于未鼓泡區域的,而Fe含量要略少于未鼓泡區域的,說明鼓泡處仍有一定腐蝕,但腐蝕非常弱。這是由于涂層的電流屏蔽作用,尤其是在涂層鼓泡失效后,涂層下的金屬可能未達到完全停止腐蝕所需的保護電流。對于-950 mV保護電位而言,陰極剝離程度與-850 mV保護電位下的相比略有增加 (增至183 mm2),但破損處與剝離處均未發生腐蝕,保護效果良好。-1050 mV保護電位下,破損處發生了嚴重的析氫現象,基體雖未發生腐蝕,但涂層剝離面積劇增 (增至243 mm2)。
2.2 EIS測試
EIS技術常被用于腐蝕過程的研究。本實驗對不同保護電位下的試樣進行EIS測試,其測試結果采用圖5中的等效電路圖進行擬合。由于破損區域較大,電化學阻抗主要反映破損處及涂層剝離區域的信息。其中,Rs是電解質溶液電阻;Qc是常相位角元件,代表沉淀膜電容;Rf是沉淀膜層電阻;Qdl代表雙電層電容;Rt代表電荷轉移電阻。
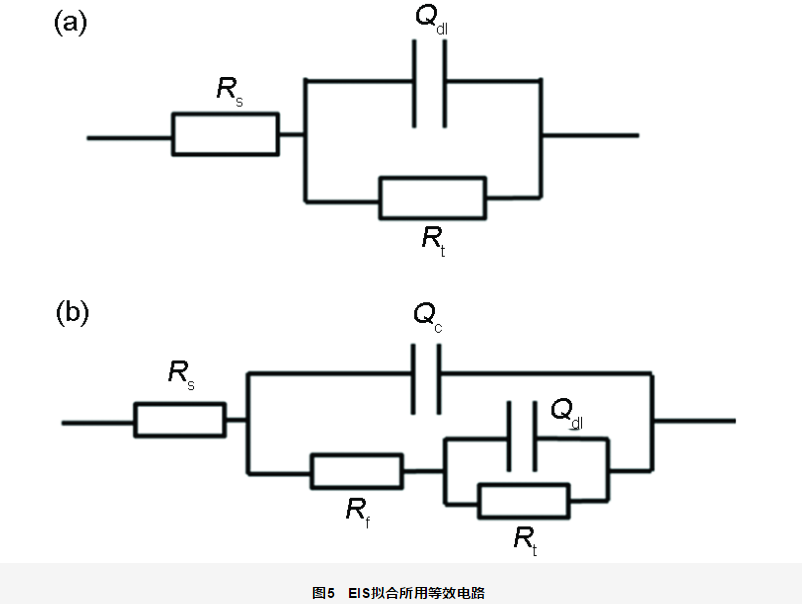
圖6a為開路電位下試樣的EIS測試結果。結果顯示,隨著浸泡時間的延長,容抗弧半徑減小,測試體系的低頻阻抗模值不斷地下降,說明隨著浸泡時間的延長,試樣腐蝕程度不斷加劇。在浸泡開始階段 (100 h),由于涂層破損處無保護作用,采用一個時間常數進行擬合 (圖5a) ;隨著浸泡時間的延長,腐蝕產物不斷堆積,在破損處的表面形成了腐蝕產物膜,浸泡后期采用兩個時間常數進行擬合 (圖5b)。
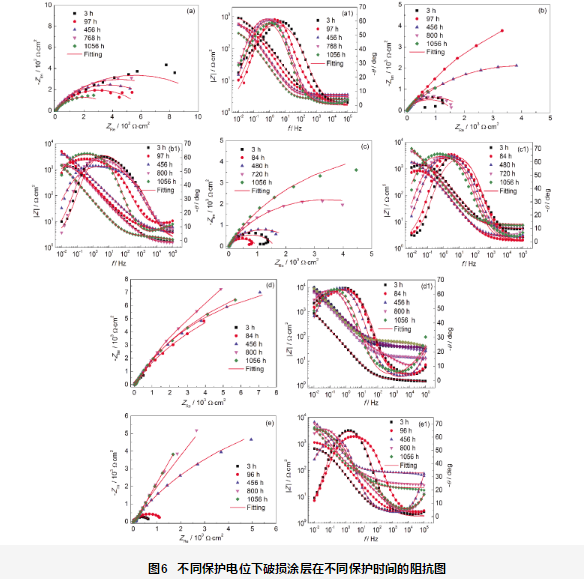
圖6b是在-750 mV保護電位下的EIS測試結果。在浸泡97 h內,涂層容抗弧稍有增大,這可能是破損處產生了稀疏的沉積層導致阻抗略增大;之后,破損處發生了腐蝕,阻抗下降,說明在模擬海水中,-750 mV保護電位不能完全為基體提供保護。在實驗初期 (100 h),采用一個時間常數 (圖5a) 進行擬合,隨著時間的延長,破損處表面生成稀疏的沉積層,采用兩個時間常數 (圖5b) 進行擬合。
圖6c是-850 mV保護電位下的EIS圖。隨著時間的延長,涂層的容抗弧增大,阻抗值呈現上升趨勢,腐蝕傾向較小,說明破損處金屬處于保護狀態。在實驗過程中,破損處逐漸形成了一層白色沉積層,導致體系中阻抗上升。說明這層沉積層對破損處的金屬有一定的保護作用,采用兩個時間常數 (圖5b) 進行擬合 (100 h之后)。
圖6d是在-950 mV保護電位下的EIS圖,與圖6c相似,隨著時間的延長,涂層的阻抗值呈現上升趨勢,說明破損處金屬處于保護狀態,腐蝕傾向較小。破損處形成了沉淀層,采用兩個時間常數的等效電路圖 (圖5b) 進行擬合 (100 h之后)。
圖6e是在-1050 mV保護電位下的EIS圖。在施加1056 h陰極保護期間,體系的阻抗值先升高后稍有降低,50 h后譜圖體現出兩個時間常數的信息,采用圖5b進行擬合,并且在實驗過程中破損處可觀察到十分嚴重的析氫現象。
2.3 不同保護電位對鈣質沉積層保護性能的影響分析
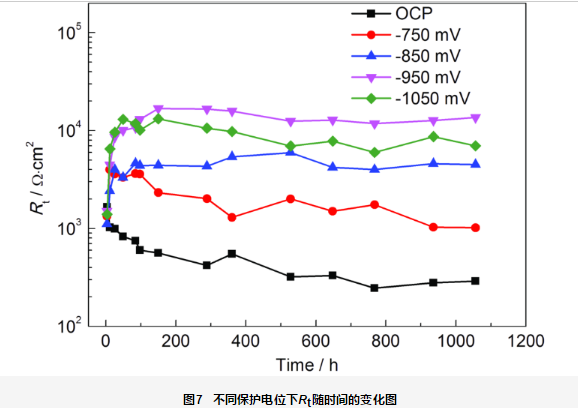
Rt表征金屬腐蝕發生的難易程度,Rt越高,金屬越不容易發生腐蝕。圖7為不同保護電位下的EIS數據擬合的Rt隨時間的變化曲線。由等效電路圖可知,在實驗過程中,EIS主要反映破損處金屬基體的信息。在開路電位下,Rt從開始的103 Ω·cm2下降到400 Ω·cm2,之后穩定在約200 Ω·cm2,表明金屬基體隨著浸泡時間的延長,更容易發生腐蝕。-750 mV保護電位下,實驗初期Rt稍有上升,100 h后略有下降,之后穩定在約3×103 Ω·cm2;-850 mV保護電位下,Rt逐漸上升,100 h后穩定在約4×103 Ω·cm2。-950 mV保護電位下,Rt逐漸上升,180 h后達到約2×104 Ω·cm2,之后穩定在1.2×104 Ω·cm2,具有最好的耐蝕性能。-1050 mV保護電位下,Rt逐漸上升,84 h后達到最高值約1.2×104 Ω·cm2;之后稍有降低,耐蝕性能略有下降。
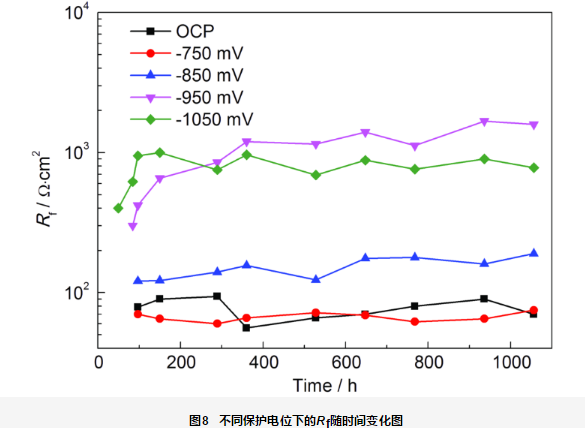
Rf一定程度上反映了鈣質沉積層保護性能的好壞,Rf值越高,鈣質沉積層保護性能越好。圖8為施加保護電位1056 h期間不同保護電位下的Rf隨時間的變化曲線。由圖可知,在開路電位及-750 mV保護電位下,Rf均很小,在10~100 Ω·cm2之間變化,沉積層幾乎無保護作用。-850 mV保護電位下,破損處Rf較開路電位和-750 mV保護電位下的略大,約在100 Ω·cm2變化。-950 mV保護電位下的Rf值一直呈現增大趨勢,在350 h后穩定在約2000 Ω·cm2。施加-1050 mV保護電位前期 (150 h),Rf值上升,之后略有下降,穩定在約800 Ω·cm2。結果顯示,-950 mV保護電位下,鈣質沉積層的保護性能最佳。
圖9為施加不同保護電位破損處沉積層物相分析結果。可見,在開路電位下破損處的腐蝕產物膜層成分為Fe2O3;-750 mV保護電位下,沉淀膜成分為CaCO3和Fe2O3,無Mg(OH)2;-850,-950和-1050 mV保護電位下沉積層的成分均為CaCO3和Mg(OH)2的混合物,無Fe2O3。李成杰等[17]研究了在靜態及動態條件下鈣質沉積層中Ca/Mg比值的變化,結果表明在-800~-1000 mV (vs SCE) 電位下均能形成不同Ca/Mg比值的鈣質沉積層。
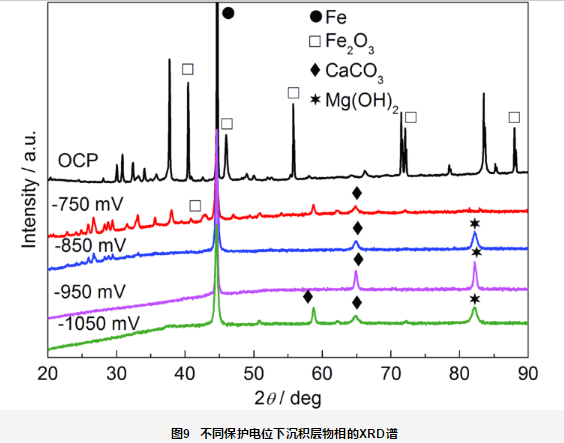
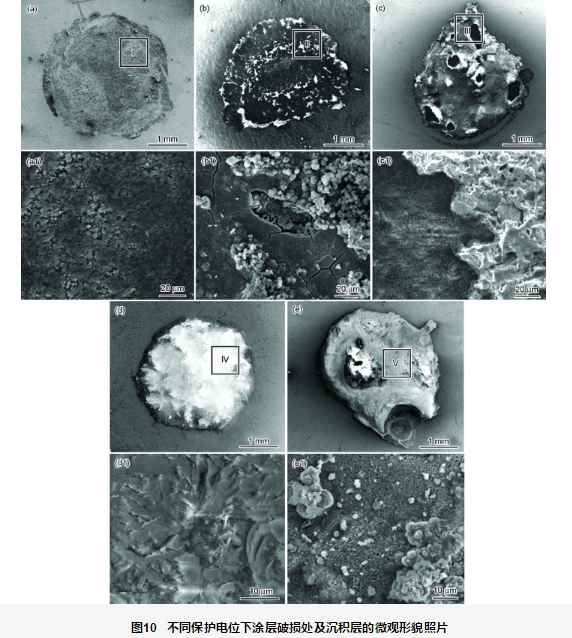
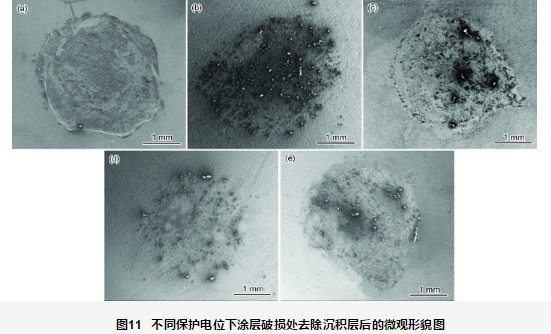
圖10為施加不同保護電位下浸泡1056 h后破損處的表面微觀形貌圖,圖11為相應地去除沉積層后的微觀形貌圖。開路電位下破損處的金屬基體經1056 h浸泡,表面生成大量的腐蝕產物 (圖10a),去除腐蝕產物后可見明顯的腐蝕坑 (圖11a)。在此過程中,涂層阻抗值不斷下降,電荷轉移電阻最低,但涂層的剝離程度較小。當不施加保護電位時,隨著水溶液沿著涂層破損處滲透到涂層/金屬界面區,溶解氧也隨水溶液一起擴散到界面區,導致作為陽極的金屬基材發生腐蝕溶解反應,陰極發生溶解氧的還原,發生如下反應:
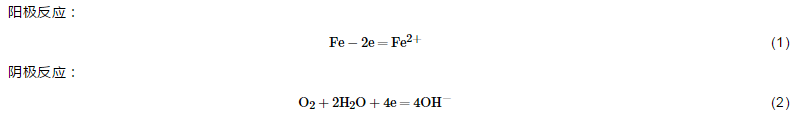
Fe的溶解量與OH-的生產量成正相關,受到腐蝕的金屬少,產生的OH-少,引起界面的堿化程度低,故而涂層未鼓泡,剝離面積小。
從圖10b可看出,-750 mV保護電位下,破損處有腐蝕產物,同時有稀疏的CaCO3沉積產生,無Mg(OH)2,沉淀層不完整,這是由于在靜態條件下CaCO3容易成核,而Mg(OH)2的形成需要在pH值達到9.3以上才能成核[17,18]。而在-750 mV電位下的界面堿性較弱,不能形成Mg(OH)2沉淀。去除表面的沉積層及腐蝕產物后,金屬沒有形成腐蝕坑。施加陰極保護電位時,仍主要發生式 (2) 的陰極反應。由外加陰極極化提供電子。當外電流提供的電子不能完全滿足氧的去極化反應時,金屬則會發生腐蝕以提供電子,即發生反應式 (1)。結合圖3b可看出,施加-750 mV保護電位時保護不足,此時的腐蝕速率小于自然浸泡下的金屬腐蝕速率,但陰極保護造成的界面堿化程度較高,造成涂層的剝離面積遠遠大于不施加陰極電位涂層的剝離面積。
從圖10c可看出,-850 mV保護電位下鈣質沉積層較-750 mV的多,沉積層分布不均勻,與基體表面相接觸的沉積層成分主要為Mg(OH)2,比較疏松,呈絮狀物沉積在表面,有的區域表面沉積層相對較厚,顆粒較大,其主要成分為CaCO3。這可能是因為在陰極極化條件下,帶正電的Mg(OH)2會被吸附到帶負電的金屬表面,而呈現顆粒狀的CaCO3的生長是在Mg(OH)2生長之后[17,19]。整個區域的沉淀層生長不均勻,膜層不完整,因此沉淀膜電阻較低。去除鈣質沉積層之后,金屬基體表面未見明顯腐蝕坑。
從圖10d可看出,-950 mV保護電位下整個鈣質沉積層則較為均勻完整,無明顯孔洞,鈣質沉積層較為致密,膜層質量較好,鈣質沉積層成分主要為CaCO3和Mg(OH)2。結合圖8可知,此時有較高的膜層電阻,約在103 Ω·cm2波動。去除沉淀膜層之后,金屬基體未見腐蝕坑。說明-950 mV保護電位對破損處金屬體系具有較好的保護效果。
在外加-850或-950 mV保護電位時,涂層剝離面積增大,仍主要發生式 (2) 的陰極反應。由于陰極極化增大,離子及氧的遷移加快,氧被還原成OH-的速度加快,局部pH值上升,堿性環境增強,使得涂層剝離加大。
從圖10e可看出,-1050 mV保護電位條件下的鈣質沉積層較厚,為CaCO3和Mg(OH)2的混合鈣質層,鈣質沉積層表面隨機分布著絮狀的Mg(OH)2及顆粒狀的CaCO3,沉積層存在明顯孔洞。去除沉淀膜層后,破損處的金屬基體未見明顯腐蝕痕跡。-1050 mV保護電位時,陰極除了發生式 (2) 的反應外還發生式 (3) 的反應:
![]()
H2的產生破壞了沉積層的完整性,表現為多孔的膜層和相對較低的膜層電阻,雖然金屬基體未發生腐蝕,但嚴重的析氫導致OH-的增多,生成大量的OH-加劇了涂層的陰極剝離 (圖3)。
綜上結果,-850,-950和-1050 mV保護電位對金屬基體的保護效果較好,開路電位及-750 mV保護電位下的保護性較弱。-1050 mV保護電位下,陰極主要發生式 (2) 和 (3) 兩個界面反應,界面堿性較強,嚴重破壞了涂層與金屬界面的附著力;從圖3及表4可以看出,涂層剝離面積大 (243 mm2)。而在-850和-950 mV電位下,主要發生式 (2) 的反應,界面堿化程度相對較低,陰極剝離程度相對較小,涂層剝離面積分別為169和183 mm2,在此保護電位范圍內,破損處的基體均未發生腐蝕。但對于涂層鼓泡處,由于涂層的電流屏蔽作用,-850 mV (vs SCE) 不能完全抑制涂層鼓泡處的金屬發生腐蝕,但腐蝕非常微弱。-950 mV保護電位下的沉淀膜層較為完整致密,阻抗及沉淀膜層電阻均較高。故而綜合考慮陰極保護電位的保護效果、界面堿化程度、陰極剝離程度等結果,認為在本實驗所研究的電位范圍內涂層防護與陰極保護協同作用最佳的保護電位是-950 mV。
3 結論
(1) 在本實驗選擇的保護電位中,隨著電位的負移,涂層剝離面積逐漸增大。
(2) 不同保護電位下破損處都生成了CaCO3或者CaCO3和Mg(OH)2的混合鈣質沉積層。其中,-950 mV (vs SCE) 保護電位下生成的沉積層完整致密。
(3) 保護電位-750 mV不能完全為金屬基體提供保護;在此保護電位下,破損處金屬仍會發生腐蝕。-850和-950 mV保護電位均能對破損處金屬提供良好的保護,使金屬基體不發生腐蝕。但由于涂層的電流屏蔽作用,-850 mV不能完全抑制涂層鼓泡處的金屬腐蝕,但腐蝕程度很輕;-1050 mV保護電位下金屬基體未發生腐蝕,但破損處發生了嚴重的析氫現象,界面堿化程度較大,涂層剝離程度最大。
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《中國腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62313558-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護網官方QQ群:140808414