6.5.1.1 腐蝕防護技術的進展和發展歷程概述
生物醫用材料的腐蝕防護技術實際上就是防腐材料的選擇和材料表面的處理技術。從生物醫用材料技術內涵的發展來看,已經有了3代。
第一代是生物惰性材料。它是從已經成熟的工程材料中篩選出有生物相容性和替代修復組織功能的材料,如廣泛采用的金屬心血管支架、鈦關節、陶瓷關節、碳材心臟瓣膜(如圖6-104)、隱形眼鏡(如圖6-105)等。其特征是植入體內有盡量小的免疫反應并長期維持其功能。

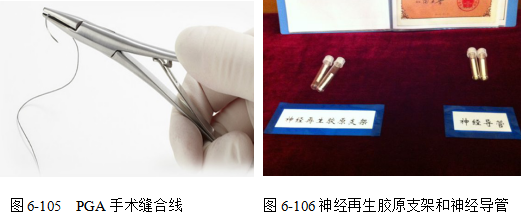
第二代是1990年代發展起來的生物活性材料和可吸收材料。生物活性材料植入體內可以和周圍環境發生良性生理作用,如生物無機材料,生物活性玻璃、生物降解陶瓷、生物玻璃陶瓷、納米生物材料等。生物可吸收高分子材料如PLA、PGA 等,用于手術縫合線(如圖6-106)、骨折固定用骨釘和骨板、可控藥物釋放體系、神經導管、醫用藥膜等。
第三代生物醫用材料涉及組織工程和基因控制及活化治療。組織工程技術修復組織器官缺陷的過程是將組織細胞吸附于生物相容性好并可被人體逐步降解吸收的框架材料上,同時細胞逐漸繁殖(在生長因子的控制下)出人體的組織。該框架材料為細胞提供一個生存的三維空間,有利于細胞獲得足夠的營養物質,進行營養物交換,使細胞能在按照預先設計的三維形狀支架上生長。這一技術的內涵是制造一個具有生命的器官,其技術參數是該器官具有全部生物功能,是一個新的人工器官。基因控制和活化治療材料能活化細胞的基因,使其表達特定的蛋白以影響細胞的功能。在材料上接枝特定的蛋白、多肽等生物分子以模擬細胞外的基質環境,以提供一個多功能的細胞結合的表面,特定的細胞識別因子可能激發基因顯性以激勵活組織的再生。
隨著生物材料這些年的應用,第二類材料在植入后10~25年內有1/3~1/2的患者因為植入失效需要重新手術,這就促進了第三代生物醫用材料的發展,第三代生物醫用材料采用材料自組裝技術和材料改性技術,這就大大的加大了材料的防腐性能并延長其使用壽命。
6.5.1.2 腐蝕問題發生的部位,主要材料
1. 腐蝕部位
生物醫用材料體積小,并且它自己就是一個完整的整體,一般一個生物醫用產品只有一種材料構成,這種材料處于人體內復雜的環境中,因此生物醫用材料的腐蝕部位就是它本身。與生物系統直接結合是生物醫學材料最基本的特征,如直接進入人體內的人工骨、牙及心、肺、腎等裝置中與血液直接接觸的材料等,除了應滿足各種生物功能等理化性質要求。生物醫學材料毫無例外地必須具有與生物體的組織相容性,這是生物醫學材料區別于其它功能材料的最重要的特征。組織相容性要求生物醫用材料不對生物產生明顯有害效應,并且會降低與生物系統直接結合而產生的腐蝕失效延長其使用壽命。
2. 主要材料:
1、醫用不銹鋼材料
按照不銹鋼材料金相組織的不同,將其分為奧氏體型、奧氏體-鐵素體型、馬氏體型以及沉淀硬化型。奧氏體型不銹鋼具有無磁性、耐腐蝕性能好和易加工成形的特點,并且價格低廉,添加鉬、鉻等元素可增強其合金結構的穩定性和強度等,是目前應用較多的一類不銹鋼,其中,316L 不銹鋼被廣泛作為支架植入材料(如圖6-108),美國材料實驗協會(ASTM)也推薦 316L 作為金屬植入材料。

2、鈦合金
鈦是具有高度化學活性的金屬,表面極易氧化成二氧化鈦形成惰性鈍化膜,很好地保護了基體,從而使鈦合金成為除了金、鉑以外最耐腐蝕的金屬。另外,鈦合金具有良好的生物相容性,能與有機體有效匹配,被認為是一種很有前途的種植體材料。鈦與鋁、釩、鐵、鋯、鉬、鎳等元素形成合金,在不同程度上提高了材料的物理機械性能。有些鈦合金材料還具有形狀記憶功能,如Ti-Ni、Ti-Ni-Nb、Ti11.5V1.7Fe3.3Al等。第一代醫用鈦金屬材料以純鈦和Ti-6Al-4V為代表,占目前醫用鈦合金市場的60%。第二代以Ti-5Al-2.5Fe、Ti-5Al-2.5Sn為代表。第三代以最新研制開發的生物相容性與力學相容性更優良的鈦合金材料為主。
3、鈷合金
生物醫用鈷合金材料通常指的是鈷鉻合金,一般分為CoCrMo合金(鑄造產品)和CoNiCrMo合金(經鍛造精密加工所得)兩類。ASTM建議使用四類鈷合金作為植入材料:鑄造CoCrMo合金(F75);鍛造CoCrWNi合金(F90);鍛造CoNiCrMo合金(F562);鍛造CoNiCrMoWFe合金(F563)。這四種鈷合金中的鑄造CoCrMo合金(F75)和CoNiCrMo合金(F562)已廣泛作為醫用植入材料。
4、鉭金屬
最近幾年,由于鉭與鉭合金具有生物相容性優良、耐腐蝕、抗疲勞強度高、加工性能和力學性能好等特點,值得一提的是,即使在腐蝕介質中,該類材料仍然具有這些性能,已經被許多研究者所關注。Chen 等指出,由于鉭具有良好的血液相容性以及 X 射線和MRI 可視性,且其氧化物基本上不會被吸收,并未顯示有毒性,可以作為血管支架的候選材料。1998 年,北京醫科大學第三醫院進行了自制的鉭絲支架植入實驗,將 17 枚支架植入 12 頭小型豬的冠狀動脈內,其實驗結果表明這種自制的鉭絲支架具有良好的 X 光下可視性,能夠快速、準確進行植入實驗,且生物相容性良好。但是鉭的價格高,資源少,加工成型困難,所以鉭合金的推廣應用受到很大限制。
5、生物醫用高分子材料(Biomedical Polymer)
醫用高分子材料是生物醫學材料中發展最早、應用最廣泛、用量最大的材料, 也是一個正在迅速發展的領域。它有天然產物和人工合成兩個來源。該材料除應滿足一般的物理、化學性能要求外, 還必須具有足夠好的生物相容性。按不同性質,醫用高分子材料可分為非降解型和可生物降解型兩類。對于前者, 要求其在生物環境中能長期保持穩定, 不發生降解、交聯或物理磨損等, 并具有良好的物理機械性能。雖然不要求它絕對穩定, 但是要求其本身和少量的降解產物不對機體產生明顯的毒副作用, 同時材料不致發生災難性破壞。該類材料主要用于人體軟、硬組織修復體、人工器官、人造血管、接觸鏡、膜材、粘接劑和管腔制品等方面。這類材料主要包括聚乙烯、聚丙烯、聚丙烯酸酯、芳香聚酯、聚硅氧烷、聚甲醛等。而可降解型高分子主要包括膠原、線性脂肪族聚酯、甲殼素、纖維素、聚氨基酸、聚乙烯醇、聚己丙酯等。它們可在生物環境作用下發生結構破壞和性能蛻變, 其降解產物能通過正常的新陳代謝被機體吸收利用或被排出體外, 主要用于藥物釋放和送達載體及非永久性植入裝置。按使用的目的或用途, 醫用高分子材料還可分為心血管系統、軟組織及硬組織等修復材料。用于心血管系統的醫用高分子材料應當著重要求其抗凝血性好, 不破壞紅細胞、血小板, 不改變血液中的蛋白并不干擾電解質等。
6、鐵
純鐵材料制備的血管支架是指鐵含量在 99.5%以上的鐵支架,具有很高的彈性模量,可用在細小血管中,且純鐵支架在人體內被氧化成亞鐵離子后,溶解到血液中,減少了平滑肌細胞的增殖,可以有效抑制血管內膜增生。Peuster 等在 2001年,用純鐵(Fe>99.8%)制備了可腐蝕性鐵支架 NOR-1,并評價了其生物安全性。將支架植入 16 只新西蘭大白兔正常降主動脈,術后 6-18 個月未見副作用,且血管一直處于擴張狀態,未見血栓。另外,組織病理學檢測也未見新生內膜增生和毒性效應。2006 年,該研究小組又在 29 頭小型豬降主動脈植入了純鐵血管支架,術后的 360 天,均未發現鐵降解產物導致的毒性。組織病理學檢測也未發現鐵超載現象以及器官毒性。Muller 等指出,鐵血管支架上的鐵離子通過影響與生長相關的基因表達水平來抑制血管平滑肌細胞的增生,從而降低了再狹窄率。不過,鐵的降解速率較慢,還需要更多的研究工作來改善其降解性能。
7、生物可降解鎂支架
鎂及鎂合金支架由于其優異的機械性能和可降解性能被認為是最具發展潛力的可降解吸收支架。鎂基材料與其他可降解材料相比具有其獨特的優點:1、鎂離子在各種生理新陳代謝中起重要作用,是人體內必須元素,在體內含量極大,對于成年男性每天的攝入量為 420 mg/day,成年女性為 320 mg/day ;鎂離子具有拮抗血管內血栓形成的作用,且有抗心率失常和治療重度抑郁癥等作用;2、具有密度小(1.7g/cm3)、與骨類似的彈性模量(41~45GPa)和良好的屈服強度(65–100MPa),鎂支架植入后有足夠的力學性能支持血管的修復,且防止血管的早期彈性回縮;3、良好的組織相容性,鎂支架降解產物為鎂離子,對細胞和組織不存在毒性,植入后能夠抑制平滑肌的增殖和促進內皮細胞的生長,加速內皮化進程,從而血栓的發生率低。4、鎂及鎂合金的腐蝕動力學使得其腐蝕能夠通過各種表面改性的方法得到可控。鎂及鎂合金的優異的力學性能、可降解性及良好的生物相容性,為解決心血管支架材料研究提供了一個新的突破點。
8、 陶瓷材料:陶瓷材料硬度高、磨損率低、磨損顆粒小。能夠解決金屬和高分子假體材料的磨損顆粒引起的骨溶解問題;另外陶瓷還可以克服假體在體內潮濕環境下容易釋放金屬離子的問題。①氧化鋁陶瓷化學性能穩定,耐磨損、生物相容性能優良。②氧化鋯陶瓷的斷裂強度是氧化鋁的2~4 倍,斷裂韌性約為其2 倍。③羥基磷灰石是骨骼無機物的主要成分,生物相容性優良,但其力學性能差,作為涂層材料可以發揮其優勢。陶瓷材料不僅具有良好的生物相容性,而且具有超高硬度、耐磨性和耐蝕性,其硬度僅次于金剛石。目前最常用的是Al2O3 和ZrO2 陶瓷。

官方微信
《中國腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62313558-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護網官方QQ群:140808414



