0 引言
鎂及鎂合金具有良好的生物相容性、可降解性與力學(xué)性能,作為生物可降解骨植入材料得到了廣泛關(guān)注[ 1]。但鎂活潑的化學(xué)性質(zhì)限制了其在這一領(lǐng)域的應(yīng)用。微弧氧化是一種減緩鎂腐蝕的有效方法[ 2]。微弧氧化層的存在使鎂合金在生理環(huán)境中的耐蝕性得到明顯的提高。然而,一方面由于作為微弧氧化層的主要成分MgO不能誘導(dǎo)羥基磷灰石形成,導(dǎo)致微弧氧化層具有較低的生物活性[ 3],另一方面,微弧氧化層多孔的結(jié)構(gòu)難以對(duì)鎂提供持續(xù)的防護(hù)[ 4]。
為提升鎂的耐蝕性能與生物性能,并保持體系的可降解性,采用陰極電沉積的方法在微弧氧化的鎂表面構(gòu)建鈣磷生物涂層。一方面,利用鈣磷涂層促進(jìn)微弧氧化鎂的生物活性,另一方面, 利用鈣磷涂層對(duì)微弧氧化層進(jìn)行封孔,增加體系的耐蝕性能[5]。鈣磷涂層的成分與人骨組織中的無(wú)機(jī)成分羥基磷灰石( Hydroxyapatite,HA) 相近,可以誘導(dǎo)HA的再沉積,有助于骨組織的修復(fù)和再生[6]。羥基磷灰石盡管生物相容性良好, 但在體液中溶解度很低,不利于降解。除了HA外,其他鈣磷組分被認(rèn)為是HA在體液中的前驅(qū)體。尤其是二水合磷酸氫鈣( Calcium hydrogen phosphate dihydrate, DCPD),在體液中的溶解度很高,其溶解轉(zhuǎn)化后會(huì)促進(jìn)HA的形成[7]。 Shi等[8] 嘗試在微弧氧化AZ80 鎂合金表面制備DCPD涂層,該涂層體系有效地誘導(dǎo)了HA在鎂合金表面的沉積。盡管在浸泡后表面出現(xiàn)了一些裂紋,但氫氣析出量的測(cè)試表明體系腐蝕性能并沒(méi)有出現(xiàn)明顯的降低。鈣磷相的轉(zhuǎn)化過(guò)程對(duì)促進(jìn)骨愈合, 保持植入材料的降解具有重要作用[9]。
目前,鎂表面復(fù)合涂層體系的報(bào)道多集中在涂層的腐蝕性能上[10]。有關(guān)鈣磷涂層在微弧氧化層表面的沉積過(guò)程及涂層之間協(xié)同作用的報(bào)道較少。此外,由于制備方法、工藝參數(shù)以及電解液選擇存在差別,各研究所報(bào)道的涂層的腐蝕性能也不盡相同[11-12]。文中主要研究涂層在模擬體液( SBF) 和細(xì)胞培養(yǎng)液中的生物性能。詳細(xì)地討論了鈣磷相在微弧氧化層表面的形成過(guò)程,以及鈣磷層及微弧氧化層之間的協(xié)同作用對(duì)體系性能的影響。
1 試驗(yàn)
1.1 涂層制備
選擇商業(yè)用純鎂(純度99.9%)為研究材料, 試樣尺寸為15 mm× 15 mm× 3 mm。采用400~2500 號(hào)SiC砂紙對(duì)試樣進(jìn)行打磨,然后用乙醇清洗2 min。利用直流單向脈沖電源對(duì)鎂片進(jìn)行微弧氧化(MAO)處理。鎂片為陽(yáng)極,不銹鋼板為陰極,電參數(shù)為恒電壓模式400 V,頻率100 Hz,占空比10%。電解液組成為20 g Na3PO4 + 1 g KOH。處理時(shí)間10 min。之后,對(duì)微弧氧化鎂進(jìn)行陰極電沉積。石墨板為陽(yáng)極,沉積電解液為0.0835 mol/L Ca(NO3)2 +0.05 mol/L KH2PO4 的混合溶液,溶液pH值調(diào)整至4.6。在初始電流密度為4.2 mA/cm 2,溫度為47℃,沉積電壓為3.5 V的條件下沉積60 min。
1.2 結(jié)構(gòu)表征及電化學(xué)性能測(cè)試
采用XRD、SEM、EDS和激光共聚焦顯微鏡(CLSM)對(duì)涂層組織結(jié)構(gòu)和形貌進(jìn)行觀察分析。采用Gamry R3000 電化學(xué)工作站對(duì)涂層的電化學(xué)性能進(jìn)行評(píng)價(jià)(包括動(dòng)電位極化曲線和電化學(xué)阻抗譜測(cè)試)。測(cè)試介質(zhì)為模擬體液( SBF),成分見(jiàn)參考文獻(xiàn)[13],測(cè)試溫度為(37±0.5)℃。測(cè)試前將試樣浸泡在SBF中30 min,使試樣表面狀態(tài)達(dá)到穩(wěn)定。動(dòng)電位極化曲線的測(cè)試從開(kāi)路電位以下0.2 V開(kāi)始,終止電流密度為2 mA/cm 2,掃描速率為0.5 mV/s。采用Corrview軟件對(duì)測(cè)得的極化曲線進(jìn)行擬合。電化學(xué)阻抗譜(EIS)測(cè)量頻率范圍為10 5~10-2 Hz。輸入信號(hào)為開(kāi)路電位上下擾動(dòng)10 mV。采用Zsimpwin軟件對(duì)阻抗譜進(jìn)行擬合。
1.3 生物性能測(cè)試
對(duì)涂層生物性能的評(píng)價(jià)包括骨形成能力和細(xì)胞黏附能力。骨形成能力試驗(yàn)時(shí),將涂層分別浸泡到SBF和組織液中,觀察涂層的組織結(jié)構(gòu)變化及HA沉積狀況。細(xì)胞黏附試驗(yàn)時(shí),將涂層浸泡到細(xì)胞培養(yǎng)液中,在涂層表面植入50 000 個(gè)髖關(guān)節(jié)組織細(xì)胞,細(xì)胞中添加染色劑,采用光學(xué)顯微鏡觀察細(xì)胞的增殖狀況。
2 結(jié)果與討論
2.1 涂層結(jié)構(gòu)特征
涂層的物相組成如圖1 所示。微弧氧化層的相組成是Mg3(PO4)2 和MgO。鈣磷涂覆后,涂層的主要成份是二水合磷酸氫鈣(DCPD)。

圖1 鈣磷涂覆前后微弧氧化鎂的XRD圖譜
涂層的表面和截面形貌如圖2 所示。微弧氧化層表面呈現(xiàn)出多孔結(jié)構(gòu),微孔不均勻地分布在試樣表面(圖2(a))。在表面可以觀察到少量的裂紋,這是由于在陶瓷層成膜過(guò)程中電解液的冷卻作用導(dǎo)致的[14]。
微弧氧化層的截面形貌(圖2(c))呈現(xiàn)明顯的雙層結(jié)構(gòu),約為1~2 μm的內(nèi)部致密層均勻地形成在鎂基體表面,外部多孔層存在著大量的微孔和放電通道(Discharge channels),其厚度約為25 μm。
鈣磷涂層形貌為片狀結(jié)構(gòu)(圖2( b)),其尺寸大約在幾十微米,呈現(xiàn)出典型的DCPD形貌特征[15]。
涂層的橫截面顯示鈣磷層的厚度約為15 μm( 圖2( d)),其中,微弧氧化外層的微孔幾乎完全被鈣磷相填充,鈣磷層和微弧氧化層交錯(cuò)結(jié)合在一起,表現(xiàn)出良好的界面結(jié)合狀況。
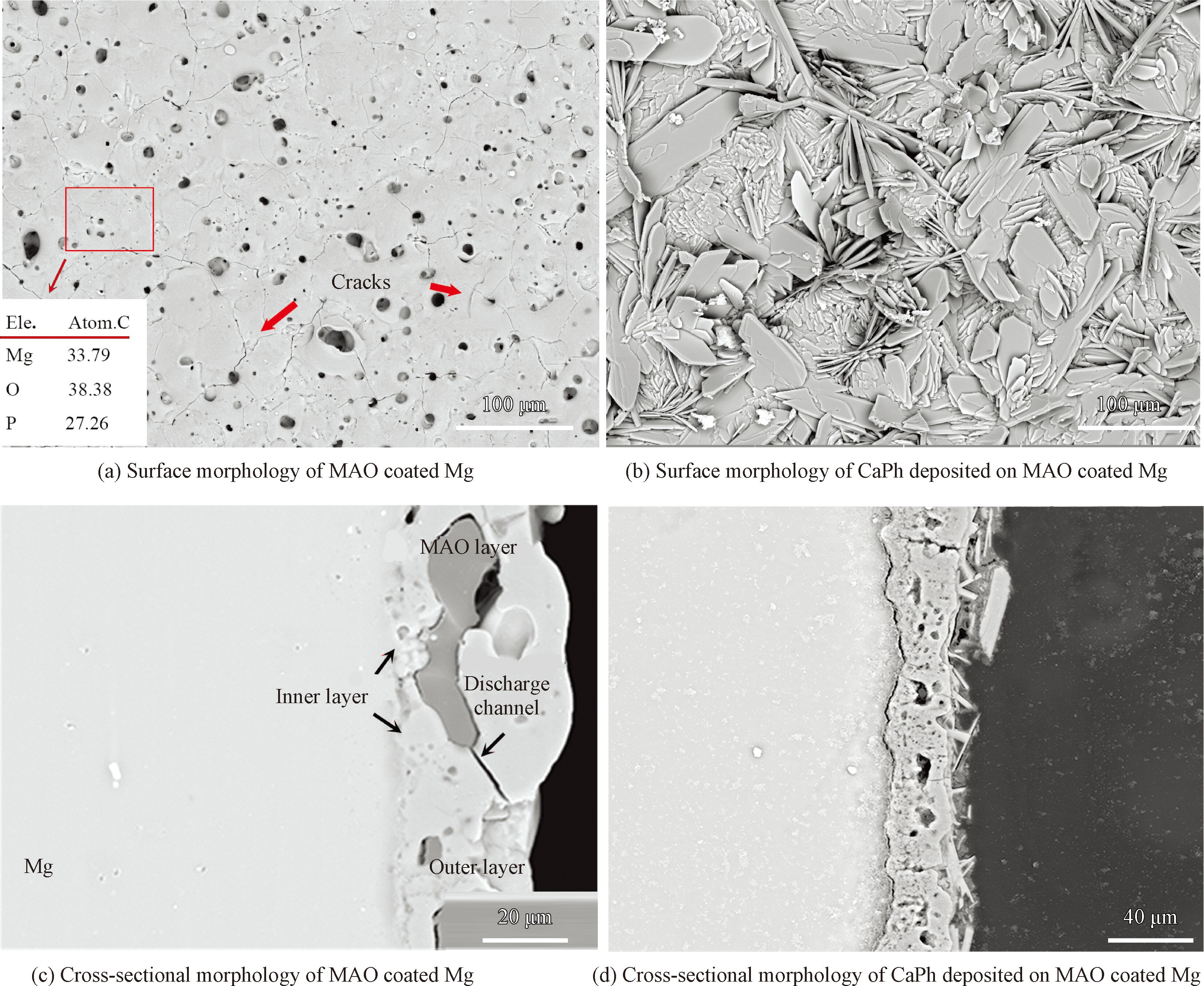
圖2 鈣磷涂覆前后微弧氧化鎂的表面和截面形貌
2.2 DCPD在微弧氧化層上的沉積機(jī)制
由于涂層中不存在HA或磷酸八鈣(Octacalcium phosphate, OCP) 等含有PO 3- 4 基團(tuán)的化合物,沉積過(guò)程中電解液中的H2PO- 4 只需一步水解,即可與Ca2+相結(jié)合生成DCPD,形成過(guò)程并不復(fù)雜,如反應(yīng)式(1)~(3)所示:
為了便于討論DCPD在微弧氧化鎂表面的形核規(guī)律,觀察了不同沉積時(shí)間(5 和30 s) 下DCPD的形核位置及分布規(guī)律,如圖3 所示。同時(shí),采用EDS掃描Ca元素的分布圖(Elemental mapping)。值得注意的是, 在電場(chǎng)的作用下,DCPD在微弧氧化層表面的形核長(zhǎng)大并不是隨機(jī)發(fā)生的。沉積開(kāi)始時(shí),形核的位置主要集中在微弧氧化層表面的微孔處(圖3( a)),對(duì)應(yīng)的鈣元素分布圖中可見(jiàn)微孔附近Ca的分布較多(圖3( c))。隨沉積時(shí)間的增加,微弧氧化層表面的Ca分布越來(lái)越多(圖3(d)),意味著DCPD不斷聚集長(zhǎng)大(圖3(b))。由于微弧氧化層的結(jié)構(gòu)特點(diǎn),其微孔結(jié)構(gòu)可分為通孔和半封閉孔,此外,高壓下形成的微弧氧化層中還存在大量的放電通道(圖2(c))。這些通孔和放電通道為電沉積過(guò)程提供了離子交換通道。沉積開(kāi)始時(shí), DCPD在電場(chǎng)力作用下優(yōu)先在通孔位置沉積。與此同時(shí),微弧氧化層的MgO在弱酸性的電解液中會(huì)發(fā)生部分溶解,其反應(yīng)如方程式(4)所示:
(4)

圖3 沉積不同時(shí)間下DCPD的SEM形貌與對(duì)應(yīng)的元素分布圖
微弧氧化層的溶解使涂層中的半封閉孔暴露在電解液中,成為通孔。這為離子的交換提供了更多的通道,使DCPD持續(xù)沉積并覆蓋整個(gè)表面。最終在微弧氧化層表面形成一層均勻的DCPD。
2.3 涂層的電化學(xué)腐蝕行為
鈣磷涂覆前后微弧氧化鎂的電化學(xué)阻抗譜及相應(yīng)的等效電路如圖4( a)~4( d) 所示[16]。 Bode圖表明,微弧氧化試樣在0~48 h內(nèi)呈現(xiàn)出3 個(gè)時(shí)間常數(shù)(圖4(a)),分別分布在高頻(10 3~10 4 Hz)、中頻(1~10 2 Hz)和低頻(10-2~1 Hz)區(qū)域。 3 個(gè)時(shí)間常數(shù)分別涉及微弧氧化外層、內(nèi)層和基體與涂層之間的雙電層在體系中的電化學(xué)響應(yīng)。鈣磷涂覆后,阻抗譜圖仍呈現(xiàn)出3 個(gè)時(shí)間常數(shù)(圖4( c)),但其所代表的物理意義發(fā)生了變化。高頻的時(shí)間常數(shù)代表鈣磷層和微弧氧化外層相結(jié)合的電化學(xué)響應(yīng),中頻和低頻分別代表微弧氧化內(nèi)層和雙電層的電化學(xué)響應(yīng)。
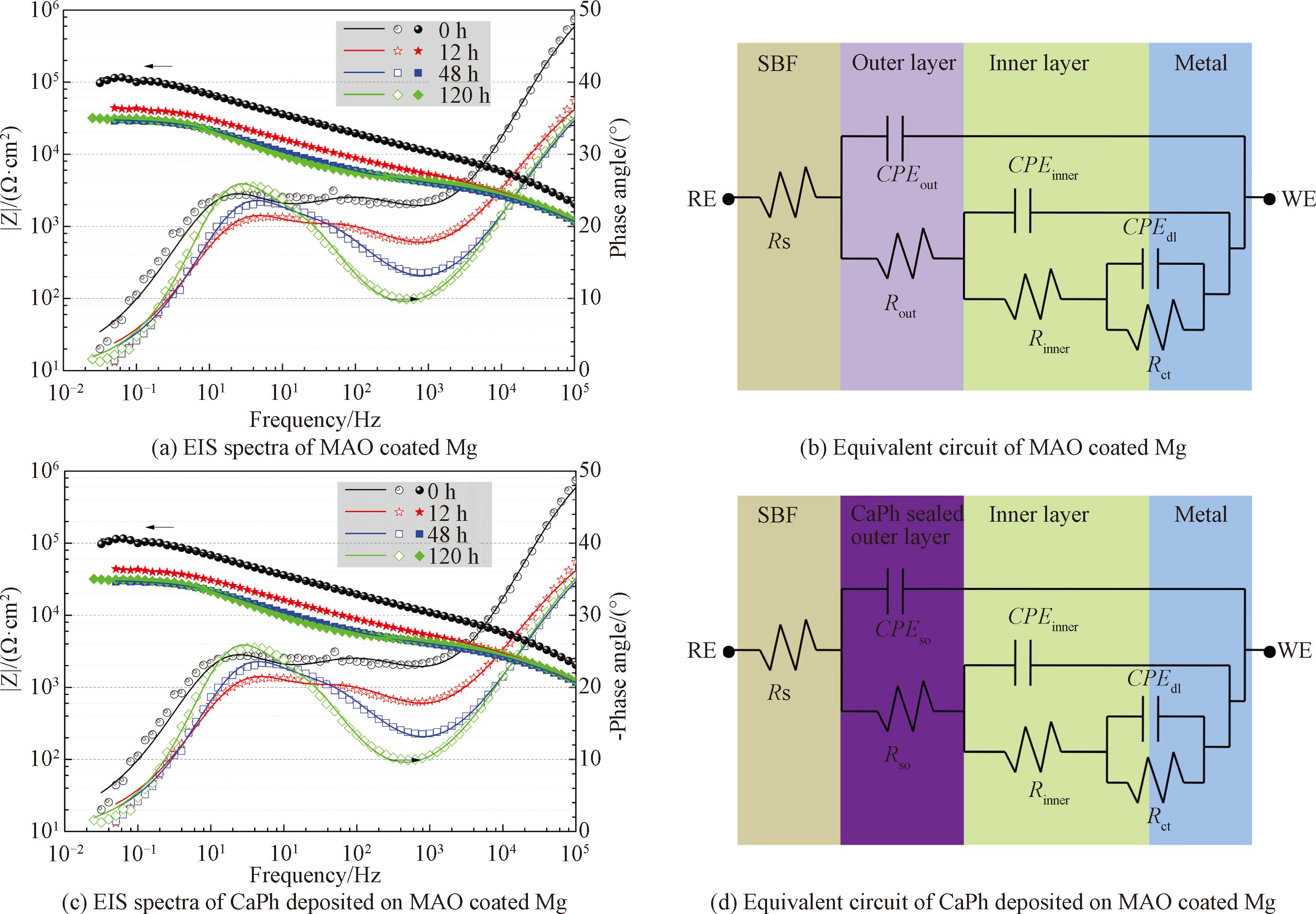
圖4 復(fù)合涂層在SBF中的電化學(xué)阻抗譜和相應(yīng)的等效電路[16]
在圖4(b)和4( d)的等效電路中,R 與 CPE 分別代表各自元件對(duì)應(yīng)的極化電阻值與常相位元件值。其中,Rs 為溶液電阻,Rout、 CPEout、Rinner 與 CPEinner 分別表示微弧氧化外層和內(nèi)層的極化電阻值與電容值。 Rso 與 CPEso 分別表示鈣磷涂覆后微弧氧化外層的極化電阻值與電容值。 Rct 與 CPEdl 分別表示鎂基體和微弧氧化層之間的電荷轉(zhuǎn)移電阻和雙電層電容。
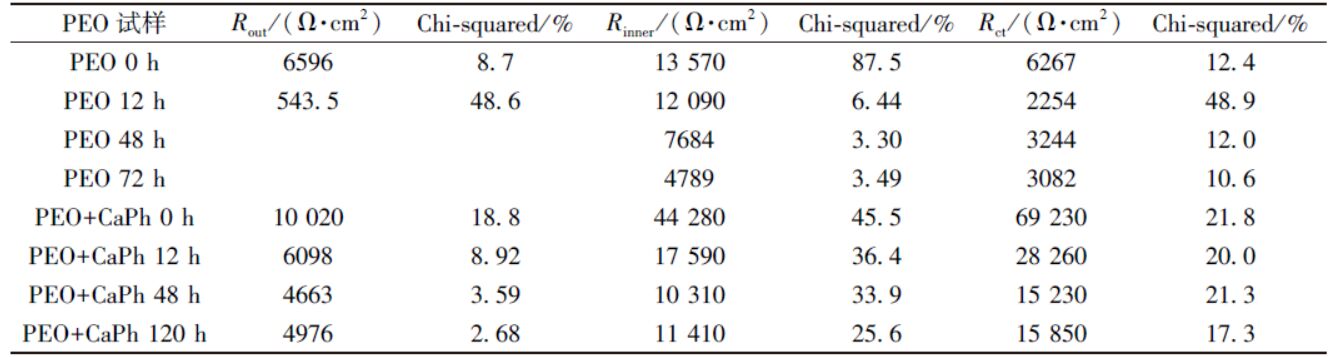
低頻的阻抗模值可以反應(yīng)體系的耐蝕性能。通常鎂及鎂合金的阻抗模值僅為10 3 Ω·cm 2 左右,在SBF浸泡過(guò)程中阻抗模值通常迅速降低[17]。微弧氧化試樣浸泡初期(0 h)低頻阻抗模值為3×10 4 Ω·cm 2。在6 h內(nèi)下降到10 4 Ω·cm 2左右,但在隨后的浸泡過(guò)程中基本保持穩(wěn)定。對(duì)于大多數(shù)的生物植入材料而言,在植入初期耐蝕性能下降最為明顯。此后,腐蝕產(chǎn)物和HA的沉積會(huì)阻止腐蝕介質(zhì)與基體的接觸,阻抗模值會(huì)在一定的時(shí)間范圍內(nèi)保持不變。鈣磷涂覆后,試樣的低頻阻抗模值達(dá)到了10 5 Ω·cm 2,表明體系的耐蝕性能得到進(jìn)一步提升。阻抗模值在0~12 h內(nèi)下降到4×10 4 Ω·cm 2,之后幾乎保持不變,表現(xiàn)出了穩(wěn)定的耐蝕性能。擬合后各元件的總電阻值(鈣磷層、微弧氧化層和雙電層擬合后電阻值的總和)如圖5 所示,其變化趨勢(shì)與低頻阻抗模值變化趨勢(shì)相同,在浸泡初期總電阻值快速下降, 而后基本保持不變,進(jìn)一步說(shuō)明了復(fù)合涂層在SBF中耐蝕性能較為穩(wěn)定。擬合后各元件極化電阻值及相應(yīng)誤差如表1 所示。各元件所對(duì)應(yīng)阻抗均呈現(xiàn)出緩慢下降的趨勢(shì),擬合誤差較低, 說(shuō)明采用的等效電路與試樣的阻抗譜圖匹配良好。
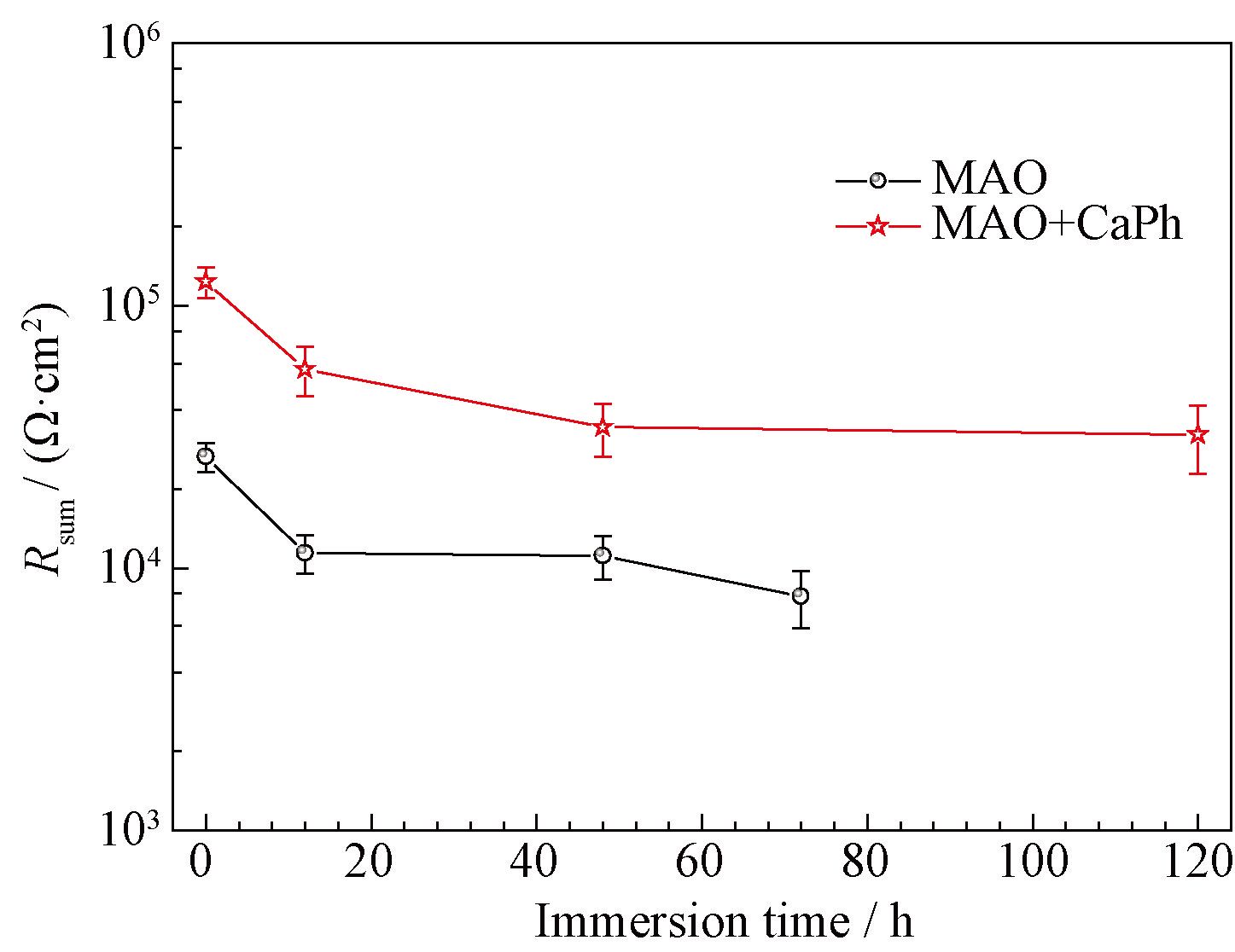
圖5 鈣磷涂覆前后微弧氧化鎂的總極化電阻值
表1 電化學(xué)阻抗譜圖的擬合結(jié)果
鈣磷涂覆前后的動(dòng)電位極化曲線如圖6 所示。純鎂的腐蝕電流密度( i corr) 和腐蝕電位(Ecorr)僅為(1.74±0.52) × 10-4 A·cm-2和-1.92 V。經(jīng)微弧氧化處理后,i corr 下降了約2 個(gè)數(shù)量級(jí), Ecorr 上升了200 mV。鈣磷涂覆試樣的 i corr 略有下降,Ecorr 則繼續(xù)上升了約200 mV。該試樣在SBF中浸泡120 h后,Ecorr 降低了60 mV,但 i corr沒(méi)有明顯變化。說(shuō)明在120 h浸泡過(guò)程中,腐蝕速率并沒(méi)有顯著增加。 EIS和極化曲線結(jié)果表明復(fù)合涂層大幅度提升了鎂基體的耐蝕性能。
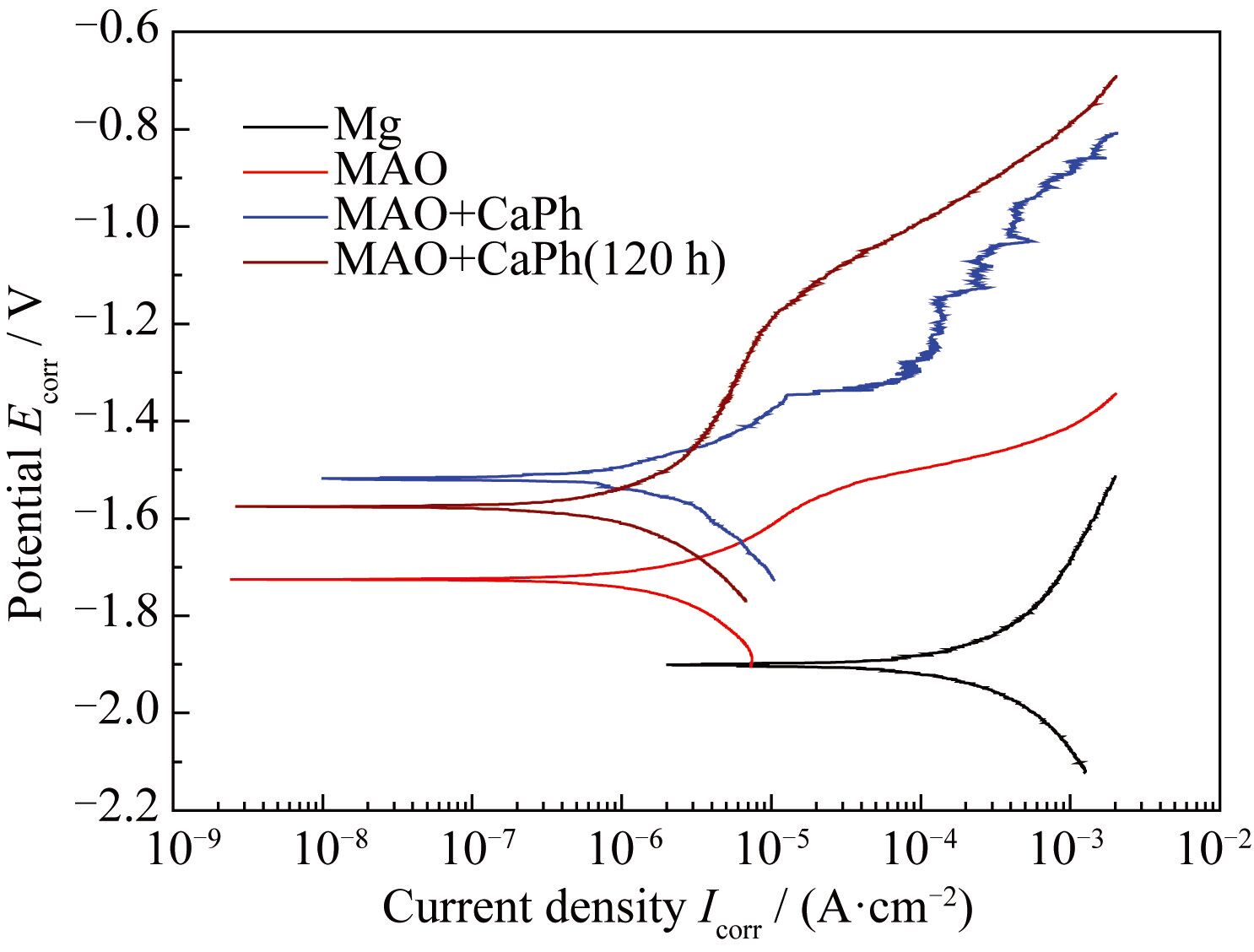
圖6 涂覆前后鎂在SBF中的動(dòng)電位極化曲線
2.4 涂層的生物性能
為了評(píng)價(jià)涂層的骨形成能力,鈣磷涂覆的微弧氧化鎂被分別浸泡在SBF和細(xì)胞培養(yǎng)液中。在SBF中浸泡120 h后涂層的表面形貌和物相組成分別如圖7(a)和7(b)所示。浸泡后DCPD片的尺寸明顯減小,XRD結(jié)果表明,DCPD衍射峰的相對(duì)強(qiáng)度明顯降低,與此同時(shí),發(fā)現(xiàn)了新的HA衍射峰。這表明隨著DCPD的溶解,HA逐漸沉積到試樣表面。
在細(xì)胞培養(yǎng)液中浸泡14 d后的表面形貌如圖8(a)和8(b)所示。圖中仍可以清晰地觀察到DCPD的片狀結(jié)構(gòu),且其尺寸沒(méi)有明顯的變化。在高的放大倍數(shù)下(圖8(b))可以觀察到球狀和菜花狀結(jié)構(gòu)。 EDS分析結(jié)果表明,該結(jié)構(gòu)中所含有的鈣磷元素原子百分比約為1.6。同樣比例的鈣磷結(jié)構(gòu)在其他研究中也有報(bào)道,其為典型的類(lèi)骨羥基磷灰石組織結(jié)構(gòu)[18]。
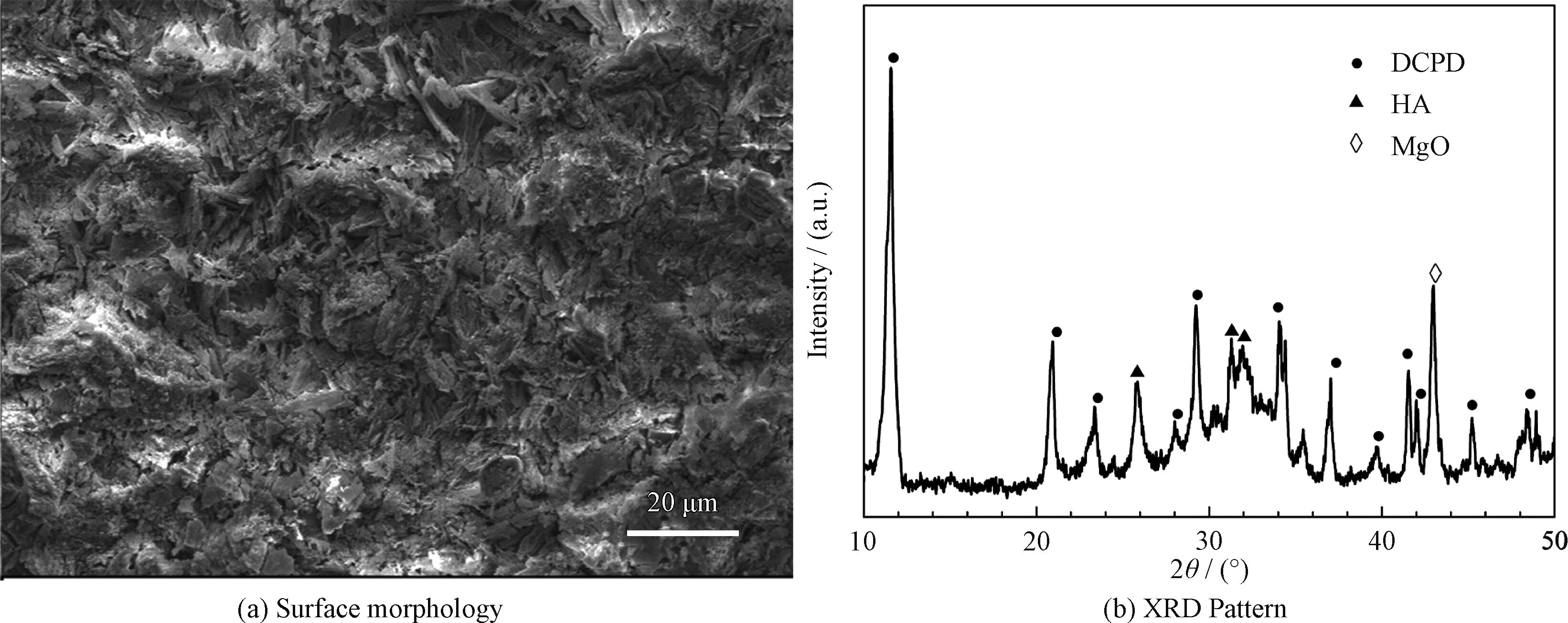
圖7 復(fù)合涂層在SBF中浸泡120 h后的表面形貌和XRD圖譜

圖8 復(fù)合涂層在細(xì)胞培養(yǎng)液中浸泡14 d后的表面形貌
浸泡試驗(yàn)結(jié)果表明,無(wú)論是在SBF還是細(xì)胞培養(yǎng)液中,涂層均表現(xiàn)出了誘導(dǎo)HA沉積的能力。 DCPD在弱堿性體液中的溶解度較高,溶解后依據(jù)反應(yīng)式(5)及(6)在涂層表面附近釋放出一定量的Ca2+和PO 3- 4。試樣表面局部鈣磷離子濃度的升高,會(huì)促進(jìn)HA的沉積,如反應(yīng)式( 7) 所示:
有所不同的是,通過(guò)比較DCPD在兩種介質(zhì)中的結(jié)構(gòu)演化發(fā)現(xiàn),DCPD在SBF中的溶解速率更快,從而更易于誘導(dǎo)HA沉積在試樣表面。由于SBF的化學(xué)成分與細(xì)胞培養(yǎng)液中的無(wú)機(jī)成分相似,其主要用于評(píng)估HA的體外沉積能力,與體液中蛋白物質(zhì)的氧化還原和細(xì)胞間反應(yīng)無(wú)關(guān)。同時(shí),SBF溶液每2 d更換一次,及時(shí)地補(bǔ)充了試樣表面由于HA沉積所消耗的Ca和P原子,從而加速了HA的沉積過(guò)程。因此, 在SBF中DCPD的溶解和HA的轉(zhuǎn)化速率更快。
在細(xì)胞培養(yǎng)液中培養(yǎng)14 d后的細(xì)胞黏附情況如圖9 所示。大量的活細(xì)胞黏附在了涂層表面,且細(xì)胞形狀狹長(zhǎng),表明細(xì)胞在培養(yǎng)后出現(xiàn)了的增殖分化,表現(xiàn)出了良好的細(xì)胞黏附和增殖分化能力。研究報(bào)道,與鎂的氧化物或無(wú)機(jī)鹽相比,細(xì)胞的絲狀偽足更優(yōu)先于在鈣磷相上沉積[19]。從圖9 中可以觀察到,黏附的細(xì)胞呈帶狀或者網(wǎng)狀分布,其特征與DCPD的結(jié)構(gòu)相似,可以推斷,細(xì)胞更優(yōu)先地在鈣磷物相上粘附。此外,細(xì)胞的黏附還與涂層的表面狀態(tài)和腐蝕性能有關(guān)[20]。在整個(gè)培養(yǎng)過(guò)程中,DCPD不斷地溶解并轉(zhuǎn)化成HA,在一定程度上降低了細(xì)胞在涂層上的黏附數(shù)量。但由于體系的耐蝕性較高, DCPD向HA轉(zhuǎn)化進(jìn)行緩慢,保持了表面狀態(tài)的穩(wěn)定性,因而對(duì)細(xì)胞在表面粘附影響有限。
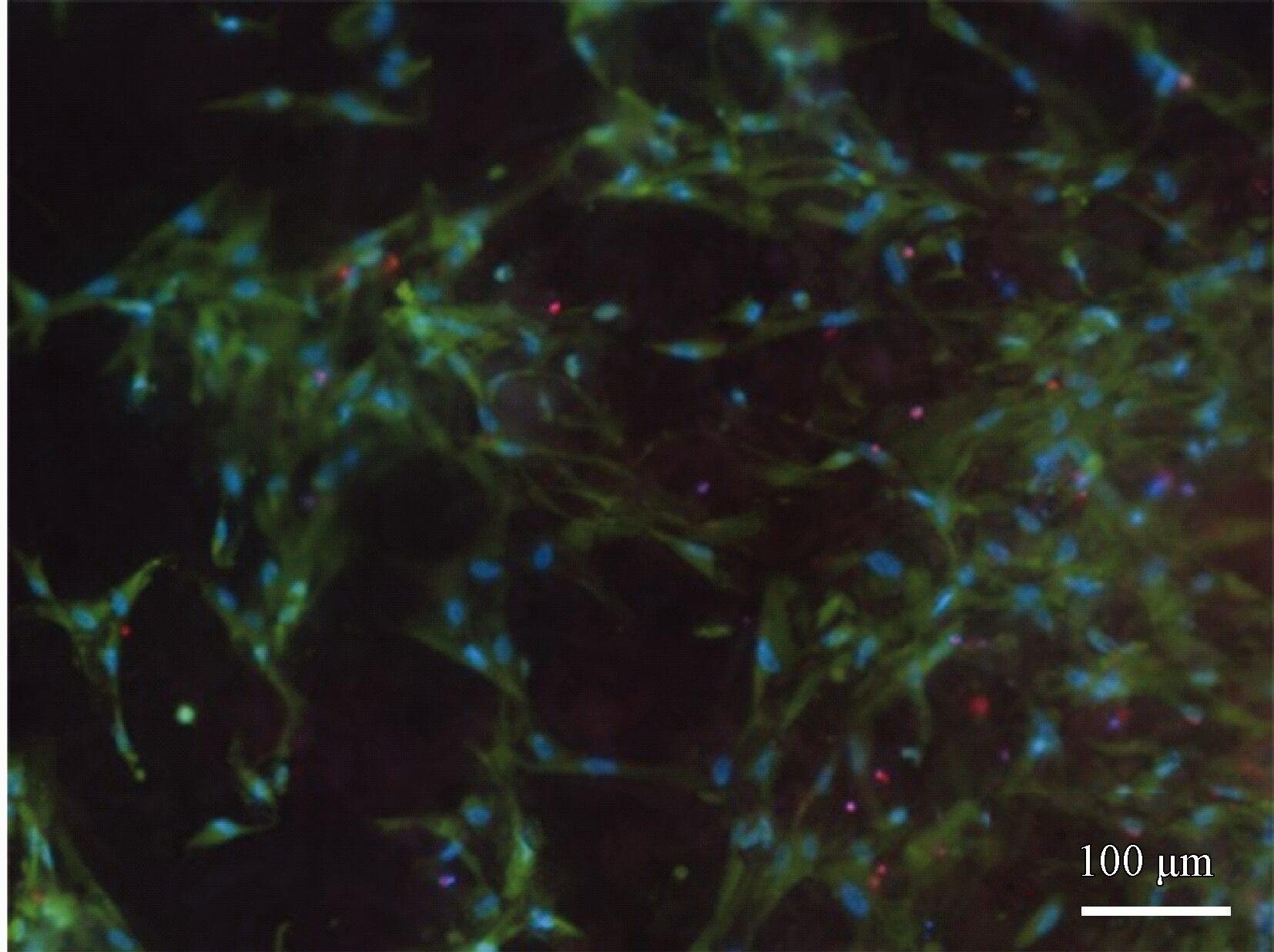
圖9 復(fù)合涂層在細(xì)胞培養(yǎng)液中浸泡14 d后的細(xì)胞粘附
2.5 復(fù)合涂層的耐蝕性及生物活性
作為骨植入材料,鈣磷涂層具有明顯的優(yōu)勢(shì)。 DCPD被認(rèn)為是HA在體液中的前驅(qū)體,擁有較高的Gibbs自由能,在模擬體液中浸泡后可以溶解釋放出Ca2+ 和PO 3- 4,誘導(dǎo)HA形成[21]。這一過(guò)程對(duì)于促進(jìn)骨愈合、誘導(dǎo)骨生長(zhǎng)具有顯著的作用。因此,研究者們更愿意嘗試在鎂表面構(gòu)建DCPD涂層,而不是直接沉積HA涂層[22]。但直接在鎂表面沉積DCPD并不是最佳選擇,由于涂層與鎂基體靠物理吸附,兩者之間的結(jié)合力較差,DCPD在體液中的快速溶解伴隨部分脫落會(huì)導(dǎo)致鎂基體裸露在腐蝕介質(zhì)中,從而造成基體的快速腐蝕失效。
采用微弧氧化與電沉積相結(jié)合的復(fù)合涂層可以有效地解決這一問(wèn)題。微弧氧化層的存在,不僅阻礙了腐蝕介質(zhì)的滲透,提高了鎂的耐蝕性,而且其粗糙的表面為鈣磷相的形核提供了更多的位置。此外,微弧氧化層和鈣磷層之間通過(guò)機(jī)械交錯(cuò)咬合(圖2( d)),可有效提高涂層與基體的結(jié)合力,從而降低DCPD在SBF和細(xì)胞培養(yǎng)液中的溶解速率,使整個(gè)涂層體系可以穩(wěn)定降解。在浸泡初期,由于DCPD層的封孔作用,延緩了腐蝕介質(zhì)的快速滲透,提高了涂層體系的耐蝕性。隨著浸泡時(shí)間的延長(zhǎng),盡管DCPD的溶解會(huì)加速涂層體系的腐蝕,但由于促進(jìn)了HA的沉積,在一定程度上保持了體系的穩(wěn)定性。
毫無(wú)疑問(wèn),體系的耐蝕性能對(duì)其骨形成和細(xì)胞黏附過(guò)程起到至關(guān)重要的影響。以往有關(guān)DCPD涂層細(xì)胞黏附報(bào)道較少的主要原因是涂層體系的腐蝕性能較差,腐蝕反應(yīng)阻礙了HA的沉積和細(xì)胞絲狀偽足的吸附[23]。通過(guò)構(gòu)建微弧氧化和鈣磷復(fù)合涂層,強(qiáng)化了涂層與基體之間的界面結(jié)合,提升了體系的穩(wěn)定性。保證了DCPD向HA轉(zhuǎn)化和細(xì)胞絲狀偽足的黏附過(guò)程的平穩(wěn)進(jìn)行。在細(xì)胞培養(yǎng)液中浸泡14 d后,仍可觀察到DCPD的存在,同時(shí)觀察到類(lèi)骨狀HA結(jié)構(gòu)(圖8(b)),活細(xì)胞幾乎分布在整個(gè)復(fù)合涂層試樣的表面(圖9), 表現(xiàn)出了良好的骨形成和細(xì)胞黏附能力。
3 結(jié)論
采用微弧氧化和電沉積相結(jié)合的方法,在鎂表面制備了微弧氧化層及鈣磷復(fù)合涂層,通過(guò)復(fù)合涂層組織及性能研究,得到的主要結(jié)論如下。
(1) 微弧氧化層的相組成為Mg3( PO4)2 和MgO,鈣磷涂層的主要相結(jié)構(gòu)為DCPD;鈣磷相優(yōu)先在微弧氧化層中的通孔和放電通道處形核,鈣磷相的沉積對(duì)微弧氧化層起到封孔作用,鈣磷層和微弧氧化層之間通過(guò)機(jī)械咬合方式結(jié)合在一起。
(2) 復(fù)合涂層表現(xiàn)出較高的耐蝕性能和生物活性,與未涂覆的鎂基體相比,腐蝕電位上升了400 mV,腐蝕電流密度降低了約3 個(gè)數(shù)量級(jí), 在SBF中浸泡120 h后的阻抗測(cè)量過(guò)程中,體系總極化電阻值穩(wěn)定在4×10 4 Ω·cm 2。
(3) 在SBF及細(xì)胞營(yíng)養(yǎng)液的浸泡過(guò)程中, DCPD逐漸溶解并促進(jìn)類(lèi)骨狀HA在涂層表面析出,涂層表現(xiàn)出良好的細(xì)胞活性,活細(xì)胞幾乎粘附在整個(gè)涂層表面。
參考文獻(xiàn)
[1] STAIGER M P,PIETAK A M,HUADMAI J,et al.Magne-sium and its alloys as orthopedic biomaterials:A review[J].Biomaterials,2006,27:1728-1734.
[2] YANG J J,LU X P,BLAWERT C,et al.Microstructure and corrosion behavior of Ca/P coatings prepared on magnesi-um by plasma electrolytic oxidation[J].Surface & Coatings Technology,2017,319:359-369.
[3] KHALAJABADI S Z,KADIR M R A,IZMAN S,et al.The effect of MgO on the biodegradation,physical properties and biocompatibility of a Mg/HA/MgO nanocomposite manufac-tured by powder metallurgy method [J].Journal of Alloys and Compounds,2016,655:266-280.
[4] GAO J H,GUAN S K,CHEN J,et al.Fabrication and characterization of rod-like nano-hydroxyapatite on MAO coat-ing supported on Mg-Zn-Ca alloy[J].Applied Surface Sci-ence,2011,257:2231-2237.
[5] TIAN P,LIU X,DING C.In vitro degradation behavior and cytocompatibility of biodegradable AZ31 alloy with PEO/HT composite coating[J].Colloids and Surfaces B-Biointerfac-es,2015,128:44-54.
[6] SONG Y W,ZHANG S,LI J,et al.Electrodeposition of Ca-P coatings on biodegradable Mg alloy:In vitro biomineralization behavior[J].Acta Biomaterialia,2010,(6):1736-1742.
[7] BAKHSHESHI-RAD H R,IDRIS M H,KADIR M R,Syn-thesis and in vitro degradation evaluation of the nano-HA/MgF2 and DCPD/MgF2 composite coating on biodegradable Mg-Ca-Zn alloy[J].Surface & Coatings Technology,2013,222:79-89.
[8] SHI Y,QI M,CHEN Y,et al.MAO-DCPD composite coat-ing on Mg alloy for degradable implant applications[J].Ma-terials Letters,2011,65:2201-2204.
[9] SHADANBAZ S,DIAS G J.Calcium phosphate coatings on magnesium alloys for biomedical applications:A review[J].Acta Biomaterialia,2012,8:20-30.
[10] GAO Y H,YEROKHIN A,MATTHEWS A.Deposition and evaluation of duplex hydroxyapatite and plasma electrolytic oxidation coatings on magnesium [J].Surface & Coatings Technology,2015,269:170-182.
[11] SHI H,YE X,HE F,et al.Improving osteogenesis of calci-um phosphate bone cement by incorporating with lysine:An in vitro study [J].Colloids and Surfaces B-Biointerfaces,2019,177:462-469.
[12] ANAWATI,ASOH H,ONO S.Enhanced uniformity of apa-tite coating on a PEO film formed on AZ31 Mg alloy by an al-kali pretreatment [J].Surface & Coatings Technology,2015,272:182-189.
[13] BAKHSHESHI H R,HANZAH E,ISMAIL A F,et al.In vitro degradation behavior,antibacterial activity and cytotox-icity of TiO2-MAO/ZnHA composite coating on Mg alloy for orthopedic implants [J].Surface & Coatings Technology,2018,334:450-460.
[14] LU X P,BLAWERT C,HUANG Y D,et al.Plasma elec-trolytic oxidation coatings on Mg alloy with addition of SiO2 particles[J].Electrochimica Acta,2016,187:20-33.
[15] CHENG Z,LIAN J,YANG H,et al.Biocompatible DCPD coating formed on AZ91D magnesium alloy by chemical depo-sition and its corrosion behaviors in SBF [J].Journal of Bionic Engineering,2014,11:610-619.
[16] HAN J P,BLAWERT C,TANG S W,et al.Effect of sur-face pre-treatments on the formation and degradation behavior of a caluium phosphate coationg on pure magnesium [J].Coatings,2019,259:1-18.
[17] MAO L,ZHOU H,CHEN L,et al.Enhanced biocompati-bility and long-term durability in vivo of Mg-Nd-Zn-Zr alloy for vascular stent application[J].Journal of Alloys and Com-pounds,2017,720:245-253.
[18] SUNDAR L S,ANJUM N A,FERRO M C,et al.Biocom-patibility and biotoxicity of in-situ synthesized carboxylated nanodiamond-cobalt oxide nanocomposite[J].Journal of Ma-terials Science & Technology,2017,33:879-888.
[19] KHALAJABADI S Z,KADIR M R A,IZMAN S,et al.The effect of MgO on the biodegradation,physical properties and biocompatibility of a Mg/HA/MgO nanocomposite manufac-tured by powder metallurgy method [J].Journal of Alloys and Compounds,2016,655:266-280.
[20] ASRI R I M,HARUN W S W,SAMYKANO M,et al.Cor-rosion and surface modification on biocompatible metals:A review[J].Materials Science & Engineering C,Materials for Biological Applications,2017,77:1261-1274.
[21] HAN J P,TANG S W,SAN H S,et al.Formation mecha-nism of calcium phosphate coating on a plasma electrolytic oxidized magnesium and its corrosion behavior in simulated body fluids[J].Journal of Alloys and Compounds,2020,818:152834.
[22] ZENG C Y,ZENG R C,LI C L,et al.Comparison of calci-um phosphate coatings on Mg-Al and Mg-Ca alloys and their corrosion behavior in Hank′s solution[J].Surface & Coat-ings Technology,2010,204:3636-3640.
[23] SURMENEV R A,SURMENEVA M A,IVANOVA A A,Significance of calcium phosphate coatings for the enhance-ment of new bone osteogenesis-A review[J].Acta Biomate-rialia,2014,10:557-579.
免責(zé)聲明:本網(wǎng)站所轉(zhuǎn)載的文字、圖片與視頻資料版權(quán)歸原創(chuàng)作者所有,如果涉及侵權(quán),請(qǐng)第一時(shí)間聯(lián)系本網(wǎng)刪除。

官方微信
《中國(guó)腐蝕與防護(hù)網(wǎng)電子期刊》征訂啟事
- 投稿聯(lián)系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 中國(guó)腐蝕與防護(hù)網(wǎng)官方QQ群:140808414





