金屬的腐蝕速度與極化作用
文/林玉珍·北京化工大學(xué)
在實(shí)際中,人們不僅關(guān)心金屬設(shè)備和材料的腐蝕傾向,更重要的是關(guān)心腐蝕過(guò)程進(jìn)行的速度。一個(gè)大的腐蝕傾向不一定對(duì)應(yīng)著一個(gè)高的腐蝕速度。例如鋁,從熱力學(xué)角度看,它的腐蝕傾向很明顯,但在某些介質(zhì)中,它的腐蝕速度卻極低,比那些腐蝕傾向較小的金屬更耐蝕。可見,腐蝕傾向并不能作為腐蝕速度的尺度。對(duì)于金屬設(shè)備來(lái)說(shuō),要設(shè)法來(lái)降低腐蝕反應(yīng)的速度,以達(dá)到延長(zhǎng)其使用壽命的目的。為此,必須了解腐蝕過(guò)程的機(jī)理,掌握不同條件下腐蝕的動(dòng)力學(xué)規(guī)律以及影響腐蝕速度的各種因素,并尋求有效地解決方案。
腐蝕原電池
腐蝕發(fā)生的根本原因是由于環(huán)境中有氧化劑存在。而在工程中“材料/環(huán)境”組成的電極系統(tǒng),由于種種原因(如材料成份等)使金屬表面各處的電位不相等,統(tǒng)稱為電化學(xué)不均勻性,從而形成腐蝕原電池,加速了腐蝕。例如工業(yè)鋅,因其中含雜質(zhì)(如Cu),存在著腐蝕電池,所以它的腐蝕速度要比純鋅大的得多如圖1所示。
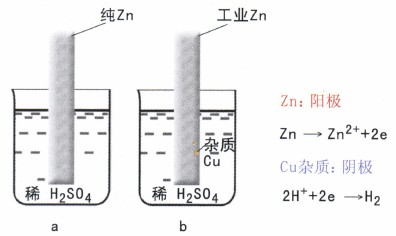
腐蝕電池的工作歷程
腐蝕電池的工作原理與—般原電池相同,如圖2所示。陽(yáng)極(區(qū))上發(fā)生失去電子的氧化反應(yīng)(陽(yáng)極反應(yīng)),電位相對(duì)較低,是電池中的負(fù)極,也是發(fā)生腐蝕的地方。陰極(區(qū))上發(fā)生接收電子的還原反應(yīng)(陰極反應(yīng)),電位相對(duì)較高,是電池中的正極。腐蝕電流Ic的流向是指正電荷流動(dòng)的方向,電流從陽(yáng)極流出進(jìn)入溶液中,再?gòu)娜芤褐辛魅腙帢O。
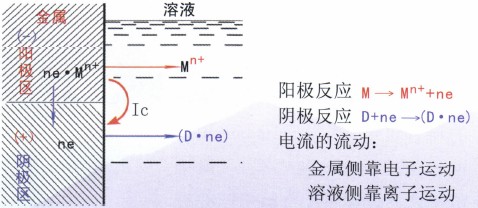
腐蝕電池中,這三部分工作,相互聯(lián)系,缺—不可。只要其中任何一個(gè)步驟停止,整個(gè)電池工作就停止,體系中的金屬腐蝕也就停止。
腐蝕電池的特點(diǎn)
①腐蝕電池是短路的原電池,它將化學(xué)能變成電能,但卻不能被利用,而是以熱的形式散失掉了。
②腐蝕電池的存在,只能加速腐蝕,而不是腐蝕發(fā)生的根本原因。如果環(huán)境中沒有氧化劑存在,即使有腐蝕電池的存在,也不會(huì)發(fā)生腐蝕。
③根據(jù)腐蝕電池中的電極大小,常把腐蝕電池分為宏觀腐蝕電池和微觀腐蝕電池兩類。
極化作用
極化作用及其表征
觀察一個(gè)簡(jiǎn)化的腐蝕電池的工作,如圖3所示。
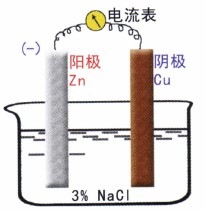
當(dāng)電池接通的瞬間,可觀察到一個(gè)很大的起始電流。根據(jù)歐姆定律,其電流為:
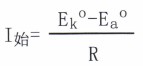 式中Ek°為陰極(銅)的開路電位;Ea°為陽(yáng)極(鋅)的開路電位;R為電池系統(tǒng)的總電阻。當(dāng)電流瞬間達(dá)到最大值后,隨時(shí)間的增長(zhǎng)電流卻很快減小,最后穩(wěn)定在一個(gè)較小的電流值。
式中Ek°為陰極(銅)的開路電位;Ea°為陽(yáng)極(鋅)的開路電位;R為電池系統(tǒng)的總電阻。當(dāng)電流瞬間達(dá)到最大值后,隨時(shí)間的增長(zhǎng)電流卻很快減小,最后穩(wěn)定在一個(gè)較小的電流值。從歐姆定律可知,影響電流強(qiáng)度I的因素有二,電池兩極間的電位差和電池內(nèi)外電阻的總和R。電池接通,總電阻R并沒有變化,那么電流I的減小只能是電池兩極間的電位差降低的結(jié)果。實(shí)驗(yàn)測(cè)得的情況也完全證明了這一現(xiàn)象。
如圖4所示,當(dāng)電路接通后,陰極(銅)的電位變得越來(lái)越負(fù);而陽(yáng)極(鋅)的電位變得越來(lái)越正;兩極間的電位差變得越來(lái)越小,最后當(dāng)電流減小并穩(wěn)定在某值時(shí),陰極的電位負(fù)移至Ek,而陽(yáng)極的電位正移至Ea;兩極的電位差減小到Ek-Ea,由于Ek-Ea《Ek°-Ea° ,所以在R不變的情況下,I移要比I始小很多。

同時(shí),消除或堿弱陽(yáng)極和陰極極化作用的過(guò)程稱為去極化作用或去極化過(guò)程。能消除或減弱極化作用的物質(zhì)稱為去極化劑。因此,可以認(rèn)為環(huán)境中存在的氧化劑就是—種去極化劑。
可見,腐蝕電池的極化作用,導(dǎo)致腐蝕電流減小,從而降低了腐蝕速度。如果沒有極化作用,金屬材料和設(shè)備的腐蝕速度也將大得多。極化相當(dāng)于—種阻力,增大極化有利防腐。
免責(zé)聲明:本網(wǎng)站所轉(zhuǎn)載的文字、圖片與視頻資料版權(quán)歸原創(chuàng)作者所有,如果涉及侵權(quán),請(qǐng)第一時(shí)間聯(lián)系本網(wǎng)刪除。
-
標(biāo)簽: 腐蝕金屬極化作用

官方微信
《腐蝕與防護(hù)網(wǎng)電子期刊》征訂啟事
- 投稿聯(lián)系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 腐蝕與防護(hù)網(wǎng)官方QQ群:140808414





