摘要
基于自行設計組裝的鹽酸液膜腐蝕模擬裝置,采用腐蝕掛片、電阻探針、Tafel極化、電化學阻抗等方法,研究了316L和HR-2不銹鋼在濃度分別為1、0.5和0.1 mol/L,溫度分別為90、70和60 ℃的鹽酸蒸汽環境中的鈍化和點蝕行為,并利用金相顯微鏡、XRD對腐蝕試樣和腐蝕產物進行了分析。結果表明:兩種不銹鋼的腐蝕速率隨時間先加快后減慢最后趨于穩定,316L不銹鋼的腐蝕速率相對較高;兩種不銹鋼均能形成穩定鈍化區,且維鈍電流密度相差不大,HR-2孔蝕電位的鈍化區間總體都比316L不銹鋼高,說明HR-2不銹
關鍵詞: 不銹鋼,液膜環境,模擬裝置,電化學測試,鈍化與點蝕,表征及分析
鹽酸液膜是由鹽酸蒸汽冷凝到材料表面形成的液膜,對材料造成的腐蝕比直接由同濃度和溫度環境的鹽酸溶液腐蝕更快。而且其腐蝕速率與鹽酸濃度和材料所處的溫度環境有關,形成的液膜穩定性不強,對于電化學實驗難度較大。鹽酸液膜的腐蝕就相當于鹽酸露點腐蝕,引起露點腐蝕的氣體一般包括SO2、SO3、HCl、NOx、H2S等,這些酸性混合蒸汽冷凝生成的硫酸、鹽酸、氫硫酸等易造成工業設備的嚴重點腐蝕穿孔。在實際工程生產中,酸性液膜腐蝕主要位于初餾塔、閃蒸塔的頂部、塔頂冷回流時的常壓塔頂部、塔頂溫度跨初凝區的油氣冷凝冷卻器及其相關管道。其中腐蝕最嚴重的是常減壓塔頂冷卻系統。所以,酸性液膜腐蝕在電力、石油化工等領域造成的破壞備受關注,耐腐蝕材料的研究和防腐措施亟待優化。
王彥亮等[1]采用Tafel極化、阻抗譜及Mott-Schottky技術研究了316L不銹鋼在pH值分別為4.7和11的硼酸溶液中的電化學,結果表明均能形成穩定的鈍化膜,鈍化區間隨pH值升高而減小,過鈍電位明顯降低。周多等[2]討論了化學清洗對凝汽器316L不銹鋼管腐蝕穿孔的影響,化學清洗劑中存在的Cl-會對凝汽器材料腐蝕穿孔。陳宇等[3]研究了316L不銹鋼在硼酸溶液中鈍化膜的電化學性能,結果表明,316L不銹鋼在硼酸溶液中能形成良好的鈍化膜,使腐蝕速率降低。楊柳青等[4]的研究表明,316L和HR-2不銹鋼在6%的酸性FeCl3溶液中都呈現出良好的耐腐蝕性,在相同的環境和腐蝕時間后,316L不銹鋼表面的點腐蝕總是比HR-2不銹鋼更嚴重。316L奧氏體不銹鋼常用于制造管道、熱交換器等;HR-2奧氏體不銹鋼具有一般奧氏體不銹鋼所具有的穩定性和抗腐蝕性,在能源及相關領域中得到了廣泛應用[5]。對316L不銹鋼的耐腐蝕性能的研究[6]表明,腐蝕環境中C1-濃度增大、溫度升高或pH值降低能使316L不銹鋼的腐蝕加快[7,8,9,10]。C1-在鈍化膜表面的吸附是孔蝕形核的必經之路,Cl-能增強電解液的導電性能,促進表面活性點的活化,加速小孔的溶解,降低孔蝕電位[11,12]。然而,有關HR-2不銹鋼腐蝕行為的研究報道卻較少[13]。
本文采用Tafel極化、電化學阻抗譜 (EIS)、掛片腐蝕、電阻探針和X射線衍射譜等方法,研究鹽酸濃度和溫度對316L和HR-2不銹鋼在鹽酸液膜中的電化學行為的影響、點蝕情況及其鈍化膜的性質。
1 實驗方法
實驗裝置如圖1中,電極從左到右依次為Ag/AgCl參比電極、石墨電極、工作電極以及探針溫度計。油浴溫度設置在130 ℃,蒸發瓶里配制一定濃度的鹽酸溶液,在油浴鍋的加熱作用下產生HCl氣體和水蒸氣。兩種混合氣體在冷凝管的三電極體系表面遇冷后形成液膜或液滴,電極試樣通過上方的銅導線與外界電化學工作站相連,將浸濕NaOH溶液的棉花球塞住冷凝管頂部出口,用于尾氣吸收,測試所用溶液為1、0.5和0.1 mol/L鹽酸溶液,溶液體積為0.4 L。
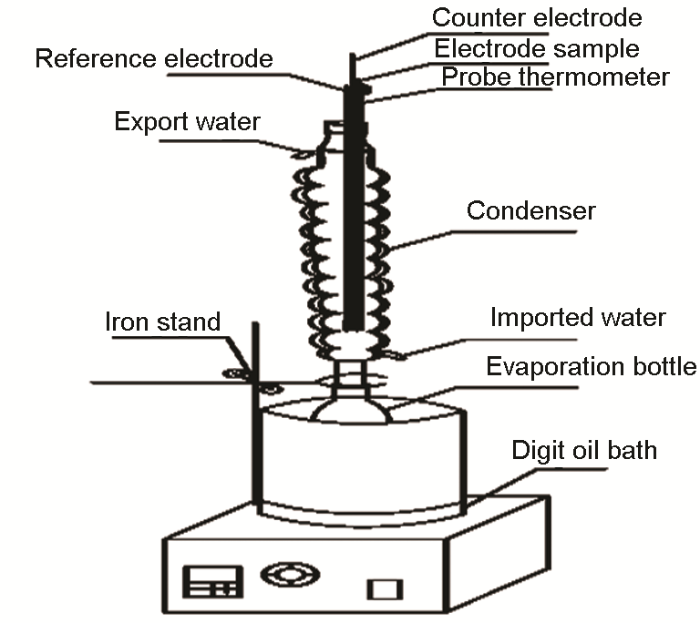
圖1 電化學測試實驗裝置
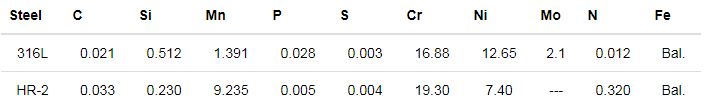
采用316L 和HR-2奧氏體不銹鋼作為實驗材料,其化學成分 (質量分數,%) 如表1。
表1 兩種不銹鋼的化學成分 (mass fraction / %)
實驗用金屬腐蝕失重掛片,掛片位置為溫度90 ℃位置,掛片直徑為4 mm、高度為50 mm的帶孔柱體試樣,用240#,360#,400#,600#,800#,1000#的金相砂紙由粗到細依次打磨后用去離子水、丙酮和酒精清洗干凈,然后吹干,在干燥箱內干燥,稱重精確到0.1 mg。電化學測試電極的尺寸為Φ4 mm×2 mm,用Cu導線焊接后進行固封,用金相砂紙逐級打磨工作面后用去離子水、無水乙醇和丙酮進行清洗并吹干備用。
電阻探針試樣為兩種不銹鋼 (316L和HR-2不銹鋼) 用線切割加工成的Φ0.4 mm×12 mm的線狀探針,腐蝕掛片實驗前,將兩根同種材料加工好的探針用丙酮和乙醇依次沖洗,吹干至室溫下測量一頭至另一頭10 mm位置處的電阻穩定值,并做好記錄。將測量的10 mm位置處系上細繩,并與掛片試樣一起掛入已加熱沸騰的冷凝管90 ℃位置,互不接觸,而且底端齊平。待實驗結束后,取出探針,用蒸餾水輕輕沖洗后,吹干降至常溫后測量電阻值,帶入公式計算腐蝕速率,并繪制兩種材料電阻探針腐蝕動力學曲線。
本實驗設計3個濃度 (1、0.5和0.1 mol/L) 鹽酸溶液,在設定條件下將電阻探針試樣用細線掛好放入同一高度位置 (T=90 ℃位置),掛片時間為24、48、96和144 h;每種材料每個時間掛片為2片,實驗數據求其平均值。完成掛片實驗后,腐蝕試樣用去離子水清洗干凈,放入干燥箱內干燥24 h,稱量精確到0.1 mg。用BM-200C金相顯微鏡、D/max-2500/PCX射線衍射儀 (XRD) 分析表面腐蝕產物和測定腐蝕區域的化學組成。
Tafel極化和電化學阻抗譜 (EIS) 測試在型號為CS350電化學工作站上進行,采用經典三電極體系,316L和HR-2不銹鋼試樣制成工作電極,石墨電極作為輔助電極,探針溫度計測量腐蝕體系中三電極體系末端溫度,并且這三個電極連接緊密與探針溫度計底部始終在同一水平線上。本文所有電位如無特殊說明,均相對于所用的參比電極而言。Tafel極化實驗,掃描范圍為相對開路電位-0.1~0.2 V。EIS測試擾動電位為10 mV,頻率測試范圍為105~10-2 Hz,電壓擾動振幅為50 mV,掃描速率范圍為105~10-2 Hz。
2 結果與討論
2.1 兩種材料在不同溫度和濃度下電化學分析
2.1.1 Tafel極化測試分析
從表2,3,4可以看出,兩種材料隨著溫度的增大自腐蝕電位Ecorr逐漸降低。腐蝕電位的降低是由于C1-在鋼體表面上的局部聚集和氯化物被水解,導致局部酸性環境[14],引起腐蝕電位的降低。此外,隨著Cl-濃度的增加,316L和HR-2不銹鋼的腐蝕電流密度Ip增加,根據Farady第二定律,腐蝕電流密度與腐蝕速率成正比,這表明隨著腐蝕速率的溫度增加,316L和HR-2不銹鋼的腐蝕速率增加。同時,對比發現316L不銹鋼的Ip一直大于同濃度下HR-2不銹鋼的Ip,表明316L不銹鋼腐蝕速率一直大于HR-2不銹鋼的腐蝕速率。
表2 316L和HR-2不銹鋼在1 mol/L HCl溶液不同溫度的Tafel擬合數據
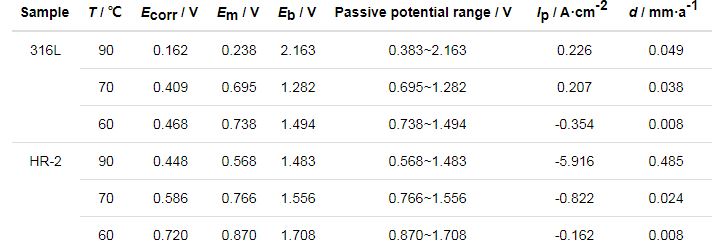
表3 316L和HR-2不銹鋼在0.5 mol/L HCl溶液不同溫度的Tafel擬合數據
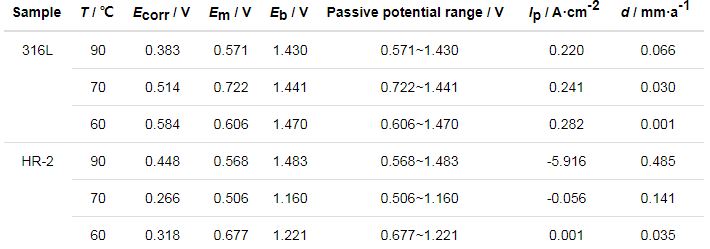
表4 316L和HR-2不銹鋼在0.1 mol/L HCl溶液中不同溫度Tafel擬合數據
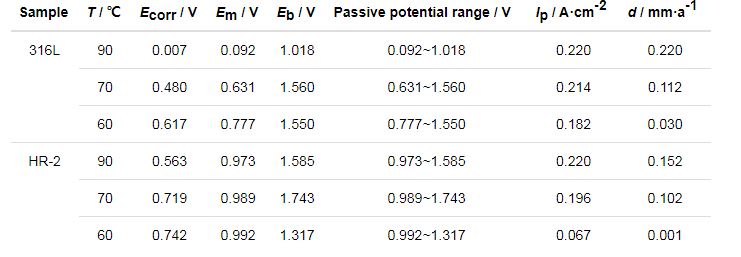
兩種不銹鋼在3種不同鹽酸濃度環境中均能形成穩定鈍化區,且電位Em相差不大。隨著HCl濃度的增加,鈍化間隔通常會增加。如果極化電位超過過電位,腐蝕電流將迅速增加,表明此時鈍化膜不穩定并溶解。另外,隨著Cl-濃度的增加,電極的點蝕電位Eb降低,金屬鈍化膜不穩定,容易破壞,材料更容易發生點腐蝕,加速腐蝕速度。HR-2孔蝕電位總體比316L不銹鋼高,并且HR-2不銹鋼的鈍化區間總體也比316L不銹鋼高,說明HR-2不銹鋼更耐腐蝕。
2.1.2 EIS測試結果
研究[14]表明,容抗弧半徑大小既反映了電荷傳質阻力的大小,容抗弧越大,表明電荷傳質阻力越大,越耐腐蝕,反之表明電荷傳質阻力越小;又可反映鈍化膜阻抗的大小以及鈍化能力的強弱,容抗弧半徑越大則鈍化膜阻抗越大、鈍化能力越強。圖2為電化學阻抗譜的等效電路,圖3,4,5分別為316L和HR-2不銹鋼在HCl濃度為1、0.5和0.1 mol/L,溫度為60、70和90 ℃環境的EIS擬合圖。
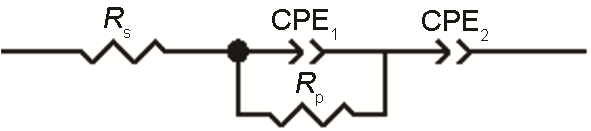
圖2 電化學阻抗譜的等效電路圖
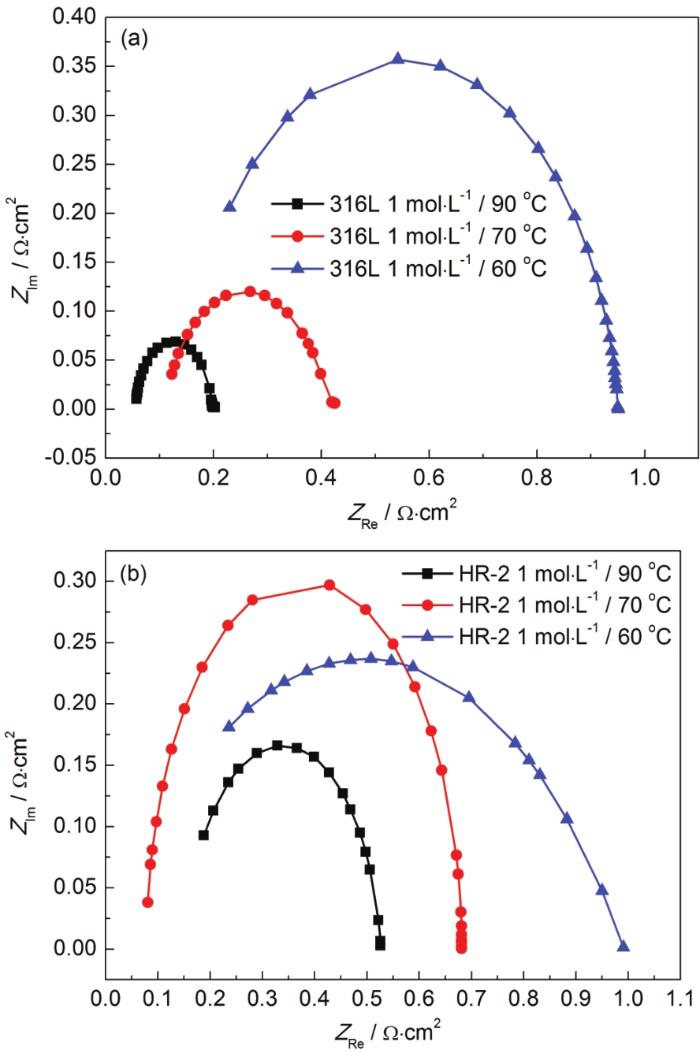
圖3 316L和HR-2不銹鋼在1 mol/L 90、70和60 ℃ HCl溶液中的電化學阻抗圖
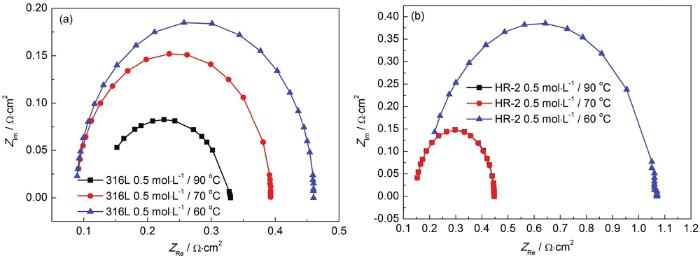
圖4 316L和HR-2不銹鋼在0.5 mol/L 90、70和60 ℃ HCl溶液中的電化學阻抗圖
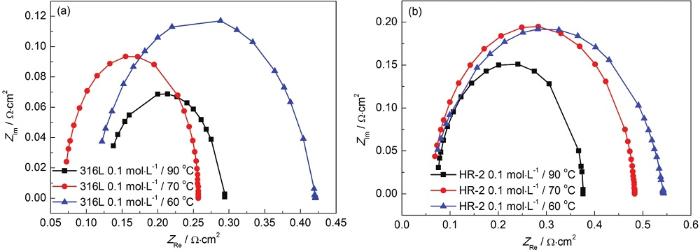
圖5 316L和HR-2不銹鋼在0.1 mol/L 90、70和60 ℃ HCl溶液中的電化學阻抗圖
對于同一種不銹鋼,同一濃度下,隨著溫度的升高,容抗弧越小,溶液電阻Rs逐漸減小,蝕點內溶液極化電阻Rp也變小,代表電容量的CPE-T逐漸增大。所以HR-2不銹鋼比316L不銹鋼更耐腐蝕,這一點與Tafel極化曲線的結果是一致的。在相同的溫度和材料下,隨著HCl濃度的增加,C1-濃度繼續增加。隨著反應的進行,金屬表面上的腐蝕產物膜不斷增厚,阻礙氧和Cl-的傳質過程,然后引起腐蝕過程減速;腐蝕后期,隨著腐蝕產物的增多,無法均勻地覆蓋金屬表面,在其間隙Cl-會發生富集,促進點蝕的產生,從而使腐蝕速率逐漸變快。因此,兩種不銹鋼在HCl液膜環境中腐蝕速率是先減小后逐漸增大。
2.2 兩種材料不同時間下腐蝕特性研究
2.2.1 失重腐蝕速率分析
圖6為兩種材料在1和0.5 mol/L HCl溶液不同模擬時間后的腐蝕動力學曲線,掛片位置為85~90 ℃區域。由圖6可知,兩種材料的腐蝕速率在兩種濃度環境下腐蝕速率變化趨勢相近。24~48 h時腐蝕不斷加快,第48 h時速率達到最大;48~96 h時腐蝕逐步減慢;由于腐蝕產物在腐蝕前48 h不太可能形成薄膜,腐蝕性介質可以完全接觸鋼體,并且腐蝕速率加快。48~96 h腐蝕后,在金屬表面形成穩定致密的鈍化膜,增強了對鋼體的保護作用。阻礙腐蝕性介質的進一步滲透,腐蝕速率減慢。96 h之后腐蝕速率增大,表面鋼體生成的鈍化膜被液膜中的大量Cl-侵入,破壞了鈍化膜,使腐蝕速率加快。由整體腐蝕情況來可看出,HR-2不銹鋼整體腐蝕失重較小,腐蝕速率較慢;并且兩種鋼在1 mol/L HCl溶液環境下腐蝕各階段的腐蝕速率均高于0.5 mol/L HCl溶液;由于HR-2鋼中Cr含量較高,Cr具有抗氧化性能并能促進內銹層中穩定相α-FeOOH的生成[15],使腐蝕銹層與金屬結合更緊密,對鋼體保護作用更強;所以HR-2比316L鋼更耐腐蝕。
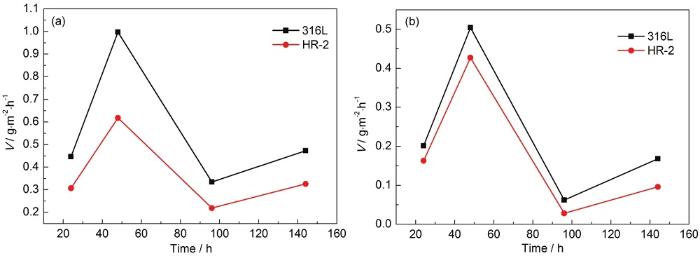
圖6 兩種材料在1和0.5 mol/L HCl溶液中不同模擬時間后的腐蝕動力學曲線
2.2.2 電阻探針腐蝕速率分析
圖7為兩種材料電阻探針在1和0.5 mol/L HCl溶液的不同模擬時間后的腐蝕動力學曲線,掛片位置為85~90 ℃區域。兩種材料的腐蝕速率在24~48 h腐蝕時不斷加快,第48 h時腐蝕速率達到最大;48~96 h時腐蝕逐步減慢。由于腐蝕前48 h腐蝕產物較少,未能成膜,腐蝕介質能充分與鋼體接觸,腐蝕速率不斷加快;腐蝕后期即48~96 h時金屬表面形成穩定致密的銹層,對鋼體的保護作用加強進而阻礙了腐蝕介質進一步滲入,腐蝕速率減慢。96 h之后腐蝕速率增大,表面鋼體生成的鈍化膜被液膜中的大量Cl-侵入,破壞了鈍化膜,使腐蝕速率加快。這與腐蝕失重數據結果一致。
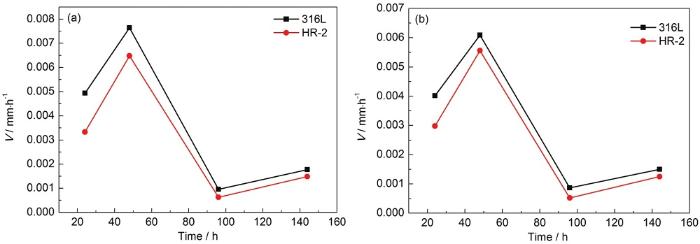
圖7 兩種材料電阻探針在1和0.5 mol/L HCl溶液中不同模擬時間后的腐蝕動力學曲線
2.2.3 金相微觀形貌觀測
兩種不銹鋼在腐蝕24、96和144 h后的表面腐蝕形貌如圖8所示,觀察可知,在0.5 mol/L HCl溶液中腐蝕24 h,316L和HR-2不銹鋼表面出現很少腐蝕坑,而且較分散;腐蝕96 h后,試樣表面呈現較多明顯腐蝕坑,呈片區狀連接,顏色類似暗紅色銹層;腐蝕144 h時,兩種不銹鋼表面出現較多腐蝕層,腐蝕坑更多。對比同一時間下,316L不銹鋼都比HR-2不銹鋼腐蝕現象更明顯,所以HR-2不銹鋼比316L不銹鋼更耐腐蝕,這與之前電化學、腐蝕掛片和電阻探針結果一致。

圖8 兩種材料在0.5 mol/L HCl溶液中腐蝕24、96和144 h后的金相形貌
2.2.4 腐蝕產物XRD分析
圖9為316L和HR-2不銹鋼在0.5 mol/L HCl溶液中腐蝕144 h的XRD圖,由圖可知,在鹽酸液膜環境下,兩種管線鋼的腐蝕產物包括Fe2O3,Fe3O4,FeOOH,Cr和FeC12·4H2O,對于耐腐蝕性能不同的兩種不銹鋼,腐蝕產物層基本一樣,說明對腐蝕產物的成分沒有顯著影響。
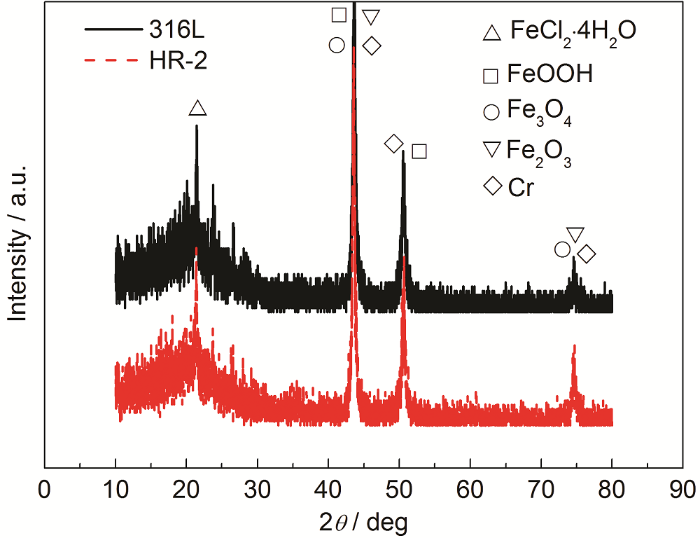
圖9 316L和HR-2不銹鋼0.5 mol/L HCl溶液中腐蝕144 h的XRD譜
在高濃度Cl-條件下,不銹鋼發生陽極溶解[16],電化學反應如下:
Fe2++2H2O=Fe(OH)2+2H+
(1)
Fe(OH)2很容易進一步氧化成FeOOH
Fe(OH)2→FeOOH+H2O+e
(2)
FeOOH脫水后生成Fe2O3和Fe3O4[17]。
由于C1-當量的酸性陰離子,該過程使得不銹鋼表面呈弱酸性,繼而促進不銹鋼表面的活性位點優先腐蝕:
Fe+2H+=Fe2++H2↑
(3)
Fe2++2C1-=FeC12
(4)
另一個是競爭吸附理論[18]。由于O的吸附被C1-的競爭所取代,不銹鋼的表面部分地被剝奪氧,然后Cr的氧化大大減少。因此,鋼體表面上的鈍化膜難以形成或破壞,并且更可能導致不銹鋼點蝕。另外,C1-會穿入鋼體表面的鈍化膜消耗其中的氧,然后直接點蝕。
3 結論
(1) 兩種材料在兩種HCl濃度環境下,失重腐蝕速率變化趨勢相近。腐蝕24~48 h,腐蝕速率不斷加快;48 h時腐蝕速率達到最大;48~96 h時腐蝕速率逐步減慢,金屬表面形成穩定致密的鈍化膜;96 h之后腐蝕速率增大,表面鋼體生成的鈍化膜被液膜中的大量Cl-侵入,破壞鈍化膜,形成了點蝕,使腐蝕速率加快。由整體腐蝕情況可看出,HR-2不銹鋼腐蝕失重較小,腐蝕速率較慢。
(2) 在兩種不同濃度溶液3種不同溫度環境中,316L和HR-2不銹鋼均能形成穩定鈍化區,且維鈍電流密度相差不大,在兩種不同濃度下,316L不銹鋼具有比HR-2不銹鋼更高的自腐蝕電流密度。隨著濃度的增加,鈍化間隔逐漸縮短,自腐蝕電位發生負移。隨著反應的進行,在金屬表面的間隙中Cl-發生富集,這促進了點腐蝕的產生,從而腐蝕速率逐漸變快;在相同的濃度環境下,腐蝕溫度越高,電容電抗弧越小,電荷傳質電阻越小,鈍化膜阻抗越小,鈍化能力越弱,點蝕電位越低,越嚴重腐蝕。HR-2不銹鋼孔蝕電位總體比316L不銹鋼高,并且HR-2不銹鋼的鈍化區間總體也比316L不銹鋼高,鈍化膜阻抗較大,說明HR-2不銹鋼更耐腐蝕。
(3) 兩種鋼1 mol/L HCl溶液腐蝕144 h的XRD分析得出,兩種不銹鋼的腐蝕產物包括Fe2O3,Fe3O4,FeOOH,Cr,FeC12·4H2O,對于耐腐蝕性能不同的兩種不銹鋼,腐蝕產物層基本相同,C1-競爭性吸附導致不銹鋼表面局部缺氧,阻礙不銹鋼表面Cr的氧化,從而阻礙富Cr鈍化膜的形成,導致不銹鋼鈍化膜的動態平衡失效,膜的鈍化變薄促進了不銹鋼中點蝕的發生。
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《中國腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護網官方QQ群:140808414





