摘要
采用牛白蛋白和右旋糖酐40模擬EPS中的蛋白質、多糖,開展了蛋白質、多糖對碳鋼腐蝕速率、表面形貌、腐蝕產物、電化學行為以及浸涂前后蛋白質、多糖官能團變化研究。結果表明:碳鋼浸涂蛋白質、多糖后,由于氧含量降低使腐蝕產物中具有致密性的Fe3O4含量分別上升了113.6%和145.5%,腐蝕速率分別下降了17.7%和24.0%。對EIS進行等效電路擬合后表明,未浸涂的等效電路為R(QR),浸涂蛋白質、多糖后等效電路為R(Q(R(QR)))。紅外光譜實驗結果顯示,浸涂前后蛋白質分子中的—C=O—和—COO—,以及多糖分子中的—C—OH,—CH3,—CH2—和—COO—出現峰值減弱或消失的現象,表明碳鋼浸涂蛋白質、多糖后表面形成了一層保護層,上述官能團參與了腐蝕反應且對保護層的形成起著關鍵作用。
關鍵詞: 蛋白質 ; 多糖 ; 碳鋼 ; 腐蝕 ; 保護層 ; 微生物胞外聚合物
微生物胞外聚合物 (EPS) 是生物垢中除了微生物和水之外最主要的組成部分,其主要來自于細胞新陳代謝過程中的分泌物、脫落的細胞表面物質、細胞自溶物以及細胞從環境中吸附的物質[1,2]。研究[3]表明,某些微生物生物膜中的EPS可以抑制金屬的腐蝕。Stadler等[4]研究了脫硫弧菌的EPS對碳鋼的腐蝕抑制作用,認為吸附在金屬表面的脫硫弧菌的EPS能夠減少細胞的吸附,抑制生物膜的生成。Dong等[5]通過研究耐熱硫酸鹽還原菌 (SRB) 產生的EPS對碳鋼的腐蝕,證明吸附在碳鋼表面的EPS層可以通過阻止氧的還原,抑制腐蝕的進行。Dong等[6]用陽離子交換樹脂法從Vibrio natriegens提取EPS,碳鋼試樣浸涂EPS后在表面形成保護層,阻礙氧的擴散并抑制陰極氧的還原。Finkenstadt等[7]的研究結果也表明,提純的腸膜明串珠菌的EPS能夠對低碳鋼表面起保護作用。Jin等[8]通過研究再生水中EPS對鑄鐵腐蝕的影響,使用電化學手段證明EPS使得腐蝕產物致密,阻隔溶解氧的傳遞,從而抑制腐蝕。Ignatova-Ivanova等[9]研究認為,Lactobacillus sp的EPS可以作為低碳鋼的腐蝕抑制劑,在低碳鋼表面形成保護層。Li等[10]研究海水中SRB的EPS對不銹鋼腐蝕的影響,通過原子力顯微鏡觀察顯示不銹鋼的表面形成了一層魚鱗狀的生物膜,可以抑制腐蝕,而且膜生長越來越致密。
EPS中含有多糖、蛋白質、脂肪酸以及無機物[11,12]等其他小分子化合物,其中蛋白質、多糖含量高達70%~80%[13,14]。Zhang等[15]研究了從海洋貽貝的EPS中提取的牛貽貝黏著蛋白對金屬腐蝕的抑制作用,認為這種蛋白質在NaCl溶液中可以在碳鋼表面生成一層保護層,這層高分子層對碳鋼起到了保護作用。Ghafari等[16]針對從細菌的EPS中提取的多糖進行研究,認為羧基在與Fe(Ⅱ/Ⅲ) 二者結合后會在碳鋼表面形成一層保護膜,進而抑制了碳鋼的腐蝕。Ignatova-Ivanova等[9]的研究也得出類似結論。Zhang等[17]則通過人工合成的玉米秸稈多聚糖研究其對低碳鋼的腐蝕影響,結果證明這種多聚糖能很好地抑制低碳鋼在1.0 mol/L鹽酸溶液中的腐蝕,而其作用機理是多聚糖中具有的N、C原子和羥基中的O原子能很好地與Fe結合吸附到低碳鋼的表面,在這一過程中其吸附原理符合Langmuir等溫吸附模型,同時實驗證明吸附在低碳鋼表面的多聚糖能很好地抑制低碳鋼的陽極腐蝕。Finkenstadt等[18]也認為,提純乳酸菌的胞外多糖通過吸附在金屬表面,降低離子擴散速率,從而抑制低碳鋼的腐蝕。Mobin等[19]認為,從Plantago提取的Polysaccharide在1 mol/L的HCl溶液中可以作為碳鋼的綠色緩蝕劑。
目前,國內外關于EPS防腐蝕的研究剛剛起步,大部分研究是從菌種中提取的蛋白質、多糖,操作相對復雜,且并未對蛋白質、多糖抑制碳鋼腐蝕的機理開展研究。因此,本實驗用人工合成的牛白蛋白 (BSA)、右旋糖酐40替代從菌種中提取的蛋白質、多糖,探究蛋白質、多糖對碳鋼腐蝕的抑制效果;并通過電化學實驗以及對表面形貌、腐蝕產物成分分析,進一步揭示二者抑制腐蝕的機理。
1 實驗方法
1.1 實驗材料
1.1.1 蛋白質和多糖
蛋白質采用牛白蛋白BSA,多糖采用右旋糖酐40,均購自國藥集團。牛白蛋白分子由583個氨基酸殘基組成,含有少量的色氨酸、苯丙氨酸和異亮氨酸和大量的半胱氨酸、亮氨酸、谷氨酸和賴氨酸。右旋糖酐40分子量為 (2.5~5.0)×104,是一種由若干葡萄糖脫水形成的高分子聚合物,分子式為 (C6H10O5)n。
1.1.2 碳鋼試片
碳鋼試片尺寸為5.0 cm×2.5 cm×0.2 cm,其化學成分 (質量分數,%) 為:C 0.095,Si 0.170,Mn 0.290,P 0.012,S 0.012,Fe 99.421。實驗前將碳鋼試片依次浸泡在丙酮、蒸餾水、無水乙醇中清洗脫脂,然后放在干燥的濾紙上,自然風干,放入干燥器中,24 h后用分析天平稱重備用。
1.2 碳鋼腐蝕實驗
取一定質量的蛋白質/多糖,加入超純水,在室溫下溶解并穩定2 h,制成濃度為1 mg/mL溶液[20];將處理后的碳鋼試片置于溶液中浸泡24 h;自然風干6 h后用濾紙將試片包好,放入干燥器中;24 h后用分析天平稱重備用。實驗采用容積為6 L的AR反應器 (圖1) 模擬實際管網中的水力條件。設置3組裝置,分別對應未浸涂、浸涂蛋白質、浸涂多糖工況。在每個裝置中放入5組掛片,每組掛片設置3個平行樣。實驗用腐蝕液為人工配置的腐蝕性較強的溶液,其成分為:NaCl 58.5 mg/L+Na2SO4 213 mg/L+NaHCO3 4.2 mg/L,Larson指數為2,pH值為8.3。實驗溶液溫度設置為30 ℃,攪拌葉片的轉速為155 r/min。
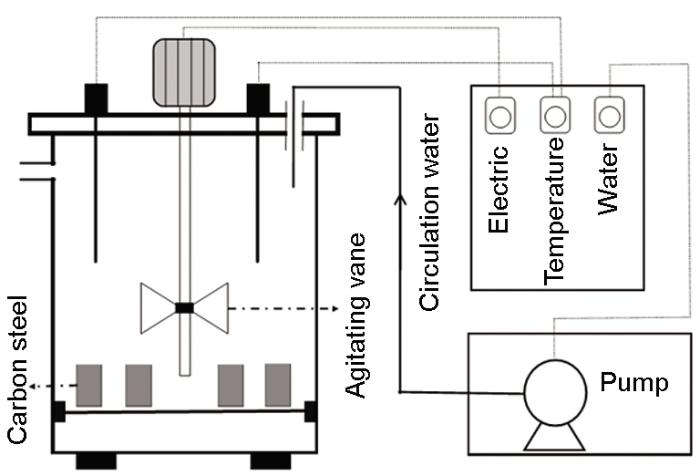
圖1 實驗裝置示意圖
分別在浸泡2,4,8,12和16 d后取出試片,冷凍干燥24 h后利用日立S4330型掃描電鏡 (SEM) 觀察碳鋼在不同階段的腐蝕形貌。利用QUANTAX型能譜儀 (EDS) 和帕納科X“pert PRO型X射線衍射儀 (XRD) 分別分析腐蝕產物的化學成分及相組成。
實驗結束后將掛片進行清洗,冷凍干燥24 h后用分析天平稱重,計算腐蝕速率。腐蝕速率Vw(g/(m2·h)) 的計算公式[21]如下:

式中,ΔW為金屬試片腐蝕前及腐蝕后重量差 (g);S為金屬試片總的表面積 (m2),為28×10-4 m2;t為實驗時間 (h)。
腐蝕抑制率η的計算公式如下:
![]()
式中,和分別為未浸涂和浸涂蛋白質/多糖工況時的腐蝕速率 (g/(m2·h))。
1.3 碳鋼試樣浸涂過程中的電化學性能測試實驗
取一定質量的蛋白質、多糖,加入超純水,在室溫下溶解并穩定2 h,分別制成濃度為1 mg/mL的溶液[20]。平行設置3組燒杯,分別加入超純水以及1 mg/mL的蛋白質和多糖溶液,對應未浸涂、浸涂蛋白質、浸涂多糖工況。在每組燒杯中,分別插入碳鋼電極,在浸涂第1,3,6,9,12,18和24 h時進行電化學測試。浸涂前后,使用Nicolet 8700型紅外光譜儀 (FT-IR) 分析腐蝕前后蛋白質、多糖的官能團差異。
采用CHI660C型電化學工作站開展電化學測試,測試條件為:三電極體系,參比電極為飽和甘汞電極 (SCE),輔助電極為Pt電極,工作電極為碳鋼電極。電化學阻抗頻率范圍為105~10-2 Hz,施加正弦電位幅值5 mV;采用ZSimpWin軟件分析實驗數據。
碳鋼電極制作方法如下:將試片切割成1 cm×1 cm的圓柱形,在非工作面焊接Cu導線,然后用環氧樹脂封裝。實驗前用360#,600#,800#,1000#,1500#和2000#的水砂紙對碳鋼電極表面逐級打磨,然后用Al2O3拋光粉拋光,之后用去離子水沖洗,丙酮除油,再用沾有乙醇的脫脂棉球擦拭電極表面,冷風吹干放入干燥器備用。
2 結果與討論
2.1 蛋白質、多糖對碳鋼腐蝕行為的影響
2.1.1 腐蝕速率
未浸涂和浸涂蛋白質/多糖后的碳鋼在NaCl+Na2SO4+NaHCO3溶液中的腐蝕速率隨時間的變化如圖2所示。可知,浸涂了蛋白質、多糖后,碳鋼的平均腐蝕速率比未浸涂的分別下降了17.7%和24.0%,即蛋白質、多糖對碳鋼腐蝕的抑制率分別為17.7%和24.0%,且多糖對碳鋼腐蝕的抑制效果高于蛋白質。這與Chongdar等[22]和Stadler等[23]的結論類似。Harimawan等[24]通過對B.subtilis和P.aeruginosa兩菌種EPS的蛋白質、多糖研究認為,多糖與碳鋼的粘附力比蛋白質更強,形成的生物膜更加致密,從而多糖抑制腐蝕的效果更好。王婧[25]的研究也表明,同質量的多糖與Fe(Ⅱ/Ⅲ) 的結合能力高于蛋白質的,EPS中多糖起到主導作用。從圖2看出,碳鋼第8 d的腐蝕速率較第4 d的、第16 d的腐蝕速率較第12 d的,皆有不同程度的上升,這有可能是腐蝕產物分布不均勻,加劇了碳鋼點蝕,腐蝕速率升高[26,27]。
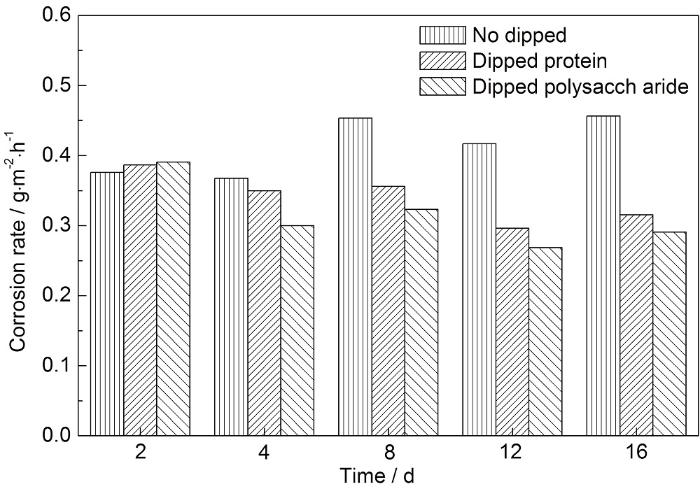
圖2 未浸涂和浸涂蛋白質/多糖后的碳鋼試片腐蝕速率
2.1.2 腐蝕形貌
未浸涂和浸涂蛋白質/多糖后的碳鋼試片在NaCl+Na2SO4+NaHCO3溶液中浸泡16 d后的表面形貌和對應的EDS分析結果如圖3所示。
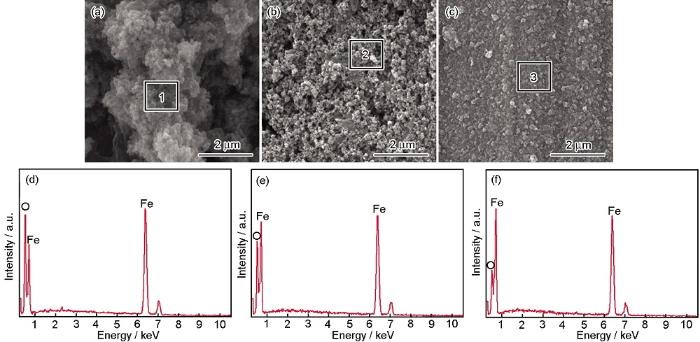
圖3 未浸涂和浸涂蛋白質/多糖后的碳鋼試樣在浸泡16 d后表面形貌和能譜分析
未浸涂工況下,碳鋼表面腐蝕產物疏松多孔 (圖3a)。浸涂蛋白質 (圖3b) 和多糖 (圖3c) 工況下,碳鋼腐蝕產物膜明顯變得致密;且浸涂多糖要比浸涂蛋白質的表面孔隙明顯減少,表明浸涂多糖后碳鋼表面的腐蝕產物膜更加致密。Stadler等[4]和Ghafari等[16]的研究結果也證實EPS能使腐蝕產物表面形貌更為致密。
EDS分析結果顯示,3種工況下試樣的腐蝕產物均含有Fe和O,其中O的峰值按照從大到小的順序依次為未浸涂工況、浸涂蛋白質工況、浸涂多糖工況,表明未浸涂工況下氧含量最多,浸涂多糖工況下氧含量最少。文獻[28]表明,在氧含量較低時,腐蝕產物更加致密,這與本文的結果一致。
2.1.3 腐蝕產物
未浸涂和浸涂蛋白質/多糖后的碳鋼試樣浸泡第16 d的腐蝕產物XRD分析結果如圖4所示。可知,3種試樣的腐蝕產物主要成分均為FeOOH,Fe2O3和Fe3O4。說明蛋白質、多糖對碳鋼腐蝕產物的類型未產生影響,蛋白質、多糖抑制碳鋼的腐蝕并不是通過改變腐蝕產物來實現的。王婧[25]的研究也表明,羅伊氏乳桿菌EPS對碳鋼表面生成的腐蝕產物種類沒有影響。
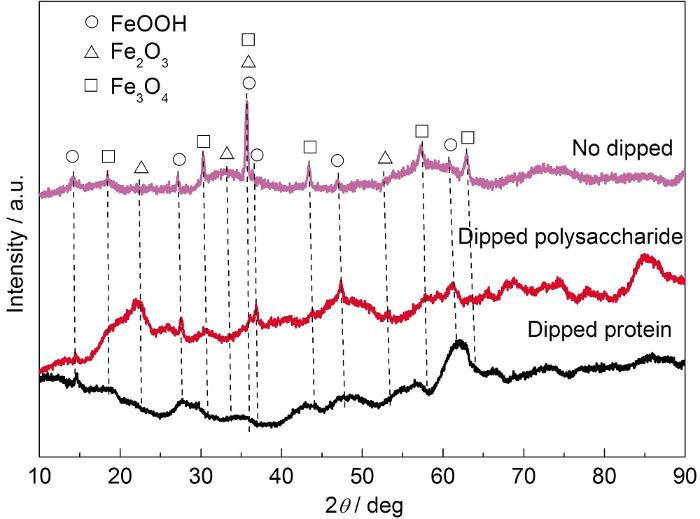
圖4 未浸涂和浸涂蛋白質/多糖后的碳鋼試樣在浸泡16 d后的表面XRD分析結果
2.2 蛋白質、多糖抑制碳鋼腐蝕的機理
2.2.1 電化學阻抗譜與等效電路
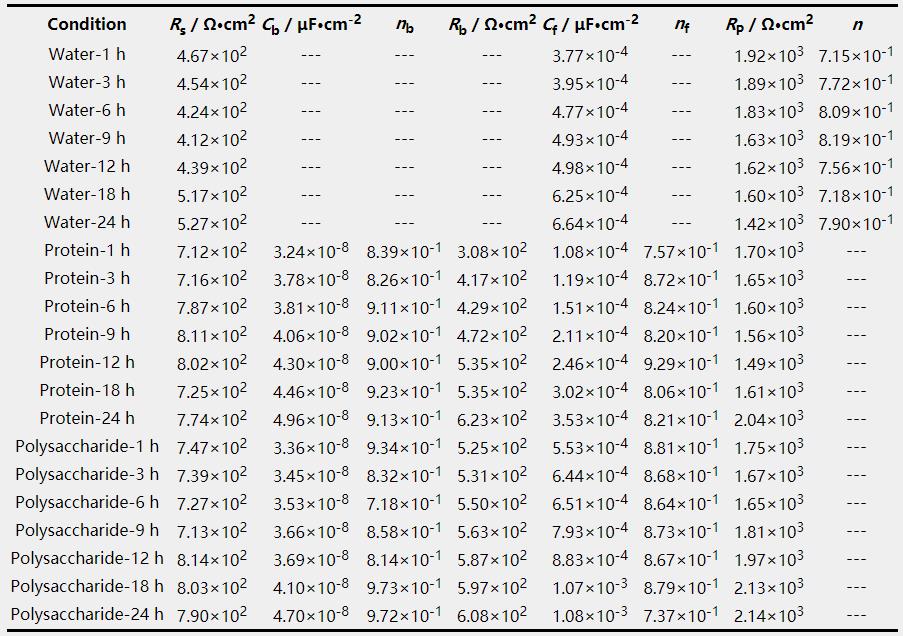
圖5和6分別為碳鋼電極在超純水以及蛋白質和多糖溶液中浸涂過程中的電化學阻抗譜和Bode圖,對阻抗譜進行電路擬合的等效電路如圖7所示,表1為各元件擬合參數值。其中,Rs為擬合電路中的溶液電阻;Rp為極化電阻,即腐蝕電極反應中電荷轉移電阻;Cf為溶液與電極之間的雙電層電容,腐蝕產物層介電性能的變化可以由Cf反映出來;用Rb和Cb分別表示保護層的電阻及電容。
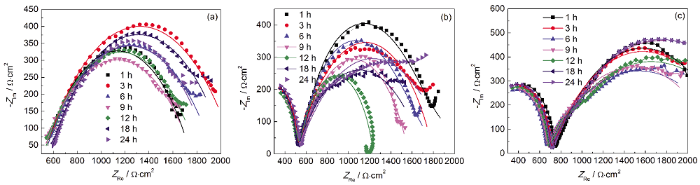
圖5 碳鋼電極浸泡在純水、蛋白質溶液和多糖溶液中的Nyquist圖
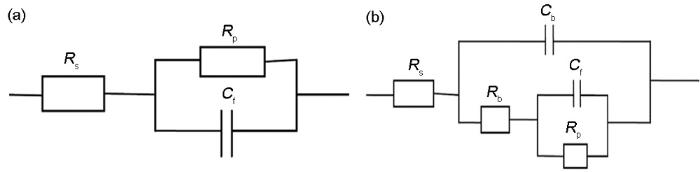
圖7 電化學阻抗譜擬合的等效電路圖
表1 在純水以及蛋白質溶液和多糖溶液浸涂24 h過程中碳鋼電極等效電路擬合參數
在純水中,試樣的Bode圖只有一個峰,說明反應體系有一個時間常數,這與碳鋼電極擬合等效電路為R(QR) 結果一致,表明未浸涂蛋白質/多糖的碳鋼表面未形成保護層[29]。從表1可見,未浸涂試樣的Rp值從1917 Ω·cm2降低到1415 Ω·cm2,說明碳鋼在未浸涂工況下腐蝕過程中,轉移電荷的阻力不斷減小,腐蝕逐漸加快。
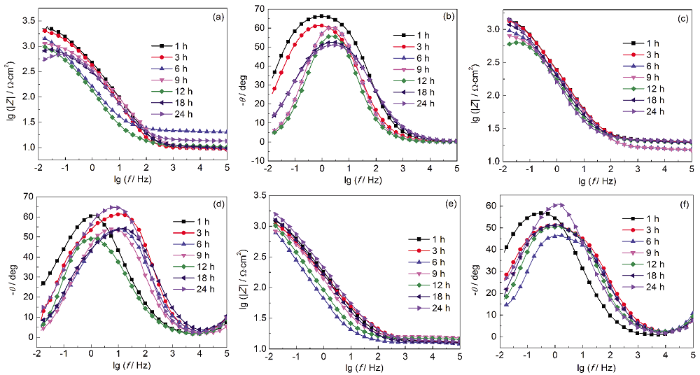
圖6 碳鋼電極浸泡在純水、蛋白質溶液和多糖溶液中的Bode圖
由Nyquist圖可知,浸涂在蛋白質溶液和多糖溶液中試樣的電化學阻抗譜由一個高頻區的接近半圓的容抗弧和一個低頻區接近半圓的容抗弧組成,說明反應體系有兩個時間常數,Bode圖中的兩個峰也證實了這一點。浸涂蛋白質和多糖試樣的等效電路為R(Q(R(QR))),表明浸涂了蛋白質、多糖后碳鋼表面有保護層存在[29],驗證了前期的推測。其中高頻區容抗弧的出現與電極表面的腐蝕產物膜有關,低頻區的容抗弧認為是由電荷轉移過程引起的。
浸涂蛋白質工況下,碳鋼電極的Rp值在第1 h為1702 Ω·cm2,第12 h降到低谷為1487 Ω·cm2,第24 h又逐漸回彈到2040 Ω·cm2。說明碳鋼在浸涂蛋白質過程中轉移電荷的阻力先減小后增大,即腐蝕先加快后又受到抑制。即將碳鋼浸入蛋白質溶液過程中,腐蝕分為兩個階段,這與Jin等[8]和Zhang等[30]的研究結果類似。第一階段 (第12 h之前):浸涂蛋白質工況下的Rp值小于未浸涂工況下的,在同一時間為未浸涂工況的87.26%~96.25%,表明浸涂蛋白質溶液過程中不但發生水分子與Fe(Ⅱ/Ⅲ) 的反應[29],蛋白質分子也與Fe(Ⅱ/Ⅲ) 發生反應,加劇了Fe(Ⅱ/Ⅲ) 的消耗從而加速了碳鋼的腐蝕[31,32]。第二階段 (第12 h之后):浸涂蛋白質工況的Rp值大于未浸涂工況的,此時浸涂蛋白質工況轉移電荷的阻力逐漸增大,這可能是由于前期腐蝕產物的沉積使溶液中的溶解氧減少從而抑制腐蝕。
浸涂多糖工況下的等效電路擬合參數變化與浸涂蛋白質工況的趨勢相同。Rp值在第1 h為1745 Ω·cm2,第6 h降到低谷為1651 Ω·cm2,第24 h又逐漸回彈到2140 Ω·cm2。浸涂多糖工況下第一階段腐蝕持續時間為6 h,且與浸涂蛋白質工況相比,浸涂多糖工況下在同一時間Rp值是浸涂蛋白質工況下的1.01~1.33倍,這也從另一方面表明多糖對碳鋼腐蝕的抑制效果好于蛋白質。
Rb反映保護層的電阻,兩種浸涂工況下,Rb值分別由307.6和525.2 Ω·cm2增大到607.6和622.7 Ω·cm2,表明保護層內轉移電荷的阻力不斷增大。多糖工況下Rb值是蛋白質工況下的1.02~1.71倍,表明多糖比蛋白質工況下保護層的電荷轉移阻力更大,這與SEM分析結果一致。
2.2.2 紅外光譜
將純蛋白質、多糖粉末與經蛋白質、多糖溶液浸泡后碳鋼試樣表面的腐蝕產物粉末進行紅外光譜檢測,結果見圖8。
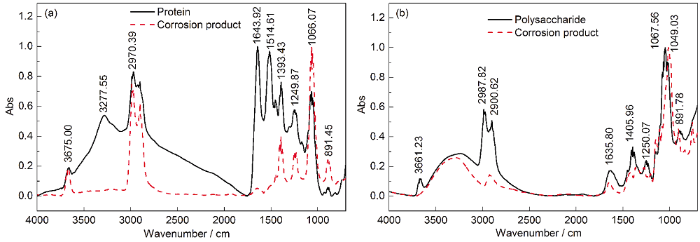
圖8 純蛋白質、多糖粉末和經蛋白質、多糖溶液浸涂24 h后碳鋼試樣腐蝕產物的紅外光譜圖
圖8a中,與純蛋白質相比,將蛋白質浸涂到碳鋼表面檢測可見,在1697~1641 cm-1的酰胺C=O伸縮,1543~1442 cm-1中的氨基酸COO—反對稱伸縮,1411~1340 cm-1中的氨基酸COO—對稱伸縮等幾處峰值明顯減弱或消失,表明在浸涂過程中酰胺C=O、—COO—起著主要作用,它們對蛋白質吸附在碳鋼表面起著關鍵作用。Jin等[8]研究認為,EPS中的羧酸是導致碳鋼耐腐蝕的原因。在有關聚天冬氨酸的研究中顯示,Fe能與羧基螯合,并附著在金屬表面阻隔侵蝕性離子的侵蝕[33]。葉小青等[34]和Liu等[2]研究認為,蛋白質中羧基、羥基等官能團含有孤對電子易與金屬離子發生反應,加強EPS在碳鋼表面的化學吸附作用。
圖8b的紅外光譜結果顯示,與純多糖相比將多糖浸涂到碳鋼表面檢測可見,在1119~966 cm-1基團頻率區—C—OH伸縮振動發生了輕微偏移,在1411~1340 cm-1頻率區的—COO—對稱伸縮、2912~1831 cm-1頻率區中的—CH3反對稱伸縮、—CH2—對稱伸縮峰值發生了明顯的減弱,表明這些官能團在多糖浸涂到碳鋼表面過程中起著重要的作用。Ghafari等[16]和Scheerder等[35]認為,EPS中多糖類物質的羧基基團中含有C—O、C=O鍵,可以與Fe(Ⅱ/Ⅲ) 等金屬離子絡合形成致密的保護層。紅外光譜結果表明,蛋白質、多糖的某些官能團參與了腐蝕反應,對保護層的形成起了關鍵作用。
2.3 討論
在碳鋼表面浸涂蛋白質、多糖后,蛋白質分子中的—C=O—和—COO—,多糖分子的—C—OH,—CH3,—CH2—和—COO—會與Fe(Ⅱ/Ⅲ) 絡合,絡合物與腐蝕產物共同在碳鋼表面形成一層保護層。XRD和SEM分析結果表明,蛋白質、多糖并未改變碳鋼的腐蝕路徑。碳鋼初期腐蝕產物有可能起到了骨架的作用,使蛋白質、多糖絡合物與腐蝕產物共同組成碳鋼表面保護層,附著在碳鋼表面阻止腐蝕性溶液中的腐蝕性粒子及溶解氧的侵蝕,對碳鋼起到保護作用。而多糖與Fe(Ⅱ/Ⅲ) 的結合能力比蛋白質強,因此多糖工況形成的保護層更加致密,對碳鋼腐蝕的抑制能力更強。
保護層的形成過程見圖9a,這一階段主要發生如下反應:第一,如圖9a中 (1),在水分子以及溶解氧的作用下碳鋼界面會發生腐蝕反應生成鐵氧化物[30];第二,如圖9a中 (2),蛋白質與多糖分子的某些官能團會與Fe(Ⅱ/Ⅲ) 發生絡合反應[34],加劇了Fe(Ⅱ/Ⅲ) 的消耗,從而加速了碳鋼的腐蝕。兩步反應生成的鐵氧化物和絡合物沉積到碳鋼表面,逐漸生成”絡合物-腐蝕產物“復合保護層。在保護層的作用下,Fe(Ⅱ/Ⅲ) 與水分子、溶解氧、蛋白質/多糖分子的結合幾率降低,電子的轉移阻力逐漸增大,腐蝕受到抑制,對碳鋼起很好的保護作用。Ghafari等[16]的研究結果也證實,EPS確實能使腐蝕產物更為致密。與此同時,保護層的存在很好地隔絕了溶解氧對碳鋼的侵蝕,在這樣一種缺氧環境中,已經生成的腐蝕產物會逐漸轉化成Fe3O4 (圖9b中白色虛線區域),使腐蝕產物更加致密,進一步抑制碳鋼的腐蝕。但是,關于絡合物與鐵氧化物之間的作用,還需要作進一步的研究。
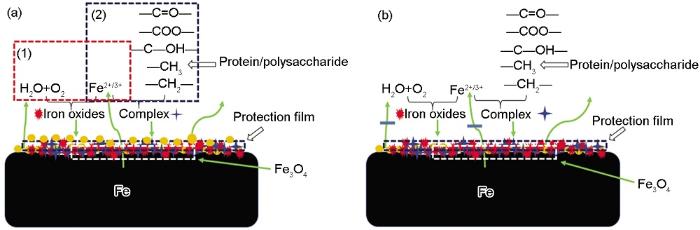
圖9 ”絡合物-腐蝕產物“保護層的形成機理圖
3 結論
(1) 浸涂蛋白質、多糖工況下碳鋼表面的腐蝕速率分別下降17.7%和24.0%,說明多糖對碳鋼腐蝕的抑制效果強于蛋白質。
(2) 浸涂蛋白質、多糖后腐蝕產物仍主要為FeOOH,Fe2O3和Fe3O4,表明蛋白質、多糖抑制腐蝕不是通過改變腐蝕產物種類實現的。
(3) 在浸涂蛋白質、多糖過程中,電化學阻抗先增大后減小,表明碳鋼會發生一定程度的腐蝕而后又被抑制,即保護層的形成經歷兩個主要階段,第一階段,碳鋼利用蛋白質、多糖溶液中的水分子以及溶解氧在碳鋼界面發生初期腐蝕;第二階段,隨著腐蝕進行,溶液中的蛋白質、多糖分子中相關官能團會與Fe(Ⅱ/Ⅲ) 結合,逐漸生成”絡合物-腐蝕產物“保護層。
(4) 蛋白質分子中的—C=O—和COO—,多糖分子中—C—OH,—CH3,—CH2—和—COO—等官能團對保護層的形成起著關鍵作用。
參考文獻
[1] Xu P. Microbiological characteristic of recycling cooling water system makeup by municipal reclaimed water in a power plant [D]. Beijing: Beijing Jiaotong University, 2013
[1] 許萍. 市政再生水補水的電廠循環冷卻水系統微生物特征及控制技術研究 [D]. 北京: 北京交通大學, 2013
[2] Liu H W, Ge T Y, Asif M, et al. The corrosion behavior and mechanism of carbon steel induced by extracellular polymeric substances of iron-oxidizing bacteria [J]. Corros. Sci., 2017, 114: 102
[3] Batmanghelich F, Li L, Seo Y. Influence of multispecies biofilms of Pseudomonas aeruginosa and Desulfovibrio vulgaris on the corrosion of cast iron [J]. Corros. Sci., 2017, 121: 94
[4] Stadler R, Wei L, Fürbeth W, et al. Influence of bacterial exopolymers on cell adhesion of desulfovibrio vulgaris on high alloyed steel: Corrosion inhibition by extracellular polymeric substances (EPS) [J]. Mater. Corros., 2010, 61: 1008
[5] Dong Z H, Liu T, Liu H F. Influence of EPS isolated from thermophilic sulphate-reducing bacteria on carbon steel corrosion [J]. Biofouling, 2011, 27: 487
[6] Dong Y H, Guo N, Liu T, et al. Effect of extracellular polymeric substances isolated from Vibrio natriegens on corrosion of carbon steel in seawater [J]. Corros. Eng., Sci. Technol., 2016, 51: 455
[7] Finkenstadt V L, C?té G L, Willett J L. Corrosion protection of low-carbon steel using exopolysaccharide coatings from Leuconostoc mesenteroides [J]. Biotechnol. Lett., 2011, 33: 1093
[8] Jin J T, Wu G X, Zhang Z H, et al. Effect of extracellular polymeric substances on corrosion of cast iron in the reclaimed wastewater [J]. Bioresour. Technol., 2014, 165: 162
[9] Ignatova-Ivanova T, Ivanov R. Exopolysaccharides from lactic acid bacteria as corrosion inhibitors [J]. Acta Sci. Nat., 2016, 3: 51
[10] Li F S, An M Z, Duan D X. Corrosion inhibition of stainless steel by a sulfate-reducing bacteria biofilm in seawater [J]. Int. J. Miner., Metall. Mater., 2012, 19: 717
[11] Flemming H C, Wingender J. The Biofilm Matrix [J]. Nat. Rev. Microbiol., 2010, 8: 623
[12] Beech I B, Zinkevich V, Tapper R, et al. Study of the interaction of sulphate-reducing bacteria exopolymers with iron using X-ray photoelectron spectroscopy and time-of-flight secondary ionisation mass spectrometry [J]. J. Microbiol. Meth., 1999, 36: 3
[13] Urbain V, Block J C, Manem J. Bioflocculation in activated slud-ge: An analytic approach [J]. Water Res., 1993, 27: 829
[14] Keiding K, Nielsen P H. Desorption of organic macromolecules from activated sludge: Effect of ionic composition [J]. Water Res., 1997, 31: 1665
[15] Zhang F, Pan J S, Claesson P M. Electrochemical and AFM studies of mussel adhesive protein (Mefp-1) as corrosion inhibitor for carbon steel [J]. Electrochim. Acta, 2011, 56: 1636
[16] Ghafari M D, Bahrami A, Rasooli I, et al. Bacterial exopolymeric inhibition of carbon steel corrosion [J]. Int. Biodeterior. Biodegrad., 2013, 80: 29
[17] Zhang H X, Wang D D, Wang F, et al. Corrosion inhibition of mild steel in hydrochloric acid solution by quaternary ammonium salt derivatives of corn stalk polysaccharide (QAPS) [J]. Desalination, 2015, 372: 57
[18] Finkenstadt V L, Bucur C B, C?té G L, et al. Bacterial exopolysaccharides for corrosion resistance on low carbon steel [J]. J. Appl. Polym. Sci., 2017, 134: 45032
[19] Mobin M, Rizvi M. Polysaccharide from Plantago as a green corrosion inhibitor for carbon steel in 1 M HCl solution [J]. Carbohydr. Polym., 2017, 160: 172
[20] Xu P, Si S, Zhang Y J, et al. Effect of extracellular polymeric substances (EPS) on anti-corrosion behavior of metals [J]. Corros. Prot., 2016, 37: 384
[20] 許萍, 司帥, 張雅君等. 微生物胞外聚合物 (EPS) 對金屬耐蝕性的影響 [J]. 腐蝕與防護, 2016, 37: 384
[21] Guo X M, Li C G, Chen W, et al. GB/T 18175-2014 Determination of corrosion inhibition performance of water treatment agents-rotation specimen method [S]. Beijing: China Standard Press, 2014
[21] 郭喜民, 李成國, 陳偉等. GB/T 18175-2014水處理劑緩蝕性能的測定 旋轉掛片法 [S]. 北京: 中國標準出版社, 2014
[22] Chongdar S, Gunasekaran G, Kumar P. Corrosion inhibition of mild steel by aerobic biofilm [J]. Electrochim. Acta, 2005, 50: 4655
[23] Stadler R, Fuerbeth W, Harneit, et al. First evaluation of the applicability of microbial extracellular polymeric substances for corrosion protection of metal substrates [J]. Electrochim. Acta, 2008, 54: 91
[24] Harimawan A, Ting Y P. Investigation of extracellular polymeric substances (EPS) properties of P. aeruginosa and B. subtilis and their role in bacterial adhesion [J]. Colloids Surf., 2016, 146B: 459
[25] Wang J. Inhibition behavior of Lactobacillus reuteri extracellular polymeric substances on carbon steel corrosion [D]. Beijing: Beijing University of Civil Engineering and Architecture, 2015
[25] 王婧. 羅伊氏乳桿菌胞外聚合物抑制碳鋼腐蝕行為研究 [D]. 北京: 北京建筑大學, 2015
[26] Liu S N, Su W, Wei Z F, et al. Corrosion behavior analysis of carbon steel in natural and sterile seawater [J]. Equip. Environ. Eng., 2013, 10(4): 16
[26] 劉世念, 蘇偉, 魏增福等. 碳鋼在自然海水和滅菌海水中的腐蝕行為分析 [J]. 裝備環境工程, 2013, 10(4): 16
[27] Hu J Y. Study on the corrosion mechanism and anticorrosion methods of carbon steel in RO product waste of seawater [D]. Wuhan: Wuhan University, 2013
[27] 胡家元. 碳鋼在海水淡化一級反滲透產水中腐蝕機理及防腐方法研究 [D]. 武漢: 武漢大學, 2013
[28] Benali O, Abdelmoula M, Refait P, et al. Effect of orthophosphate on the oxidation products of Fe(II)-Fe(III) hydroxycarbonate: The transformation of green rust to ferrihydrite [J]. Geochim. Cosmochim. Acta, 2001, 65: 1715
[29] Liu H W, Xu D K, Dao A Q, et al. Study of corrosion behavior and mechanism of carbon steel in the presence of Chlorella vulgaris [J]. Corros. Sci., 2015, 101: 84
[30] Zhang H Y, Tian Y M, Wan J M, et al. Study of biofilm influenced corrosion on cast iron pipes in reclaimed water [J]. Appl. Surf. Sci., 2015, 357: 236
[31] Beech I B, Sunner J. Biocorrosion: Towards understanding interactions between biofilms and metals [J]. Curr. Opin. Biotechnol., 2004, 15: 181
[32] Moradi M, Song Z L, Tao X. Introducing a novel bacterium, Vibrio neocaledonicus sp., with the highest corrosion inhibition efficiency [J]. Electrochem. Commun., 2015, 51: 64
[33] Huo Y N, Liu S, Lu Z. Research on synthesis and behavior of Polyaspartic acid—A new type polymeric scale inhibitors [J]. Fine Chem., 2000, 17: 581
[33] 霍宇凝, 劉珊, 陸柱. 新型聚合物阻垢劑聚天冬氨酸的合成與性能 [J]. 精細化工, 2000, 17: 581
[34] Ye X Q, Peng T Y, Ji Y X, et al. Application progress of microorganism extracellular polymeric substances in environmental engineering [J]. J. Hangzhou Norm. Univ. (Nat. Sci. Ed.), 2016, 15: 387
[34] 葉小青, 彭亭瑜, 姬玉欣等. 微生物胞外聚合物在環境工程中的應用進展 [J]. 杭州師范大學學報 (自然科學版), 2016, 15: 387
[35] Scheerder J, Breur R, Slaghek T, et al. Exopolysaccharides (EPS) as anti-corrosive additives for coatings [J]. Prog. Org. Coat., 2012, 75: 224
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《中國腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護網官方QQ群:140808414





