摘要
將具有(111)擇優取向的島狀奧氏體相嵌入連續鐵素體的2205雙相不銹鋼(2205 DSS)工作面浸泡在銅綠假單胞菌(P. aeruginosa)中進行電化學測試,研究浸泡時間對2205 DSS 微生物腐蝕行為的影響。開路電位(OCP)、線性極化電阻(LPR)以及電化學阻抗譜(EIS)表明,在7 d浸泡期的無菌溶液中測得的EOCP、極化電阻(Rp)和電荷轉移電阻(Rct)均比在有菌溶液中的大,表明銅綠假單胞菌加速了2205 DSS的腐蝕。動電位極化曲線表明,2205 DSS在無菌和有菌溶液中的維鈍電流密度(ip)都隨著浸泡時間的延長而不斷增大,且在浸泡1 d、3 d、7 d的每個時間點有菌溶液的ip均比無菌環境的大,進一步證明銅綠假單胞菌加速了2205 DSS的腐蝕進程。掃描電子顯微鏡(SEM)結果表明,在有菌溶液中隨著浸泡時間的延長表面粘附的細菌量逐漸增多,浸泡3 d后樣品表面的細菌聚集成一個個小團簇,浸泡7 d菌落進一步聚集形成細菌生物膜。對腐蝕后樣品表面局部腐蝕形貌的觀察發現,細菌生物膜的形成加速了表面局部腐蝕的發生,導致嚴重的局部腐蝕。X射線光電子能譜(XPS)結果表明,在存在銅綠假單胞菌的條件下2205 DSS表面形成溶于水的CrO3,使MIC點蝕發生。
關鍵詞: 金屬材料 ; 雙相不銹鋼 ; 微生物腐蝕 ; 銅綠假單胞菌 ; 生物膜
雙相不銹鋼(Duplex Stainless Steel,DSS)具有良好的機械性能和優異的耐氯離子腐蝕性能,廣泛應用在海洋工程領域[1,2,3]。但是,海洋環境中的微生物等腐蝕性活性介質使雙相不銹鋼發生局部腐蝕[4,5,6,7,8]。由微生物腐蝕引起的失效,已成為海洋工程材料領域的重要問題[9,10,11]。銅綠假單胞菌(Pseudomonas aeruginosa,P. aeruginosa)系革蘭氏陰性桿菌,是海洋中常見的腐蝕性細菌。銅綠假單胞菌能使2205 DSS表面產生可溶性鉻化合物CrO3,從而加速表面鈍化膜的溶解,顯著降低2205 DSS的耐腐蝕性[12,13,14]。銅綠假單胞菌的生物催化對2205 DSS鈍化膜產生長期的破壞作用,7 d或14 d的連續電化學腐蝕研究已有報道[15]。但是,針對7 d內每個時間節點詳細的電化學腐蝕研究,如動電位極化曲線測定以及表面細菌生物膜的形成對點蝕的影響,尚未有深入的報道。此外,由于軋制方向不同,2205 DSS的金相組織往往表現出不同形態。現有報道中的2205 DSS,其金相組織分布特征為長條帶狀奧氏體相嵌入連續的鐵素體基體[16]。本文模擬海洋環境,將具有島狀奧氏體相嵌入連續鐵素體的2205 DSS工作面浸泡在銅綠假單胞菌液中,采用電化學測試并結合表面分析技術研究浸泡時間對2205 DSS腐蝕行為的影響。
1 實驗方法
1.1 實驗用材料
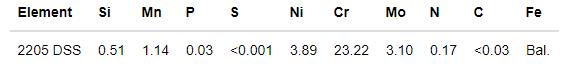
本文實驗用材料為2205雙相不銹鋼(2205 DSS),其化學成分(質量分數,%)列于表1。用線切割方法將2205 DSS加工成尺寸為10 mm×10 mm×5 mm的樣品。將部分樣品用環氧樹脂封樣并預留出10 mm×10 mm的工作面積用于電化學測試。將所有樣品依次采用150、400、600、800、1000和1200粒度的碳化硅砂紙打磨(金相樣品另用水溶性金剛石研磨膏作拋光處理)、丙酮除油、去離子水沖洗,再用無水乙醇超聲清洗30 min,干燥后備用。
表1 2205 DSS的化學成分(質量分數,%)
1.2 培養基和細菌
實驗用細菌為銅綠假單胞菌(1A00099),取自中國海洋微生物菌種保藏管理中心(MCCC)。使用2216 E培養基用于模擬營養海水環境,培養基的組分(g·L-1)為:19.45 NaCl,5.98 MgCl2,3.24 Na2SO4,1.8 CaCl,0.55 KCl,0.16 Na2CO3,0.08 KBr,0.034 SrCl2,0.08 SrBr2,0.022 H3BO3,0.004 NaSiO3,0.0024 NaF,0.0016 NH4NO3,0.008 NaH2PO4,5.0蛋白胨,1.0酵母提取物和0.1檸檬酸鐵。使用前將培養基在121℃、高壓滅菌15 min。配制菌液的初始濃度為106 CFU/mL。
1.3 電化學測試
測試前,將樣品在75%乙醇溶液中滅菌30 min,隨后暴露在紫外光下滅菌30 min。在電化學工作站(Zahner Zennium,Germany)進行測試,采用三電極體系,參比電極為飽和甘汞電極(SCE),對電極為鉑片,工作電極為2205 DSS。對樣品進行連續7 d的開路電位(OCP)、線性極化電阻(LPR)和交流阻抗譜(EIS)測試,和1 d,3 d 和7 d的動電位極化曲線測試。為了保證體系的穩定,每次測量OCP 1 h后依次進行電化學阻抗譜(EIS)和極化曲線測試。LPR測試電位為-5 mV至+5 mV(vs. OCP),掃描速率為0.125 mV/s。EIS測試振幅為5 mV,測試頻率范圍為0.01 Hz~100 kHz。動電位極化掃描速率為0.5 mV/s,掃描范圍為-200 mV(vs. OCP)至1.6 V。電解液為37℃的無菌和菌液濃度為106 CFU/mL的2216E培養基。為保證結果的可重復性,每次實驗使用三個平行試樣。
1.4 表面分析
用光學顯微鏡(徠卡DM500)觀察樣品的金相組織。觀察前對拋光的樣品進行電解侵蝕:使用可編程直流電源(艾德克斯 IT-6123),設置電壓6 V,電流1 A,電解液是濃度為20 %的NaOH溶液,侵蝕時間為10 s。
用掃描電子顯微鏡(SEM,Carl Zeiss)觀察樣品的表面形貌。對表面具有銅綠假單胞菌的樣品(極化測試后的樣品)用無菌水漂洗3次,使用2.5%戊二醛在4℃固定4 h,之后依次用50%,60%,70%,80%,90%,95%和100%的酒精脫水,噴Pt后進行SEM觀察。對部分極化測試后的樣品,根據GB / T4334.4-2000[17],采用硝酸-氫氟酸溶液去除樣品表面生物膜和腐蝕產物,然后采用SEM觀察樣品表面形貌。用3D激光共聚焦掃描顯微鏡(LSM,KEYENCE VK-X200)測量局部腐蝕坑深度,對樣品表面6個典型腐蝕坑的深度進行掃描測量,得到平均腐蝕坑深度柱狀圖,使用Excel進行雙樣本方差分析和F-檢驗以確定統計學顯著性。P<0.05表示有顯著的統計學意義。
用X射線光電子能譜儀(XPS,ULVAC-PHI 1800) 分析表面元素的化學態。使用單色X射線源(15 kV和350 W的Al kα電極),能量58.70 eV、步長0.125 eV記錄0~1400 eV范圍內的光譜的通過能量和高分辨率光譜。C 1s峰值為284.8 eV,用于校正峰位偏移。
2 結果和討論
2.1 金相組織和XRD譜
已報道的2205 DSS的工作面金相組織如圖1a所示[16],本文采用的2205 DSS工作面的金相組織如圖1b所示。圖中亮白色的組織為奧氏體,灰白色組織為鐵素體,兩相各占50%左右。圖1a中2205 DSS的金相組織分布特征為長條帶狀分布的奧氏體相嵌入連續的鐵素體中,而本文采用的2205 DSS工作面具有島狀奧氏體相嵌入連續的鐵素體的特點(圖1b)。對兩種組織形態的2205 DSS的XRD譜進行分析,結果如圖2所示。已報道的2205 DSS工作面的奧氏體的擇優取向為(220)晶面,而本文的擇優取向為(111)晶面。由于軋制方向不同,奧氏體的擇優取向不同,因而表現為不同形態的奧氏體分布。

圖1 已報道的[16]和本文使用的2205 DSS的金相組織
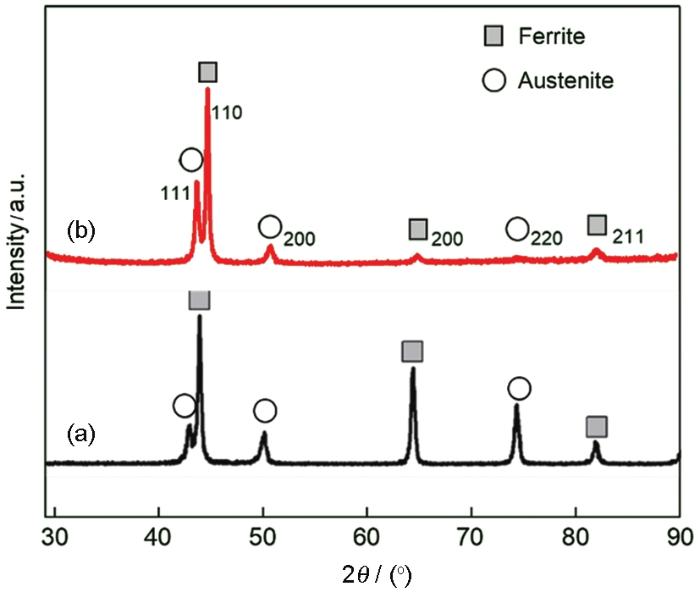
圖2 已報道的[16]和本文使用的2205 DSS工作面的XRD譜
2.2 OCP和LPR
圖3給出了在無菌和有菌電解液中對2205 DSS進行連續7 d電化學測試的OCP和LPR結果。從OCP結果可以看出,在無菌環境中樣品的開路電位EOCP在1 d內由0.034 V急降至-0.324 V,隨后穩定在-0.360 V左右;而在有菌環境中樣品EOCP由0.024 V迅速下降至-0.356 V,隨后趨于平穩(-0.381 V)。LPR結果表明,無論是在無菌環境還是在有菌環境中,樣品的線性極化電阻值Rp在1 d內均顯著降低,隨后表現得相對平穩,其中無菌環境中樣品的Rp穩定在24 kΩ·cm2,大于有菌環境的14 kΩ·cm2。OCP和LPR結果表明,無論無菌環境還是有菌環境,2205 DSS在浸泡1 d內腐蝕速度均迅速增加,之后趨于平穩,但是在整個7 d浸泡期有菌環境中樣品的腐蝕更嚴重。其原因可能是,在浸泡早期即1 d 內樣品表面鈍化膜的完整性迅速遭到腐蝕性介質的破壞,因而腐蝕進程加快。但是之后鈍化膜的破壞與修復漸趨平衡,表現為腐蝕趨于平緩。與無菌環境比較,銅綠假單胞菌的存在對鈍化膜的破壞更嚴重,因而整體腐蝕更快。
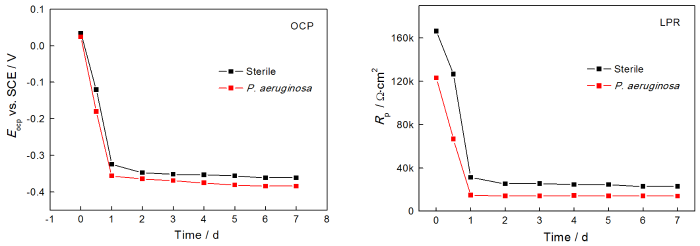
圖3 在無菌和有菌溶液中對2205 DSS 連續7 d測試的OCP和LPR結果
2.3 EIS
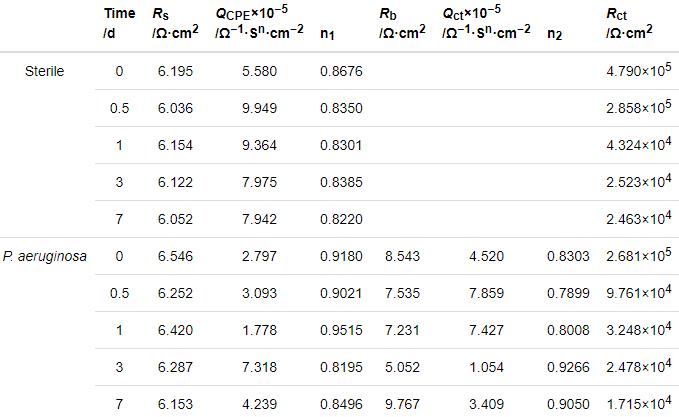
圖4給出了2205 DSS在無菌和含銅綠假單胞菌的溶液中連續測試7 d的EIS譜圖。從圖4可以看出,無論是在無菌還是有菌的條件下,能奎斯特圖中的阻抗弧半徑在前24 h均隨著時間的延長而急劇減小,隨后1 d至7 d減小趨勢大幅度減緩。由波德圖可知,較低頻率下的阻抗模值在前24 h急劇減小,隨后1 d至7 d趨于平緩,變化規律與能奎斯特圖相同。使用ZsimpWin擬合軟件擬合EIS測試結果,采用的等效電路如圖5所示,其中Rs為溶液電阻,Rct為電荷轉移電阻,Rb為試樣表面上形成的鈍化膜/生物膜的電阻,電極和溶液之間的雙電層電容非純電容,因此用常相位角元件Q表示。擬合參數列于表2。溶液電阻和鈍化膜電阻非常低并且隨時間波動很小,因此Rct的變化是影響樣品耐腐蝕性能的主要因素。從表2可以看出,在無菌環境中2205 DSS的Rct在24 h內由4.790×105 Ω·cm2迅速下降至4.324×104 Ω·cm2,在隨后幾天下降速度大幅度降低,7 d時降至2.463×104 Ω·cm2。在有菌環境中2205 DSS的Rct在24 h內由 2.681×105 Ω·cm2急劇下降至3.248×104 Ω·cm2,隨后幾天的下降速度也趨于平緩,7 d時降至1.715×104 Ω·cm2。EIS結果表明,2205 DSS在第1 d內腐蝕進程急劇加快,隨后趨于平緩,但是隨著時間的延長腐蝕仍然在不斷進展。此外,在整個浸泡期的每個時間點有菌環境中的電阻值均小于無菌環境,說明銅綠假單胞菌的生命活動對鈍化膜完整性的破壞更嚴重,從而導致樣品的電阻值減小,腐蝕程度加深。
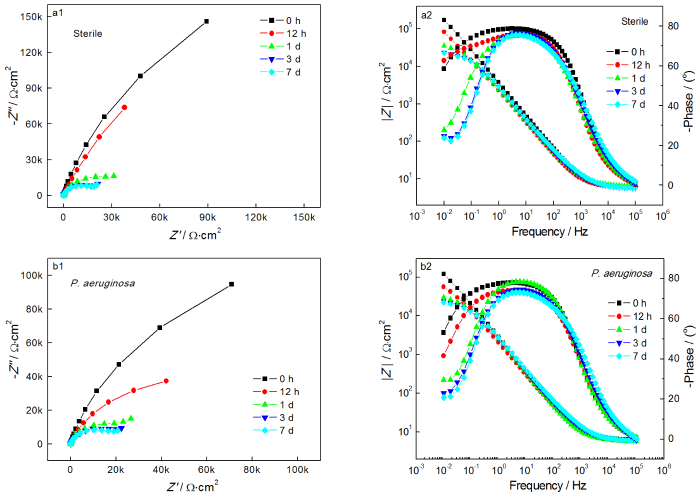
圖4 2205 DSS在無菌溶液和有菌溶液中的能奎斯特圖和波德圖
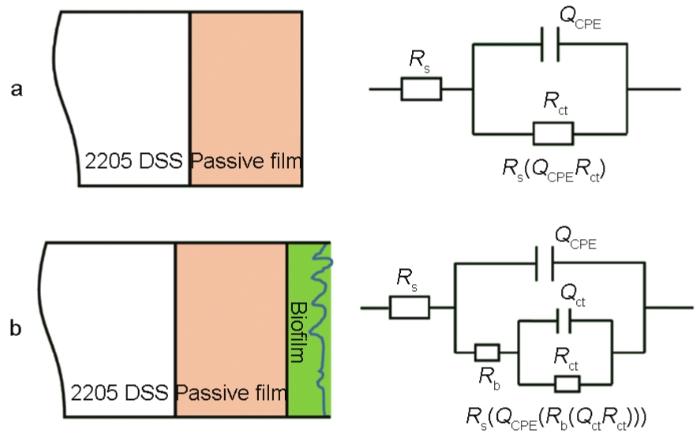
圖5 用于擬合2205 DSS在無菌溶液和有菌溶液中阻抗譜的物理模型和相應的等效電路
表2 2205 DSS在無菌溶液和有菌溶液中的阻抗譜的擬合參數
2.4 動電位極化曲線
2205 DSS在無菌和有菌溶液中浸泡1 d,3 d和7 d的動電位極化曲線,如圖6所示。對極化曲線進行擬合,相應的擬合參數列于表3。從圖6可以看出,浸泡1 d,3 d和7 d后,與在無菌溶液中的測試結果相比,樣品在有菌溶液中的極化曲線均明顯右移。從表3可知,浸泡1 d后樣品在有菌溶液中的ip(2.269 μA·cm-2) 明顯大于無菌溶液中(1.490 μA·cm-2),且有菌溶液的維鈍區間ΔE(1.7883 V)略小于無菌溶液的ΔE(1.8031 V),說明浸泡1 d后2205 DSS在有菌環境下的腐蝕比無菌環境更為嚴重。浸泡3 d后有菌溶液中樣品的ip為2.917 μA·cm-2,明顯大于無菌溶液中樣品的ip(1.754 μA·cm-2),說明浸泡3 d后銅綠假單胞菌加速了2205 DSS的腐蝕。浸泡7 d后樣品在有菌環境的自腐蝕電位(Ecorr)、擊破電位(Epit)電位都略小于無菌環境,有菌溶液的ip(3.515 μA·cm-2)大于無菌溶液中ip(2.004 μA·cm-2),說明在浸泡7 d后2205 DSS樣品在有菌溶液中的腐蝕更嚴重。浸泡1 d,3 d和7 d后的極化曲線進一步表明,銅綠假單胞菌的存在使表面鈍化膜的破壞更嚴重,從而使樣品的腐蝕程度更嚴重。
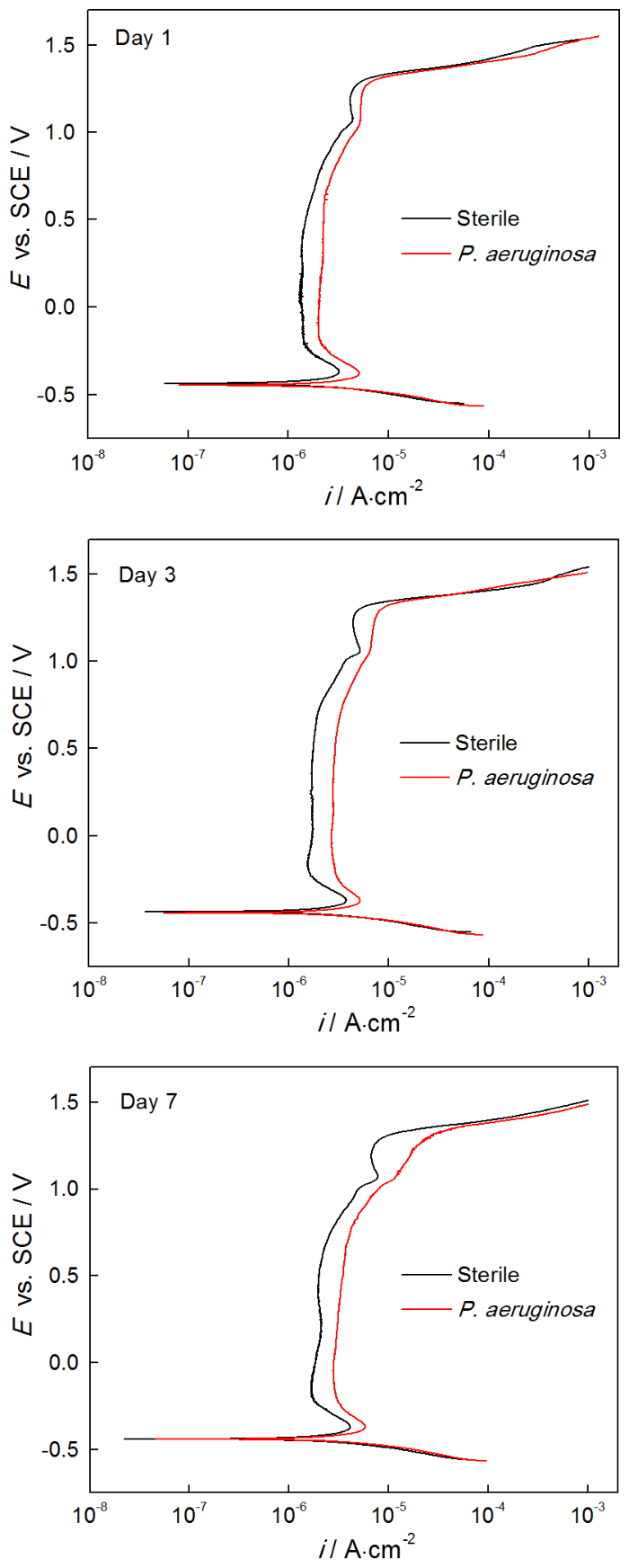
圖6 2205 DSS在無菌和有菌溶液中浸泡1 d、3 d和7 d的動電位極化曲線
表3 2205 DSS動電位極化曲線的相關擬合參數
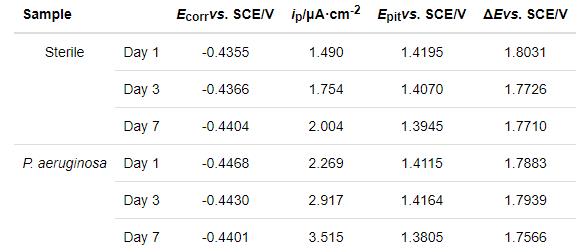
對2205 DSS不同工作面的電化學腐蝕結果作比較,將實驗結果與文獻[16]中的動電位極化曲線比較。可以發現,在無菌條件浸泡1 d時,文獻中樣品的維鈍電流密度ip為0.74 μA·cm-2略小于本研究的ip (1.490 μA·cm-2);在有菌條件下,文獻中的ip為2.86 μA·cm-2略大于本研究的ip(2.269 μA·cm-2)。但是,文獻中樣品在無菌條件浸泡1 d的擊破電位為1.505 V (vs. SHE),有菌條件為1.112 V (vs. SHE),轉換為相對于飽和甘汞電極電位,文獻中樣品在無菌條件浸泡1 d的擊破電位為1.264 V (vs. SCE),有菌條件為0.871 V (vs. SCE),顯著小于本文的擊破電位(表3),說明本文用的工作面(即奧氏體的擇優取向為(111)晶面)比文獻報道的(即奧氏體的擇優取向為(220)晶面)耐點蝕性能更佳。
2205 DSS樣品在無菌溶液和有菌溶液中浸泡不同時間的動電位極化曲線,如圖7所示。從圖7可以看出,無菌環境中樣品的極化曲線隨著浸泡時間的增加而右移,其中1 d 時ip為1.490 μA·cm-2,3 d時ip為1.754 μA·cm-2,7 d時ip為2.004 μA·cm-2(表3)。由此可知,ip隨浸泡時間延長而增大,說明在無菌環境下2205 DSS的腐蝕不斷加劇。此外,從表3還可以看出,自腐蝕電位Ecorr,擊破電位Epit和維鈍區間ΔE隨時間延長而減小,說明樣品在無菌環境中隨浸泡時間的延長更易腐蝕且耐點蝕性能下降。從圖7還可以看出,2205 DSS在有菌環境下極化曲線隨腐蝕時間延長右移,相應地樣品在1 d 時ip為2.269 μA·cm-2,3 d時ip為2.917 μA·cm-2,7 d時ip為3.515 μA·cm-2(表3),由此可知維鈍電流密度隨時間的增加而不斷增大。此外,由表3還可以發現,有菌環境下樣品的擊破電位Epit和維鈍區間ΔE呈現隨時間延長而減小的趨勢,說明有菌環境下2205 DSS隨浸泡時間增加而腐蝕不斷加劇。
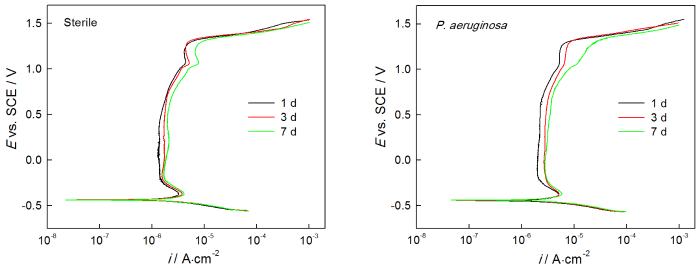
圖7 2205 DSS在無菌溶液和有菌溶液中的動電位極化曲線
動電位極化曲線的結果說明,無論在無菌環境還是在有菌環境,2205 DSS的腐蝕均隨著時間的延長而加劇,而在有菌環境下腐蝕加劇的程度更高。
2.5 極化后樣品表面的分析
在動電位極化曲線測試結束后,對2205 DSS表面形貌進行觀察,結果如圖8所示。從圖8可見,在無菌溶液中分別浸泡1 d,3 d和7 d后并極化的樣品其表面形貌沒有顯著的差別,而在含銅綠假單胞菌的溶液中極化后樣品表面粘附桿狀銅綠假單胞菌。且隨浸泡時間的延長,表面粘附的細菌量逐漸增多,浸泡3 d后樣品表面的細菌發生聚集形成一個個小團簇,浸泡7 d后表面菌落簇的面積與厚度較3 d進一步增加,菌落聚集形成細菌生物膜。以上結果說明,在有菌溶液中2205 DSS表面易發生細菌粘附,且隨浸泡時間的延長而聚集長大。細菌生物膜是金屬產生MIC的主要因素,銅綠假單胞菌為好氧菌,消耗氧氣,導致生物膜下方形成厭氧環境,從而阻礙了2205 DSS鈍化膜的再鈍化[18,19]。生物膜厚度是評估材料MIC的重要指標[20],可解釋為什么在浸泡7d內2205 DSS在有銅綠假單胞菌的條件下腐蝕都隨著時間的延長而加劇,且腐蝕速度高于無菌環境。

圖8 動電位極化后2205 DSS樣品表面的SEM形貌
去除2205 DSS樣品表面生物膜和腐蝕產物后,用SEM觀察無菌和有菌溶液中浸泡7 d并極化后的樣品表面形貌(圖9)。從圖9可見,與無菌環境相比,有菌環境中樣品表面形成的局部腐蝕面積和深度更大。用激光共聚焦掃描顯微鏡觀測無菌和有菌溶液中浸泡7 d并極化后樣品表面的局部腐蝕形貌及腐蝕坑深度,結果如圖10所示。從圖10(d)中可見,在無菌條件下浸泡7 d后樣品的平均腐蝕坑深度為1.96 μm,明顯小于有菌條件的坑深4.09 μm,進一步證明銅綠假單胞菌生物膜加速了2205 DSS的局部腐蝕。

圖9 2205 DSS在無菌環境和有菌溶液浸泡7 d除去腐蝕產物和生物膜后表面的SEM形貌
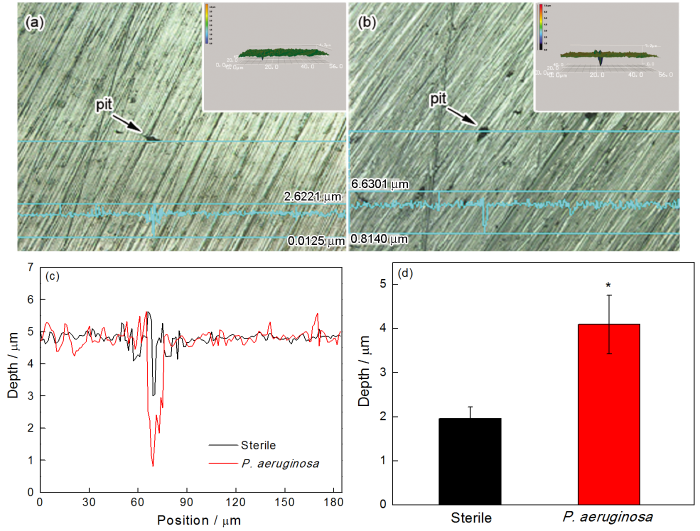
圖10 2205 DSS在無菌環境和有菌溶液下浸泡7 d除去膜后的局部腐蝕形貌和局部腐蝕深度分析和平均腐蝕深度比較 (*P < 0.05 與無菌環境比較)
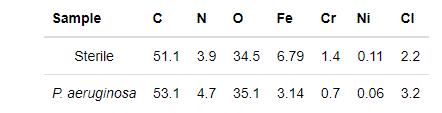
圖11a給出了樣品在無菌和有菌溶液中浸泡7 d后表面的XPS寬譜結果,表4列出了相應的樣品表面的元素含量。從圖11和表4可見,2205 DSS在銅綠假單胞菌溶液中Fe和Cr的相對含量均低于無菌溶液的,表明銅綠假單胞菌生物膜消耗了樣品表面的Fe和Cr,而鐵的氧化物以及鉻的氧化物是鈍化膜的主要成分,可見Fe和Cr的消耗不利于鈍化膜的形成[20]。圖11b和c分別給出了在無菌溶液和有菌溶液中浸泡7 d后2205 DSS表面的高分辨XPS Cr 2p譜。無菌溶液中樣品的XPS的Cr 2p譜可擬合為Cr的四個特征峰,分別對應于Cr 2p 1/2譜中Cr(583.5 eV),Cr(OH)3(586.1 eV),Cr 2p 3/2譜的Cr(574.5 eV),Cr2O3(576.4 eV),而有菌溶液中樣品的Cr 2p譜可擬合為Cr的五個特征峰,分別對應于Cr 2p 1/2譜中Cr(583.5 eV),Cr(OH)3(586.4 eV),Cr 2p 3/2譜中的Cr(574.4 eV),Cr2O3(576.4 eV)和CrO3(578.3 eV)[21,22],顯然有菌溶液中2205 DSS在Cr 2p 3/2譜中有新的產物CrO3形成。
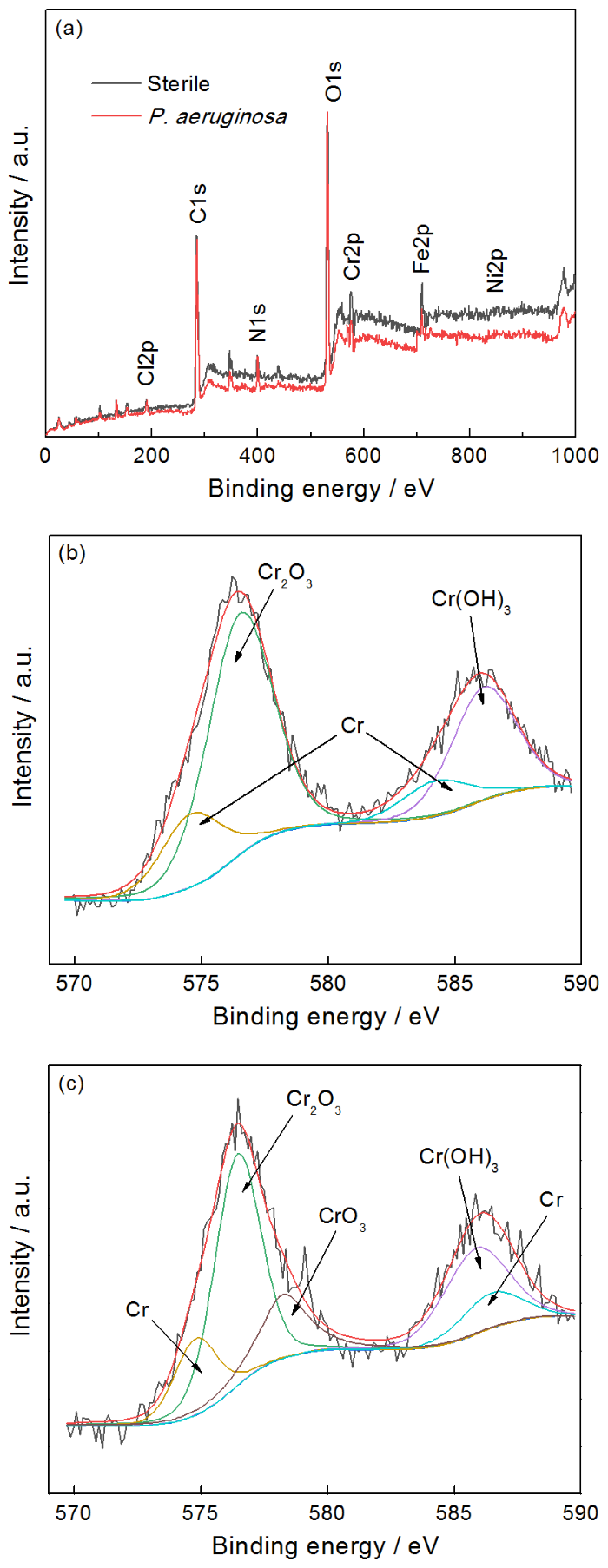
圖11 2205 DSS在無菌環境和有菌環境下浸泡7 d后表面的XPS寬譜和高分辨XPS Cr 2p光譜
表4 2205 DSS在無菌和有菌環境下浸泡7 d后表面元素含量(原子分數,%)
XPS測試結果表明,與樣品在無菌溶液中浸泡相比,2205 DSS在銅綠假單胞菌溶液中浸泡后表面形成CrO3。其原因是,銅綠假單胞菌的分泌物如綠膿菌素(PYO)可加速金屬基體與銅綠假單胞菌間的電子轉移,從而催化Cr氧化形成易溶于水的CrO3,進而加速表面鈍化膜的溶解并加劇與生物膜接觸的材料的局部腐蝕[23,24,25,26,27]。此外,2205 DSS在含銅綠假單胞菌溶液中隨著浸泡時間的延長,表面粘附的細菌量逐漸增多,菌落簇的面積與厚度不斷增加,最后聚集形成細菌生物膜,導致其耐腐蝕性能不斷降低。
3 結論
具有(111)擇優取向的島狀奧氏體相嵌入連續的鐵素體基體的2205 DSS,在含銅綠假單胞菌溶液中的腐蝕速率顯著比在無菌環境中的高。無論樣品表面粘附少量細菌還是菌落聚集長大形成團簇或細菌生物膜,都加劇了2205 DSS的腐蝕,且粘附細菌數量的增加使腐蝕更趨嚴重。銅綠假單胞菌使樣品表面形成溶于水的CrO3,破壞了2205 DSS鈍化膜的完整性,使其耐局部腐蝕性能下降,腐蝕加劇。
參考文獻
[1] SongZ, FengH, HuS. Development of Chinese duplex stainless steel in recent years [J]. Journal of Iron and Steel Research, International, 2017, 24: 121
[2] HanD, JiangY M, ShiC, et al. Effect of temperature, chloride ion and pH on the crevice corrosion behavior of SAF 2205 duplex stainless steel in chloride solutions [J]. Journal of Materials Science, 2011, 47(2): 1018
[3] WangL X, LiH B, LiG P, et al. Microstructural Evolution and Flow Behavior of 2205 and 2507 Duplex Stainless Steel during Double Pass Hot Compressive Deformation [J]. Chinese Journal of materials Research, 2016, 32(12): 888
[3] 王立新, 李花兵, 李國平等. 2205和2507雙相不銹鋼雙道次熱壓縮條件下的微觀組織演變及變形行為 [J]. 材料研究學報, 2016, 32(12): 888)
[4] AntonyP J, Singh RamanR K, MohanramR, et al. Influence of thermal aging on sulfate-reducing bacteria (SRB)-influenced corrosion behaviour of 2205 duplex stainless steel [J]. Corrosion Science, 2008, 50(7): 1858
[5] MoradiM, SongZ, YangL, et al. Effect of marine Pseudoalteromonas sp. on the microstructure and corrosion behaviour of 2205 duplex stainless steel [J]. Corrosion Science, 2014, 84: 103
[6] LiuW. Rapid MIC attack on 2205 duplex stainless steel pipe in a yacht [J]. Engineering Failure Analysis, 2014, 42: 109
[7] XuF L, DuanJ Z, LinC G, et al. Influence of Marine Aerobic Biofilms on Corrosion of 316L Stainless Steel [J]. Journal of Iron and Steel Research, International, 2015, 22(8): 715
[8] GabrielA A, UgayM C C F, SiringanM A T, et al. Atmospheric pressure plasma jet inactivation of Pseudomonas aeruginosa biofilms on stainless steel surfaces [J]. Innovative Food Science & Emerging Technologies, 2016, 36: 311
[9] ZhaoX D, WuP, JiangJ, et al. Study of effect of sulfate-reducing bacteria on corrosion interface between Q235 steel and sea mud [J]. Chinese Journal of Materials Research, 2007, 21(3): 230
[9] 趙曉棟, 吳 鵬, 姜 江等. 硫酸鹽還原菌對海泥中Q235鋼腐蝕界面的影響 [J]. 材料研究學報, 2007, 21(3): 230)
[10] BasheerR, GangaG, ChandranR K, et al. Effect of W-TiO2 composite to control microbiologically influenced corrosion on galvanized steel [J]. Appl Microbiol Biotechnol, 2013, 97(12): 5615
[11] MachucaL L, BaileyS I, GubnerR, et al. Effect of oxygen and biofilms on crevice corrosion of UNS S31803 and UNS N08825 in natural seawater [J]. Corrosion Science, 2013, 67: 242
[12] ZhaoY, ZhouE, LiuY, et al. Comparison of different electrochemical techniques for continuous monitoring of the microbiologically influenced corrosion of 2205 duplex stainless steel by marine Pseudomonas aeruginosa biofilm [J]. Corrosion Science, 2017, 126: 142
[13] XuD, XiaJ, ZhouE, et al. Accelerated corrosion of 2205 duplex stainless steel caused by marine aerobic Pseudomonas aeruginosa biofilm [J]. Bioelectrochemistry, 2017, 113: 1
[14] ZhaoY, ZhouE, XuD, et al. Laboratory investigation of microbiologically influenced corrosion of 2205 duplex stainless steel by marine Pseudomonas aeruginosa biofilm using electrochemical noise [J]. Corrosion Science, 2018, 143: 281
[15] XuD, ZhouE, ZhaoY, et al. Enhanced resistance of 2205 Cu-bearing duplex stainless steel towards microbiologically influenced corrosion by marine aerobic Pseudomonas aeruginosa biofilms [J]. Journal of Materials Science & Technology, 2017, 34(8): 1325
[16] LiP, ZhaoY, LiuY, et al. Effect of Cu Addition to 2205 Duplex Stainless Steel on the Resistance against Pitting Corrosion by the Pseudomonas aeruginosa Biofilm [J]. Journal of Materials Science & Technology, 2017, 33(7): 723
[17] Chinese National Standards,Method of nitric-hydrofluoric acids test for stainless steel,GB/T4334. 4–2000. [M]
[18] AbdulkareemE H, MemarzadehK, AllakerR P, et al. Anti-biofilm activity of zinc oxide and hydroxyapatite nanoparticles as dental implant coating materials [J]. J Dent, 2015, 43(12): 1462
[19] ZhouH, WeirM D, AntonucciJ M, et al. Evaluation of three-dimensional biofilms on antibacterial bonding agents containing novel quaternary ammonium methacrylates [J]. International Journal of Oral Science, 2014, 6(2): 77
[20] LiH, YangC, ZhouE, et al. Microbiologically influenced corrosion behavior of S32654 super austenitic stainless steel in the presence of marine Pseudomonas aeruginosa biofilm [J]. Journal of Materials Science & Technology, 2017, 33(12): 1596
[21] YuanS J, PehkonenS O. Microbiologically influenced corrosion of 304 stainless steel by aerobic Pseudomonas NCIMB 2021 bacteria: AFM and XPS study [J]. Colloids and Surfaces B: Biointerfaces 2007, 59: 87
[22] ZhouE, LiH, YangC, et al. Accelerated corrosion of 2304 duplex stainless steel by marine Pseudomonas aeruginosa biofilm [J]. International Biodeterioration & Biodegradation, 2018, 127: 1
[23] XiaJ, XuD K, NanL, et al. Study on Mechanisms of Microbiologically Influenced Corrision of Metal from the Perspective of Bioelectrochemistry and Bio-energetics [J]. Chinese Journal of Materials Research, 2016, 30 (3): 161
[23] 夏 進, 徐大可, 南 黎等. 從生物能量學和生物電化學角度研究金屬微生物腐蝕的機理 [J]. 材料研究學報, 2016, 30 (3): 161)
[24] ChenG, ClaytonC R. The Influence of Sulfate-Reducing Bacteria on the Passivity of Type 317L Austenitic Stainless Steel [J]. Journal of The Electrochemical Society, 1998, 145(6): 1914
[25] LiH, ZhouE, ZhangD, et al. Microbiologically Influenced Corrosion of 2707 Hyper-Duplex Stainless Steel by Marine Pseudomonas aeruginosa Biofilm [J]. scientific reports, 2016, 6: 20190
[26] YongX Y, FengJ, ChenY L, et al. Enhancement of bioelectricity generation by cofactor manipulation in microbial fuel cell [J]. Biosens Bioelectron, 2014, 56: 19
[27] YongX Y, ShiD Y, ChenY L, et al. Enhancement of bioelectricity generation by manipulation of the electron shuttles synthesis pathway in microbial fuel cells [J]. Bioresour Technol, 2014, 152: 220
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《中國腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護網官方QQ群:140808414





