閆濤1,2 宋振綸2 Masoumeh Moradi2 楊麗景2 肖濤1,2 侯利鋒1
1. 太原理工大學材料科學與工程學院太原030024;2. 中國科學院寧波材料技術與工程研究所中國科學院海洋新材料與應用技術重點實驗室寧波315201
1 前言
金屬材料浸泡在海水中,微生物會迅速附著,并在材料表面形成一層生物膜。這層生物膜將改變材料的表面狀態及周圍微環境,如溶氧量、離子濃度和pH值等,從而影響材料的腐蝕行為。通常微生物附著會加速金屬構件的腐蝕,如厭氧的硫酸鹽還原菌(SRB),在厭氧環境下,SRB將會大量繁殖并產生黏性物質加速金屬的腐蝕。人們對此投入了大量的研究,并提出了SRB 加速腐蝕的多種機理[1,2]。近期,研究人員發現[3],部分微生物可以抑制碳鋼、鋁合金和銅合金等的腐蝕。微生物抑制金屬腐蝕的機理主要有:微生物的呼吸作用會降低金屬表面的氧濃度,從而減緩金屬的腐蝕[4];微生物分泌產物胞外聚合物與金屬離子耦合,在金屬表面形成致密的生物膜,從而抑制金屬的腐蝕[5]。此外,部分導電性固體材料表面形成的生物膜具有電活性,它們可以將培養基中的電子傳遞至材料表面,抑制腐蝕的進行[6]。同一種微生物往往可以抑制多種金屬材料的腐蝕,相對于化學緩蝕劑,微生物防腐是一種高效及綠色環保的材料保護方法,因此一些學者提出使用再生生物膜來控制腐蝕的觀點[7],并已在實驗室將Al2024、碳鋼和彈殼黃銅作為基體進行了研究。但是需要指出的是,生物膜的形成是一個復雜的生物和化學過程,其緩蝕作用往往是通過多種形式共同作用來實現的,因此在將生物膜作為抑制腐蝕性物質前,必須了解微生物抑制金屬腐蝕的機理。
本課題組[8]在前期研究階段分離出一種新的具有高度緩蝕作用的細菌,經鑒定屬于新喀里多尼亞弧菌(Vibrio neocaledonicus),它可以在碳鋼表面形成一層致密的生物膜,從而使其腐蝕速率降低60倍。為了進一步研究該微生物的緩蝕機理,本文選取Cu為研究對象,通過電化學方法和表面分析技術研究了新喀里多尼亞弧菌對Cu 在人工海水中腐蝕行為的影響,并討論了該細菌對Cu的腐蝕抑制作用機理。
2 實驗方法
2.1 實驗材料
實驗中所用材料分為純Cu 和鍍銅硅片兩種。其中,鍍銅硅片采用物理氣相沉積法(PVD) 制備,Cu 薄膜厚度為6 μm,用來觀察細菌的吸附及生物膜的形成過程。純Cu 樣品經水砂紙逐級打磨至2000#后拋光,丙酮脫脂后用蒸餾水清洗,然后在無水乙醇中超聲清洗5 min,用N2吹干備用。實驗前將樣品浸泡在無水乙醇中,紫外照射滅菌30 min。
2.2 菌種來源及培養
實驗所用菌種來源于東海海域,是一種好氧型細菌。采用Axygen 基因組DNA提取試劑盒提取純化培養獲得的細菌DNA。利用引物27F和1492R擴增16sRNA 基因序列全長,PCR 產物連接轉化測得序列全長,然后通過細菌模式種網站對比,發現該菌種與Vibrio neocaledonicus (NC470(T)) 相似度最高,達到99.72%,因此,判斷該細菌為Vibrio neocaledonicussp.。
使用修正過的2216e 培養基對細菌進行好氧富集培養。培養基成分為人工海水1 L,魚粉蛋白胨3 g,瓊脂20 g。人工海水的成分(g/L) 為:NaCl 23.476,Na2SO4 3.917,KCl 0.667,KBr 0.096,MgCl2·6H2O10.61,CaCl2·6H2O 1.469,H3BO3 0.026 和NaHCO30.192。將該菌種均勻的涂抹在滅菌后的新鮮培養基中,4 ℃保存于冰箱中備用。使用時先將細菌接種在新鮮的培養基中,放置在30 ℃恒溫培養箱中培養1 d,之后按一定比例接種到實驗溶液中,即為有菌介質。實驗溶液中不含瓊脂,其余成分與培養基一致。實驗前將實驗溶液及實驗器材用壓力蒸汽滅菌器在120 ℃下高溫滅菌15 min,冷卻后紫外照射滅菌30 min。
本實驗采用比濁法測定細菌的生長曲線,利用紫外分光光度計(Lambda 950) 測定有菌介質中的光密度(O.D.) 值來推知菌液的濃度,將所測得的O.D.值與對應的培養時間作圖,即可繪出該菌在一定條件下的生長曲線,本實驗選擇的波長為600 nm。
2.3 失重實驗
試樣分別浸泡在無菌介質和有菌介質中密封好,放置在恒溫培養箱中培養2,5 和10 d。浸泡前稱重,浸泡結束后先用去離子水沖洗,然后放在10% (質量分數) H2SO4溶液中浸泡3 min 以除掉Cu表面的腐蝕產物,酒精沖洗,吹干后稱重。
2.4 電化學測試
電化學阻抗譜和極化曲線測試在電化學工作站(PGSTAT302,Autolab) 上進行,采用三電極體系,輔助電極為Pt 電極,參比電極為飽和KCl 甘汞電極(SCE),工作電極為Cu,電極暴露面積為3.125 cm2,非工作面用環氧樹脂封裝。測試前,將Pt 電極、Cu 電極及鹽橋浸泡在無水酒精中,紫外照射滅菌30 min。電化學阻抗譜(EIS) 測試擾動電位幅值為±10 mV,測試頻率范圍為10-2~105 Hz,極化測試掃描范圍為相對開路電位±500 mV,掃描速率為2 mV/s。電化學實驗時,在300 mL細口瓶中加入150 mL滅菌的2216e 液體培養液,然后接種過夜培養的新喀里多尼亞弧菌作為有菌介質,無菌介質為滅菌的2216e 培養液,通過定期更換滅菌培養液來保持無菌環境。將Cu試樣浸泡在實驗溶液中密封好,放置在30 ℃恒溫震蕩培養箱中培養,定期進行電化學測試。
2.5 細菌的吸附及生物膜的組成分析
利用激光共聚焦顯微鏡(LeiCa TCS SP5) 觀察Cu 表面的細菌吸附情況。將浸泡在有菌介質中的Cu 片取出后,用3 mL/L 熒光染色劑SYT09 對Cu 表面進行染色處理(SYT09 可以穿透細胞壁與DNA結合發出藍色熒光),避光靜置20 min 后,用超凈水將Cu表面的染色劑沖洗掉,放置在空氣中干燥后用于激光共聚焦顯微鏡(CLSM) 觀察。
將浸泡在無菌介質中的試樣取出后,依次用濃度為50%,70%,90%和100%的乙醇脫水15min,然后用N2 吹干,表面噴金,利用掃描電子顯微鏡(SEM,Quanta FEG 250) 觀察樣品表面形貌。樣品表面元素含量可用自帶的能譜儀(EDS) 進行分析。有菌介質中浸泡的試樣,取出后先放在戊二醛中硬化2 h,然后經脫水、干燥、噴金后用于SEM觀察及EDS分析。
3 結果與討論
3.1 細菌生長曲線
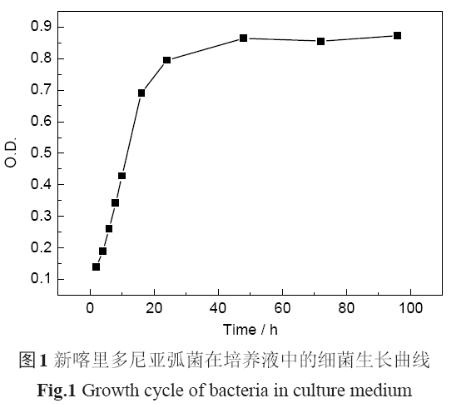
圖1 為細菌在培養液中的生長曲線。縱坐標為O.D.值,反映了溶液中細菌的數量,O.D.值越大說明細菌濃度越高。可以看出,細菌數量在前24 h 迅速增長,由于開始培養液中的營養豐富,細菌生長繁殖不受底物的限制,此時細菌處于對數生長期。24 h浸泡后,細菌數量維持在一個相對恒定的階段,處于穩定生長期,直到96 h,依然沒有進入衰落期。為了使培養液中細菌一直處于生命活躍狀態且數量大致恒定,選擇每72 h 更換1/3的培養液。
3.2 失重實驗
Cu的腐蝕速率按下式計算:
V = (W -W0)/ST(1)
其中,V 為腐蝕速率(g/(m2·h));W0為試樣浸泡前的質量(g);W為浸泡后的質量(g);S 為試樣面積(m2);T 為浸泡時間(h)。此外,可以用生物膜保護效率η來表征細菌的緩蝕作用:
η = Vbacteria/Vsterile(2)
式中,Vbacteria為試樣浸泡在有菌介質中的腐蝕速率,Vsterile為試樣浸泡在無菌介質中的腐蝕速率。η<1,表明微生物會抑制材料的腐蝕;η>1,表明此時微生物會促進腐蝕[9]。Cu浸泡在有菌介質和無菌介質中的失重數據見表1。
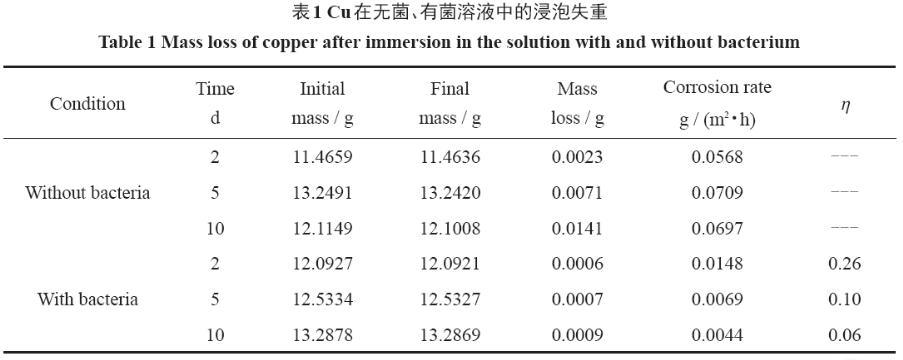
由表1 可知,在無菌環境中,Cu的腐蝕速率隨浸泡時間延長而增大,原因是在溶液中有害離子的侵蝕下,Cu 表面初始形成的鈍化膜逐漸被破壞,使Cu的腐蝕速率變大。在有菌介質中,浸泡2,5 和10 d后,η<1,說明微生物對基體具有保護作用。同時還發現,在有菌介質中,Cu在浸泡前后質量變化不大,說明在細菌的保護作用下,Cu表面幾乎沒有腐蝕。
3.3 電化學測試
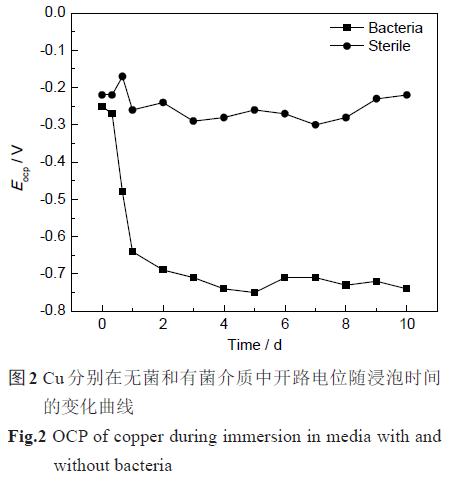
3.3.1 開路電位 Cu 電極在無菌介質和有菌介質中開路電位隨時間的變化曲線如圖2 所示。可見,在無菌介質中,Cu 的開路電位變化較為平穩。在有菌介質中,經過短暫的平穩期,Cu 的開路電位即發生了較大程度的負移,浸泡1 d 后負移390 mV;在浸泡后期,穩定在-0.7 V附近。Cu 電極開路電位的負移是因為微生物的吸附和新陳代謝活動改變了Cu表面的電化學性質。吸附在Cu表面的細菌通過呼吸作用消耗金屬表面的溶解氧,從而導致Cu的開路電路負移[10],1 d 后,Cu表面吸附的細菌數量飽和,使Cu的開路電位穩定在約-0.7 V。
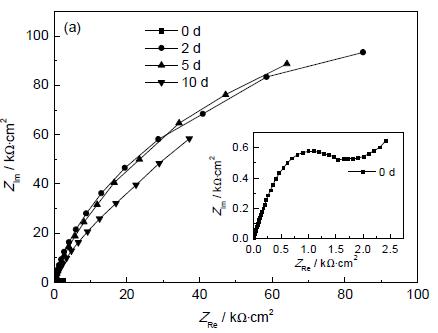
3.3.2 電化學阻抗譜 圖3 和4 分別為Cu 在有/無菌介質中的EIS 測試結果。從圖3a 中可看出,在有菌介質中,Cu從浸泡開始到第5 d,其容抗弧直徑急劇增大;浸泡至第10 d,Cu 的容抗弧直徑有所降低,但仍遠大于浸泡初始(0 d) 的容抗弧直徑。從Bode 圖中可以看出,Cu 從浸泡開始,其低頻區的阻抗模值|Z |及相位角急劇增大,到第5 d,達到最大值,之后略有降低。在無菌介質中,Cu 的容抗弧直徑、低頻區的阻抗模值|Z |及其相位角在浸泡初期均緩慢增大,之后有所降低。
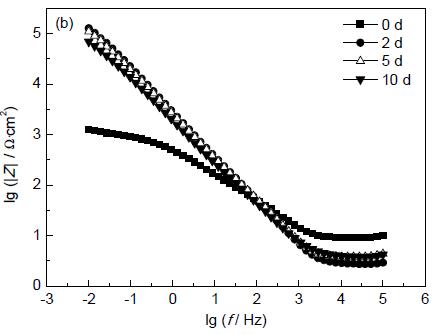
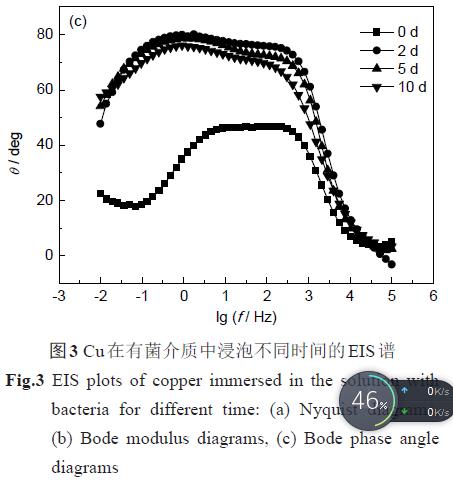
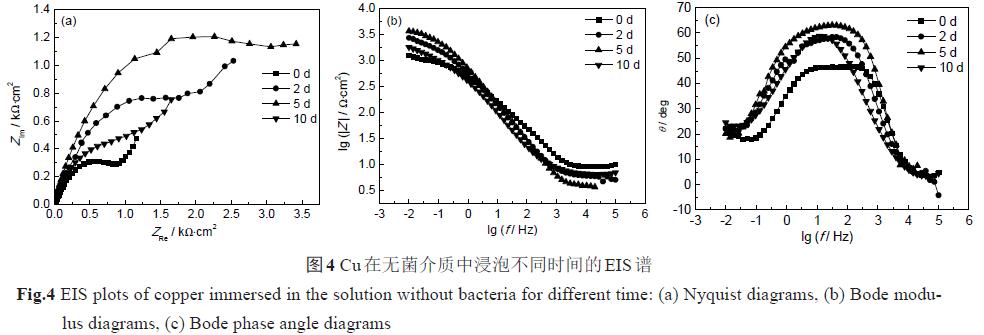
根據Cu電極的EIS 特征,選擇圖5a 所示等效電路對Cu 電極在浸泡前及浸泡在無菌介質中的EIS進行擬合,選擇圖5b 對Cu浸泡在有菌介質中的EIS進行擬合。其中,Rs表示溶液電阻,Qdl為電極表面雙電層電容,Rct表示電極表面電荷傳遞電阻,Rf為電極表面的膜電阻,Qf為電極表面膜電容。各參數擬合結果列于表2 中,其中,Y01為膜電容,Y02為雙電層電容。
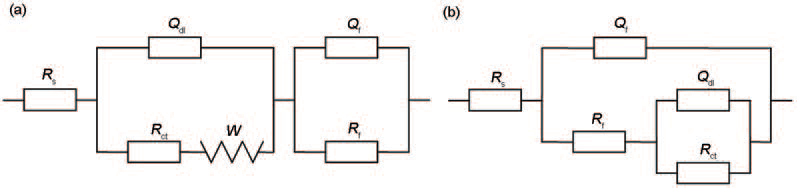
圖5 Cu在浸泡前和浸泡在無菌介質中及浸泡在有菌溶液中的等效電路圖
Fig.5 Equivalent circuit models of copper immersed in the solutions without (a) and with (b) bacteria
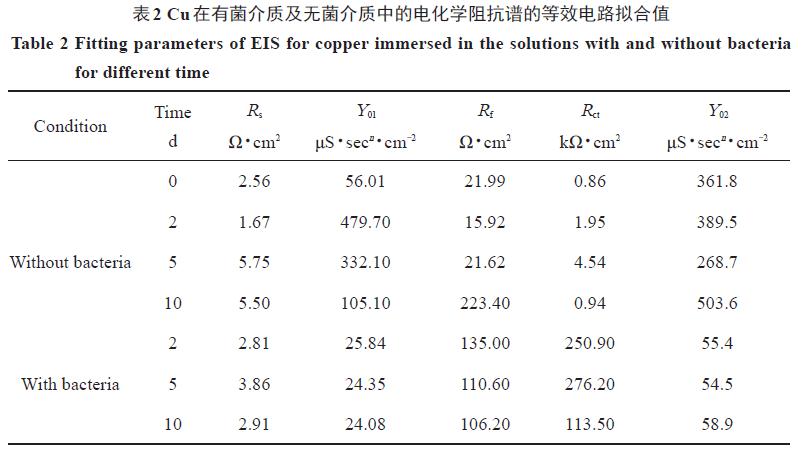
從表2 可以看出來,Cu試樣浸泡在無菌介質中,其Rct 隨浸泡時間的延長而緩慢增大,最后有所降低。這說明在浸泡初期,Cu表面初始形成的鈍化膜具有一定的保護作用,減緩了Cu 的腐蝕;在浸泡后期,由于有害離子的侵蝕,鈍化膜逐漸被破壞,其保護作用消失,Cu 的腐蝕速率變大。在有菌介質中,Cu電極從浸泡開始到第5 d,其Rct由初始的0.86 kΩ·cm2增大到第5 d的276.2 kΩ·cm2,約為初始值的321倍;到第10 d,Rct降低為117 kΩ·cm2,但依然遠大于初始值,且遠大于同期下Cu在無菌介質中的表面電荷傳遞電阻,說明該細菌可以強烈抑制Cu 的腐蝕,并且這種抑制作用經歷了一個先增強后減弱的過程。
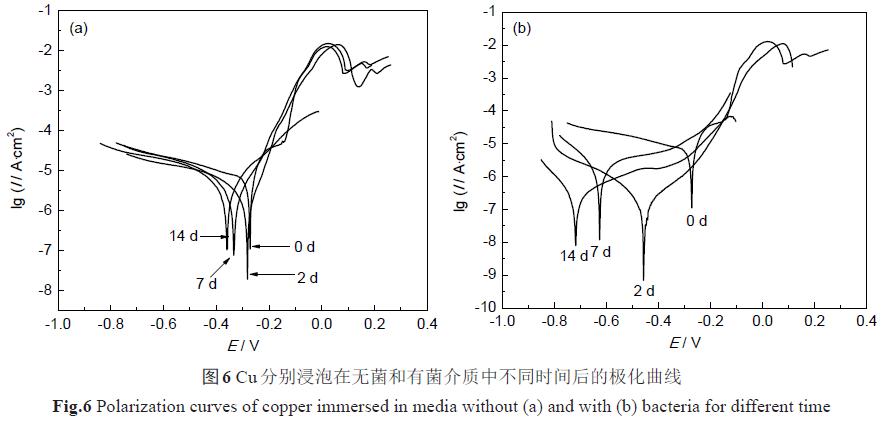
3.3.3 動電位極化曲線測試 圖6 是Cu 浸泡在無菌和有菌介質中不同時間后的動電位極化曲線。在無菌介質中,Cu 的腐蝕電流密度變化不大,在浸泡后期,自腐蝕電位負移,說明Cu 的耐蝕性變差。Cu 在有菌介質中浸泡過程中,浸泡初期,其腐蝕電流密度迅速降低,在第2 d 達到最小值;隨著浸泡時間的延長,Cu的腐蝕電流密度開始上升,但是,實驗結束時Cu 的腐蝕電流密度仍然小于同期下浸泡在無菌介質中的,說明新喀里多尼亞弧菌能抑制Cu 的腐蝕。這一結果與EIS 結果一致。同時還發現,細菌的加入會使Cu 的自腐蝕電位降低,說明細菌的加入抑制了陰極反應的進行[11]。
3.4 細菌的吸附及生物膜的形成
3.4.1 細菌的吸附 圖7 為Cu 浸泡在有菌介質中1 和10 d 后的激光共聚焦顯微鏡圖片。從圖7a中可以看出,在有菌介質中浸泡1 d 后,Cu表面已基本覆滿細菌,這會使Cu 的開路電位明顯負移、阻抗值迅速增大,腐蝕電流密度明顯降低。10 d 后,Cu表面吸附的細菌已經聚集并形成菌落。

圖7 純Cu試樣浸泡在有菌介質中1 和10 d 后的CLSM圖
Fig.7 CLSM images of copper immersed in the solution with bacteria for 1 d (a) and 10 d (b)
3.4.2 表面形貌分析 圖8 所示為Cu 分別在無菌介質(圖8a) 和有菌介質(圖8b) 中浸泡10 d 后的SEM像。可以看出,在無菌介質中,由于溶液中存在高濃度的有害離子,如Cl-和SO42-等,Cu腐蝕非常嚴重。在有菌介質中,Cu表面可見吸附的細菌及生物膜,并未見明顯的腐蝕產物,Cu 表面狀態變化不大,這一結果與失重實驗結果一致。但是需要指出的是,Cu表面生物膜較少,而CLSM結果顯示,Cu表面幾乎被細菌所覆蓋,這說明,Cu 表面吸附的細菌難以形成生物膜。原因可能是細菌與Cu 的吸附僅為可逆吸附,Cu表面的細菌處于吸附與脫附的動態平衡中,并不易形成生物膜。

圖8 純Cu試樣分別浸泡在有菌介質和無菌介質中10 d后的SEM像
Fig.8 SEM images of copper after immersion in the solutions without (a) and with (b) bacteria for 10 d
3.4.3 生物膜的形成 圖9 為鍍銅硅片浸泡在有菌介質中不同時間后的SEM像。表3 是鍍銅硅片分別在有菌和無菌介質中浸泡不同時間后的EDS結果。從圖9a 中可以看出,鍍銅硅片浸泡在有菌介質中后,細菌會附著到銅鍍層缺陷處,原因是Cu 表面缺陷處容易腐蝕,易產生氫鍵,在van der waals力、靜電作用力及氫鍵作用下,細菌傾向于吸附在Cu表面缺陷處。隨著浸泡時間的延長,細菌胞外產物(EPS) 會黏附在Cu 表面[12]并形成一層由EPS、細菌及腐蝕產物組成的生物膜。從表3 中可知,相對于無菌環境,在有菌介質中浸泡后的Cu表面氧含量降低,說明細菌會減緩Cu 的腐蝕。同時還發現,在有菌環境下,Cu表面出現P,N和S 等元素,說明這3種元素均是生物源元素。在浸泡1 d 后,Cu 表面出現P,而此時Cu 表面吸附有大量的細菌,表明細菌中P 含量較高;在浸泡5d 后,Cu表面P 含量降低,說明生物膜中細菌數量減少,細菌從生物膜中脫附出去。從圖9c 可以看出,細菌的脫附使金屬表面生物膜變得不均勻,金屬表面Cl-含量也增加,這些都會減弱微生物的緩蝕作用。

圖9 鍍銅硅片浸泡在有菌介質中不同時間的SEM像
Fig.9 SEM images of the Cu deposited Si wafer after immersion in the solution with bacteria for 1 d (a), 2 d (b) and 5 d (c)
3.5 新喀里多尼亞弧菌對Cu的腐蝕抑制機理
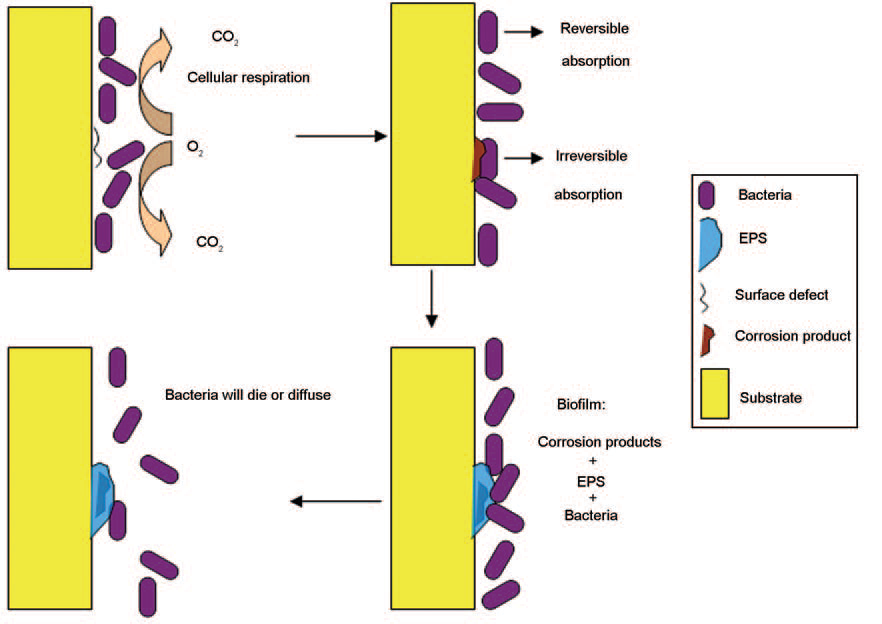
圖10 細菌在Cu表面附著及生物膜的形成機理
Fig.10 Schematic illustrations of bacterial adhesion and biofilm formation on copper
如圖10 中的模型所示,在浸泡初期,細菌大量吸附在Cu 的表面,這些細菌一方面會消耗Cu 表面溶解氧,另一方面作為阻礙層阻礙有害離子如Cl-向金屬表面擴散,從而抑制Cu的腐蝕。由于受到細菌的保護,Cu表面溶解較為緩慢,幾乎沒有腐蝕,因而缺乏足夠的活性中心,此時細菌的吸附多為可逆吸附[13],EPS 因為缺乏足夠的配位離子而不會黏附在Cu 的表面。隨著浸泡時間的增加,Cu 表面某些缺陷處被優先腐蝕,細菌及其分泌產物EPS 便會牢固吸附至腐蝕產物的表面,并進一步形成生物膜。在浸泡后期,Cu 表面氧含量降低,細菌會向氧含量較高的溶液中擴散,導致Cu 表面細菌吸附量減少,細菌的保護作用較弱。同時,由于Cu表面的生物膜并不均勻致密,容易形成氧濃差電池,這些將會降低細菌的緩蝕作用。
4 結論
(1) 新喀里多尼亞弧菌可以抑制Cu在人工海水中的腐蝕。在浸泡初期,細菌大量吸附至Cu 的表面,對基體起保護作用,從而抑制Cu的腐蝕。
(2) 隨著浸泡時間的延長,Cu 表面的細菌逐漸向溶液中擴散,細菌的保護作用減弱,同時不均勻的生物膜會產生氧濃差電池,這些都會降低新喀里多尼亞弧菌的緩蝕作用。
參考文獻
[1] Booth G H, Tiller A k. Cathodic characteristics of mild steel in suspensionsof sulphate- reducing bacteria [J]. Corros. Sci., 1968, 8:583
[2] Antony P, Chongdar S, Kumar P, et al. Corrosion of 2205 duplexstainless steel in chloride medium containing sulfate-reducing bacteria[J]. Electrochim. Acta, 2007, 52(12): 3985
[3] Nagiub A, Mansfeld F. Evaluation of microbiological influencedcorrosion inhibition using electrochemical noise analysis [J]. Corros.Sci., 2001, 43: 2001
[4] Jayaraman A, Cheng E T, Earthman J C, et al. Axenic aerobic biofilmsinhibit corrosion of SAE 1018 steel through oxygen depletion[J]. Appl. Microbiol. Biotechnol., 1997, 48: 11
[5] Masoumeh M. Effect of marine Pseudoalteromonas sp. on the microstructureand corrosion behavior of 2205 duplex stainless steel[J]. Corros. Sci., 2014, 84: 103
[6] Benjamin E, Narcis M D, Ghangrekar M M, et al. Application ofelectro-active biofilms [J]. Biofouling, 2010, 26(1): 57
[7] Jackson G, Beyenal H, Rces W M, et al. Growing reproducible biofilmswith respect to structure and viable cell counts [J]. J. Microbiol.Methods, 2001, 47: 1
[8] Masoumeh M. Introducing a novel bacterium, Vibrio neocaledonicussp., with the hignest corrosion inhibition efficiency [J]. Electrochem.Commun., 2015, 51: 64
[9] Liu H F, Xu L M, Zheng J S. Effect of biofilm on corrosion of carbonsteel [J]. J. Chin. Soc. Corros. Prot., 2000, 20(1): 41(劉宏芳, 許立銘, 鄭家燊。 SRB 生物膜與碳鋼腐蝕的關系[J]. 中國腐蝕與防護學報, 2000, 20(1): 41)
[10] Potekhina J S. Role of microorganisms in corrosion inhibition ofmetals in aquatic habitats [J]. Appl. Micriol. Biotechnol., 1999,52: 639
[11] Du X Q, Duan J Z, Hou B R. Corrosion behavior of 316L stainlesssteel influenced by iron- reducing bacteria shewanella algae biofilms[J]. J. Chin. Soc. Corros. Prot., 2013, 33(5): 363(杜向前, 段繼周, 侯寶榮。 鐵還原細菌Shewanella algae 生物膜對316L不銹鋼腐蝕行為的影響[J]. 中國腐蝕與防護學報, 2013,33(5): 363)
[12] Kumari K. Characterisation and anti-biofilm activity of extracellularpolymeric substances from oceanobacillus iheyensis [J]. Carbohydr.Polym., 2014, 101: 29
[13] Valcaece M B. The influence of the surface condition on the adhensionof pseudomonas fluorescens (ATCC 17552) to copper and aluminiumbrass [J]. Int. Biodeterior. Biodegrad., 2002, 50: 61
責任編輯:王元
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《中國腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62313558-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護網官方QQ群:140808414





