陰極保護(hù)與防腐蝕涂層聯(lián)合使用,是目前公認(rèn)的對埋地或浸沒金屬結(jié)構(gòu)物進(jìn)行腐蝕防護(hù)的有效手段。早在1823年,英國化學(xué)家戴維受海軍部委托,著手研究銅皮包覆的木船在海洋中的防腐蝕問題。他經(jīng)過長期試驗發(fā)現(xiàn)銅和鋅或銅和鐵的接觸可以使銅得到保護(hù)。1824年,戴維在船體上進(jìn)行了實用性試驗,用鐵作為陽極,面積為銅皮總面積的1/80,取得良好的保護(hù)效果。他在1826年的報告中提出:當(dāng)浸沒在液體中的不同金屬用導(dǎo)線連接成回路時,一種金屬的腐蝕受到促進(jìn),而另一種金屬的腐蝕會受到抑制,這就是銅船通過連接鐵或鋅而受到保護(hù)的原因。
戴維的研究結(jié)論被后世視為最早的陰極保護(hù)理論。雖然戴維早在1823年就發(fā)現(xiàn)了活潑金屬可以對不活潑金屬起到陰極保護(hù)的作用,但是陰極保護(hù)的作用機(jī)理在此后很長一段時間內(nèi)都沒有發(fā)展和確立。即便是現(xiàn)在,陰極保護(hù)的作用機(jī)理仍處于爭論狀態(tài)。
陰極保護(hù)機(jī)理
部分陰極保護(hù)標(biāo)準(zhǔn)中給出了陰極保護(hù)的定義:
NACE SP0169-2013規(guī)定:
陰極保護(hù)的定義是:通過使金屬表面成為電化學(xué)電池的陰極來減少金屬表面腐蝕的一種技術(shù)。
ISO 8044-2020規(guī)定:
陰極保護(hù)的定義是:通過降低電極電位使金屬的腐蝕速率顯著降低的電化學(xué)保護(hù)方法。
以上兩個定義都未涉及到陰極保護(hù)機(jī)理。但通常認(rèn)為,在施加陰極保護(hù)之前腐蝕結(jié)構(gòu)同時具有陰極和陽極,陰極是發(fā)生還原反應(yīng)的電極,陽極是發(fā)生氧化反應(yīng)即腐蝕的電極。因此,如果所有的陽極區(qū)域都能轉(zhuǎn)化為陰極區(qū)域,那么整個結(jié)構(gòu)就會變成陰極,腐蝕就會消除。
目前最為流行的陰極保護(hù)機(jī)理是MEARS和BROWN以及HOAR分別提出的經(jīng)典陰極保護(hù)機(jī)理即陽極溶解減緩機(jī)理;除此之外,陰極保護(hù)機(jī)理還有基于熱力學(xué)的免蝕機(jī)理和鈍化機(jī)理。
1 陽極溶解減緩機(jī)理
在早期對陰極保護(hù)的防腐蝕作用的多種闡釋中,HOAR利用局部腐蝕電池的概念對陰極保護(hù)機(jī)理進(jìn)行了解釋,他提出陰極保護(hù)的機(jī)理應(yīng)該是陽極溶解的受阻,而不是亞鐵離子的再沉積;M?LLER提出當(dāng)陰極的電位極化至與陽極電位一致時,腐蝕將停止,這里陽極電位的定義是陽極金屬的平衡電極電位。
在同一時期,MEARS和BROWN以及HOAR等都嘗試使用電偶對來描述、驗證陰極保護(hù)的機(jī)理。MEARS和BROWN在1938年發(fā)表的文章中提出:當(dāng)腐蝕類型屬于完全的電化學(xué)腐蝕時,有必要將腐蝕電池的陰極電位極化至陽極的開路電位,以獲得完全的陰極保護(hù)。
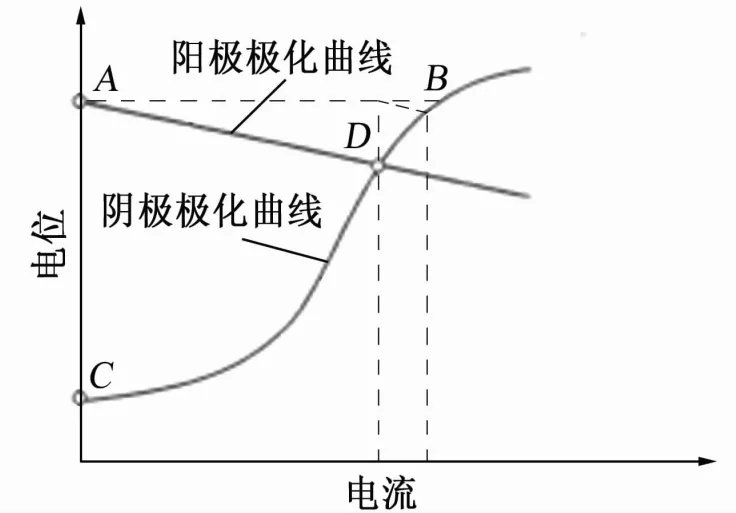
基于腐蝕電化學(xué)理論,MEARS和BROWN認(rèn)為金屬表面的不均勻性以及腐蝕介質(zhì)的差異等原因會造成金屬表面不同位置之間存在電位差,從而產(chǎn)生腐蝕電流。金屬表面電位較正的陰極極化曲線和電位較負(fù)的陽極極化曲線相交,如圖1所示。如果忽略IR降,則兩條曲線交叉點(diǎn)(D點(diǎn))所對應(yīng)的橫坐標(biāo)數(shù)值即為腐蝕電流。在該腐蝕電池中,陽極極化和陰極極化都是由腐蝕電流引起的。如果使用外部直流電源給該腐蝕電池提供電流,將陰極電位極化到陽極電位(B點(diǎn)),此時整個金屬表面處于等電位狀態(tài),不存在釋放腐蝕電流的陽極。如果腐蝕屬于完全的電化學(xué)腐蝕且陰極周邊的產(chǎn)物不會導(dǎo)致腐蝕,就可實現(xiàn)100%的有效保護(hù)。
圖1 陰極極化曲線和陽極極化曲線示意
為了驗證所提出的陽極溶解減緩機(jī)理,MEARS和BROWN設(shè)計了電偶對試驗裝置。在該裝置中,銅電極作為腐蝕電池的陰極,鋅電極作為腐蝕電池的陽極,鉑電極作為外加電流陰極保護(hù)的輔助陽極。試驗電解質(zhì)為質(zhì)量分?jǐn)?shù)為20%的NaCl溶液。用兩個毫安表分別測量陰極與陽極之間的電流以及外部直流電源的輸出電流。測試中使用甘汞電極測量陰極和陽極的混合電位,使用電壓表直接測量陰極與陽極之間的電位差。在外部直流電源回路中安裝有可調(diào)電阻,通過調(diào)整可調(diào)電阻的電阻值來調(diào)整陰極保護(hù)電流。開關(guān)S1用于控制陰極(銅)與陽極(鋅)之間的導(dǎo)通與隔斷。
在S1閉合的情況下,隨著外部陰極保護(hù)電流逐步增大,陰極與陽極之間的電流(腐蝕電流)逐步減小至零;當(dāng)腐蝕電流減少至零時,陰極的電位為-1.1687V,陽極的電位為-1.1689V,電位差接近于零。試驗結(jié)果很好地驗證了MEARS和BROWN提出的陽極溶解減緩機(jī)理,即當(dāng)腐蝕電流降至零時,陰極的電位應(yīng)降至陽極的開路電位。
在試驗中,銅電極作為外加電流保護(hù)系統(tǒng)的陰極,調(diào)整可調(diào)電阻的阻值,得到不同的陰極電位。每調(diào)整一次阻值后,都相應(yīng)的臨時閉合S1測量陰極和陽極間的電流,在臨時閉合S1 后,使用甘汞電極測量兩種金屬的混合電位。當(dāng)陰極電位被極化到陽極的開路電位時,閉合S1,陰極和陽極之間的腐蝕電流為零。可見,當(dāng)陰極(銅)被極化到陽極(鋅)的開路電位后,與銅的連接不會對鋅造成電化學(xué)腐蝕。
2 基于熱力學(xué)的免蝕機(jī)理
陰極保護(hù)的熱力學(xué)免蝕機(jī)理是指將結(jié)構(gòu)物極化到在特定環(huán)境中的熱力學(xué)穩(wěn)定電位,即Pourbaix(電位-pH)圖中的免蝕區(qū)。
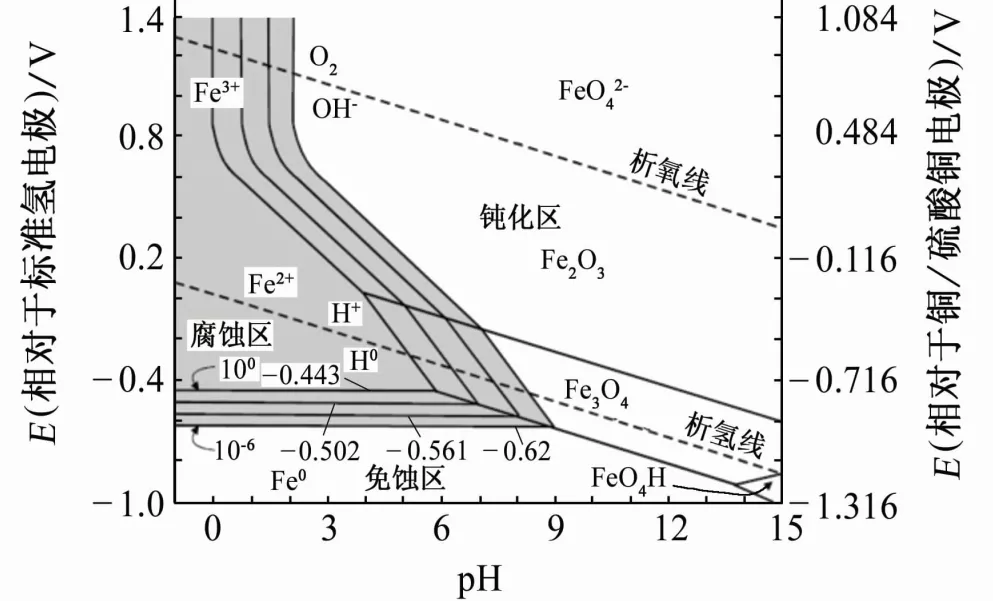
基于熱力學(xué)數(shù)據(jù)所繪制的鐵-水體系的Pourbaix圖中存在腐蝕區(qū)、免蝕區(qū)和鈍化區(qū)3種區(qū)域,如圖2所示。在免蝕區(qū)內(nèi),電位和pH的變化不會引起金屬腐蝕,即在熱力學(xué)上金屬處于穩(wěn)定狀態(tài)。陰極保護(hù)的理論保護(hù)電位即為金屬進(jìn)入免蝕區(qū)的臨界電位。
圖2 鐵-水體系的Pourbaix圖
根據(jù)Pourbaix圖,理論保護(hù)電位與介質(zhì)pH有密切的關(guān)系。從熱力學(xué)的角度來看,只要鐵電極的電位比上述電位值更負(fù)就不會發(fā)生腐蝕。比如,pH小于9時,只要鐵電極的電位負(fù)于-0.620V(相對于標(biāo)準(zhǔn)氫電極),鐵就不會發(fā)生腐蝕。由此基于熱力學(xué)免蝕概念確定了陰極保護(hù)的作用機(jī)理。
3 基于熱力學(xué)的鈍化機(jī)理
1). 陰極極化造成pH增大及表面堿性化
KUHN在1928年的文章中介紹了他在埋地鑄鐵管道上應(yīng)用陰極保護(hù)的開創(chuàng)性工作,他在文中提出電流可能流入陰極區(qū)形成氫氧化物膜從而保護(hù)這些區(qū)域免于腐蝕。EVANS也基于試驗提出,陰極保護(hù)的有效性是通過表面鈍化實現(xiàn)的。
當(dāng)對結(jié)構(gòu)物施加陰極保護(hù)電流時,在結(jié)構(gòu)物與電解質(zhì)的界面發(fā)生陰極反應(yīng),常見的陰極反應(yīng)包括:
H++ e- → Ho
2H2O + O2 + 4e- → 4OH-
2H2O + 2e- → H2 +2OH-
上述所有陰極反應(yīng)都令反應(yīng)界面的pH上升,呈現(xiàn)堿性。
BARLO等研究了在充氣、充氧和除氣條件下,界面pH對鋼鐵腐蝕速率的影響。結(jié)果表明:在除氣條件下,當(dāng)鋼表面的pH從8上升到9.3時,腐蝕速率降低到0.0254mm/a以下;在充氣條件下,當(dāng)pH上升到10時,腐蝕速率降低到0.0254mm/a以下;在充氧條件下,當(dāng)pH上升到10.7時,腐蝕速率降低到0.0254mm/a以下。這表明界面的堿性化可以有效抑制腐蝕。
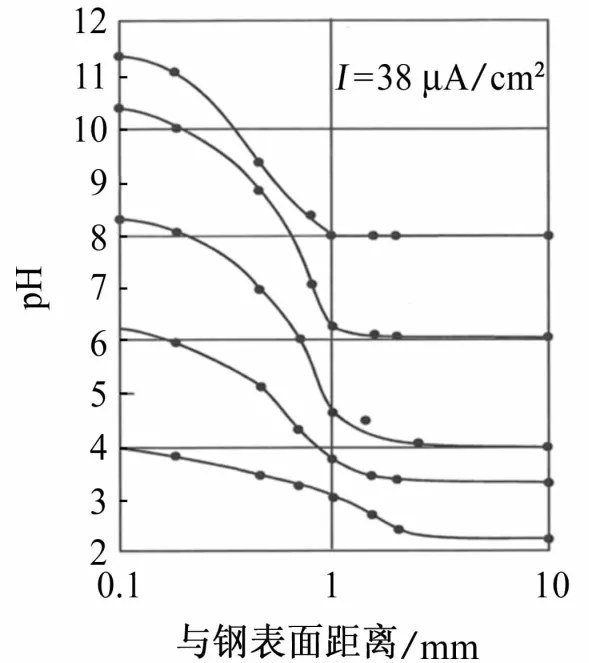
由陰極極化造成的pH上升現(xiàn)象在結(jié)構(gòu)物與電解質(zhì)的界面處最明顯,在遠(yuǎn)離界面方向,pH逐漸恢復(fù)至電解質(zhì)本體水平。圖3為在不同本體pH環(huán)境中對結(jié)構(gòu)物施加密度為38μA/cm2的陰極極化電流時界面附近pH的梯度分布。測試結(jié)果表明,在距離界面1mm處,pH基本降低到電解質(zhì)本體pH水平。
圖3 結(jié)構(gòu)與電解質(zhì)界面處pH的梯度分布
諸多研究表明鋼材表面堿性化能有效減緩腐蝕,但陰極保護(hù)有效性的鈍化機(jī)理一直未得到廣泛的認(rèn)可。
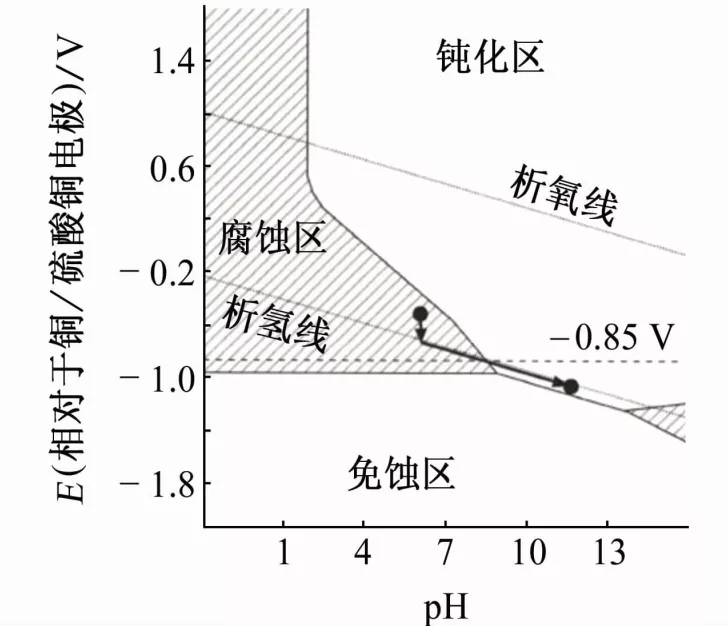
當(dāng)對鋼材施加陰極極化電流時,如果鋼的電位已經(jīng)達(dá)到了析氫電位,很難再將鋼電位極化到比析氫電位更負(fù)的程度,鋼的極化電位與析氫電位基本一致。此時繼續(xù)增大陰極極化電流密度,電位將繼續(xù)變負(fù)而pH繼續(xù)增大,且鋼表面電位與pH近似存在線性關(guān)系,如圖4所示,電位就是pH的間接指示,隨著陰極電流密度增大,鋼的狀態(tài)從腐蝕區(qū)逐漸轉(zhuǎn)入鈍化區(qū)。
圖4 鋼表面pH與電位的線性關(guān)系
在上文關(guān)于免蝕機(jī)理的討論中提到,只要鐵的電位處于免蝕區(qū),就能達(dá)到陰極保護(hù)的要求。但在實踐中,通常使用正于免蝕電位的陰極保護(hù)準(zhǔn)則就可以達(dá)到有效的保護(hù)。事實上當(dāng)陰極電位極化到析氫電位時,較難將電位再繼續(xù)極化到更負(fù)水平而進(jìn)入免蝕區(qū)。此時反應(yīng)界面的氧已經(jīng)基本消耗殆盡,腐蝕速率顯著降低。當(dāng)pH大于9時,鐵進(jìn)入鈍化區(qū)(電流密度非常大時才可能進(jìn)入免蝕區(qū)),不再有腐蝕的風(fēng)險,對應(yīng)的析氫平衡電位為-847mV(相對于銅/硫酸銅電極),這個電位與諸多標(biāo)準(zhǔn)中的極化電位準(zhǔn)則吻合。
2). LEEDS的研究介紹
LEEDS等研究了低碳鋼在三種不同溶液(3.5%鹽水pH7、人造海水pH7.5、堿性溶液pH10)中的極化和表面鈍化現(xiàn)象。在試驗中,以恒電位模式對試樣施加陰極電流,電位控制區(qū)間為-1.40~-0.65V(相對于Ag/AgCl電極,電極內(nèi)溶液為3.5%NaCl)。
結(jié)果表明,在以恒電位模式施加陰極極化電流后,所有試樣的電流密度都出現(xiàn)了顯著下降。在試驗開始的第3天,所有試樣的表面都出現(xiàn)了膜/沉積物,膜/沉積物的成分取決于pH及電位。在3.5%鹽水溶液中,試樣表面沒有鈣質(zhì)沉積物,當(dāng)極化至-1.3~-1.4V時,表面的氧化物膜最完整,這些試樣的腐蝕速率最低,膜的主要成分是磁性氧化鐵和少量氫氧化亞鐵。通常磁性氧化鐵具有良好的導(dǎo)電性,但是氫氧化亞鐵會使磁性氧化鐵膜失去導(dǎo)電性,從而降低維持陰極保護(hù)所需的電流密度。在堿性溶液中的試樣表面出現(xiàn)一層黑色的膜,但因厚度太小無法進(jìn)行XRD分析。該層黑色的膜上覆蓋著鈣質(zhì)沉積物。溶液中的鈣和鎂限制了鐵氧化物的形成,所以氧化物膜的厚度很小。在試驗中,電流密度持續(xù)降低,這意味著有一層“絕緣防腐蝕層”逐漸覆蓋了鋼鐵表面。在人造海水中,試樣表面覆蓋了鈣質(zhì)沉積物,沒有發(fā)現(xiàn)氧化物膜。
綜上,LEEDS認(rèn)為施加陰極保護(hù)可以使鋼表面出現(xiàn)鐵氧化物膜或鈣質(zhì)沉積物,它們可以和防腐蝕層一樣,起到良好的防腐蝕作用,且膜/沉積物的組成成分取決于界面的pH和極化電位等因素。
基于試驗所總結(jié)出的陰極保護(hù)電位準(zhǔn)則:對于陸地應(yīng)用,保護(hù)電位范圍為-0.90~-1.1V(相對于銅/硫酸銅電極),pH為7~13;對于海洋應(yīng)用,保護(hù)電位范圍為-0.95~-1.1V(相對于銅/硫酸銅電極),pH 范圍7~11。
3). BUCHLER的研究介紹
在BUCHLER等的研究工作中,基于界面是否可以積聚氫氧根離子(pH是否可以升高)提出了兩種陰極保護(hù)準(zhǔn)則。
(1)氫氧根離子可以在鋼表面積聚
在沒有硫酸鹽還原菌、流動水或其他阻礙陰極保護(hù)令pH升高的環(huán)境中,可以使用較正的保護(hù)電位。在金屬/溶液界面可以積聚氫氧根離子,有利于濃差極化和表面鈍化。在這種情況下推薦斷電電位準(zhǔn)則:瞬間斷電電位至少達(dá)到-850mV(相對于銅/硫酸銅電極)。在良好敷設(shè)情況下,所測試的斷電電位不是Fe/Fe(II)電極電位,而是氫電極的平衡電極電位,-850mV(相對于銅/硫酸銅電極)對應(yīng)的pH為9,只要pH大于9,防腐蝕層上所有破損點(diǎn)都會得到有效保護(hù)。
(2)不確定氫氧根離子是否可以在鋼表面積聚
如果防腐蝕層破損點(diǎn)周邊有硫酸鹽還原菌、流動水或其他阻礙陰極保護(hù)令pH上升的條件存在,比-850mV(相對于銅/硫酸銅電極)更負(fù)的電位未必能消除腐蝕。此時建議使用-950 mV(相對于銅/硫酸銅電極)的保護(hù)電位準(zhǔn)則。
討論
1 對陽極溶解減緩機(jī)理的討論
MEARS和BROWN以及HOAR差不多在相同的時間提出了類似的陽極溶解減緩機(jī)理,即將陰極電位極化到陽極的開路電位,消除金屬表面的電位差,從而使陽極不再腐蝕溶解。在他們的驗證實驗中,使用銅和鋅分別模擬陰極和陽極,將陰極極化到陽極的開路電位,就消除了陰極與陽極之間的電位差。雖然這種方法可以形象地展示由陰、陽極電位差變小帶來的腐蝕電流降低效應(yīng)。但是該理論存在瑕疵,其中的“開路電位”是指金屬的自腐蝕電位,不是平衡電極電位,所以“陽極”還是處于自腐蝕狀態(tài)。
從消除電位差、降低陽極腐蝕的角度來看,使用混合電位理論可以更準(zhǔn)確地描述陰極保護(hù)的機(jī)理。將結(jié)構(gòu)物從其自腐蝕電位極化到陽極的平衡電極電位,就完全消除了腐蝕。
陰極保護(hù)機(jī)理與熱力學(xué)免蝕機(jī)理在某種程度上是一致的。如果陽極溶解減緩機(jī)理中的“開路電位”即平衡電極電位對應(yīng)的亞鐵離子活度為10-6mol/L,那么這個“開路電位”與Pourbaix中的免蝕電位就是相同的(pH小于9時)。
2 對熱力學(xué)鈍化機(jī)理的討論
在有陰極保護(hù)管道的防腐蝕層破損點(diǎn)或鼓包處經(jīng)常可以觀察到黑色的覆蓋膜。這種膜顯然與管道表面pH升高有關(guān),但是它的產(chǎn)生機(jī)理有待研究和澄清,它可能是由陰極保護(hù)單獨(dú)作用產(chǎn)生的,或外部其他因素與陰極保護(hù)共同作用產(chǎn)生的。
陰極保護(hù)產(chǎn)生的高pH環(huán)境可促進(jìn)鋼表面氧化物鈍化膜的形成,但這并不是唯一影響因素,土壤溶液成分、含氧量、硫酸鹽還原菌、外部交直流干擾、鈣鎂沉積物等因素都可能對鈍化膜的形成產(chǎn)生影響。
鋼結(jié)構(gòu)物表面在陰極保護(hù)狀態(tài)下產(chǎn)生鈍化膜的理論一直受到質(zhì)疑。業(yè)界中較普遍的看法是發(fā)生陰極反應(yīng)的碳鋼/溶液界面具有很強(qiáng)的還原性,不具備形成鈍化膜的條件。
業(yè)界尚需對埋地管道表面膜的形成機(jī)理進(jìn)行更深入的研究。明確破損點(diǎn)表面氧化物膜的生成機(jī)理,對交流干擾、動態(tài)直流干擾的防護(hù)工作具有重大意義。
結(jié)論
MEARS和BROWN的陽極溶解減緩機(jī)理可以形象地展示腐蝕電池中電壓差減小帶來的腐蝕電流降低效應(yīng),但該機(jī)理在描述上有瑕疵。基于消除腐蝕電池的原理,陽極溶解減緩機(jī)理更準(zhǔn)確的描述是:陰極保護(hù)將腐蝕電池中的陰極電位極化到陽極的平衡電極電位從而消除了腐蝕。
在施加陰極保護(hù)后,隨著時間的推移,外加電流密度也顯著降低,特別是在應(yīng)用陰極保護(hù)的初始階段,這被認(rèn)為是表面膜或鈣質(zhì)沉積物形成導(dǎo)致的效應(yīng)。陰極保護(hù)帶來的界面堿性化是發(fā)生上述變化的起因之一。
陰極保護(hù)鈍化理論受到廣泛的質(zhì)疑,發(fā)生陰極反應(yīng)的碳鋼/溶液界面具有很強(qiáng)的還原性,不具備形成鈍化膜的條件。碳鋼表面發(fā)生陰極極化時,表面產(chǎn)物膜的形成機(jī)理仍需進(jìn)一步研究。
陰極保護(hù)能緩解腐蝕可能是多種因素共同作用的結(jié)果,包括且不僅限于:腐蝕電池中的陰極得到極化,令腐蝕電池中的電位差降低從而降低了腐蝕速率;界面的溶解氧被陰極反應(yīng)消耗;氯離子等有害陰離子被驅(qū)離界面;施加陰極電流后界面呈現(xiàn)堿性,所形成的氧化物膜或鈣質(zhì)沉積物起到良好的屏蔽作用,減小了氧還原反應(yīng)的極限電流密度。
無論是陽極溶解減緩機(jī)理、免蝕機(jī)理還是鈍化機(jī)理,各種機(jī)理所對應(yīng)的保護(hù)電位準(zhǔn)則與現(xiàn)行標(biāo)準(zhǔn)中提出的-850mV(相對于銅/硫酸銅電極)極化電位準(zhǔn)則基本是一致的。雖然目前還未明確陰極保護(hù)效應(yīng)的機(jī)理,但這并不妨礙業(yè)界對該技術(shù)的應(yīng)用。
免責(zé)聲明:本網(wǎng)站所轉(zhuǎn)載的文字、圖片與視頻資料版權(quán)歸原創(chuàng)作者所有,如果涉及侵權(quán),請第一時間聯(lián)系本網(wǎng)刪除。

官方微信
《中國腐蝕與防護(hù)網(wǎng)電子期刊》征訂啟事
- 投稿聯(lián)系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護(hù)網(wǎng)官方QQ群:140808414