摘要
采用電化學(xué)測(cè)試方法研究了不同Cl-濃度下,304不銹鋼在兩種模擬混凝土孔隙液中的點(diǎn)蝕行為,確定了304不銹鋼的臨界Cl-濃度;采用SEM觀察了304不銹鋼表面鈍化膜在臨界Cl-濃度前后的狀態(tài)。結(jié)果表明,通過動(dòng)電位極化和恒電位阻抗方法確定了304不銹鋼的臨界Cl-濃度,且數(shù)值基本一致,并SEM觀測(cè)結(jié)果相一致;而開路電位下的阻抗測(cè)試并不能確定臨界Cl-濃度。
關(guān)鍵詞: 304不銹鋼 ; 模擬混凝土孔隙液 ; 臨界Cl-濃度 ; 點(diǎn)蝕
Cl-對(duì)碳鋼的腐蝕已被廣泛認(rèn)為是導(dǎo)致鋼筋混凝土結(jié)構(gòu)過早破壞的主要原因之一。針對(duì)這一問題,相關(guān)學(xué)者提出了許多改善鋼筋混凝土質(zhì)量的策略和措施,一些研究者已經(jīng)開始研究不銹鋼鋼筋在模擬混凝土孔溶液中的腐蝕行為。Freire等[1,2]研究了堿性溶液 (NaOH+KOH) 中AISI 304和316不銹鋼上鈍化膜的電化學(xué)行為和化學(xué)成分,結(jié)果表明,溶液pH和Cl-濃度對(duì)兩種不銹鋼的膜組成和腐蝕行為有重要影響。Moser等[3]研究了幾種高強(qiáng)度不銹鋼在模擬混凝土溶液中的耐蝕性,表明這些材料在含有Cl-的堿性溶液中均表現(xiàn)出較高的耐蝕性。
不銹鋼的臨界點(diǎn)蝕條件一直是腐蝕研究的熱點(diǎn)。Frankel[4]總結(jié)了影響金屬點(diǎn)蝕的關(guān)鍵因素,包括合金成分、環(huán)境、電位和溫度等,列出了幾種不銹鋼允許的最高溫度和氯化物濃度,以避免在氯化物中出現(xiàn)點(diǎn)蝕。對(duì)這些臨界條件的研究有助于闡明點(diǎn)蝕形成和擴(kuò)展機(jī)理,許多經(jīng)典理論都是基于對(duì)臨界點(diǎn)蝕條件的深入研究。Cl-作為最危險(xiǎn)的點(diǎn)蝕影響因素之一,一直是研究人員關(guān)注的重點(diǎn)。Leckie和Uhlig[5]在1966年首次報(bào)道了電化學(xué)方法研究不銹鋼的臨界點(diǎn)蝕電位和Cl-活性的對(duì)數(shù)之間的線性關(guān)系。其它研究者也基于動(dòng)電位極化曲線討論了Cl-濃度對(duì)各種不銹鋼的影響,包括AISI304,AISI 316L,LDX 2003,DSS 2205[6-8]。臨界點(diǎn)蝕Cl-濃度 (CPCC) 是評(píng)價(jià)各種不銹鋼在鹽溶液中點(diǎn)蝕敏感性的較為直接的指標(biāo)。2000年,Yang和Luo[9]通過在不同氯化物濃度的硼酸鹽緩沖溶液中施加恒定電位,研究了氯化物對(duì)陽極電流密度的影響;并在此基礎(chǔ)上,研究了不同充氫電流密度下的304不銹鋼腐蝕的臨界Cl-濃度。每一種不銹鋼都有一個(gè)CPCC值,它可以像臨界點(diǎn)蝕溫度 (CPT) 那樣用電化學(xué)方法測(cè)量[10],采用簡(jiǎn)便的電化學(xué)方法測(cè)定不銹鋼的CPCC是十分必要和有意義的。本文采用動(dòng)電位極化、電化學(xué)阻抗法和SEM等,研究了304不銹鋼在不同模擬溶液下的臨界Cl-濃度。
1 實(shí)驗(yàn)方法
采用的實(shí)驗(yàn)材料為304不銹鋼,其化學(xué)成分 (質(zhì)量分?jǐn)?shù),%) 如下:C 0.046、Si 0.57、Mn 1.22、P 0.046、S 0.005、Ni 8.01、Cr 18.06、Fe余量。模擬混凝土孔隙溶液為飽和Ca(OH)2溶液和HCO3-/CO32-溶液。溶液的初始pH是通過pH計(jì)直接測(cè)量得到,飽和Ca(OH)2溶液的pH為12.56;HCO3-/CO32-溶液由0.015 mol/L NaHCO3和0.005 mol/L Na2CO3組成,pH為10.07,選擇這種溶液組成是為了模擬混凝土孔隙液碳化初期對(duì)304 SS點(diǎn)蝕行為的影響[11]。實(shí)驗(yàn)中所有使用的化學(xué)藥品都為分析純?cè)噭T谡麄€(gè)實(shí)驗(yàn)過程中,溶液溫度控制在 (23±2) °C。
將304不銹鋼機(jī)械加工成尺寸為10 mm×10 mm×2 mm的試樣,4個(gè)側(cè)面用1500#的SiC砂紙打磨后再在60 ℃的硝酸鈍化液中預(yù)鈍化1 h,用銅導(dǎo)線焊接后,再用環(huán)氧樹脂封在PVC管內(nèi)以保證暴露于溶液中的工作電極面積為1 cm2。在進(jìn)行電化學(xué)測(cè)試之前,先后用SiC砂紙依次濕磨至2000#,用酒精脫脂,在水中清洗,然后在冷空氣中干燥。
在Zennium E電化學(xué)工作站上進(jìn)行動(dòng)電位極化測(cè)試、開路電位下阻抗測(cè)試和恒電位阻抗譜測(cè)試。采用三電極體系,鉑片作為對(duì)電極,飽和甘汞電極 (SCE) 作為參比電極,工作電極 (WE) 是304不銹鋼試樣。動(dòng)電位極化測(cè)量是在30 min的 OCP測(cè)試后獲得的。掃描電位范圍為-1.0~+1.0 VSCE,掃描速率為0.5 mV/s。
304不銹鋼在兩種模擬混凝土孔隙液中的開路電位下的電化學(xué)阻抗測(cè)試是在30 min的OCP測(cè)試后測(cè)得。交流電位幅度為10 mV,頻率范圍為105~10-2 Hz,并且通過Zsimpwin軟件進(jìn)行數(shù)據(jù)分析。
在飽和Ca(OH)2溶液中,將試樣在+450 mVSCE的陽極電位極化1 h后測(cè)量電化學(xué)阻抗,在HCO3-/CO32-溶液中則將試樣在+600 mVSCE的陽極電位極化1 h后測(cè)量電化學(xué)阻抗。交流電位幅度為10 mV,頻率范圍為105~10-2 Hz,并且通過Zsimpwin軟件進(jìn)行數(shù)據(jù)分析。所有電化學(xué)測(cè)試均在室溫 (23±2) ℃下進(jìn)行,并至少重復(fù)3次以確保實(shí)驗(yàn)的可重復(fù)性。
304不銹鋼在除去表面鈍化膜后,在兩種不同測(cè)試溶液中的臨界Cl-濃度前后分別對(duì)試樣進(jìn)行恒電位極化1 h,最后使用JSM-6700F掃描電子顯微鏡 (SEM) 對(duì)表面形貌進(jìn)行觀察。
2 結(jié)果與討論
2.1 動(dòng)電位極化曲線分析
304不銹鋼在具有不同Cl-含量的飽和Ca(OH)2溶液和HCO3-/CO32-堿性溶液中的動(dòng)電位極化曲線如圖1所示。在飽和Ca(OH)2溶液中,添加各個(gè)濃度的Cl-之后,所有樣品的腐蝕電位基本都是集中在-500 mVSCE。當(dāng)Cl-濃度從0增加到0.2 mol/L時(shí),從腐蝕電位到+400 mVSCE時(shí),鈍化電流密度先增大并出現(xiàn)一個(gè)峰值,然后出現(xiàn)二次鈍化區(qū)。在這個(gè)Cl-濃度范圍內(nèi),只觀察到鈍化行為,材料表面形成的鈍化層保護(hù)鋼材免受侵蝕[8],點(diǎn)蝕未發(fā)生,這表明并未達(dá)到臨界Cl-點(diǎn)蝕濃度。當(dāng)電位上升到較高水平時(shí),電流迅速增加,這是由于析氧反應(yīng)引起的[12]。304不銹鋼在析氧前保持了良好的鈍性,隨著氯化物濃度的增加,鈍化區(qū)寬度顯著降低。結(jié)果表明,樣品的點(diǎn)蝕敏感性明顯提高。當(dāng)Cl-濃度從0.2 mol/L提高到1 mol/L時(shí),直至鈍化膜的發(fā)生破裂,樣品表面開始出現(xiàn)點(diǎn)蝕。當(dāng)溶液中添加的Cl-濃度大于0.2 mol/L時(shí),就可能出現(xiàn)點(diǎn)蝕。不銹鋼表面的點(diǎn)蝕電位是最廣泛報(bào)道的臨界條件之一,超過點(diǎn)蝕電位會(huì)形成穩(wěn)定的點(diǎn)蝕[6],隨著Cl-濃度的提高,點(diǎn)蝕發(fā)生所需要的時(shí)間與電位變低[13]。在飽和Ca(OH)2溶液中,在鈍化區(qū)出現(xiàn)了一些明顯的電流波動(dòng),這是由于在穩(wěn)定點(diǎn)蝕之前發(fā)生了亞穩(wěn)態(tài)點(diǎn)蝕[14,15]。
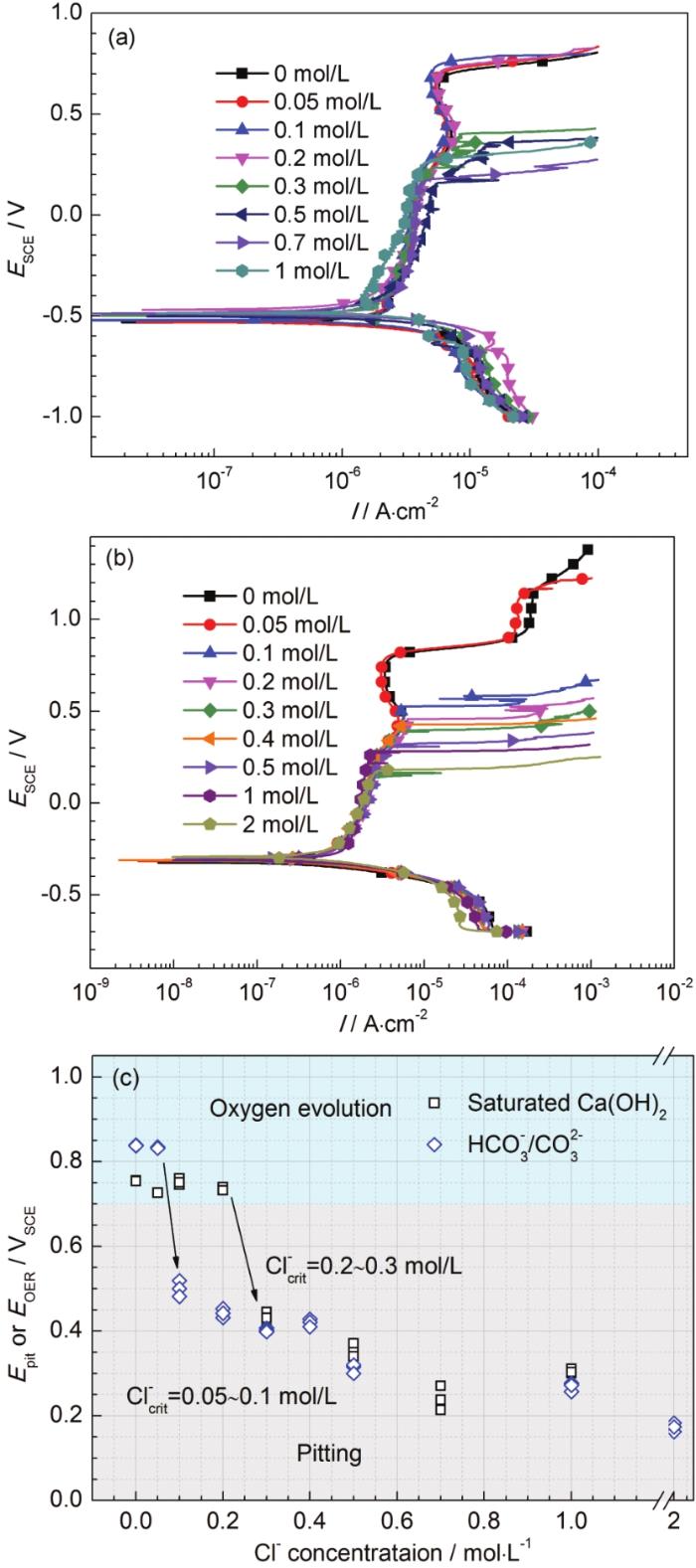
圖1 304不銹鋼在含氯化物飽和Ca(OH)2溶液和HCO3-/CO32-堿性溶液中的極化曲線及臨界Cl-濃度
在HCO3-/CO32-堿性溶液中,各個(gè)Cl-濃度下的腐蝕電位都集中在-300 mVSCE。當(dāng)Cl-濃度從0增加到0.05 mol/L,從腐蝕電位到+400 mVSCE時(shí),304不銹鋼依然出現(xiàn)過鈍化溶解和二次鈍化區(qū),直至氧析出的發(fā)生未發(fā)現(xiàn)點(diǎn)蝕。當(dāng)Cl-濃度從0.05 mol/L提高到2 mol/L時(shí),鈍化電流密度一直增加,直至鈍化膜發(fā)生破裂,點(diǎn)蝕坑出現(xiàn)。HCO3-/CO32-堿性溶液中的樣品在Cl-濃度達(dá)到0.05 mol/L后,可能出現(xiàn)點(diǎn)蝕。而且隨著Cl-濃度的升高,點(diǎn)蝕發(fā)生所需要電位變低,在Cl-濃度達(dá)到2 mol/L時(shí),點(diǎn)蝕電位達(dá)到最低的+200 mVSCE。
304不銹鋼鋼筋在沒有到達(dá)臨界Cl-濃度的模擬混凝土孔隙液中會(huì)直接進(jìn)入鈍化狀態(tài),鈍化區(qū)范圍比較大,如果沒有發(fā)生擊破,一直到氧析出時(shí),電流密度才明顯升高[16]。當(dāng)?shù)竭_(dá)臨界Cl-濃度時(shí),鈍化區(qū)范圍變窄,在遠(yuǎn)低于氧析出電位處,電流值會(huì)突變?cè)黾樱g化膜破裂,點(diǎn)蝕電位明顯負(fù)移[17]。
從圖1c中不同Cl-濃度下的點(diǎn)蝕電位看出,在飽和Ca(OH)2溶液中,Cl-濃度在0.2 mol/L及以下時(shí),可以看到樣品未出現(xiàn)點(diǎn)蝕電位,而在0.3 mol/L時(shí),出現(xiàn)了點(diǎn)蝕電位;同樣的,在HCO3-/CO32-堿性溶液中,Cl-濃度在0.05 mol/L及以下時(shí),樣品并不能出現(xiàn)點(diǎn)蝕坑,直到增加到0.1 mol/L時(shí),才會(huì)出現(xiàn)點(diǎn)蝕電位。綜上所述,在飽和Ca(OH)2溶液中樣品的點(diǎn)蝕發(fā)生臨界Cl-濃度為0.2~0.3 mol/L,而在HCO3-/CO32-堿性溶液中樣品的點(diǎn)蝕發(fā)生臨界Cl-濃度為0.05~0.1 mol/L。
2.2 開路電位下阻抗分析
為了研究Cl-對(duì)模擬混凝土孔隙液中304不銹鋼鈍化膜結(jié)構(gòu)性能的影響,在飽和Ca(OH)2溶液和HCO3-/CO32-堿性溶液中進(jìn)行開路電位下的EIS測(cè)試,結(jié)果如圖2所示。所有的阻抗曲線呈半圓弧狀,表明304不銹鋼在不同Cl-濃度下的兩種模擬混凝土孔隙液中的成膜機(jī)制相同,Cl-含量的變化對(duì)阻抗弧形狀的變化產(chǎn)生明顯的影響。從圖中可以看出,隨著飽和Ca(OH)2溶液中Cl-濃度的不斷增加,直到0.1 mol/L,容抗弧的半徑逐漸減小;Cl-濃度從0.1到0.3 mol/L時(shí),容抗弧的半徑基本不變;然而當(dāng)Cl-濃度逐漸從0.3 mol/L增加到0.7 mol/L時(shí),容抗弧半徑又逐漸增大;此后,在測(cè)試濃度范圍內(nèi)隨著Cl-濃度的增加,容抗弧又基本保持不變。在HCO3-/CO32-堿性溶液中,隨著濃度的不斷增加,容抗弧半徑逐漸減小;當(dāng)Cl-濃度高于1 mol/L后,容抗弧半徑又增大。經(jīng)過以上分析可知,開路電位下的EIS不適合測(cè)試304不銹鋼的臨界Cl-濃度,這是由于點(diǎn)蝕的萌生和擴(kuò)展是一個(gè)非常漫長(zhǎng)的過程,短暫的開路電位測(cè)試之后的阻抗測(cè)試不能得到點(diǎn)蝕發(fā)生的臨界Cl-濃度。此外,開路電位未達(dá)到304不銹鋼的保護(hù)電位,所以繼續(xù)采用恒電位下的阻抗來快速評(píng)價(jià)。
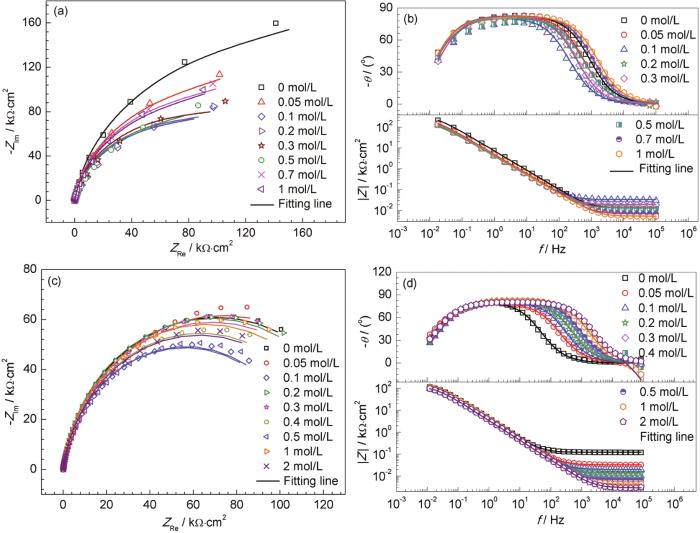
圖2 304不銹鋼在含不同Cl-濃度的飽和Ca(OH)2溶液和HCO3-/CO32-堿性溶液中的開路電位下EIS圖
2.3 恒電位下阻抗分析
根據(jù)動(dòng)電位極化曲線確定不銹鋼的鈍化區(qū)間,選擇合適的鈍化電位。在飽和Ca(OH)2溶液中,304 不銹鋼在陽極電位+450 mVSCE下極化1 h后的EIS測(cè)試結(jié)果如圖3a所示。在HCO3-/CO32-堿性溶液中,304不銹鋼在陽極電位+600 mVSCE下極化1 h后的EIS測(cè)試結(jié)果如圖3c所示。Nyquist圖均由一段容抗弧組成,隨著Cl-濃度的增加,容抗弧的半徑有所改變,阻抗譜的高頻區(qū)表征的是電解液和電極表面電阻的信息,低頻區(qū)對(duì)應(yīng)的是腐蝕過程中電化學(xué)反應(yīng)的電荷轉(zhuǎn)移電阻的大小。
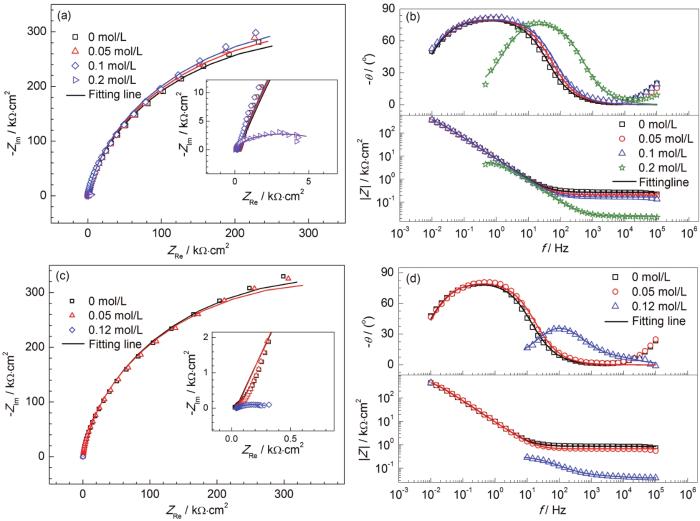
圖3 304 不銹鋼在含不同Cl-濃度的飽和Ca(OH)2和HCO3-/CO32-堿性溶液中的恒電位下EIS圖
在飽和Ca(OH)2溶液中,304不銹鋼的Nyquist圖呈現(xiàn)出的是一段圓弧,容抗弧的半徑不同,0、0.05和0.1 mol/L的Cl-濃度下的樣品差距不大,對(duì)應(yīng)的時(shí)間常數(shù)基本相同,此時(shí)不銹鋼處于鈍化狀態(tài)[18]。由于容抗弧半徑的大小直接反映了金屬電極表面電荷轉(zhuǎn)移電阻的大小,電阻越大,腐蝕速率越小。當(dāng)Cl-濃度達(dá)到0.2 mol/L時(shí),容抗弧發(fā)生了明顯變化,半徑遠(yuǎn)遠(yuǎn)小于其他的濃度。此時(shí)界面電阻值較小,樣品的腐蝕速率加快。這表明鈍化膜的破裂以及點(diǎn)蝕的發(fā)生,即已經(jīng)超過發(fā)生點(diǎn)蝕的臨界Cl-濃度;Bode圖中,0.2 mol/L Cl-濃度下樣品的阻抗模值最低,而且其出現(xiàn)了不同的時(shí)間常數(shù),阻抗數(shù)值不再向低頻區(qū)移動(dòng),說明腐蝕已經(jīng)發(fā)生。
在HCO3-/CO32-堿性溶液中,0和0.05 mol/L的Cl-濃度下的樣品的容抗弧半徑相差不大,處于鈍化狀態(tài);當(dāng)Cl-濃度達(dá)到0.12 mol/L時(shí),容抗弧半徑急劇減小,同樣說明此時(shí)Cl-濃度超過臨界值以及點(diǎn)蝕的發(fā)生。而在Bode圖中,0和0.05 mol/L Cl-濃度下,304不銹鋼沒有點(diǎn)蝕發(fā)生,而且其阻抗模值也比0.12 mol/L Cl-濃度下的樣品高。阻抗值或容抗半徑的顯著下降是點(diǎn)蝕的標(biāo)志[19]。
在這兩種模擬溶液中,均出現(xiàn)了低頻區(qū)阻抗數(shù)據(jù)的缺失。這是因?yàn)楦g已經(jīng)發(fā)生,且速率很快,儀器未能輸出結(jié)果,所以阻抗結(jié)果未能呈現(xiàn)出低頻區(qū)的數(shù)據(jù)。綜上所述,304不銹鋼在飽和Ca(OH)2溶液中的點(diǎn)蝕發(fā)生臨界點(diǎn)蝕Cl-濃度是在0.1~0.2 mol/L,而HCO3-/CO32-堿性溶液中的點(diǎn)蝕發(fā)生臨界點(diǎn)蝕Cl-濃度是0.05~0.12 mol/L。
用于模擬EIS結(jié)果的等效電路圖如圖4所示,根據(jù)該模型提取的參數(shù)如表1所示。可以看出,在比較低的Cl-濃度下,304不銹鋼表面為完整鈍化膜,可以采用如圖4a中的簡(jiǎn)單等效電路擬合。當(dāng)溶液中的Cl-濃度超過臨界值時(shí),鈍化膜表面會(huì)形成穩(wěn)定的點(diǎn)蝕坑,其等效電路與低于臨界Cl-濃度時(shí)的電路不同。此時(shí)可以將表面分為兩個(gè)可區(qū)分的部分,即鈍化表面和點(diǎn)蝕區(qū)域。在鈍化表面處,所提出的電路類似于低于臨界Cl-濃度時(shí)的電路。然而,在表面存在穩(wěn)定點(diǎn)蝕的情況下,增加了一個(gè)與鈍化表面平行的物理單元 (點(diǎn)蝕)。同時(shí)采用CPEpit、Rpit和Ri 3個(gè)元件對(duì)穩(wěn)態(tài)點(diǎn)蝕進(jìn)行擬合,它們分別代表了表面與坑內(nèi)溶液界面形成的雙電層結(jié)構(gòu)、與點(diǎn)蝕坑有關(guān)的電荷轉(zhuǎn)移電阻和點(diǎn)蝕坑內(nèi)溶液電阻。在這些模型中,引入了頻率相關(guān)的恒定相位元件 (CPE) 而不是純電容 (C),以解釋界面上存在的不均勻性[20],CPE用于更準(zhǔn)確地分析雙電層的阻抗行為。
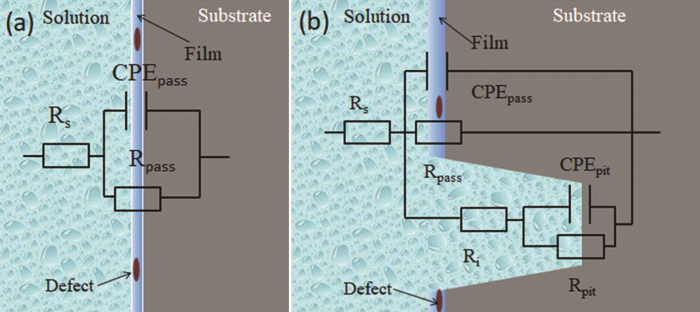
圖4 低于臨界Cl-濃度和高于臨界Cl-濃度的等效電路模型
表1 304 不銹鋼在不同模擬混凝土孔隙液中的EIS擬合參數(shù)
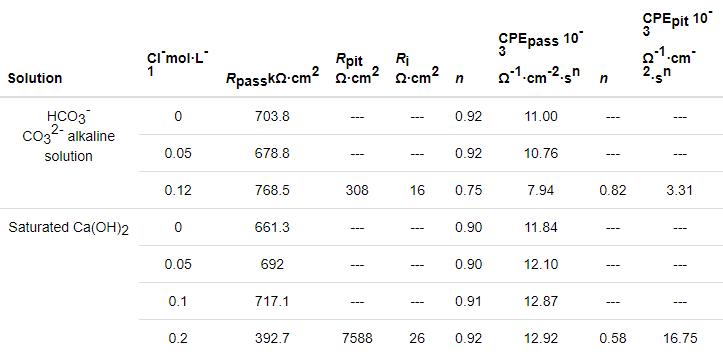
從表1可以看出,在飽和Ca(OH)2溶液中,當(dāng)?shù)陀谂R界Cl-濃度時(shí),隨著Cl-濃度增加,Rpass的增大可能是由于離子通過鈍化膜的擴(kuò)散減少,這表明鈍化膜受高堿性環(huán)境的保護(hù)。而在HCO3-/CO32-堿性溶液中,則出現(xiàn)相反的結(jié)果,Rpass的減小可能是由于離子通過鈍化膜的擴(kuò)散增加,這表明鈍化膜上的缺陷增加。此外,n值的變化也表明了Cl-對(duì)鈍化層均勻性產(chǎn)生了影響[21]。
臨界Cl-濃度可以認(rèn)為是Rtotal急劇下降時(shí)的氯離子濃度。當(dāng)Cl-濃度低于臨界Cl-濃度時(shí),Rtotal的值與Rpass相同。而當(dāng)Cl-濃度高于臨界Cl-濃度時(shí),Rtotal的計(jì)算公式如下:

式中,Rtotal是總電阻,Rpit是電荷轉(zhuǎn)移電阻,Ri是點(diǎn)蝕坑內(nèi)的溶液電阻,Rpass是膜電阻。
圖5顯示了在兩種模擬混凝土孔隙液中304不銹鋼鈍化膜上的Rtotal值 (根據(jù)表1中的數(shù)據(jù)計(jì)算) 隨Cl-濃度的變化。可以看出,對(duì)于飽和Ca(OH)2溶液,Rtotal的急劇下降發(fā)生在0.1~0.2 mol/L之間,對(duì)于HCO3-/CO32-堿性溶液,這種急劇下降在0.05~0.12 mol/L之間。綜合恒電位阻抗法和動(dòng)電位極化法的結(jié)果,可以看出恒電位阻抗法與動(dòng)電位極化法的結(jié)果密切相關(guān),說明恒電位阻抗法可以作為不銹鋼臨界Cl-濃度的測(cè)定方法。
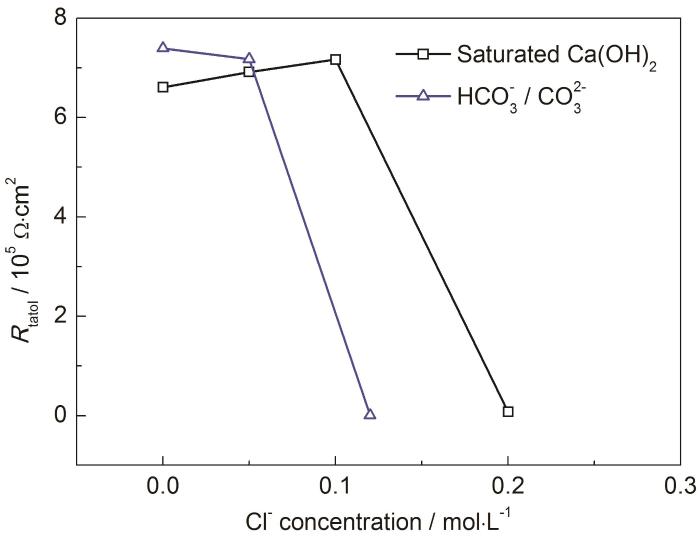
圖5 在不同模擬混凝土孔隙液中304不銹鋼的Rtotal值隨Cl-濃度的變化曲線
2.4 腐蝕形貌的SEM觀察結(jié)果
分別對(duì)在含0.1和0.2 mol/L NaCl的飽和Ca(OH)2溶液中的304不銹鋼進(jìn)行恒電位極化測(cè)試之后,在SEM下觀察試樣的表面形貌。同樣,對(duì)304不銹鋼在含0.05和0.12 mol/L NaCl的HCO3-/CO32-堿性溶液中進(jìn)行1 h的恒電位極化測(cè)試,分析試樣的表面微觀形貌,結(jié)果如圖6所示。可以明顯的觀察到,含有不同Cl-濃度的兩種溶液中,在尚未達(dá)到臨界Cl-濃度之前,304不銹鋼試樣表面沒有任何明顯的點(diǎn)蝕坑;當(dāng)溶液中Cl-濃度超過臨界值時(shí),試樣的表面出現(xiàn)了非常明顯的點(diǎn)蝕坑。SEM觀察結(jié)果進(jìn)一步證實(shí)了恒電位下阻抗譜所得出的結(jié)論。

圖6 在不同模擬混凝土孔隙液中304 不銹鋼恒電位極化后的SEM像
3 結(jié)論
(1) 304不銹鋼在不同的模擬混凝土孔隙液中進(jìn)行動(dòng)電位極化測(cè)試結(jié)果表明,在飽和Ca(OH)2溶液中,點(diǎn)蝕發(fā)生的臨界Cl-濃度在0.2~0.3 mol/L之間,而在HCO3-/CO32-堿性溶液中是0.05~0.1 mol/L之間。
(2) 在兩種不同的模擬混凝土孔隙液中的恒電位阻抗譜結(jié)果表明,304不銹鋼在飽和Ca(OH)2溶液中,點(diǎn)蝕發(fā)生的臨界Cl-濃度是0.1~0.2 mol/L之間,而在HCO3-/CO32-堿性溶液中的點(diǎn)蝕發(fā)生的臨界Cl-濃度是在0.05~0.12 mol/L之間。與動(dòng)電位極化所得的臨界Cl-濃度相對(duì)一致,SEM的測(cè)試結(jié)果同樣證明了這一結(jié)論。
(3) 304不銹鋼的開路電位下和恒電位下的阻抗測(cè)試結(jié)果表明,恒電位下的阻抗測(cè)試可以作為判定304不銹鋼臨界Cl-濃度的方法,而開路電位下的阻抗測(cè)試不適合。
參考文獻(xiàn)
免責(zé)聲明:本網(wǎng)站所轉(zhuǎn)載的文字、圖片與視頻資料版權(quán)歸原創(chuàng)作者所有,如果涉及侵權(quán),請(qǐng)第一時(shí)間聯(lián)系本網(wǎng)刪除。

官方微信
《中國腐蝕與防護(hù)網(wǎng)電子期刊》征訂啟事
- 投稿聯(lián)系:編輯部
- 電話:010-62316606-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護(hù)網(wǎng)官方QQ群:140808414





