過渡金屬硼化物(TMBs) 是一類具有高硬度、高熔點、耐高溫、耐腐蝕等優異性能的材料。硼原子的多價態結合方式和過渡金屬原子的高價電子密度決定了過渡金屬硼化物中電荷轉移的多樣性及化學鍵成鍵的特殊性,進而導致這類物質具有豐富的結構和潛在的多功能性。其中,ZrB2具有相對較低的密度(6.12 g/cm3)、極高的熔點(3245 ℃)、強度、硬度和導電率(其導電率溫度系數為正) 以及低的熱膨脹系數,還具有好的化學穩定性、補集中子、阻燃、耐腐蝕等特殊性質,使得其在高溫結構陶瓷材料、電極材料、薄膜材料、耐火材料、核控制材料等諸多領域有著廣泛的應用前景。ZrB2的制備方法主要有直接合成法、硼熱/碳熱還原法、氣相法、溶膠-凝膠法[、熔鹽電沉積法等。與其他方法相比,熔鹽電沉積法具有如下優勢:(1) 可以在很大程度上簡化合成過渡金屬化合物的技術路線,無需制備過渡金屬和非金屬粉末的中間步驟;(2) 反應過程在原子尺度上進行,因此反應溫度相對較低;(3)用于合成的反應物可以選擇價格相對低廉的物質;(4) 可以人為控制合成過程和沉積物的形態,這使得最終產物既有可能以粉體形式存在,又可能以涂層形態存在。
本文結合作者的一些研究成果,綜述了熔鹽電沉積法制備ZrB2的研究進展。主要介紹了熔鹽體系、電沉積工藝和參數對ZrB2制備的影響,總結了B(III) 和Zr(IV) 在不同熔鹽體系中的電化學還原機制以及ZrB2的合成機制,并展望了熔鹽電沉積法制備ZrB2的應用前景。
1 熔鹽電沉積法制備ZrB2
目前,關于熔鹽電沉積法制備ZrB2已有不少報道,氟化物、氯化物-氟化物、氟化物-氧化物、氯化物-氧化物[等多種熔鹽體系被應用于ZrB2的制備中,產物類型主要有粉體、枝晶和涂層等,相應結果總結見表1。
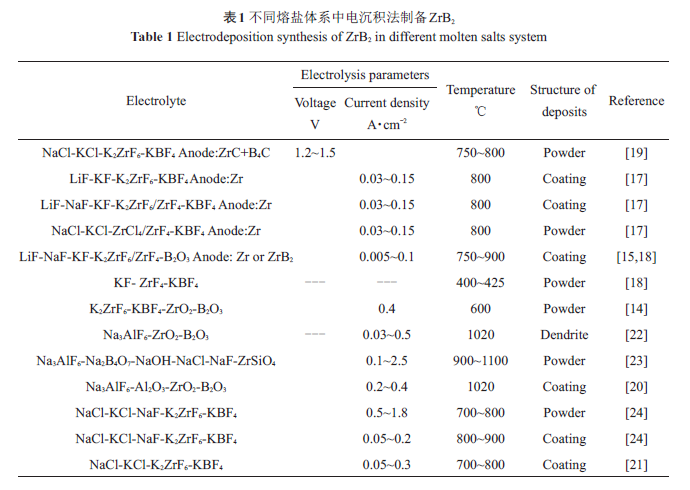
Mellors 等首先采用全氟化物熔鹽體系,即在LiF- KF-K2ZrF6-KBF4 中,以Zr 作為陽極材料,在800 ℃、0.03 A/cm2的電流密度下成功在鉬基體表面沉積了一層致密的ZrB2涂層。同時還嘗試在石墨基體上進行電沉積,但獲得的ZrB2涂層與基體之間的結合力較差。采用LiF-NaF-KF-ZrF4-KBF4的熔鹽體系,同樣可以獲得ZrB2涂層。他們還研究了在氯化物-氟化物(如NaCl-KCl-ZrCl4-KBF4 和NaCl-KCl-ZrF4-KBF4) 和氯化物-氧化物(如NaCl-KCl-ZrCl4-B2O3) 熔鹽體系中制備ZrB2,結果表明,在這兩類熔鹽中進行電沉積僅得到ZrB2粉體。Stern 等也采用氯化物-氟化物熔鹽體系,并以ZrC 和B4C的混合粉體作為陽極,在NaCl-KCl-K2ZrF6-KBF4熔鹽中進行電沉積,在750~850 ℃、1.2~1.5 V 電壓下制備出ZrB2粉體。
上述實驗中采用的硼源均為KBF4,它在高溫下易分解為KF和氣態的BF3,使得熔鹽中活性物質的濃度發生變化。為了解決這一問題,Mellors 等嘗試降低反應溫度,采用KF-ZrF4熔鹽體系,其共晶點僅為390 ℃。向其中加入KBF4 作為硼源,在400~425 ℃進行電沉積,產物為Zr 和ZrB2 粉體的混合物。他們還提出可以向LiF-NaF-KF-ZrF4熔鹽體系中持續通入BF3以維持體系中硼的濃度,但存在的問題是熔鹽中氣體流動造成了制備的ZrB2涂層表面粗糙度增大。
隨后,Mellors 等進行了在氟化物-氧化物熔鹽體系中電沉積ZrB2的研究。熔鹽體系中的氧化物主要為B2O3,以替代前述體系中在高溫下易分解揮發的硼源KBF4。在LiF-NaF-KF 熔鹽中,鋯源為ZrF4或K2ZrF6,硼源為B2O3,純鋯作為陽極材料,750~900 ℃、0.005~0.1 A/cm2的電流密度下制備了ZrB2涂層。此外,他們還利用了ZrB2作為陽極材料,目的是解決體系中活性物質濃度隨著電解過程而變化的問題。結果表明,采用ZrB2作為陽極材料,獲得的涂層質量較好,較為適宜的反應溫度為800~820 ℃,電流密度低于0.05 A/cm2。
Anthony 等也采用氟化物-氧化物熔鹽體系,以等摩爾比的K2ZrF6和KBF4作為溶劑,ZrO2和B2O3分別作為鋯源和硼源,反應溫度為600 ℃時制備出ZrB2 粉體。隨后,他們采用冰晶石作為溶劑,在Na3AlF6-ZrO2-B2O3熔鹽體系中、鎳基體上制備出枝晶態的ZrB2,反應溫度為1020 ℃。結果表明,體系中ZrO2的濃度和施加的電流密度決定了產物類型及形態。當ZrO2濃度較低且電流密度較小時,在基體表面得到的產物為硼化鎳;當ZrO2濃度較高而電流密度較小時,可以同時得到硼化鎳擴散層和枝晶態的ZrB2;而當ZrO2濃度較高且電流密度較大時,產物為枝晶態的ZrB2。Devyatkin 等同樣以冰晶石作為溶劑,并向其中加入Al2O3,以ZrO2作為鋯源,B2O3 作為硼源,在1020 ℃、0.2~0.4 A/cm2 的電流密度下在鎳基體上電沉積一層ZrB2涂層。
Gomes 等在制備ZrB2時,創新性地嘗試利用鋯石作為鋯源來降低成本。他們采用Na3AlF6-Na2B4O7-NaOH-NaCl-NaF-ZrSiO4的熔鹽體系,電流密度為0.1~2.5 A/cm2,反應溫度為900~1100 ℃,制備出枝晶態的ZrB2粉體,且反應過程中無需氣氛保護。當熔鹽體系中B和Zr 的原子比大于6 時,得到的產物其純度和產率最佳。
Malyshev 等對NaCl-KCl-NaF-K2ZrF6-KBF4熔鹽體系中制備ZrB2涂層和粉體材料進行了研究。結果表明,當反應溫度為700~800 ℃,電流密度為0.5~1.8 A/cm2時,得到的產物為ZrB2粉體;而將反應溫度提升至800~900 ℃,電流密度降至0.05~0.2 A/cm2時,可以獲得ZrB2涂層。此外,他們還通過伏安測試研究了熔鹽中氟離子對沉積產物的影響。
近些年,作者所在課題組也開展了熔鹽電沉積制備ZrB2涂層的研究工作。通過研究反應溫度和電流密度等電沉積影響因素對NaCl- KCl- NaFK2ZrF6-KBF4熔鹽體系中制備ZrB2涂層的影響,獲得了制備均勻、致密、與基體結合良好的ZrB2涂層的工藝參數。結果表明,過大或過小的電流密度都不利于ZrB2涂層的制備。電流密度較低時,涂層表面出現許多孔洞,致密性較差;然而,電流密度較高時,涂層均勻性和平整性較差。在電流密度為0.1 A/cm2時可以獲得表面平整、致密,與基體結合良好的ZrB2涂層。過高或過低的溫度均不利于ZrB2涂層的制備。溫度較低時,涂層生長速度相對較慢;而溫度過高時,表面出現大量瘤狀物,且熔鹽揮發速率增大對反應器的腐蝕性加強。綜合考慮,750 ℃為合適的反應溫度。當電流密度為0.1 A/cm2,在750 ℃沉積30 min 可以在不銹鋼基體表面獲得約25 μm的ZrB2涂層,如圖1 所示。涂層均勻、平整、致密性好、與基體結合良好,這主要是由于涂層與不銹鋼基體之間存在一層硼化物擴散層。

2 熔鹽電沉積ZrB2的陰極機理研究
掌握B(III) 和Zr(IV) 在熔鹽電沉積中的電化學還原機制及ZrB2的陰極還原過程對于制備ZrB2無疑具有重要的意義。
2.1 B(III) 在不同熔鹽體系中的電化學還原機制
研究者們對以KBF4和B2O3為代表的含硼活性物質在不同熔鹽體系中的電化學行為進行了研究。
Polyakova 等研究了在550~700 ℃的LiF-NaFKF-KBF4熔鹽中硼離子在三種工作電極(玻碳電極、Pt電極和Ag電極) 上的電化學還原過程。結果表明,當體系中KBF4的濃度低于5.7×10- 2 mol%時,B(III)還原為硼單質遵循三電子不可逆反應;當其濃度高于5.7×10-2 mol%時,歐姆電阻的存在使得其陰極過程更為復雜。Rahul 等研究了在800~850 ℃,LiFNaF-KF-KBF4熔鹽體系中硼離子在Pt 電極上的電化學還原機制。結果表明,當掃描速率低于0.1 V/s時,硼離子遵循準可逆三電子單步還原過程;當掃描速率高于0.1 V/s時,還原過程轉變為不可逆反應。
Makyta 等分別研究了LiF-KF-KBF4 和LiFKF-B2O3熔鹽中的硼離子在Pt 工作電極上的電化學還原機制。結果表明,在LiF-KF-KBF4熔鹽體系中,硼離子遵循三電子還原過程;而在LiF-KF-B2O3體系中,B2O3 會首先與熔鹽中的LiF 和KF 反應形成KBF4。他們還測量得到了硼在這兩個熔鹽體系中的沉積電位差為0.47 V。
Taranenko 等研究發現電化學活性物質濃度為3×10-5~80×10-5 mol/cm3的NaCl-KCl-MeBF4(Me=Na,K) 熔鹽體系中BF4-在玻碳電極上的電化學還原機制為三電子一步還原。他們還發現,向熔鹽體系中添加F-可以增大MeBF4的熱穩定性。Kuznetsov等提出BF4-在NaCl-KCl 和NaCl-KCl-NaF 熔鹽體系中,在玻碳電極和Ag電極上的還原是不可逆的三電子轉移過程。
Wang采用循環伏安、計時電位和方波伏安等電化學測試方法對B(III) 在NaCl-KCl-KBF4熔鹽體系中的電化學還原機制進行了研究。結果表明,B(III) 的還原過程為受擴散控制的單步三電子準可逆過程,且其可逆性在低掃描速率下較好。
通過上述討論可以看出,B(III) 的一步還原機制被廣泛認同。
2.2 Zr(IV) 在不同熔鹽體系中的電化學還原機制
目前,研究者們對含鋯的電活性物質在不同熔鹽體系中的電化學行為開展了研究工作,相應結果總結見表2。
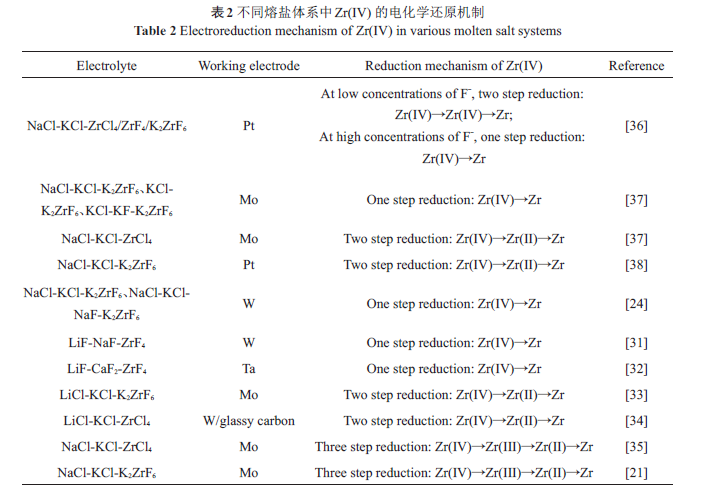
Groult 等利用循環伏安法和計時電位法研究了Zr(IV) 在W電極、LiF-NaF-ZrF4熔鹽體系中的電化學過程,結果表明Zr(IV) 的電化學還原為受擴散控制的單步反應,同時計算出Zr(IV) 在737 ℃時的擴散系數為2.92×10-5 cm2/s,在850 ℃時的擴散系數為4.89×10-5 cm2/s。Gibilaro 等研究表明Zr(IV) 在LiF-CaF2-ZrF4熔鹽體系中惰性電極Ta 上的電化學還原為一步過程。
陳增等研究表明,Zr(IV) 在LiCl-KCl-K2ZrF6熔鹽體系中鉬電極上的電化學還原過程是兩步電子轉移過程:即Zr(IV)→Zr(II)→Zr。恒電位電解產物的XRD檢測表明,中間產物以ZrCl2的形式存在,并沒有檢測到鋯的氟化物。Basile 等[34]發現Zr 在LiCl-KCl-ZrCl4熔鹽體系中的沉積分兩步進行,Zr(IV) 先被還原為ZrCl2,隨后ZrCl2還原成Zr。在此過程中,并沒有檢測到ZrCl 的存在,同時他們認為ZrCl2是一種不可溶的物質。但是,Smirnov 等在研究Zr(IV)在NaCl-KCl-ZrCl4 中的電化學行為時認為ZrCl2 是可溶性的,還原分三步進行:Zr(IV)→Zr(III)→Zr(II)→Zr。
Chen 等研究了Zr(IV) 在Pt 電極上,NaCl-KCl-ZrCl4/ZrF4和NaCl-KCl-K2ZrF6熔鹽體系中的電化學還原過程。結果表明熔鹽中的氟離子對Zr 的還原機制有較大影響。當氟離子濃度較低時,Zr(IV) 的還原分兩步進行:Zr(IV) (complex) →Zr(II)(complex)→Zr;而在氟離子濃度較高時,Zr(IV) 會一步還原成Zr。Polyakova 等認為Zr(IV) 在NaCl-KCl-ZrCl4熔鹽體系中為兩步還原:Zr(IV)→Zr(II)→Zr,而在NaCl- KCl-K2ZrF6、KCl-K2ZrF6 和KCl-KFK2ZrF6熔鹽體系中的還原機制為可逆的單步四電子過程。此外,研究發現金屬Zr 在不含鋯源的熔鹽和添加K2ZrF6的熔鹽中的腐蝕速率沒有明顯差異,說明單質Zr 不會與熔鹽中的Zr(IV) 發生反應。Wu等認為K2ZrF6在NaCl-KCl 熔鹽體系中的電化學還原過程遵循兩步反應:Zr(IV)→Zr(II)→Zr,通過計算得到Zr(IV) 絡合離子在750 ℃ 的擴散系數為4.22×10- 6 cm2/s。Malyshev 等[也研究了Zr(IV) 在NaCl-KCl 熔鹽體系中的電化學行為,并討論了氟離子的影響。他們認為Zr(IV) 的還原為一步過程,且在熔鹽中會形成含氟和氯的絡合離子。
作者采用循環伏安、線性伏安、計時電位及恒電位沉積等電化學方法,研究了K2ZrF6濃度、換向電勢及掃描速率等參數對Zr(IV) 在NaCl-KCl-K2ZrF6熔鹽中的電化學行為的影響。結果表明,Zr(IV) 在NaCl-KCl-K2ZrF6熔鹽中的電化學還原反應是一個受擴散控制的三步反應過程,即:(1) Zr(IV)+e-→Zr(III);(2) Zr(III)+e-→Zr(II);(3) Zr(II)+2e-→Zr 和Zr(IV)+4e-→Zr,對應的電子轉移數分別為1、1 和3。
最后一步鋯離子被還原單質鋯,中間過程產物則以中間價態的鋯離子形式存在于熔鹽中。
可以看出,研究者們對于Zr(IV) 在不同熔鹽體系中的電化學還原機制還存在很大的分歧,原因有以下幾點。首先,Zr 的價態有0、+1、+2、+3 和+4,多種不同價態鋯離子的存在使得Zr(IV) 的還原過程及對應的Zr 的氧化過程相對復雜;其次,不同價態鋯離子可能會與熔鹽體系中的氟離子或氯離子形成絡合離子,這也增大了體系的復雜性;最后,在熔鹽這種特殊環境下,很難對氧化還原過程的中間產物進行檢測。
2.3 ZrB2的陰極合成機理
目前,關于熔鹽體系中電化學合成ZrB2的陰極過程機理的研究,國內外的文獻報道較少。
Malyshev 等利用循環伏安法研究了NaCl-KCl-NaF-K2ZrF6-KBF4 熔鹽體系中ZrB2 的合成機制。結果表明,循環伏安曲線上出現一對陰極峰和陽極峰,對應ZrB2的還原和氧化。熔鹽中F-的濃度會影響峰電位及峰型,隨著體系中F-濃度的增大,還原峰電位向更負的方向移動,且峰寬變窄。
作者利用循環伏安法研究了ZrB2沉積的陰極過程,結果表明,在NaCl-KCl-K2ZrF6-KBF4熔鹽體系中合成ZrB2的陰極過程與體系中電活性物質Zr 和B的摩爾比有關。圖2 為鉬電極在750 ℃、3 種不同熔鹽體系(NaCl-KCl-K2ZrF6-KBF4、NaCl-KCl-K2ZrF6、NaCl-KCl-KBF4) 中的循環伏安曲線。從圖中可以看出,在NaCl- KCl-K2ZrF6(1.411×10- 4 mol/cm3)-KBF4(3.177×10-4 mol/cm3) (Zr 和B 的摩爾比為1:2.25) 對應的循環伏安曲線中出現了三個還原峰,第一個還原峰R1出現在-0.9 V (相對于Pt 參比電極) 附近,第三個還原峰R3出現在-1.7 V左右,而第二個還原峰R2的峰電位因其峰型較為陡峭而無法確定。通過與NaCl-KCl-K2ZrF6和NaCl-KCl-KBF4體系的循環伏安曲線對比,可以發現R1峰電位與B(III) 離子的還原峰電位相近,因此R1峰對應硼離子的還原。在KBF4存在的情況下,Zr(IV) 的還原峰有所不同,從圖中很難觀察到Zr(IV) 前兩個還原峰,因此,R2峰可能對應著Zr(IV) 直接還原為Zr(II) 的過程。R3峰的峰電位相比Zr 單質的析出電位向負方向略有偏移,對應Zr(II) 還原為Zr 單質的過程。因為ZrB2的吉布斯生成自由能很負(△G 01023K=-305.7 kJ/mol),所以同時Zr和B會發生化合反應生成ZrB2。
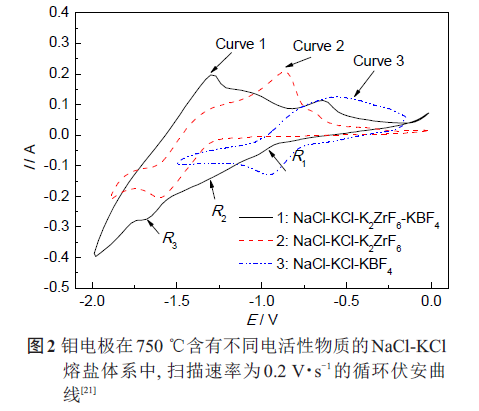
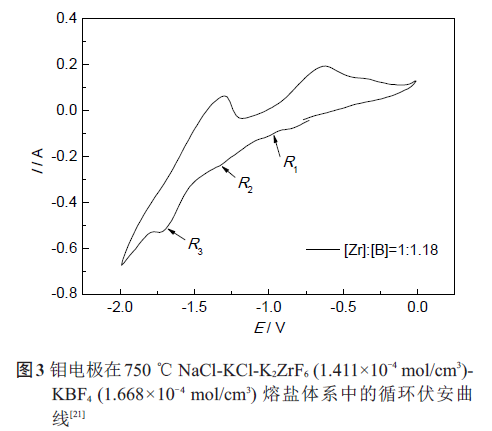
熔鹽中電活性物質K2ZrF6和KBF4的摩爾比對Zr 和B的析出電位以及ZrB2沉積的陰極過程會產生很大影響。因此,通過改變NaCl-KCl 熔鹽體系中K2ZrF6和KBF4的添加量,來觀察其循環伏安特性的相應變化。首先提高Zr 和B的摩爾比至1∶1.18,對應的循環伏安曲線如圖3 所示,圖中也出現了三個還原峰R1、R2和R3,R1峰和R3峰的峰電位與圖2 中的相近。但與圖2 中Zr 和B的摩爾比為1∶2.25 的循環伏安曲線不同,圖3 中R2峰型較為明顯,這是因為體系中B摩爾比的下降使得其對Zr(IV) 還原過程的去極化作用減弱。因此,當體系中B的含量相對較低時(如Zr 和B 的摩爾比為1∶2.25 和1∶1.18),ZrB2合成的陰極機制可以總結如下:
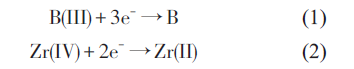

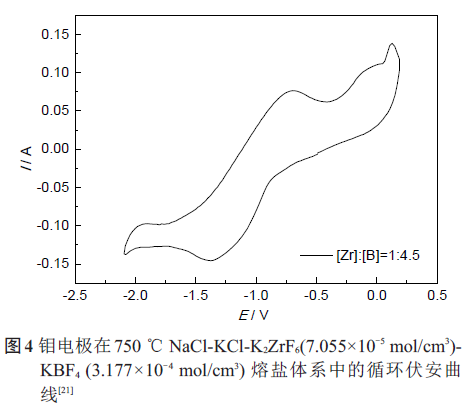
增加體系中KBF4的濃度,將Zr 和B的摩爾比例降低至1∶4.5,其循環伏安曲線如圖4 所示。可以看出曲線形狀發生了很大的變化,在還原過程中只出現了一個較寬的還原峰,峰電位在-1.4 V左右,這可能是因為B(III) 的去極化作用使得Zr(IV) 的還原峰變弱,Zr(IV) 和B(III) 的還原及ZrB2的生成都合并成如下的總反應:
![]()
目前,關于熔鹽電沉積制備ZrB2的相關應用研究較少。ZrB2在耐高溫抗氧化方面具有優良性能,是一種非常有應用前景的非燒蝕型超高溫防護材料。但是,ZrB2在1400 ℃以上的溫度服役時,氧化生成的液態B2O3開始大量蒸發,使氧化層失去保護性。為了解決上述問題,通常向ZrB2中引入含硅的添加相如SiC、Si3N4、MoSi2、ZrSi2等來提高其抗高溫氧化性能。因此,可以在制備ZrB2的熔鹽體系中加入含硅的活性物質,嘗試Zr-Si-B的三元共沉積,并研究其在高溫下的氧化行為。
此外,對ZrB2涂層的應用研究基本針對耐磨性、抗高溫氧化等方面,對其抗熔融金屬腐蝕方面的應用鮮有報道,而絕大多數的硼化物在熔融金屬中能夠保持穩定。Wang嘗試將熔鹽電沉積制備的ZrB2涂層應用于耐熔融金屬腐蝕,結果表明,ZrB2可以有效保護基體材料免受熔融金屬的侵蝕。因此,可以進一步深入研究涂層對熔融金屬腐蝕的防護性能和機理,探究ZrB2作為耐熔融金屬腐蝕備選材料的可能性。
3 結語
隨著對ZrB2研究的不斷深入,其應用也不斷拓寬,然而有關ZrB2的制備還存在許多值得研究和有待解決的問題。與其他ZrB2的制備方法相比,熔鹽電沉積法具有電流效率高、電解速度快、電鍍能力強等優點,且適用于制備與基體結合良好的涂層材料。因此,利用熔鹽電沉積法制備ZrB2具有廣泛的應用前景。目前,關于熔鹽電沉積法制備ZrB2已有不少研究報道,但大多都集中于粉體材料的制備,而對涂層制備工藝缺乏系統性研究。另外,有必要對以下幾個關鍵問題進行深入探討:
(1) 研究用于制備ZrB2的各類熔鹽體系的物理化學性質(如初晶溫度、密度、粘度、電導率等),為熔鹽體系及反應條件的選擇提供理論指導。
(2) 研究由鋯離子及硼離子組成的復雜陰離子的電化學還原機制,并發展多電子轉移過程的實現和控制原理。
(3) 探索通過工藝參數的調控實現對產物ZrB2類型(如粉末、枝晶、涂層、單晶等) 的控制。
更多關于材料方面、材料腐蝕控制、材料科普等方面的國內外最新動態,我們網站會不斷更新。希望大家一直關注中國腐蝕與防護網http://www.ecorr.org
責任編輯:王元
《中國腐蝕與防護網電子期刊》征訂啟事
投稿聯系:編輯部
電話:010-62313558-806
郵箱:fsfhzy666@163.com
中國腐蝕與防護網官方 QQ群:140808414
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《中國腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62313558-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護網官方QQ群:140808414





