一、鎖志剛(哈佛大學)
擠出打印是一種很有前途的快速成型方法,但現有的方法不能滿足基本要求:打印水凝膠和彈性體的整體結構,按任意順序,具有很強的附著力。對此問題,哈佛大學鎖志剛教授團隊與西安交通大學唐敬達實驗室合作共同提出一種軟結構3D打印的強韌粘接技術,實現了具有超強界面粘接的水凝膠/彈性體親疏水異質結構的打印1。
圖1-打印水凝膠和彈性體整體結構的方法示意圖
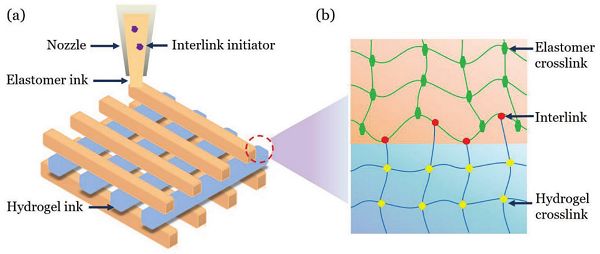
研究人員將聯接引發劑溶于彈性體材料中,分別調節彈性體預聚液和水凝膠預聚液的粘度,將兩者以任意順序3D打印在一起,然后引發聚合反應,形成具有強韌粘接的水凝膠/彈性體復合體。該方法不同于常用的表面改性,采用本體改性的策略,可為可拉伸器件、軟機器制備以及其它異質材料的復合3D打印提供一種通用的解決方法,如圖1。即在印刷打印過程中,每一種材料的墨水都在壓力梯度下流過噴嘴,但在重力和毛細作用下仍能保持形狀。固化過程中形成共價鍵,將單體單元連接成聚合物鏈,將聚合物鏈交聯到水凝膠和彈性體的聚合物網絡中,并將兩個聚合物網絡連接成一個整體結構。該方法通過在其中一種油墨中添加一種鏈接引發劑,將水凝膠網絡和彈性體網絡共價連接起來。黏附能在5000 J /m 2以上。打印出來的變形結構能夠經受住腫脹,而打印出來的人造軸突能夠經受住錘子的反復擊打。這種方法為開發廣泛應用于醫學和工程的軟設備開辟了道路。研究團隊將相關研究成果以“Printing Hydrogels and Elastomers in Arbitrary Sequence with Strong Adhesion”為題發表在國際著名期刊Advanced Functional Materials上。
柔性可拉伸材料(高彈體、凝膠等)在可拉伸電子器件、軟體機器人、藥物釋放和組織再生等領域有著廣泛的應用前景。大多數應用場景需要可拉伸材料具有低滯后性和高韌性--即材料在正常工作范圍內的拉伸和恢復過程中耗散較少的能量,當出現裂紋時在裂紋尖端區域耗散較多的能量以阻止裂紋的擴展。但是,材料的韌性和滯后性通常具有正相關性,從而不能同時滿足以上要求。例如,單聚合物網絡的高彈性彈性體或水凝膠具有低滯后和低韌性。單一網絡通常通過添加填料或者加入第二層網絡引入犧牲鍵來增韌,但犧牲鍵的斷裂和重建可能會導致明顯的滯后。從而使其無法應用到軟體機器人、傳感器和制動器等器件中。并且不管引入的犧牲鍵是否能自修復,這一類韌性材料的疲勞閾值都遠低于其斷裂韌性。
圖2-具有不同網絡結構的可拉伸材料的韌性和滯后性
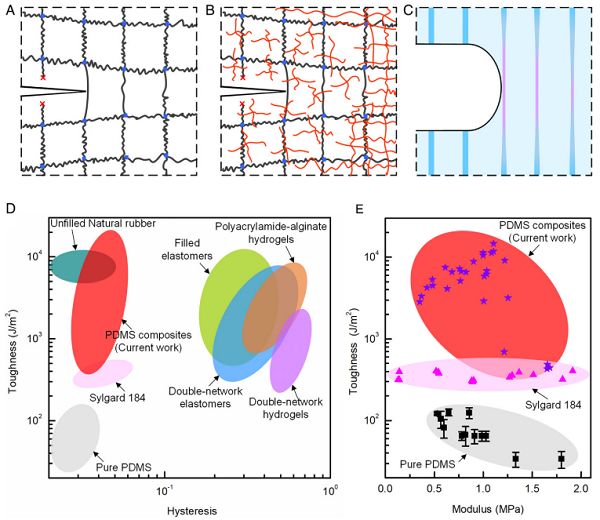
針對這一問題,美國哈佛大學鎖志剛教授團隊提出了一種打破韌性和滯后相關性,同時實現高韌性和低滯后性的設計原理2。利用這一工作原理,通過制備低彈性模量基體和高彈性模量纖維的復合材料,它破壞了韌性與滯后的關系,實現了高韌性和低滯后。復合材料保留了較低的滯后,但是具有較高的韌性(10000 J/m2)和抗疲勞性能。通過實驗和計算,確定了大模量對比降低了裂紋前沿的應力集中,強附著力使纖維與基體結合,抑制了纖維與基體之間的滑移。高韌性、低滯后的可拉伸材料為高循環、低功耗的軟機器人和軟人機界面的創造提供了機會。如圖2,在裂紋尖端,纖維和基體的高模量比能顯著降低裂尖附近的應力集中,使一大段纖維被高度拉伸。當纖維斷裂時,整個高度拉伸區域內的彈性能被釋放。這一過程類似于單一聚合物網絡的斷裂過程。但是在單一聚合物網絡中,只有裂尖的一層分子鏈被高度拉伸,當裂紋擴展時,存儲在這一層分子鏈中的彈性能被釋放。而復合材料中的高度拉伸區域的尺寸高出分子鏈長度數個數量級,從而實現高韌性。只要基體和纖維材料具有低滯后,并且界面粘接足夠強,合成的復合材料就能保持低滯后性。同時材料的抗疲勞性能也能得到顯著提升。研究團隊將相關研究成果以“Stretchable materials of high toughness and low hysteresis”為題發表在國際著名期刊PNAS上。
近年來,水凝膠基軟器件得到了廣泛的發展。例如,軟機器人,類皮膚傳感器,可拉伸光纖,透明摩擦發電機,和可拉伸電離能器件。這些應用的工作條件涉及長時間的重復機械載荷,因此水凝膠不僅需要長時間維持其功能,而且需要長時間保持良好的機械強度和可拉伸性。但是,所有的水凝膠都存在不同程度的空洞、裂紋、雜質等缺陷,易發生斷裂。由此,大多數堅韌的水凝膠都是通過吸收破壞犧牲鍵的巨大能量損耗而設計的。然而,這些水凝膠在長時間的循環載荷作用下仍然會斷裂,甚至出現小的裂紋。
圖3-制備了具有PVA晶體結構的對缺陷不敏感的PAAm-PVA-S水凝膠
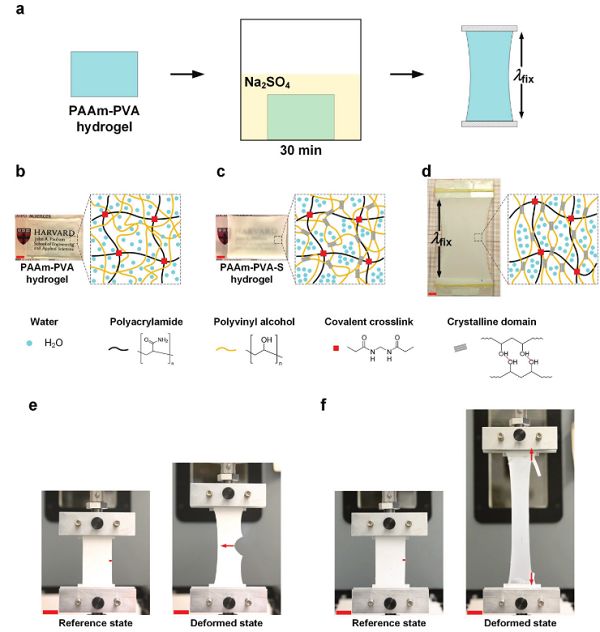
基于此,哈佛大學鎖志剛教授團隊提出了靜載和循環載荷作用下對裂紋不敏感的水凝膠的工作原理。該設計使水凝膠中的聚合物鏈在分子水平上對齊,以偏轉裂紋3。為了證明這一原理,以聚丙烯酰胺和聚乙烯醇為原料,制備了一種晶域排列整齊的水凝膠,如圖3。當水凝膠在準直方向拉伸時,初始缺陷裂紋偏轉,沿加載方向傳播,將材料剝離下來,水凝膠又變得完美無瑕。這種水凝膠對已經存在的缺陷不敏感,即使在一萬多次加載循環下也不敏感。通過實驗和斷裂力學計算,確定了各向異性達到裂紋撓度的臨界程度。并且該原理可推廣到其它水凝膠體系。研究團隊并將相關研究成果以“Flaw-Insensitive Hydrogels under Static and Cyclic Loads”為題發表在著名期刊Macromolecular Rapid Communication上。
二、趙選賀(麻省理工學院)
生物電子與人體的交互作用,包括電刺激和神經活動的記錄,是神經科學與工程、診斷、治療、可穿戴和可植入設備等領域快速發展的基礎。由于軟的、濕的和活的生物組織與硬的、干的和合成的電子系統之間的內在差異,在這兩個不同領域之間開發更兼容、更有效和更穩定的接口一直是科學和技術領域中最艱巨的挑戰之一。近年來,水凝膠因其與生物組織的相似性以及在電氣、機械和生物功能工程方面的多功能性,成為下一代生物電子界面的一種有前途的候選材料。
圖4-水凝膠可以在生物學和電子學之間架起橋梁,為生物電子學的應用提供廣闊前景
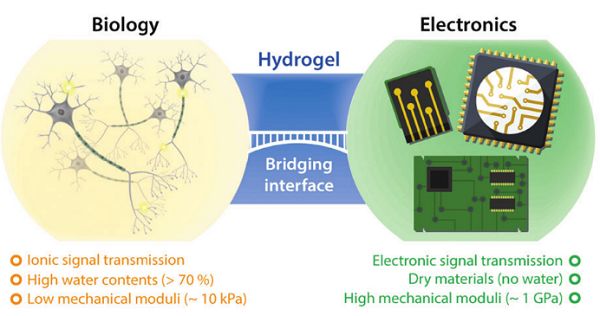
由此,麻省理工學院趙選賀研究團隊首次提出水凝膠是人機界面的最理想載體之一,系統定義了水凝膠生物電子學的基本原理和材料設計原則,給出了現有的水凝膠電子材料的例子,并建議了水凝膠生物電子學未來發展的方向4。如圖4,論文中主要綜述了(i)組織-電極相互作用的基本機理,(ii)水凝膠與人體生物電氣界面的獨特優勢,(iii)生物電子學水凝膠發展的最新進展,以及(iv)未來水凝膠生物電子學設計的合理指南。水凝膠生物電子學的進步將為生物學和電子學的緊密結合帶來前所未有的機遇,有可能模糊人類和機器之間的界限。研究團隊將特邀綜述論文以“Hydrogel bioelectronics”為題發表在國際頂級期刊Chemical Society Reviews上。
在現代的醫療技術手段中,與生物體相互作用的裝置通常是由金屬、硅、陶瓷和塑料制成。而為了長期監測或治療,植入此類設備通常是侵入性程序。這樣會給病人或醫生帶來相當大的痛苦和麻煩。比如做胃鏡,有時甚至需要麻醉,如此給病人帶來極大的痛苦和傷害,并且這些通常的可服用器件大多受限于胃腸運轉時間,最多在消化道滯留1-2天,不能長期監測體征。而水凝膠具有良好的機械順應性和生物相容性,為人機交互提供了新的機遇。使用水凝膠來完成胃的駐留需要水凝膠膨脹得非常快,并且隨著時間的推移能夠承受胃的機械力。然而,現有的水凝膠中,高膨脹比、高膨脹速度和不具有長期保持強度的特點。
圖5-水凝膠器件的設計方案
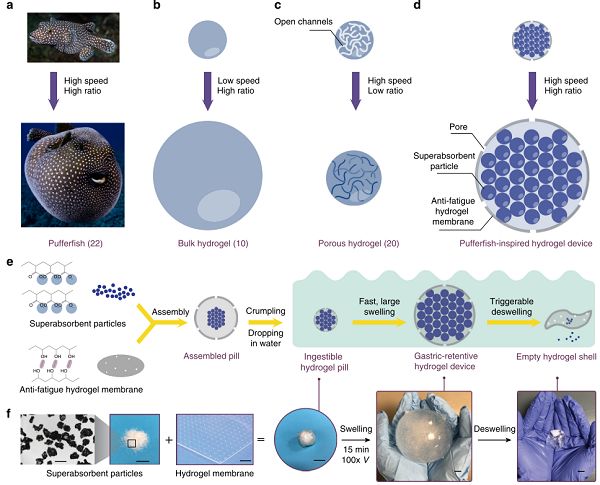
基于此,麻省理工學院趙選賀研究團隊首次提出并實現可食用水凝膠電子設備,實現了吃一顆“果凍”,就可以長期監控核心體征例如溫度、pH、進食和吃藥情況、以及消化道病變30天5。研究團隊的解決方案是根據河豚的啟發,將水凝膠設計成膠囊型,如圖5,該膠囊由兩種材料的水凝膠組成。膠囊內部是聚丙烯酸鈉,一種超吸水水凝膠顆粒,能夠實現快速吸水和大體積溶脹。口服水凝膠膠囊只有一粒藥丸大小,口服后在胃中快速吸水膨脹體積100倍左右,能夠長期滯留在胃腔內部。該水凝膠器件在胃中可以同時保持柔軟性和抗疲勞性:一方面,它能夠實現與胃腔膜的柔性接觸,避免磨損胃腔,引起胃潰瘍等不良排異反應;另一方面,能夠長期抵抗胃腔的機械蠕動和胃酸的化學腐蝕。此外,通過在水凝膠中嵌入電子傳感器 (例如溫度傳感器),可以持續監測核心體征(例如胃內溫度)長達一個月。研究團隊將相關研究成果以“Ingestible hydrogel device”為題發表在國際頂級期刊Nature Communications上。
長期穩定高效的人機界面交互及融合過程中要求界面材料同時具備高電導率、優異的穩定性、良好的生物兼容性以及與人體組織匹配的力學性能。導電聚合物水凝膠是實現人體和生物電子設備完美兼容的理想界面材料之一,然而現有導電水凝膠很難兼顧滿足應用需求的電學、力學、生物兼容性及穩定性。 導電聚合物的水凝膠,特別是聚(3,4-乙二氧噻吩):聚苯乙烯磺酸鹽(PEDOT:PSS),由于其良好的電氣和機械性能,為傳感和刺激生物組織提供了一個有前途的電氣界面。
圖6-純(PEDOT:PSS)水凝膠的制備圖
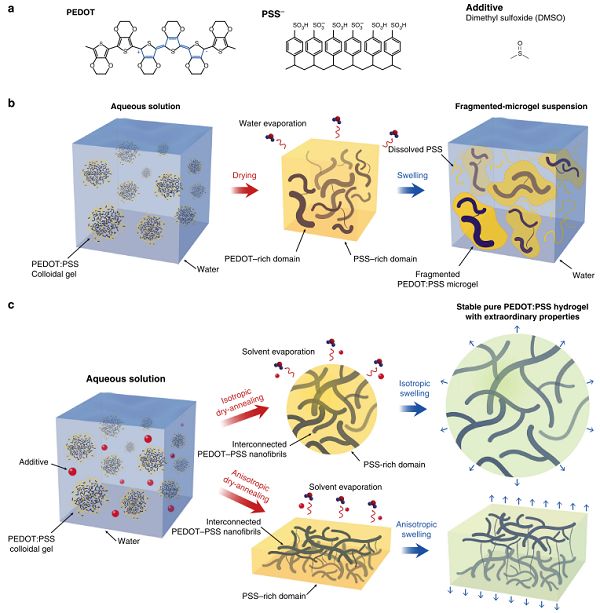
由此,麻省理工學院趙選賀研究團隊提出形成穩定的導電聚合物納米纖維互聯網絡是獲得高性能導電聚合物水凝膠的關鍵,同時發明了一種簡單有效的方法,用來設計高性能聚(3,4-亞乙二氧基噻吩):聚(苯乙烯磺酸鹽) (PEDOT:PSS)水凝膠6,如圖6。所報道的純PEDOT:PSS水凝膠電導率可達40 S/cm,力學性能良好(拉斷伸長率大于35%,楊氏模量2 MPa),同時具有良好的電學、電化學及力學穩定性。純PEDOT:PSS導電水凝膠的制備有助于加深人們對高性能導電水凝膠合理設計的理解,優越的機械、電氣和電化學穩定性和可調濕的生理環境中各向同性和各向異性腫脹,為新一代生物電子產品制作及應用提供了更佳的材料平臺。研究團隊將相關研究成果以“Pure PEDOT:PSS hydrogels”為題發表在國際頂級期刊Nature Communications上。
水凝膠在設備和機器中的新應用要求水凝膠在循環機械載荷下保持韌性和強度。當水凝膠在單周機械載荷作用下能夠抵抗斷裂時,這些增韌凝膠在多周載荷作用下仍然會發生疲勞斷裂。水凝膠是人造軟骨、關節和椎間盤的理想替代材料。這些應用要求水凝膠具備循環加載下的抗疲勞性能。現在報道的合成水凝膠的疲勞閾值在1到100 J/m2之間,因而設計具有抗疲勞斷裂的水凝膠仍是軟材料領域的一大難題。
圖7-抗疲勞斷裂水凝膠的設計原理
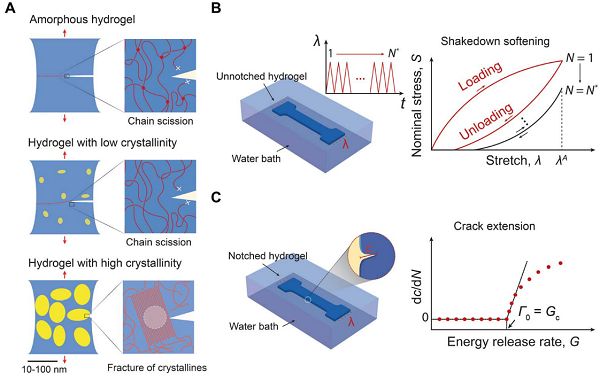
人體的韌帶肌肉大概每年承受幾百萬次兆帕級的應力,并且保持疲勞閾值在1000 J/m2以上。韌帶肌肉中膠原蛋白的有序晶區可能是它們抗疲勞的原因。受生物組織啟發,麻省工學院的趙選賀研究團隊提出,設計抗疲勞斷裂水凝膠需要使單位面積能量的疲勞裂紋遇到斷裂能遠高于一層聚合物鏈的物質7。例如納米晶域等,如圖7。并研究證明,控制水凝膠中結晶度的引入可以顯著提高其抗疲勞斷裂性能。膨脹狀態下結晶度為18.9%的聚乙烯醇(PVA)疲勞閾值可超過1000 J/m2,抗疲勞設計原理可以用來指導開發具有長期使用價值的水凝膠設備和器械。研究團隊并將相關研究成果以“Anti-fatigue-fracture hydrogels”為題發表在國際著名期刊Science Advances上。
三、江雷(中國科學院院士)維度異質結構體系中的范德華整合策略
隨著科技和社會的發展,海洋開發變得越來越必要和頻繁。在這一過程中,海洋生物污損現象十分嚴重,主要是指海洋生物在材料表面附著和聚集。從而帶來不利的影響。比如,會因此增大船只的阻力,導致航速下降,油耗增加;加速材料老化腐蝕等問題,其造成了的大量的經濟損失。為了克服這些困難,已經采取了許多措施。目前的海洋防污策略大部分還屬于無差別毒殺,不僅效率低,而且還可能導致毒物通過生物鏈富集再被人食用。因此,發展一種高效、環保的海洋防污方法仍是當務之急。其中硅藻的粘附是海洋生物污染過程中的最嚴重的問題之一。
圖8-SOSA凝膠制備示意圖
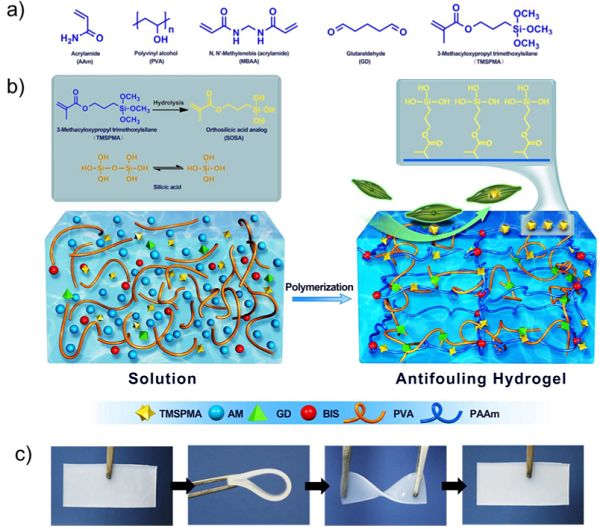
基于此,中科院理化所江雷院士研究團隊和海南大學郝萬軍教授合作首次提出利用原硅酸類似物誘導硅藻攝取,進而干擾硅藻正常的生命活動,最終實現抗硅藻附著8。由于硅藻合成二氧化硅外殼需要大量攝取硅酸,而人和其他海洋生物并不吸收硅酸。針對這一差異,研究團隊使用一種人工合成的原硅酸類似物(SOSA),如圖8。3-甲基丙烯酰氧基丙基三甲氧基硅烷(TMSPMA),通過共聚固定在凝膠中并水解得到帶有三個硅羥基的SOSA,制得柔韌的抗硅藻附著凝膠。在水凝膠中,SOSA具有與原硅酸非常類似的三個Si-OH,并且還有一個在水中穩定的C-Si鍵。當這些物質被凝膠表面的污損硅藻攝取之后,由于其中的C-Si鍵相對比較穩定,不會像原硅酸一樣縮合形成二氧化硅外殼,所以硅藻的正常生命活動將出現紊亂,最終影響硅藻的附著行為。詳細研究表明,含SOSA的水凝膠具有良好的抗硅藻粘附性能,SOSA的抗硅藻作用是有針對性的,只有試圖粘附在SOSA水凝膠表面的生物體受到影響。SOSA水凝膠具有高效、環保的特性,在海洋防污方面具有廣闊的應用前景。研究團隊將相關研究成果以“Preventing diatoms adhesion using a hydrogel with orthosilicic acid analog as deceptive food”為題發表在國際著名期刊Journal of Materials Chemistry A上。
在生命體細胞信號的傳遞中,離子分布調控在生物轉變中是十分重要的。如維持細胞的離子平衡,信號轉導以及能量采集。納米通道門控機制可以通過各種觸發物質來實現離子分布的調控,如pH、電壓、溫度以及光等的刺激都能實現控制離子或分子在人工離子通道中的傳輸及分布。近年來DNA納米技術發展迅速,特別是核酸在外界刺激下的可逆轉變響應及其豐富的刺激源,使DNA納米技術十分適用于離子通道門控機制的實現。然而,由于DNA門控納米通道的單層結構中存在少量的DNA基質,以及納米通道的尺寸較小,導致其離子轉運選擇性(整流比)和效率(離子通量)有限,這是近年來DNA門控納米通道研究的不足之處。此外,在現有的DNA納米通道中,陰陽離子傳輸的方向并不能得到控制。因此,為了提高DNA納米通道中離子傳輸能力,實現可重構的DNA結構設計是必要的。
圖9-離子通道制備過程以及DNA水凝膠網絡形成和過渡過程示意圖
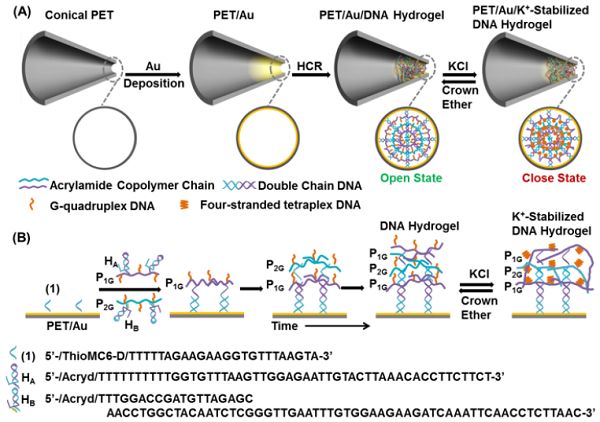
由此,中科院理化所江雷院士團隊和北化所的田野副研究員以及以色列耶路撒冷希伯來大學的I. Willner教授合作首次開發了基于智能DNA水凝膠刺激響應的離子通道9,如圖9。DNA水凝膠是一種具有空間負電荷的三維網絡結構,與納米通道中存在的其他響應分子不同,其離子通量和整流比均有顯著提高。通過K+離子和冠醚的循環處理,DNA水凝膠狀態可以在剛性較差的網絡和剛性較差的網絡之間可逆切換,從而提供了納米通道的門控機制。基于DNA水凝膠的結構和pH刺激,可以精確控制陽離子或陰離子的轉運方向,實現多個門控特性。同時,水凝膠中的G-quadruplex DNA(G-quadruplex 四聯體,是一種由富含鳥嘌呤的核酸序列所構成的四股型態)可能被其他刺激反應性DNA分子、肽或蛋白質所取代,這為智能水凝膠提高納米通道的功能開辟了一條新的途徑。研究團隊將相關研究成果以“Smart DNA Hydrogels Integrated Nanochannels with High Ion Flux and Adjustable Selective Ionic Transport”為題發表在國際頂級期刊Angewandte Chemie-International Edition上。
參考文獻
1.Yang, H.; Li, C.; Yang, M.; Pan, Y.; Yin, Q.; Tang, J.; Qi, H. J.; Suo, Z., Printing Hydrogels and Elastomers in Arbitrary Sequence with Strong Adhesion. Advanced Functional Materials 2019, 1901721.
2.Wang, Z.; Xiang, C.; Yao, X.; Le Floch, P.; Mendez, J.; Suo, Z., Stretchable materials of high toughness and low hysteresis. Proceedings of the National Academy of Sciences of the United States of America 2019,116(13), 5967-5972.
3.Bai, R.; Yang, J.; Morelle, X. P.; Suo, Z., Flaw-Insensitive Hydrogels under Static and Cyclic Loads. Macromol Rapid Commun 2019, e1800883.
4.Yuk, H.; Lu, B.; Zhao, X., Hydrogel bioelectronics. Chemical Society reviews 2019,48(6), 1642-1667.
5.Liu, X.; Steiger, C.; Lin, S.; Parada, G. A.; Liu, J.; Chan, H. F.; Yuk, H.; Phan, N. V.; Collins, J.; Tamang, S.; Traverso, G.; Zhao, X., Ingestible hydrogel device. Nature communications 2019,10(1), 493.
6.Lu, B.; Yuk, H.; Lin, S.; Jian, N.; Qu, K.; Xu, J.; Zhao, X., Pure PEDOT:PSS hydrogels. Nature communications 2019,10(1), 1043.
7.Shaoting Lin, Xinyue Liu, Ji Liu, Hyunwoo Yuk, Hyun-Chae Loh, German A. Parada, Charles Settens, Jake Song, Admir Masic, Gareth H. McKinley, Xuanhe Zhao., ScienceAdvances. 2019;5 : eaau8528.
8.Chen, W.; Hao, D.; Guo, X.; Hao, W.; Jiang, L., Preventing diatom adhesion using a hydrogel with an orthosilicic acid analog as a deceptive food. Journal of Materials Chemistry A 2018,6(39), 19125-19132.
9.Wu, Y.; Wang, D.; Willner, I.; Tian, Y.; Jiang, L., Smart DNA Hydrogel Integrated Nanochannels with High Ion Flux and Adjustable Selective Ionic Transport. Angew Chem Int Ed Engl 2018,57(26), 7790-7794.
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《中國腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62313558-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護網官方QQ群:140808414





