1.水凝膠機械性能及機理研究
單一聚合物凝膠網絡具有低滯后性和低韌性(圖1A)。目前常用的增韌策略是在第一層主網絡中添加填充顆粒或第二層弱聚合物網絡以引入犧牲鍵來提高其韌性(圖1B),但會顯著提高其滯后性,從而限制了它的應用。
圖1-具有不同網絡結構的可拉伸材料的韌性和滯后性
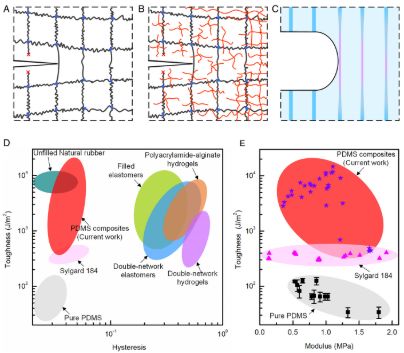
哈佛大學鎖志剛教授課題組提出了一種打破韌性和滯后相關性,同時實現高韌性和低滯后性的設計原理。該原理利用具有高模量的纖維和低模量的基體通過強界面粘接形成復合材料(圖1C)。在裂紋尖端,纖維和基體的高模量比能顯著降低裂尖附近的應力集中,使一大段纖維被高度拉伸。當纖維斷裂時,整個高度拉伸區域內的彈性能被釋放。這一過程類似于單一聚合物網絡的斷裂過程。但是在單一聚合物網絡中,只有裂紋尖的一層分子鏈被高度拉伸,當裂紋擴展時,存儲在這一層分子鏈中的彈性能被釋放。而復合材料中的高度拉伸區域的尺寸高出分子鏈長度數個量級,從而實現高韌性。只要基體和纖維材料具有低滯后,并且界面粘接足夠強,合成的復合材料就能保持低滯后性。同時材料的抗疲勞性能也能得到顯著提升。相關成果以“Stretchable materials of high toughness and low hysteresis”為題發表在PNAS上。
鏈接: https://www.pnas.org/cgi/doi/10.1073/pnas.1821420116
隨著水凝膠材料性能的大面積開發以及水凝膠應用的廣泛化,水凝膠會越來越多地被用于挑戰其性能極限的環境。許多應用已經開始要求水凝膠能夠承受長時間的靜態或循環加載。然而水凝膠的疲勞研究仍然處在初期階段。
圖2-水凝膠疲勞癥狀總結
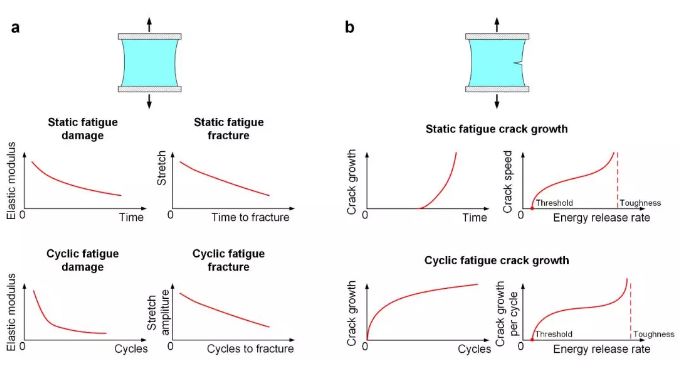
哈佛大學鎖志剛教授課題組首次在水凝膠疲勞研究領域發表了綜述文章,指出了水凝膠的疲勞來源于三個方面的綜合作用:水凝膠的化學組成,凝膠網絡的拓撲結構,以及凝膠能量耗散的力學機理,(如圖2)。相關論文以“Fatigue of Hydrogels”為題發表在European Journal of Mechanics - A/Solids上。
鏈接:
https://doi.org/10.1016/j.euromechsol.2018.12.001
熱致水凝膠有廣闊的醫學應用前景。隨溫度升高,一些兩親性嵌段共聚物的水溶液呈現可逆的溶膠-凝膠轉變。如果轉變溫度介于室溫和體溫之間,可在室溫或更低溫度下與藥物或細胞混合,并實現可注射性;一旦注射進入體內,在體溫刺激下原位物理凝膠化,自動包裹藥物或細胞,該過程不依賴于化學反應。但是,該體系的凝膠結構與物理凝膠化機理尚不夠明晰,導致對其調控手段缺乏理論指導。
圖3-熱致水凝膠的組裝過程示意圖
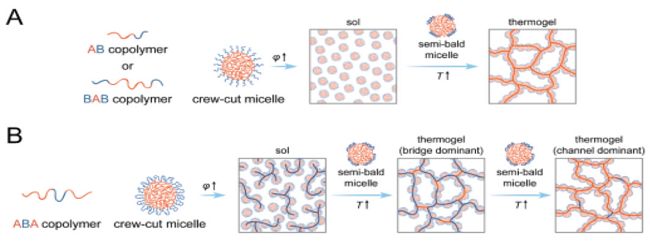
復旦大學丁建東教授課題組利用計算機模擬與實驗相結合的方法,對PEG/PLGA熱致水凝膠的凝膠結構及凝膠化機理進行了系統研究。在之前的工作中,該課題組曾探討了結構簡單的二嵌段共聚物mPEG-PLGA(AB型)水體系的凝膠化機理,提出半禿膠束并進行了詳細解釋。(如圖3)通過與AB類型,BAB類型嵌段共聚物水體系的凝膠化行為進行對比,揭示了更具應用前景結構也更加復雜的PLGA-PEG-PLGA (ABA類型)嵌段共聚物的凝膠結構與凝膠化機理。低溫溶膠狀態時,嵌段共聚物自組裝形成大量平頭膠束,它們之間會形成大量親水的PEG “橋”。隨著溫度的升高,PEG的溫敏性導致膠束收縮。在平頭膠束中,膠束核非常大,暈相對較薄,所以暈的收縮導致膠束核部分暴露于水中而形成半禿膠束。半禿膠束的不穩定而發生聚集以減少核暴露面積,最終形成疏水隧道。由此,少量的疏水隧道就可以與大量的橋結構(主要交聯點)一起形成網絡,表現為凝膠(Gel-1);隨著溫度進一步升高,更多的疏水隧道形成,并成為體系的主要物理交聯點,凝膠進入Gel-2狀態。相關成果以“Thermogelling of Amphiphilic Block Copolymers in Water: ABA Type versus AB or BAB Type”為題發表在Macromolecules上。
鏈接:
https://pubs.acs.org.ccindex.cn/doi/pdf/10.1021/acs.macromol.9b00534
MXene是二維材料家族中的最新成員之一,是兼具金屬級導電性和豐富表面化學的一種二維層狀結構的金屬碳化物和金屬氮化物材料,在能量轉化與存儲、電磁屏蔽、傳感等眾多領域表現出極大的應用潛力。然而,團聚、堆疊問題一直是制約MXene發展的重要因素之一。
圖4- Ti3C2Tx三維水凝膠的制備流程
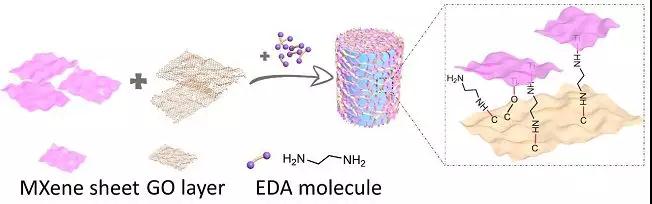
天津大學化工學院Nanoyang課題組的楊全紅教授、陶瑩副教授和法國圖盧茲大學的PatriceSimon教授團隊合作,提出氧化石墨烯(GO)引導Ti3C2Tx液相組裝構建三維水凝膠的新策略與組裝機制。Ti3C2Tx水凝膠的制備流程和組裝機制如圖4所示,在乙二胺等還原劑輔助下,僅微量的GO即可與Ti3C2Tx交聯并引導Ti3C2Tx納米片與GO片層共同自組裝,不僅獲得力學性質優異的Ti3C2Tx水凝膠,而且實現了低濃度Ti3C2Tx分散液(1 mg/mL)的凝膠化。該研究成果以“3D Macroscopic Architectures from Self-Assembled MXene Hydrogels”為題發表在Advanced Functional Materials上。
鏈接:
https://onlinelibrary.wiley.com/doi/pdf/10.1002/adfm.201903960
2.水凝膠結構多功能化(3D打印)
近年來,基于水凝膠-彈性體的親疏水結構取得明顯進展,在可拉伸電子、軟體機器人、摩擦發電機等領域有著廣泛的應用前景。3D打印技術的引入將使得這一領域在制備技術上得到進一步的提升。然而,現有的親疏水結構在打印過程中尚且不能滿足以下基本要求:以任意順序打印具有良好粘接性能的水凝膠/彈性體復合結構。
圖5-水凝膠/彈性體復合打印的粘接示意圖
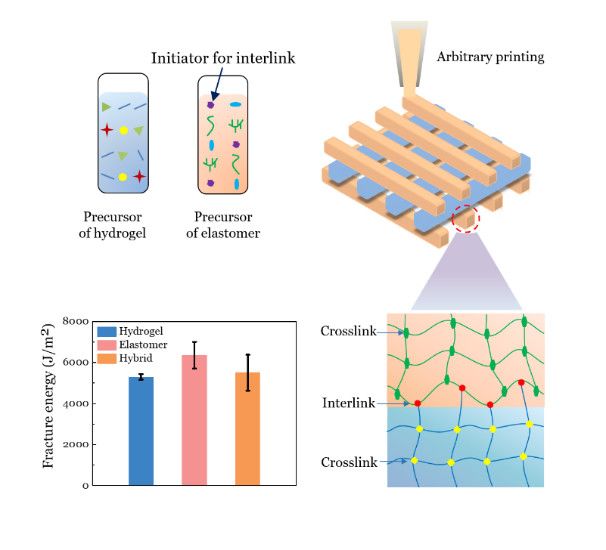
哈佛大學鎖志剛教授課題組與西安交通大學合作提出一種軟結構3D打印的強韌粘接技術,實現了具有超強界面粘接的水凝膠/彈性體親疏水異質結構的打印。研究人員將聯接引發劑溶于彈性體材料中,分別調節彈性體預聚液和水凝膠預聚液的粘度,將兩者以任意順序3D打印在一起,然后引發聚合反應,形成具有強韌粘接的水凝膠/彈性體復合體。如圖5,該方法不同于常用的表面改性,采用本體改性的策略,可為可拉伸器件、軟機器制備以及其它異質材料的復合3D打印提供一種通用的解決方法。該研究成果以“Printing Hydrogels and Elastomers in Arbitrary Sequence with Strong Adhesion”為題發表在Advanced Functional Materials上。
自然界中大多數生物組織是水凝膠,其表面的微/納米結構在許多自然系統中起著重要作用。受自然生物材料的啟發,構建具有結構化功能表面的水凝膠材料已成為研究人員解決人們對新型功能材料需求的最具前景的方案之一。
圖6-多尺度結構化功能水凝膠材料的額制備示意圖
北京航空航天大學劉明杰教授課題組報道了一種可大規模制備多尺度結構化功能表面的水凝膠材料的簡易方法。該方法依賴于聚合物鏈擴散與隨后的凍結誘導凝膠化和微相分離過程之間的相互作用。如圖6,該策略是通過兩個連續的過程:1、擴散驅動的混合過程;2、冷凍誘導的凝膠化和微相分離。前者形成擴散層,后者在此擴散層中產生結構,然后冷凍使得聚合物凝膠化到微相分離,最終固定凝膠表面的微/納米結構。由于該動態過程(即凝膠化和擴散作用)是各種聚合物材料的通用動態特性,因此本方法具有一定普適性。基于此方法,通過控制界面擴散區的溫度梯度和擴散區域,可制備具有梯度結構和圖案化的凝膠表面。由此形成的微/納米結構表面不僅使得凝膠材料具有抗脫水作用,而且可作為毛細管系統發揮輸液作用。這項研究將為大規模開發多種功能化表面的凝膠材料指明了新的研究方向。該項研究成果以“Diffusion–Freezing-Induced Microphase Separation for Constructing Large-Area Multiscale Structures on Hydrogel Surfaces”為題發表在Advanced Mterials上。
鏈接:
https://onlinelibrary.wiley.com/doi/10.1002/adma.201808217
3.電子柔性器件構建
隨著電化學儲能技術的快速發展,越來越多的研究者開始關注如何提高器件的安全性。發展非液態電解質能有效的解決傳統液態電解質容易泄露,封裝困難等問題,是目前提高電化學儲能器件安全性的重要研究方向。
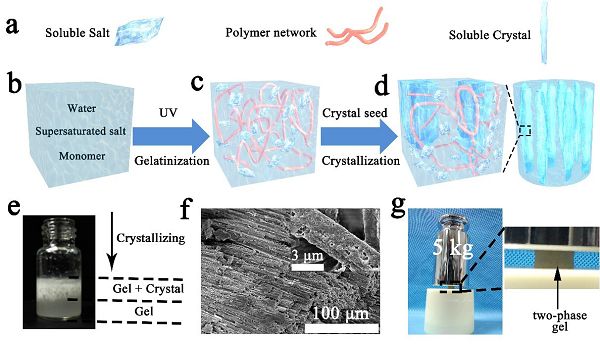
圖7-結晶性聚合物凝膠電解質的制備原理示意圖

同濟大學王啟剛教授課題組利用可溶鹽(如醋酸鈉等)過飽和析晶的原理在普通的水凝膠基礎上開發了一種全新的“結晶型聚合物凝膠電解質”,并研究了其在超級電容器中的性能。如圖7,首先是通過加熱在前驅液中溶解過量的鹽,并形成含有過飽和鹽的水凝膠電解質;之后加晶種引發水凝膠內部的過飽和鹽定向結晶,得到結晶型凝膠電解質。與其它非液態電解質相比,結晶型凝膠展現了優異的綜合性能。結晶型凝膠電解質的最大壓縮模量可以達到474.24 MPa,是水凝膠電解質的近26000倍,確保了儲能器件的機械安全性。離子電導率(>10-3 S/cm)遠高于常規的陶瓷電解質和聚合物電解質。結晶鹽對結晶水的束縛作用,有效抑制了水的電化學活性,電壓窗口可以達到2 V,遠高于普通的水系電解質,提高了能量密度。高濃度的鹽含量能降低電解質冰點,并提高其沸點,使結晶型電解質在?40-80 °C都能正常工作,拓寬了工作溫度范圍。該研究成果以“Dissolution–Crystallization Transition within a Polymer Hydrogel for a Processable Ultratough Electrolyte”為題發表在Adv. Mater上。
隨著鋰離子電池市場應用的快速增長,鋰離子電池的安全性問題日益凸顯。因此,發展固態電解質來替代傳統的易燃液態電解質是從本質上提升鋰離子電池安全性的必由之路。然而,固態電解質的離子導電率偏低是阻礙其實用化的最關鍵因素。
圖8-自修復和高導電率凝膠電解質的制備示意圖
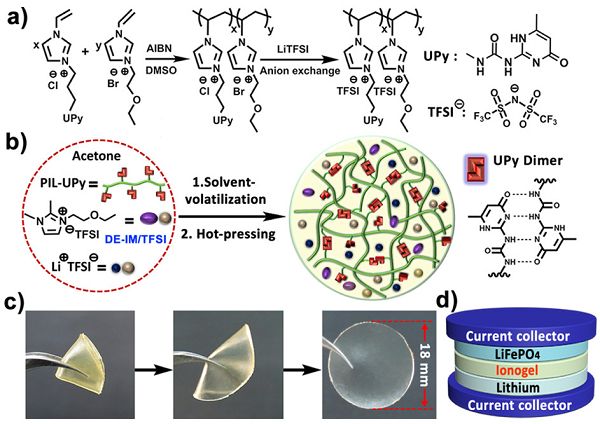
吉林大學孫俊奇教授課題組報道了一種具有自修復性能和高離子導電率的柔性固態凝膠電解質。如圖8,該凝膠電解質由含有2-脲基-4[H]啶酮(UPy)基團的聚離子液體,咪唑類離子液體和鋰鹽(雙三氟甲烷磺酰亞胺鋰)的丙酮溶液經溶劑揮發和熱壓的方法制備而成。該凝膠電解質的離子導電率高達1.41×10-3S/cm,同時表現出良好的柔性、彈性和優異的不可燃燒性質。基于該凝膠電解質組裝的Li|Ionogel|LiFePO4電池表現出了良好的充放電循環性能,該電池在0.2C倍率下循環120周期后的放電容量和庫倫效率分別為147.5mAh g-1和99.7%,這些性能均優于同等條件下以離子液體或傳統的液態電解液作為電解質所組裝的電池。由于該凝膠電解質內部基團間可逆的氫鍵和靜電相互作用,其發生斷裂后可在55℃的條件下自發修復損傷,修復過程亦可在組裝好的電池中原位進行,電池的充放電循環性能能夠得以恢復和保持。該研究成果“Healable,Highly Conductive, Flexible, and Nonflammable Supramolecular Ionogel Electrolytes for Lithium-Ion Batteries”發表在ACS Appl. Mater. Interfaces上。
鏈接:
https://pubs.acs.org.ccindex.cn/doi/10.1021/acsami.9b02182
水凝膠與人體組織具有非常相似“軟”和“濕”的特性,構筑具有各向異性網絡結構的水凝膠材料有望實現在組織工程、人工肌肉等領域的廣泛應用。
圖9-高度有序層狀網絡結構的各向異性水凝膠的制備過程
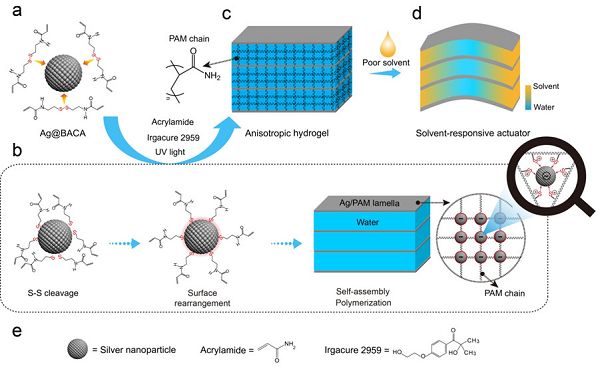
合肥工業大學從懷萍教授和中國科學技術大學俞書宏教授課題組報道了將金屬納米顆粒的自組裝與高分子聚合反應相結合從而構筑具有定向網絡結構的水凝膠。將預功能化的貴金屬銀納米顆粒在紫外光條件下的組裝形為成功引入光誘導自由基聚合反應過程中,構筑了具有高度有序層狀網絡結構的水凝膠。如圖9,銀納米顆粒的組裝體的引入可以大大增強網絡結構的機械性能,同時,動態銀-巰基配位作用的引入可以使凝膠網絡具備優異的自修復性能。且該方法具有一定普適性。該項研究成果“Anisotropic and self-healing hydrogels with multi-responsive actuating capability”發表在Nat. Commun.上。
鏈接:
https://www.nature.com/articles/s41467-019-10243-8
導電水凝膠兼具良好的電學性質,可拉伸彎折的機械性能,與人體有相似的組織結構,因此可以模擬人體肌肉和皮膚的變化,在柔性可穿戴和可植入電子器件方面顯示出巨大前景。然而,如何設計出具有高電導率和自修復能力的柔性導電水凝膠以提高其功能性和使用壽命成為近年來導電水凝膠的研究熱點。
圖10- PANI/PSS-UPy 水凝膠合成相互作用及示意圖。
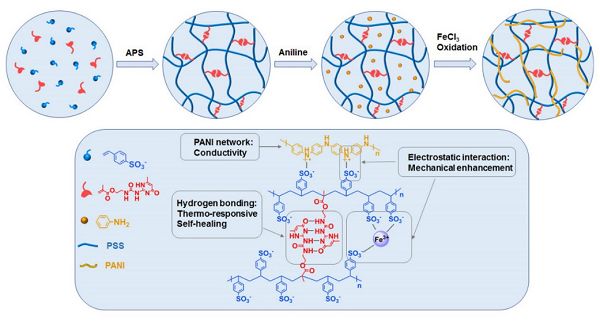
加拿大阿爾伯塔大學曾宏波教授課題組報道了一種具有高電導率,可塑性和快速修復能力的水凝膠應變傳感器。如圖10,首先,將氫鍵基團作為交聯點與苯乙烯磺酸鈉聚合形成第一個柔性水凝膠網絡(PSS-UPy),接著原位引發苯胺的聚合形成第二個剛性的導電聚苯胺網絡(PANI),兩個網絡通過靜電作用緊密結合,同時UPy 基團間可逆的氫鍵作用使凝膠表現出溫度敏感性和自修復性能。該研究成果“Stretchable, Injectable and Self-Healing Conductive Hydrogel Enabled by Multiple Hydrogen Bonding toward Wearable Electronic”發表在Chemistry of Materials上。
鏈接:
https://pubs.acs.org/doi/10.1021/acs.chemmater.9b01239
4.仿生、生物醫用水凝膠
現有的軟組織修復方法都有各自的缺點:容易造成供體部位的缺陷,容易導致排斥反應,導致組織纖維化等。目前還沒有現有材料可以應用于填補軟組織缺陷的“坑”,并同時促進早期血管的生成。因此,研究一種可以實現上述功能的復合材料具有重要的意義。
圖11-納米纖維復合水凝膠的制備過程
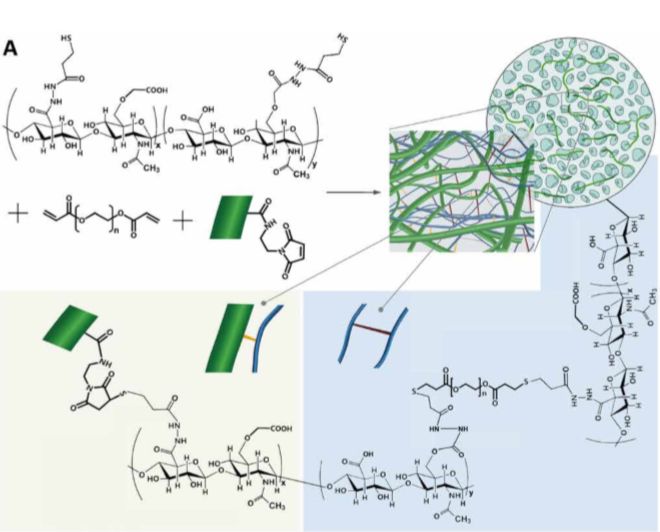
美國約翰霍普金斯醫學院Mao Hai-Quan和整形外科的Justin M. Sacks及Sashank Reddy合作報道了一種納米纖維水凝膠的復合材料,用于解決軟組織修復問題。這種復合材料由透明質酸(HA)水凝膠與電紡聚己內酯(PCL)納米纖維共價連接組成(如圖11)。這種復合設計增加了復合材料的體積孔隙率和細胞滲透率,同時實現了足夠高的儲能模量,使復合材料能夠滿足類似于天然脂肪組織的機械性能。相關論文“Nanofiber-hydrogel composite–mediated angiogenesis for soft tissue reconstruction”發表在Science Translational Medicine上。
鏈接:
https://stm.sciencemag.org/content/11/490/eaau6210
三維細胞培養技術是目前人類再造人體組織和器官的主要手段。與動物神奇的再生能力不同,人體組織和器官的損傷修復離不開組織工程技術的發展,其技術核心是構建細胞培養基質材料,實現受損組織和器官的重建。
圖12-凝膠的制備以及實現“開關”控制培養3D細胞原理示意圖
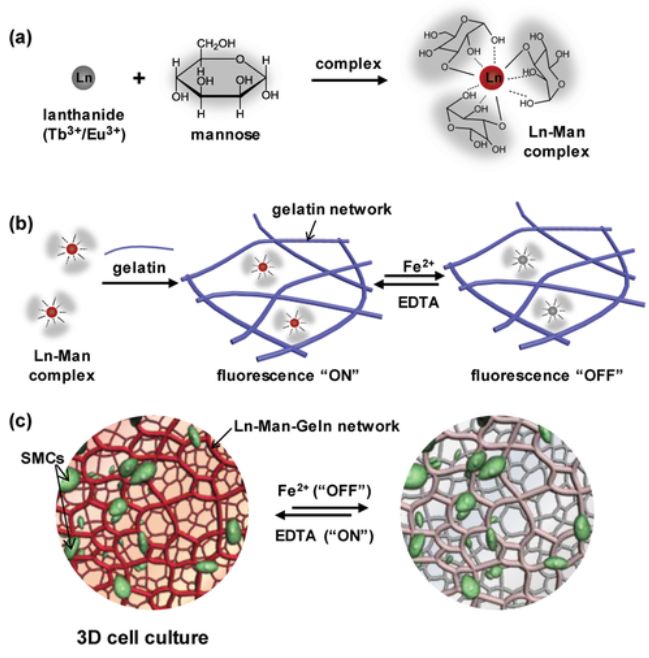
天津大學仰大勇教授世界首創新型細胞培養變色水凝膠,實現在觀測細胞三維培養過程中基質材料熒光的即時可控開關。相關材料和技術已申請中國發明專利。如圖12,這一新材料在生物醫學領域具有巨大的應用潛力,它為細胞提供了一個更加接近體內生存條件的微環境,可作為一種優良的細胞培養基質用于干細胞的三維培養,實現組織修復和器官再生,為造福人類生命健康帶來新的希望。相關研究成果“A Reversibly Responsive Fluorochromic Hydrogel Based on Lanthanide–Mannose Complex”發表在Advanced Science上。
鏈接:
https://onlinelibrary.wiley.com/doi/full/10.1002/advs.201802112
水凝膠在組織工程支架和再生醫學領域也顯示出巨大的應用前景。目前大多數水凝膠體系中應用的光化學反應都需要額外加入光引發劑或光解反應過程中伴有機副產物的產生,這些都為構建細胞3D微環境帶來潛在的生物毒性。因此,亟須尋找更加溫和的光化學反應用于水凝膠3D細胞微環境的構建。
圖13-凝膠的制備示意圖華東理工大學朱麟勇、包春燕教授團隊報道了利用鄰硝基芐醇(NB)光生醛基-亞胺偶聯(PAIL)系列反應來調控3D水凝膠中生物活性分子的表達。該反應過程中除水分子之外不產生任何有機副產物,為光調控3D水凝膠中的生物化學信號提供了一種新的、溫和的策略。進一步通過結合酶刺激降解調控生物物理信號,最終實現水凝膠中3D細胞行為的精準調控(如圖13)。該研究成果“Precise Construction of Cell-Instructive 3D Microenvironments by Photopatterning a Biodegradable Hydrogel”發表在Chem. Mater.上。
鏈接:
https://pubs.acs.org/doi/10.1021/acs.chemmater.9b00706止血材料要實現臨床快速止血需要克服4大挑戰:1.材料需要有較強的濕面組織粘附力;2.合適的力學性能來承受血壓和與周邊組織的擠壓和摩擦;3.有較好的生物相容性;4.操作簡單快速。但目前沒有一款臨床止血產品能夠滿足濕面粘附要求。
圖14-水凝膠制備示意圖浙江大學歐陽宏偉教授課題組開展以人體組織材料為模板仿生研發先進生物材料。膠體方面以人體內最強大的膠體組織---軟骨為標桿,采用軟骨的主要膠原和多糖成分,嫁接華東理工大學朱麟勇教授團隊的交聯技術,合作研發了一種能夠在數秒內完全止住大動脈損傷和心臟穿透傷大出血的仿生水凝膠材料(如圖14)。相關研究論文“A strongly adhesive hemostatic hydrogel for the repair of arterial and heart bleeds”發表在Nature Communications上。
鏈接:
https://www.nature.com/articles/s41467-019-10004-7明膠水凝膠由于其良好的生物相容性、生物降解性、生物活性、來源豐富性而被開發作為3D打印的生物墨水。但傳統的明膠水凝膠由于差的力學性能無法作為承重支架使用。
圖15-用于修復骨軟骨缺損的生物混合梯度支架的3D打印示意圖。
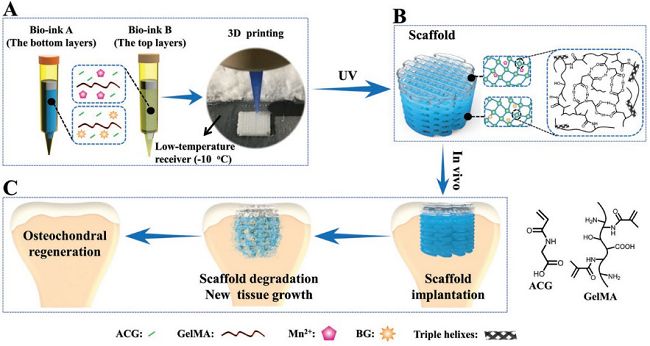
天津大學劉文廣教授和中科院深圳先進技術研究院阮長順副研究員團隊報道了一種新型可生物降解的氫鍵強化明膠水凝膠支架并將其用于骨軟骨再生。如圖15,該梯度水凝膠生物支架由可裂解的聚(N-丙烯酰基-2-甘氨酸)(PACG)和甲基丙烯酸化的明膠(GelMA)(PACG-GelMA)構成,能夠在軟骨修復的早期階段提供機械支架,并最終隨著新組織的向內生長而降解。明膠水凝膠拉伸強度高達1.1 MPa,抗壓強度高達12.4 MPa,楊氏模量高達320 kPa和高壓縮模量(837 kPa)。在模擬關節軟骨-軟骨下骨結構中,通過一步精確的熱輔助擠出打印技術及后期的UV光聚合得到PACG-GelMA-Mn2+上層軟骨層和載有生物活性玻璃的PACG-GelMA底骨層組成的雙層生物梯度水凝膠支架。BG的摻入可以改善hBMSCs的增殖,ALP活性和分化,而Mn2+的引入可以促進hBMSCs的軟骨分化,使得到的生物混合梯度水凝膠支架在大鼠膝骨軟骨缺損修復中起到同時加速軟骨和軟骨下骨分化的優越性。該研究成果“Osteochondral Regeneration with 3D‐Printed Biodegradable High‐Strength Supramolecular Polymer Reinforced‐Gelatin Hydrogel Scaffolds”發表在Advanced Science上。
I型糖尿病 (T1DM) 是一種慢性疾病, 由產生胰島素的β細胞永久破壞引起,細胞封裝技術可以在初始階段保護胰島免受宿主免疫排斥, 但長期的治療效果仍然是一個挑戰。理想的植入材料應該能夠容納功能細胞, 以及逃避體內免疫隔離稱為異物反應 (FBR)。目前, 非常有限的封裝生物材料可以逃避體內免疫識別, 因此, 它們最終被 FBR 從體內隔離。包封胰島移植是治療I型糖尿病的一種很有前途的方法。
圖16-在 STZ 誘導的糖尿病小鼠腹腔內移植后使用平衡的帶電水凝膠進行免疫保護和控制胰島素分泌的胰島封裝的示意圖。
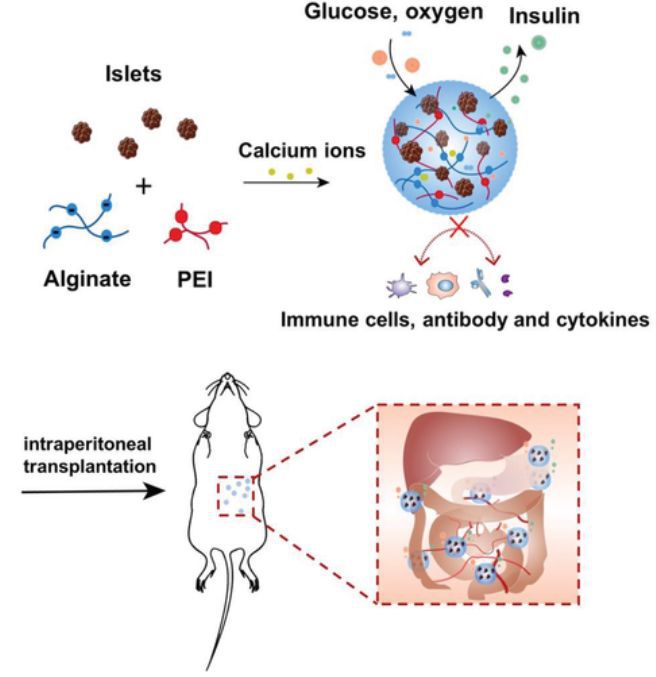
天津大學張雷教授課題組提出平衡電荷抗污原理,開發了一種具有高效抗生物粘附和“免疫屏蔽”能力的新型水凝膠材料,使用該水凝膠構建的“人造胰島”能夠在糖尿病小鼠體內實現長效控糖。研究發現,如圖16,封裝的胰島可以維持其葡萄糖反應和產生胰島素的功能。此外, 在免疫功能強的鏈球菌素誘導的糖尿病小鼠模型中, 腹腔內植入后, 水凝膠還能有效地規避體內 FBR。因此, 100% 的小鼠在 2d 內迅速恢復到正常血糖, 在沒有任何免疫抑制治療的情況下穩定維持至少 150d。這些發現揭示了 “胰島素獨立性和免疫隔離” 的包封策略, 它可以克服胰島移植的障礙, 并有可能提高目前的臨床治療效果。該項研究成果“Rapid and Long‐Term Glycemic Regulation with a Balanced Charged Immune‐Evasive Hydrogel in T1DM Mice”發表在Advanced Functional Materials上。
免責聲明:本網站所轉載的文字、圖片與視頻資料版權歸原創作者所有,如果涉及侵權,請第一時間聯系本網刪除。

官方微信
《中國腐蝕與防護網電子期刊》征訂啟事
- 投稿聯系:編輯部
- 電話:010-62313558-806
- 郵箱:fsfhzy666@163.com
- 中國腐蝕與防護網官方QQ群:140808414





